miR-377在宫颈癌中的表达及其对宫颈癌细胞增殖、侵袭和EMT的影响
蒋梦亭,施锦梅,叶文蔚,潘 丹
(台州学院附属市立医院 (台州市立医院) 妇科,浙江 台州 318000)
宫颈癌是发生在子宫颈部位的恶性肿瘤,疾病晚期的患者预后较差,且发病机制尚不清楚,因此更好地了解肿瘤进展非常重要。microRNA是一组小的非编码RNA,通过结合目标基因互补序列的3’非翻译区负调节基因。研究表明,miRNAs在多种生物过程中如细胞增殖、分化、凋亡和肿瘤发展等过程中发挥着重要作用。miR-377是染色体14q32上的大miRNA簇的成员,在一些人类恶性肿瘤中低表达,包括室管膜瘤、骨肉瘤、胃肠间质瘤和胶质瘤,有文献报道miR-377通过靶向pim3抑制胰腺癌的增殖。另有研究发现,miR-377过表达可抑制胶质母细胞瘤细胞增殖、迁移,并促进其凋亡,其机制可能与下调HDAC9、ETS-1蛋白表达有关。但目前关于miR-377与宫颈癌之间的关系尚不明了。本研究拟探究miR-377在宫颈癌中的表达及其作用机制,为进一步深入了解其在宫颈癌中发挥的调控作用而奠定基础。
1 材料与方法
1.1 主要材料 宫颈癌组织、距病变位置约为10 mm的癌旁正常组织,标本来自我院,采集的标本均获得患者或家属同意。人宫颈上皮永生化细胞株(H8细胞)、Hela、SiHa、Caski细胞购自上海奥陆生物科技有限公司;DMEM培养基购自中国赛默飞世尔科技公司;PKA通路抑制剂H-89购自美国Selleck公司;E-cadherin、N-cadherin抗体购自上海圣克鲁斯生物公司;CUL4A siRNA、miR-377 mimics、miR-377 inhibitor质粒由GenePharma公司合成。本实验经过本院伦理委员会审查和批准。
1.2 细胞培养与转染 用DMEM培养基培养宫颈癌细胞Hela、SiHa和Caski细胞、H8细胞,培养基中添加10% FBS,置于37 ℃、5% CO培养箱中,长满后传代培养。Hela细胞长满后分散铺于12孔板,密度达70%时,添加DMEM培养基,按照说明书将Turbofect、质粒、Opti-MEM混匀后静置20 min,滴至细胞中,48 h后收集细胞样用于后续检测。转染的细胞分为五组:第一组,包括Control组、mimics NC组和miR-377 mimics组;第二组,包括Control组、inhibitor NC组和miR-377 inhibitor组;第三组,包括CUL4A wt+mimics NC组、CUL4A wt+miR-377mimics组、CUL4A mut+mimics NC组、CUL4A mut+miR-377mimics组;第四组,包括Control组、siRNA NC组和CUL4A siRNA组;第五组,包括Control组、pcDNA-3.1(+)组、pcDNA-CUL4A组和pcDNA-CUL4A+H-89组。
1.3 细胞增殖测定 Hela细胞分散铺于96孔板中,细胞密度为75%时用Turbofect试剂转染重组质粒,48 h后加入100 μL PBS清洗,重复3次,取10 μL CCK-8工作液添加至细胞内,2 h后通过酶标仪读取细胞在450 nm处的吸光值。
1.4 双荧光素酶报告基因活性检测 TargetScan预测miR-377潜在靶基因以及CUL4A wt载体构建成功后,再构建CUL4A mut载体。将Hela细胞接种于12孔板,细胞长到70%~75%时,将CUL4A wt、CUL4A mut分别与miR-377 mimics、mimics NC质粒共转染至Hela细胞,48 h后测定共转细胞的荧光素酶活性。
1.5 细胞侵袭实验 从-20 ℃ 取出matrigel,加入无FBS DMEM培养基进行稀释(质量浓度为1 mg/mL),将100 μL matrigel添加于上室中凝成胶状。调整Hela细胞密度为5×10/mL,细胞悬液添加到Transwell小室,添加DMEM培养基于下室,48 h后加入PBS洗涤小室2次,多聚甲醛固定20 min,再用0.1%结晶紫染色15 min。采用直接法进行计数:随机选取5个视野细胞放在显微镜下观察,使用正置显微镜进行观察和拍照,把Transwell小室反过来底朝上可清楚看到小室底膜上下室侧附着的细胞,直接计数后进行统计分析。
1.6 细胞划痕愈合实验 将转染的细胞进行消化并制成单细胞悬液,每孔取3×10个/孔细胞置于6孔板中,48 h后取200 μL枪头在细胞表面垂直于孔板制造线性划痕,加入PBS清洗细胞,添加空培养基后在显微镜下进行观察和拍照,最后计算细胞划痕愈合率。
1.7 实时荧光定量PCR 从液氮中取出保存的组织标本,-80 ℃ 取出RNA样品,加入Trizol,并提取组织和细胞总RNA,RNA浓度和纯度测定后,反转成cDNA,进行实时荧光定量PCR,按照预变性95 ℃,10 min,变性95 ℃,10 s,退火60 ℃,20 s,延伸72 ℃,30 s,40个循环的程序进行。以GAPDH为内参,使用2法分析结果。引物序列见表1。

表1 引物序列
1.8 Western blot 提取组织和细胞中总蛋白,BCA试剂盒对蛋白裂解产物进行定量,SDS-PAGE凝胶电泳分离蛋白裂解物,将蛋白转移到PVDF膜上,5%脱脂奶粉在TBST中封闭1 h。PVDF膜与一抗在4 ℃孵育过夜,TBST洗涤3次,用二抗在37 ℃孵育1 h,最后蛋白显影及对蛋白条带灰度值定量分析。
1.9 统计学分析 使用SPSS 19.0统计软件处理数据。多组间比较采用单因素方差分析,组间两两比较采用LSD-检验,当<0.05时,表示差异有统计学意义。
2 结果
2.1 miR-377在宫颈癌中的表达 如图1所示,miR-377在宫颈癌组织的表达明显低于癌旁正常组织,在宫颈癌Hela、SiHa、Caski细胞中的表达明显低于H8细胞,差异有统计学意义(<0.01),且在Hela细胞中的表达量最低,因此选取Hela细胞进行后续实验。
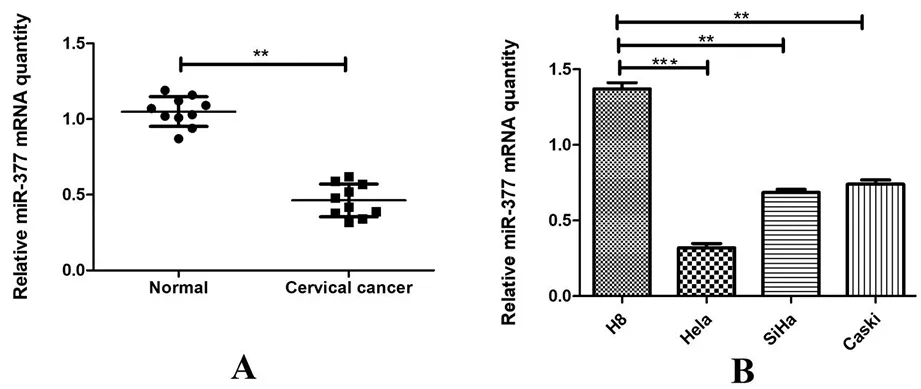
A. miR-377在宫颈癌组织和癌旁正常组织中的表达;B. miR-377在Hela、SiHa、Caski和H8细胞中的表达
2.2 过表达miR-377对Hela细胞发展的影响 RT-qPCR结果显示:miR-377 mimics组的miR-377表达量为2.83±0.57,E-cadherin表达量为0.87±0.21;Control组和mimics NC组的miR-377表达量分别为1.03±0.25、1.12±0.73,E-cadherin表达量分别为0.42±0.06和0.41±0.12;miR-377 mimics组的miR-377、E-cadherin表达量均高于Control组和mimics NC组,差异有统计学意义(<0.01)。如图2所示,与其他2组比较,miR-377 mimics组细胞侵袭数目明显减少,N-cadherin表达明显下降,Hela细胞划痕愈合率明显降低,差异有统计学意义(<0.01)。
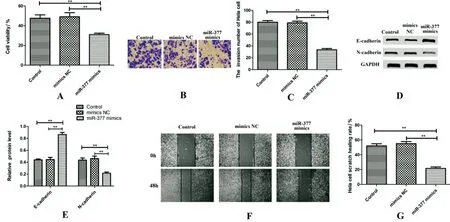
A.CCK-8检测过表达miR-377对Hela细胞增殖的影响;B.细胞侵袭实验检测过表达miR-377对Hela细胞侵袭的影响;C.Hela细胞侵袭数目;D.Western blot检测E-cadherin、N-cadherin的表达量;E.E-cadherin、N-cadherin的相对表达量;F.细胞划痕愈合实验检测下调miR-377对Hela细胞迁移的影响;G.Hela细胞的划痕愈合率
2.3 下调miR-377对Hela细胞发展的影响 RT-qPCR结果显示,miR-377 inhibitor组miR-377表达量为0.43±0.75,E-cadherin表达量为0.52±0.08;Control和inhibitor NC组miR-377表达量分别为1.12±0.22、1.09±0.27,E-cadherin表达量分别为1.15±0.23和1.06±0.35;miR-377 inhibitor组的miR-377、E-cadherin表达量均低于Control组和inhibitor NC组,差异有统计学意义(<0.01)。由图3可知,与inhibitor NC或Control组相比,miR-377 inhibitor组细胞增殖能力升高,细胞侵袭数目明显增加,N-cadherin表达明显上升,E-cadherin表达明显下降,Hela细胞划痕愈合率明显升高,差异均有统计学意义(<0.01)。
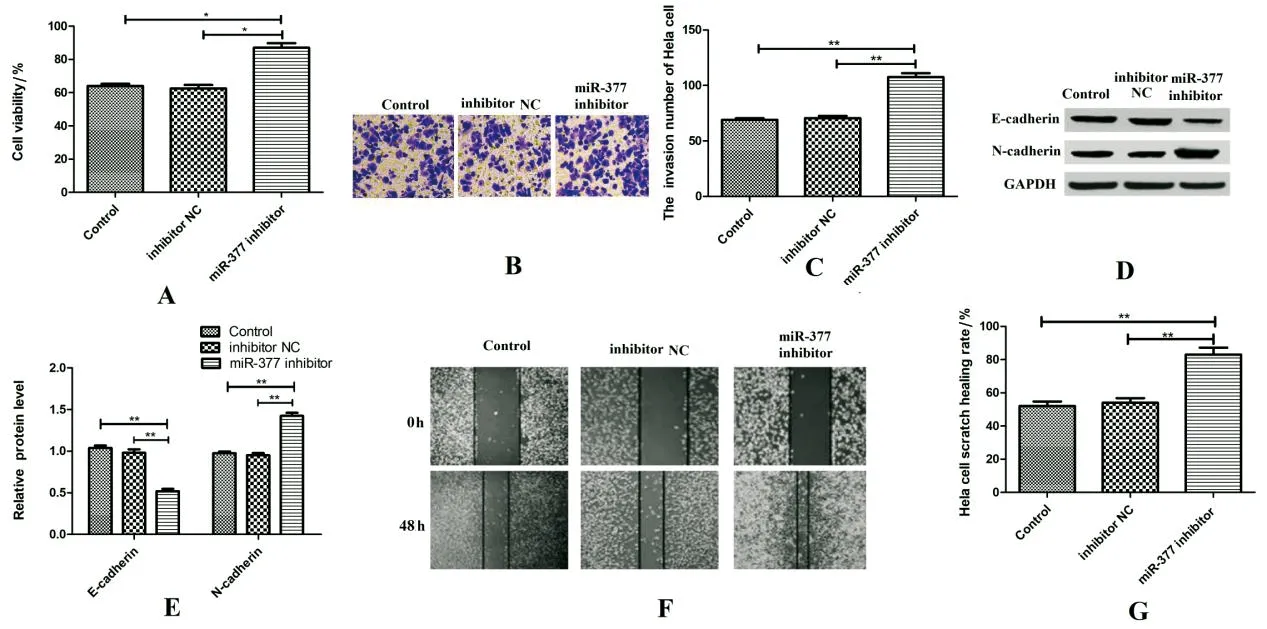
A.CCK-8检测下调miR-377对Hela细胞增殖的影响;B.细胞侵袭实验检测下调miR-377对Hela细胞侵袭的影响;C.Hela细胞的侵袭数目;D.Western blot检测E-cadherin、N-cadherin表达量;E.E-cadherin、N-cadherin相对表达量;F.细胞划痕愈合实验检测下调miR-377对Hela细胞迁移的影响;G.Hela细胞的划痕愈合率
2.4 miR-377与CUL4A的关系 预测miR-377和CUL4A之间的结合位点见图4A。由图4B结果可知,和CUL4A wt+mimics NC组相比,CUL4A wt+miR-377mimics组细胞荧光素酶活性降低,差异有统计学意义(<0.01);2组间细胞荧光素酶活性差异无统计学意义(>0.05)。由RT-qPCR结果可知:miR-377 mimics组CUL4A表达量(0.37±0.65)低于Control组(1.05±0.46)或mimics NC组(1.14±0.83),miR-377 inhibitor组CUL4A表达量(2.13±0.42)高于Control组(1.05±0.46)或inhibitor NC组(1.08±0.26),差异均有统计学意义(<0.01)。
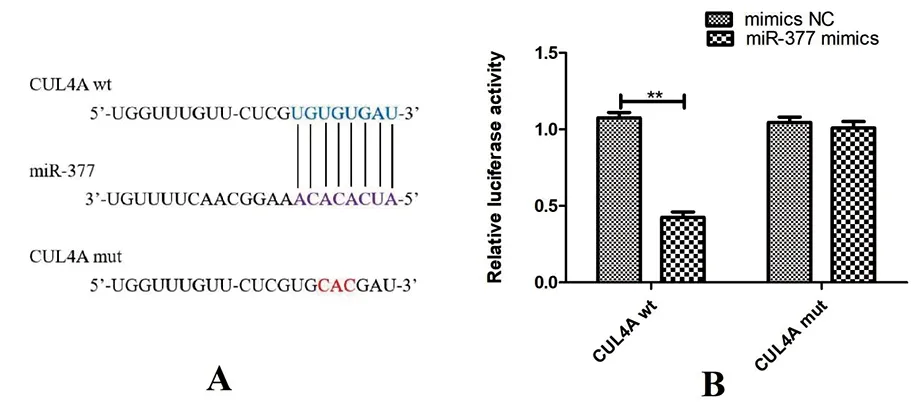
A.TargetScan预测miR-377和CUL4A之间的结合位点;B.荧光素酶表达量的测定
2.5 下调CUL4A对Hela细胞发展的影响 由图5可知,CUL4A在宫颈癌Hela细胞中的表达明显高于H8细胞,CUL4A siRNA组细胞增殖能力、细胞侵袭数目明显低于Control组或siRNA NC组,差异均有统计学意义(<0.01)。和Control组或siRNA NC组相比,CUL4A siRNA组E-cadherin表达明显上升,N-cadherin表达明显下降,Hela细胞划痕愈合率明显降低,差异均有统计学意义(<0.01)。
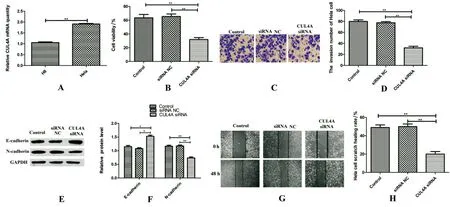
A.RT-qPCR检测CUL4A在Hela和H8细胞中的表达量;B.CCK-8检测下调CUL4A对Hela细胞增殖的影响;C.细胞侵袭实验检测下调CUL4A对Hela细胞侵袭的影响;D.Hela细胞的侵袭数目;E.Western blot检测E-cadherin、N-cadherin表达量;F.E-cadherin、N-cadherin的相对表达量;G.细胞划痕愈合实验检测下调CUL4A对Hela细胞迁移的影响;H.Hela细胞的划痕愈合率
2.6 CUL4A通过cAMP/PKA对Hela细胞发展的影响 和Control组或pcDNA-3.1(+)组相比,pcDNA-CUL4A组细胞内p-cAMP/cAMP和p-PKA/PKA比值升高(图6A、B);和Control组相比,H-89作用细胞后能够明显抑制PKA蛋白磷酸化水平(图6C);和pcDNA-3.1(+)组相比,pcDNA-CUL4A组的细胞增殖能力、侵袭数目、N-cadherin表达和细胞划痕愈合率升高、E-cadherin表达降低(图6D-6I);和pcDNA-CUL4A组相比,pcDNA-CUL4A+H-89组的细胞增殖能力、侵袭数目、N-cadherin表达和细胞划痕愈合率均降低,E-cadherin表达升高;差异均有统计学意义(<0.01)。
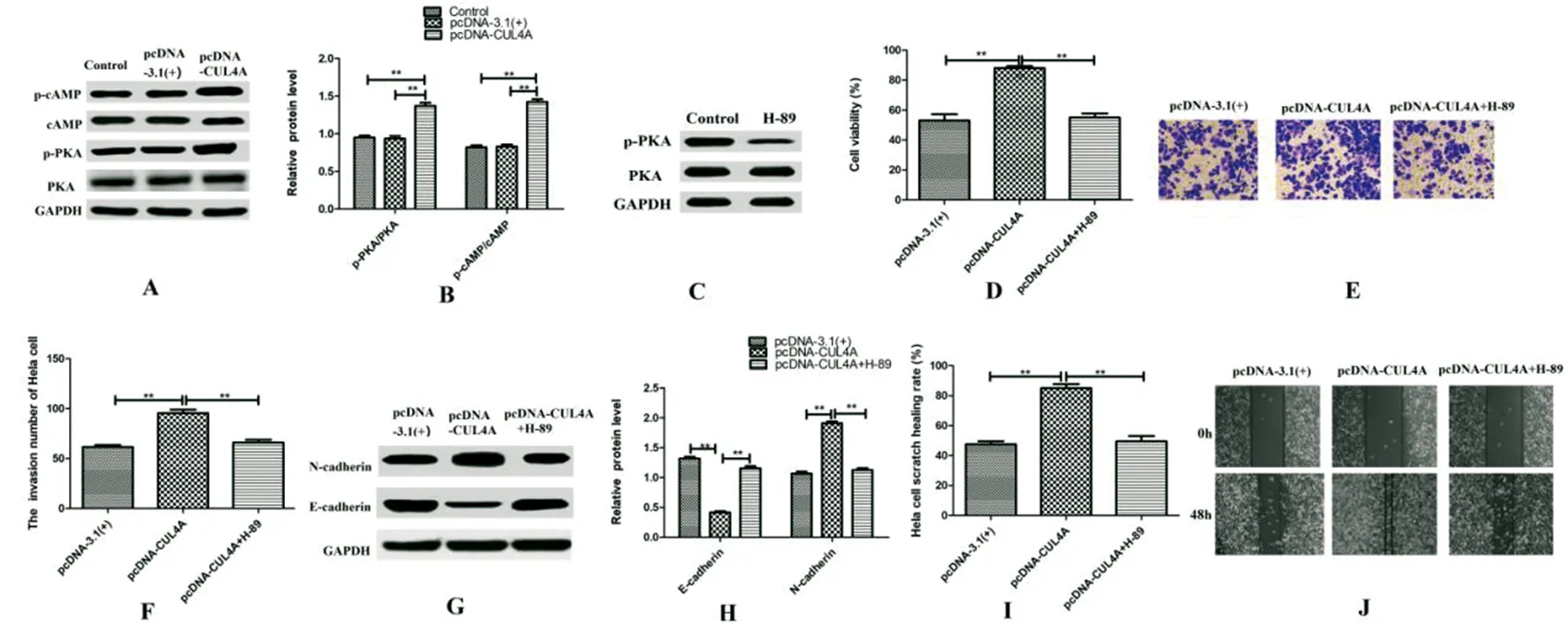
A.Western blot检测过表达CUL4A对cAMP/PKA通路的影响;B.p-cAMP/cAMP和p-PKA/PKA比值;C.Western blot检测H-89作用细胞后对p-PKA、PKA表达的影响;D.CCK-8检测过表达CUL4A通过cAMP/PKA通路对Hela细胞增殖的影响;E.细胞侵袭检测过表达CUL4A通过cAMP/PKA通路对Hela细胞侵袭的影响;F.Hela细胞侵袭数目;G.Western blot检测E-cadherin、N-cadherin表达量;H.E-cadherin、N-cadherin相对表达量;I.Hela细胞的划痕愈合率;J.细胞划痕愈合实验检测下调CUL4A对Hela细胞迁移的影响
3 讨论
研究表明在许多人类恶性肿瘤如室管膜瘤、胃肠道间质瘤和胶质瘤中,miR-377的表达被沉默。事实上,包括miR-377在内的14q32号染色体上的大miRNA簇被称为最大的miRNA肿瘤抑制簇。近些年的研究发现,miR-377在调控基因表达、细胞增殖和信号转导等方面具有丰富的功能,如miR-377的下调通过靶向HDAC9促进口腔鳞状细胞癌的生长和迁移,另外发现miR-377靶向ETS1在人透明细胞肾细胞癌中发挥抑癌作用。而在本研究中,我们发现miR-377在宫颈癌组织和Hela、SiHa、Caski细胞中表达量明显降低,且过表达miR-377降低了Hela细胞活力,抑制了癌细胞的侵袭,而下调miR-377则起到相反作用。提示miR-377可能在宫颈癌中起到抑制作用。
先前的研究表明miR-377能够靶向frizzled类受体4,该受体是前列腺癌细胞上皮间质转化和转移所必需的。miR-377还被证明靶向细胞周期蛋白依赖性激酶6和E2F转录因子3。然而,目前还不清楚miR-377在宫颈癌细胞中是否靶向CUL4A。EMT是癌细胞转移的重要过程。通过EMT,癌细胞在细胞外基质和血管基底膜获得更强的移动和迁移到循环系统中的能力,并由此形成二次转移。调控EMT在宫颈癌中的发生可能不仅是预测宫颈癌预后的重要生物标志物,也是进一步研究干预治疗以更有效地抑制或阻断宫颈癌转移的重要靶点。泛素连接酶E3,根据泛素转移方式的不同,分为环指E3泛素连接酶家族和与E6AP C端(HECT)泛素连接酶家族同源的两大类,在泛素介导的蛋白质降解中起作用。CUL4A属于cullin环基E3连接酶(CRLs),是环指E3泛素连接酶家族的主要组成部分,首先在乳腺癌中被发现,其扩增与多种癌症的发生和肿瘤转移密切相关。CUL4A在卵巢癌组织和细胞系中高表达,是miR-377的直接靶点,其活性受miR-377的调控。本研究表明,在宫颈癌中miR-377靶向和负调控CUL4A,且进一步研究发现下调CUL4A降低了Hela细胞活力,抑制了癌细胞的侵袭和EMT。
许多信号转导途径,包括转化生长因子β、丝裂原活化蛋白激酶、Notch和Wnt参与肿瘤细胞的增殖、侵袭和EMT过程。如研究发现miR-377-3p通过上调GSK-3β表达和激活NF-κB通路在hCRC细胞中驱动恶性发展。还有文献报道miR-377-3p、靶向XIAP和ZEB2负调控Wnt/catenin信号通路抑制结直肠癌。本研究表明过表达CUL4A激活了Hela细胞内cAMP/PKA信号通路,且通过该通路促进了癌细胞的发展。本研究结果提示miR-377靶向CUL4A可能通过cAMP/PKA信号通路抑制EMT过程,从而降低Hela细胞的增殖和迁移能力。
综上所述,本研究结果表明miR-377作为CUL4A的负性调节因子,导致宫颈癌细胞存活率和侵袭能力降低。本研究为深入了解宫颈癌的发病机制提供了理论依据,miR-377可能是宫颈癌患者的一个有希望的治愈靶点,值得进一步深入探讨。

