脓毒症心肌功能障碍及其预后影响因素研究
庄燕,张海东,戴林峰,陈秋华,王建
脓毒症是机体对感染反应失调导致的危及生命的器官功能障碍[1]。脓毒症心肌功能障碍(sepsis-induced myocardial dysfunction,SIMD)又称脓毒症心肌病,是脓毒症导致的心脏收缩和/或舒张功能障碍,具有发生早、发生率高的特点,明显增加了脓毒症患者的死亡率[2]。1984年,PARKER等[3]首次发现脓毒症患者发生了可逆性心肌功能障碍。SIMD的发生机制复杂,涉及冠状动脉缺血、心脏微循环障碍、炎症反应、心肌收缩异常、心脏肾上腺素受体表达下调、心肌细胞钙离子转运异常、细胞凋亡、线粒体功能障碍等机制[4-5],临床治疗亦存在一定难度。如何早期识别SIMD高危患者并采取干预措施,对于改善脓毒症患者心脏功能及预后具有重要意义。因此,本研究旨在探讨SIMD及其预后的影响因素,以期为SIMD的临床干预提供指导。
1 对象与方法
1.1 研究对象 回顾性选取2019年6月至2020年12月南京中医药大学附属医院重症医学科收治的脓毒症患者102例。纳入标准:因脓毒症收住重症监护病房的患者,其中脓毒症诊断参照2016年第3次脓毒症定义[6],不论是否存在脓毒症休克。排除标准:(1)合并急性冠脉综合征者;(2)慢性心功能不全终末期者;(3)严重肾功能不全需进行维持性血液透析者;(4)低血量性休克者;(5)行心肺复苏者。本研究经南京中医药大学附属医院伦理委员会批准(2022NL-009-01),所有患者签署知情同意书。
1.2 SIMD诊断 由2名专科主治及以上职称医师进行诊断,SIMD诊断标准:心肌肌钙蛋白Ⅰ(cardiac troponin I,cTnI)>0.04 μg/L或左心室射血分数(left ventricular ejection fraction,LVEF)<50%的脓毒症患者[7]。根据是否发生SIMD将患者分为SIMD组和非SIMD组。
1.3 临床资料收集 收集患者临床资料,包括性别、年龄,高血压、冠心病、糖尿病、慢性肾脏病(chronic kidney disease,CKD)、慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)发生情况,入院时平均动脉压(mean arterial pressure,MAP)、心率(heart rate,HR)、氧合指数(oxygenation index,OI)、血乳酸(lactate,Lac)、血肌酐(serum creatinine,Scr)、WBC、降钙素原(procalcitonin,PCT)、B型利钠肽(B-type natriuretic peptide,BNP)、肌酸激酶同工酶(creatine kinase isoenzyme,CK-MB)、急性生理学与慢性健康状况Ⅱ(Acute Physiology and Chronic Health Evaluation Ⅱ,APACHE Ⅱ)评分、序贯器官衰竭评估(sequential organ failure assessment,SOFA)评分,ICU住院时间,28 d生存情况。根据28 d死亡情况,将SIMD患者分为存活亚组和死亡亚组。
1.4 统计学方法 采用SPSS 20.0统计学软件进行数据分析。符合正态分布的计量资料以(±s)表示,组间比较采用两独立样本t检验;不符合正态分布的计量资料以M(P25,P75)表示,组间比较采用Mann-Whitney U检验。计数资料以相对数表示,组间比较采用χ2检验。采用Kaplan-Meier法绘制生存曲线,生存率比较采用Log-rank检验。采用R软件(版本4.2.1)进行多因素Logistic回归分析以探讨脓毒症患者发生SIMD的影响因素及SIMD患者28 d死亡的影响因素。采用GraphPad Prism绘制ROC曲线以评估影响因素对脓毒症患者发生SIMD及SIMD患者28 d死亡风险的预测价值。以P<0.05为差异有统计学意义。
2 结果
2.1 临床资料 102例患者中有45例发生SIMD,SIMD发生率为44.1%。SIMD组和非SIMD组患者性别、年龄,高血压、冠心病、糖尿病、CKD、COPD发生率,MAP、HR、OI、Lac、WBC、PCT、CK-MB,ICU住院时间比较,差异无统计学意义(P>0.05);SIMD组患者Scr、BNP、APACHE Ⅱ评分、SOFA评分高于非SIMD组,差异有统计学意义(P<0.05),见表1。生存曲线分析结果显示,SIMD组和非SIMD组患者28 d生存率比较,差异无统计学意义(χ2=0.527,P=0.468),见图1。

图1 SIMD组和非SIMD组患者生存曲线Figure 1 Survival curve of SIMD group and non-SIMD group

表1 SIMD组和非SIMD组患者临床资料比较Table 1 Comparison of clinical data between SIMD group and non-SIMD group
2.2 脓毒症患者发生SIMD影响因素的多因素Logistic回归分析 以脓毒症患者是否发生SIMD为因变量(赋值:发生=1,未发生=0),以脓毒症患者发生SIMD的可能影响因素(性别、年龄、HR、Scr、BNP、APACHE Ⅱ评分、SOFA评分)为自变量,进行多因素Logistic回归分析,结果显示,年龄、HR、BNP及SOFA评分是脓毒症患者发生SIMD的影响因素,见表2。绘制年龄、HR、BNP、SOFA评分及四者联合预测脓毒症患者发生SIMD的ROC曲线,结果显示,年龄、HR、BNP、SOFA评分及四者联合预测脓毒症患者发生SIMD的AUC分别为0.608、0.576、0.649、0.681及0.770,见图2、表3。

表2 脓毒症患者发生SIMD影响因素的多因素Logistic回归分析Table 2 Multivariate Logistic regression analysis of influencing factors of SIMD in patients with sepsis

表3 年龄、HR、BNP、SOFA评分及四者联合预测脓毒症患者发生SIMD的价值Table 3 Predictive value of age, HR, BNP, SOFA score and their combination for SIMD in patients with sepsis

图2 年龄、HR、BNP、SOFA评分及四者联合预测脓毒症患者发生SIMD的ROC曲线Figure 2 ROC curve of age, HR, BNP, SOFA and their combination in predicting SIMD in patients with sepsis
2.3 SIMD患者28 d死亡影响因素的多因素Logistic回归分析 45例SIMD患者中16例28 d内死亡。死亡亚组和存活亚组患者性别,高血压、冠心病、糖尿病、CKD、COPD发生率,HR、OI、Lac、Scr、WBC、PCT、CK-MB、APACHEⅡ评分比较,差异无统计学意义(P>0.05);存活亚组患者年龄、BNP、SOFA评分低于死亡亚组,MAP高于死亡亚组,差异有统计学意义(P<0.05),见表4。以SIMD患者28 d死亡情况为因变量(赋值:死亡=1,存活=0),以表4中P<0.1的指标为自变量,进行多因素Logistic回归分析,结果显示,SOFA评分为SIMD患者28 d死亡的影响因素,见表5。绘制SOFA评分预测SIMD患者 28 d死亡风险的ROC曲线,结果显示,SOFA评分预测SIMD患者28 d死亡风险的AUC为0.704〔95%CI(0.534,0.873)〕,最佳截断值为11.5分,灵敏度为0.500,特异度为0.862,见图3。

图3 SOFA评分预测SIMD患者28 d死亡风险的ROC曲线Figure 3 ROC curve of SOFA score in predicting 28-day mortality risk in SIMD patients
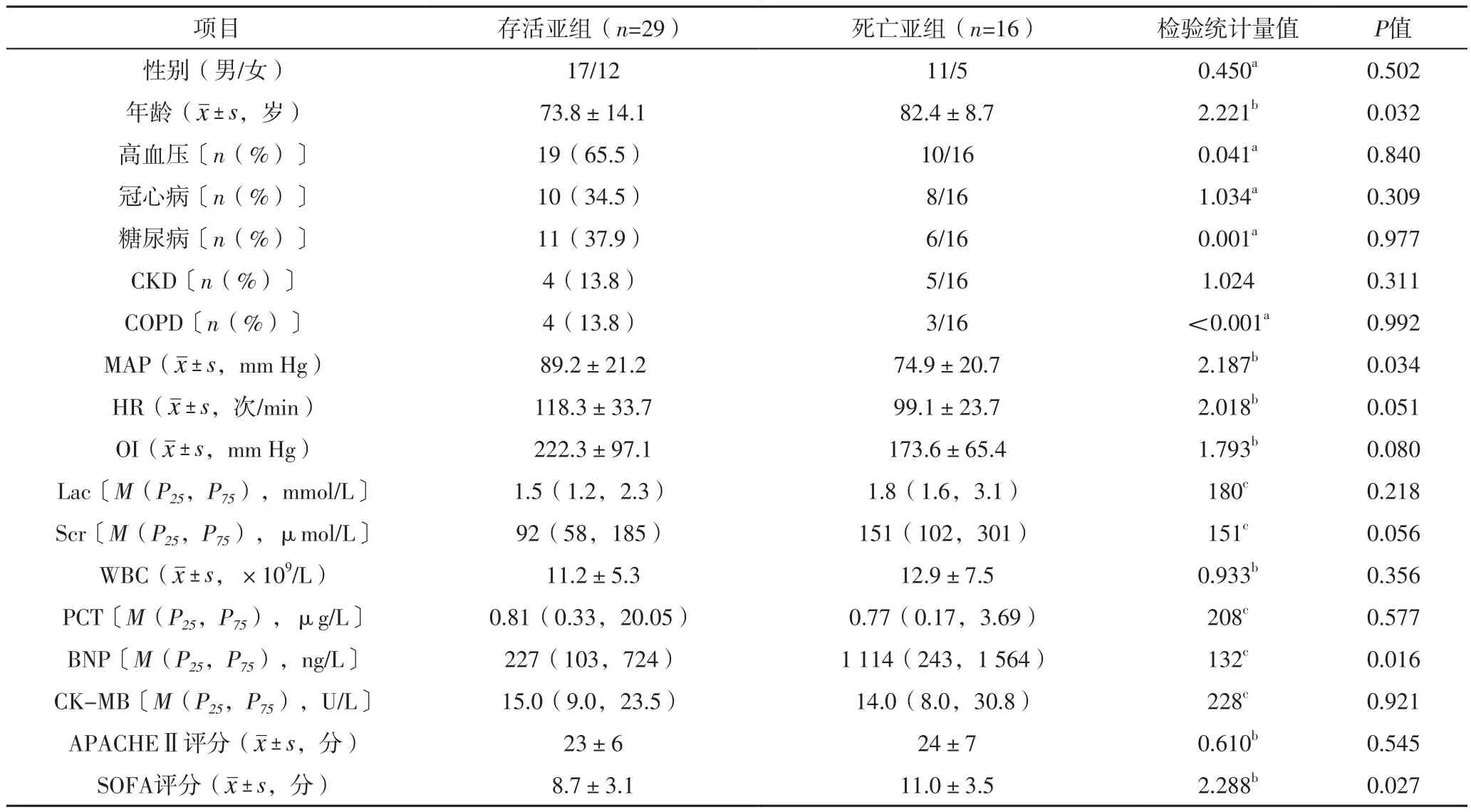
表4 存活亚组与死亡亚组患者临床资料比较Table 4 Comparison of clinical data between survival subgroup and death subgroup

表5 SIMD患者28 d死亡影响因素的多因素Logistic回归分析Table 5 Multivariate Logistic regression analysis of influencing factors of 28-day death in SIMD patients
3 讨论
SIMD是脓毒症多器官功能障碍发生的重要一环,故及时处理SIMD对于改善脓毒症患者预后具有重要意义。探索SIMD的机制并采取针对性措施是近年重症医学领域的研究热点[8-10]。基于脓毒症病因、严重程度、治疗措施等差异,重症监护病房内脓毒症患者心肌功能障碍发生率为10%~70%[11-12],且合并心肌功能障碍将明显增加脓毒症患者死亡率[2,12-13]。研究发现,SIMD的危险因素包括高龄、糖尿病病史、心功能不全病史、BNP升高、血培养阳性、电解质紊乱及APACHEⅡ评分升高等[14-16]。
本研究结果显示,SIMD发生率为44.1%,与既往研究结果[11]相似。本研究多因素Logistic回归分析结果显示,脓毒症患者发生SIMD的影响因素为年龄、HR、BNP及SOFA评分,未发现高血压、冠心病、糖尿病对SIMD有影响,考虑可能与入选患者年龄偏大、慢性病发生率较高有关。众所周知,年龄是心血管疾病的重要危险因素。随着年龄增长,心脏及血管的结构及功能将发生相应变化,其中心肌细胞线粒体能量代谢异常在衰老相关心脏疾病的发生中具有重要作用[17]。SIMD发生机制亦涉及线粒体能量代谢异常[5],而高龄带来的心脏结构及功能改变将明显增加SIMD发生风险。HR是临床常用的监测指标,研究发现,HR增快是心血管疾病的独立危险因素[18]。脓毒症患者可因缺氧、炎症、发热、疼痛、应激等因素而导致静息HR增快,其在一定程度上反映了疾病的严重程度。脓毒症休克患者HR增快已被认为是其血流动力学越来越低效、器官功能障碍程度加重以及预后不良的指标[19]。研究发现,采用β-受体阻滞剂控制HR可以改善脓毒症患者预后[20]。
BNP是由心肌细胞合成、分泌的肽类激素,主要来源于心房肌细胞。当心室压力及室壁张力增加时,BNP在心室肌细胞的表达增多,其具有利尿、舒张血管等作用,可用以评价心功能[21-23]。研究发现,脓毒症合并心肌功能障碍患者BNP水平升高,且BNP与患者预后不良相关[14,24]。导致BNP升高的因素包括心肌损伤、容量超负荷、心律失常、肾小球滤过率降低等,针对以上因素采取相应措施或可减轻SIMD。脓毒症患者存在的过度炎症反应、液体治疗过程中容量监测不及时、合并急性肾损伤等因素均可引起心肌损伤、容量超负荷,导致BNP合成增加,其在一定程度上反映了病情及心肌功能障碍严重程度;而当原发病、心肌功能障碍减轻时,BNP水平也逐渐下降。作为一种生物标志物,BNP水平与心肌功能障碍程度相关,但本研究未分析BNP升高与SIMD之间的时序关系,不能确定BNP升高与心肌功能障碍的因果关系,还需要进一步研究明确。近年急性心力衰竭指南推荐将重组人脑利钠肽用于急性心功能不全的治疗,其可以缓解患者疾病症状,改善患者预后[25-26]。重组人脑利钠肽用于伴BNP水平升高的SIMD患者或可改善其预后,但仍需要进一步临床研究评估。
SOFA评分是重症监护病房评估患者病情严重程度及判断患者预后的常用指标,可用来评估重症患者的临床结局[27]。近年SOFA评分在感染性疾病中的应用获得较多关注。PAWAR等[28]研究发现,不同感染来源的重症患者SOFA评分存在差异。MCCARTHY等[29]研究发现,SOFA评分可评估重症创伤患者后续感染风险。研究发现,与其他预后评分如床旁急性胰腺炎严重程度指数、APACHE Ⅱ评分相比,SOFA评分在急性胰腺炎患者中具有更好的特异性,可用来预测急性胰腺炎患者ICU住院率及死亡率[30]。ABDULLAH等[31]评估了SOFA评分在急诊感染患者中的应用价值,结果显示,SOFA评分≥2分预测急性感染患者28 d死亡风险的价值优于快速序贯器官衰竭评分及全身炎症反应综合征评分。本研究结果显示,SOFA评分预测脓毒症患者发生SIMD的AUC为0.681。此外,SOFA评分还是SIMD患者28 d死亡风险的独立预测因子,其预测SIMD患者28 d死亡风险的AUC为0.704。
综上所述,脓毒症患者SIMD发生率较高。年龄增大和HR增快及BNP、SOFA评分升高是脓毒症患者发生SIMD的危险因素,且SOFA评分升高是SIMD患者28 d死亡的危险因素。但本研究为回顾性研究,存在一定局限性:(1)未评估治疗措施差异对脓毒症患者发生SIMD的影响,如初始液体治疗量、血管活性药物使用量、吸氧等治疗措施可能会影响BNP及心肌肌钙蛋白I水平;(2)因部分患者病情危重,故未能及时进行超声心动图检查以评估心脏结构及功能,仅行床旁超声检查以快速评估LVEF,故未将超声心动图参数纳入分析;(3)本研究收治的脓毒症患者以内科感染居多,且年龄偏大,慢性病发生率高,不能全面反映脓毒症患者临床特征,存在一定偏倚;(4)本研究样本量偏小,不排除增加样本量会对结论产生影响。
作者贡献:庄燕进行文章的构思与设计,研究的实施与可行性分析,撰写、修订论文,负责文章的质量控制及审校,对文章整体负责、监督管理;张海东、戴林峰、王建进行资料收集;庄燕、张海东、戴林峰进行资料整理;庄燕、陈秋华进行统计学处理。
本文无利益冲突。

