Au/g-C3N4纳米复合材料可见光催化产氢
宁 靖,李广芳,陈 嵘,赵慧平*
1.武汉工程大学化学与环境工程学院,绿色化工过程教育部重点实验室(武汉工程大学),湖北 武汉 430205;
2.华中科技大学化学与化工学院,湖北 武汉 430074;
能源危机的出现,使得寻求绿色可持续的清洁能源尤为重要。其中,运用光催化技术生成氢气是能够满足未来清洁能源需求的极具潜力的研究领域之一[1]。由于许多半导体材料光响应范围较窄,只能利用太阳光谱中仅占4%的紫外光,并不能有效利用太阳能,因此,开发稳定、高效、具备可见光响应性能的光催化体系具有重要意义[2-3]。
在众多的半导体材料中,石墨相氮化碳(g-C3N4)是具有石墨类似层状结构的共轭有机聚合物,具有禁带宽度易于调控、热稳定性高、化学稳定性好、环境友好等优点,在光催化能源转化方面具有广泛的应用前景[4-6]。自从王心晨课题组报道了g-C3N4具有光催化产氢活性以来[7-8],由于g-C3N4具有合适的氧化还原电位,g-C3N4在光催化产氢领域的研究逐渐广泛[9-11]。但纯相g-C3N4的光响应范围较窄、光生电子-空穴对的复合率较高,使得其光催化活性受限[12]。为了解决这一问题,在催化剂表面负载一些助催化剂是改善g-C3N4光催化性能的有效手段[13-14]。Ag、Au 等贵金属纳米粒子具有独特的表面等离激元效应,通常可以通过改变尺寸、形状和周围介电环境来调控其光学性质,从而表现出优良的可见光响应性能[15]。研究者们通过将g-C3N4和贵金属纳米粒子复合构成纳米异质结构,有效利用贵金属表面等离激元共振效应实现了g-C3N4材料光响应范围的拓宽[16-18]。此外,当金属与半导体接触时,会产生复杂的电荷转移和共振能量转移,其中,金属-光相互作用产生的热电子可直接注入到半导体,提高入射光的利用率;表面等离激元诱导产生的局域场增强使得光-半导体相互作用增强,从而大大提高半导体的光生载流子的浓度;同时,金属纳米颗粒也可作为电子受体和氧化还原反应活性中心,将电子迅速从半导体转移使得电子-空穴快速分离,从而大大增强载流子寿命,提升纳米复合材料的光催化性能[19-21]。
基于上述背景,本文将具有表面等离激元效应的Au NPs 负载于g-C3N4制得纳米复合材料,并将该复合材料用于可见光下光催化产氢探究其催化活性,结合光电性质表征探究表面等离激元材料Au NPs 的引入对g-C3N4纳米材料催化性能的影响。
1 实验部分
1.1 化学试剂与材料
三水合氯金酸(HAuCl4·3H2O,99%,上海迈瑞尔化学技术有限公司);三羟甲基氨基甲烷[NH2C(CH2OH)3,99.99%,上海如吉生物科技发展有限公司];二水合柠檬酸钠(Na3C6H5O7·2H2O)、尿素(CH4N2O)、无水乙醇(C2H6O)(分析纯,国药集团化学试剂有限公司)。以上试剂使用前均未做任何处理及纯化。实验用水为去离子水。
1.2 实验方法
1.2.1 金纳米球(Au NPs)的制备(1)金种子(Au-seed)的制备:取48 mL 去离子水于100 mL 双口烧瓶中,保持磁力搅拌(400 r/min),水浴加热至沸腾,快速加入0.5 mL HAuCl4·3H2O(25 mol/L)水溶液,回流10 min。随后,将1.5 mL 柠檬酸三钠(质量分数为1%)水溶液快速注入反应液中,继续反应30 min,制备得到纳米金种子(样品记为Auseed),自然冷却至室温,置于冰箱中保存备用。
(2)金纳米球(Au NPs)的制备:取185 mL 去离子水于250 mL 双口烧瓶中,保持磁力搅拌(转速400 r/min),水浴加热至沸腾,快速加入8 mL 三羟甲基氨基甲烷(0.1 mol/L)水溶液,回流反应10 min。随后,将5 mL 合成好的Au-seed 和2 mL HAuCl4·3H2O(25 mmol/L)水溶液快速注入回流反应液中,继续回流30 min,最终所得样品总体积为200 mL。自然冷却至室温,置于冰箱中保存备用。所得到样品记为Au NPs。
1.2.2 氮化碳(g-C3N4)的制备 称取10 g 尿素置于坩埚中,于马弗炉中550 ℃(升温速率设定为2 ℃/min)煅烧2 h,待所得样品自然降温至室温后继续于马弗炉中500 ℃(升温速率为2 ℃/min)煅烧2 h。随后待样品再次自然冷却至室温,研磨收集样品。所得样品记为g-C3N4。
1.1.3 Au/g-C3N4复合材料的制备 将Au NPs 负载于g-C3N4得到不同负载量的Au/g-C3N4纳米材料,具体实验过程为:称取0.1 g 上述g-C3N4样品,分散于30 mL 无水乙醇中,而后分别加入质量分数为1%、2%、5%和10%的Au NPs,超声30 min,得到均匀分散的悬浊液,旋蒸至干,收集样品于40 ℃真空干燥箱干燥过夜,分别得到质量分数1%Au/g-C3N4、2.5% Au/g-C3N4、5% Au/g-C3N4和10%Au/g-C3N4复合材料,在Ar气气氛下保存备用。
1.3 样品的表征
样品的物相结构通过X-射线粉末衍射(X-ray diffraction,XRD)仪(Bruker axs D8 Advance,德国)进行表征,以Cu Kα 为辐射源。样品的微观形貌通过冷场发射扫描电镜(scanning electron microscope,SEM)(Hitachi Su8010,日本)进行表征。样品的官能团结构通过傅里叶变换红外光谱仪(Fourier transform infrared spectrometer,FT-IR)(Bruker TENSOR 27,德国)进行表征。样品的光学性质通过紫外-可见分光光度计(ultraviolet and visible spectrophotometry,UV-Vis,翱 艺A590,上海)表征,测试波长范围为350~1 100 nm。样品的光响应能力通过紫外可见漫反射光谱(UV-visible diffuse reflectance spectrum,DRS)(Hitachi UH4150,日本)进行表征,以硫酸钡作为参比。样品的光生载流子复合效率通过荧光分光光度计(fluorospectrophotometer,PL)(Hitachi F 4600)进行表征,激发波长为325 nm。
1.4 光催化产氢性能评价
样品的光催化产氢性能通过CEL-SPH2N(中教金源,北京)光催化活性评价系统进行测试。具体实验过程为:准确称取10 mg 待测样品于反应器中,加入50 mL 含有体积分数为20%的三乙醇胺水溶液,超声分散均匀;盖上反应器石英上盖,将反应器接入反应系统中,使用冷凝循环水将反应体系温度控制为10 ℃;对反应体系抽真空,去除管路中的空气和溶液中的溶解氧。打开氙灯(功率300 W,中教金源CEL-HXF300)进行光照,反应过程中持续磁力搅拌,每隔固定时间间隔自动取样,通过气相色谱(中教金源GC-7920)热导检测器(thermal conductivity detector,TCD)对产物氢气进行检测,根据峰面积和氢气摩尔数之间的标准曲线对产生的氢气进行定量。
1.5 光电性能测试
通过辰华电化学工作站(CHI-760E,上海)对样品的光电流、电化学阻抗等光电性质形成测试。在光电流测试过程中,以铂电极为对电极,饱和甘汞电极为参比电极,采用标准三电极体系对样品进行测试。工作电极的制作过程如下:准确称取0.01 g 待测样品分散于0.5 mL 无水乙醇中,加入40 μL Nafion 膜溶液,超声分散均匀。用移液器准确移取40 μL 上述分散液于铟锡氧化物(ITO)导电玻璃电极,覆盖面积为1 cm2,样品均匀铺平自然晾干后测试。以0.5 mol/L 的Na2SO4溶液为电解质,以50 W 氙灯(XD-300 冷光源,南京)作为光源,在开路电压下进行测试,通过控制工作电极光照与否,以观察并记录待测样品产生的光生电流。在电化学阻抗测试过程中,以玻碳电极为工作电极,经打磨清洗后备用。取上述工作电极分散液10 μL 于洁净的玻碳电极表面,自然晾干后测试。以25 mmol/L K3[Fe(CN)6]、25 mmol/L K4[Fe(CN)6]和0.10 mol/L KCl 混合溶液为电解质,在开路电压下进行测试。
2 结果与讨论
2.1 样品的物相、形貌与性质表征
首先通过XRD 对合成的Au NPs、g-C3N4以及不同Au NPs 负载量的Au/g-C3N4的物相结构进行表征。如图1(a)所示,单纯Au NPs 样品在衍射角2θ为38.2o、44.4o、64.6o和77.5o的衍射峰与立方晶系 的Au(ICDD 03-065-8601)的(111)、(200)、(220)和(311)晶面相对应;单纯g-C3N4样品在衍射角2θ为13.3o和27.5o处具有2 个特征衍射峰,分别对应g-C3N4的(100)和(002)晶面,前者归因于面内三嗪单元的有序排列,后者归因于芳香族单元的层间堆积,表明该样品具有类石墨烯层状结构[22]。在Au/g-C3N4样品中,2θ为27.5o处依然存在g-C3N4的特征衍射峰,此外,衍射角2θ为38.2o、44.4o、64.6o和77.5o的衍射峰与立方晶系的Au(ICDD 03-065-8601)的(111)、(200)、(220)和(311)晶面相对应,表明成功制备了Au/g-C3N4复合结构,随着Au NPs 的负载量增加,Au NPs 衍射峰的强度亦不断增强。如图1(b)所示,在g-C3N4样品中,808 cm-1处的吸收峰是三嗪结构单元伸缩振动信号,1 200~1 700 cm-1处的吸收带是CN 杂环结构的伸缩振动信号,3 000~3 500 cm-1处的宽吸收为N-H 键和O-H 的伸缩振动信号[23]。负载Au NPs 后,样品的红外光谱信号无明显变化,表明Au NPs 的引入并未改变g-C3N4的结构。

图1 样品的XRD 谱图(a)及红外光谱图(b)Fig.1 XRD patterns(a)and IR spectra(b)of samples
通过SEM 对所得Au NPs、g-C3N4以及质量分数2.5%Au/g-C3N4的形貌进行表征。图2(a、b)分别为Au NPs 的SEM 图和粒径分布图,从图中可知,成功合成了尺寸均一、单分散性好的金纳米球,Au NPs 的平均粒径约为55 nm。图2(c、d)为g-C3N4和质量分数2.5% Au/g-C3N4复合材料的SEM 图,前者为不规则的片状结构,负载Au NPs后,片状g-C3N4表面出现球形颗粒(红圈标出),表明Au NPs 成功修饰于g-C3N4表面。

图2 样品的SEM 图(a,c,d)及尺寸分布图(b)Fig.2 SEM images(a,c,d)and size distribution spectra(b)of samples
通过UV-Vis 对Au NPs 的表面等离激元特性进行表征,图3(a)为Au NPs 消光光谱,Au NPs 的表面等离激元共振峰为530 nm;通过DRS 对g-C3N4以及质量分数2.5%Au/g-C3N4的光响应范围进行表征,从图3(b)可以看出,相较单纯g-C3N4,负载Au NPs 后的质量分数2.5% Au/g-C3N4在可见光区出现明显吸收峰,该吸收峰位置为530 nm,与Au NPs 的表面等离激元共振峰位置一致,表明Au NPs 负载g-C3N4能够有效拓宽复合样品的光响应范围。进一步根据Kubelka-Munk公式αhν1/2=A(hν-Eg)计算半导体g-C3N4的禁带宽度,如图3(c)所示,单纯g-C3N4的禁带宽度约为2.84 eV[24]。
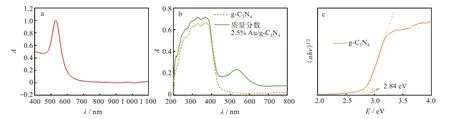
图3 样品的光学性质表征:(a)消光光谱图,(b)紫外可见漫反射光谱图,(c)(αhν)1/2-E 关系曲线Fig.3 Optical properties of samples:(a)extinction spectra,(b)diffuse reflectance spectra,(c)(αhν)1/2 versus energy curve
2.2 样品的光催化产氢活性分析
在测试样品的光催化产氢性能之前,对牺牲剂的选择和催化剂的用量进行简单优化。选取文献中常用的空穴牺牲剂[25],分别以体积分数为20%的甲醇(MeOH)、异丙醇(IPA)、乳酸(LA)和三乙醇胺(TEOA)作为牺牲剂,催化剂用量10 mg,质量分数2.5% Au/g-C3N4样品可见光下光照4 h产氢量随时间变化图及光催化产氢速率如图4 所示。其中,以体积分数20% TEOA 作为牺牲剂时,光照4 h的光催化产氢量和产氢速率最高,使用其他牺牲剂时并未表现明显的产氢活性,故在后续反应中以体积分数为20%的TEOA做为空穴牺牲剂。

图4 使用不同牺牲剂时2.5%Au/g-C3N4样品的可见光催化产氢性能:(a)产氢量随时间变化曲线,(b)光催化产氢速率Fig.4 Visible light photocatalytic hydrogen production of 2.5%Au/g-C3N4 using different sacrificial agents:(a)curves of hydrogen production amount versus time,(b)photocatalytic hydrogen production rates
图5 为改变催化剂的用量,质量分数2.5%Au/g-C3N4复合材料光见光下光照4 h 产氢量随时间变化图及光催化产氢速率。随着催化剂用量的增加,光催化产氢量呈现先增加后降低趋势,这可能是因为当加入适量催化剂时,材料表面活性位点与牺牲剂分子的结合可达到饱和,而加入过多的催化剂,会降低反应液的透光性,使得底部催化剂光吸收受阻,光催化产氢量降低,因而选取催化剂用量为10 mg。

图5 不同催化剂用量的2.5%Au/g-C3N4样品的可见光催化产氢性能:(a)产氢量随时间变化曲线,(b)光催化产氢速率Fig.5 Visible light photocatalytic hydrogen production of 2.5%Au/g-C3N4 with different phocatalyst dosages:(a)curves of hydrogen production amount versus time,(b)photocatalytic hydrogen production rates
以体积分数20% TEOA 为牺牲剂,催化剂用量为10 mg,图6 为g-C3N4和不同负载量的Au/g-C3N4样品在可见光下光照4 h 产氢量随时间变化图及光催化产氢速率。随着Au NPs 负载量的增加,复合材料光催化产氢性能先增加后降低,Au NPs 的负载量2.5%时,光催化产氢活性最优。适量的Au NPs 负载在g-C3N4表面能够促进光生载流子的生成与迁移,当Au NPs 负载量超过2.5%时,过量的Au NPs 可能会成为新的载流子复合中心,或者覆盖了g-C3N4的活性位点,使得其光催化活性反而降低[26]。
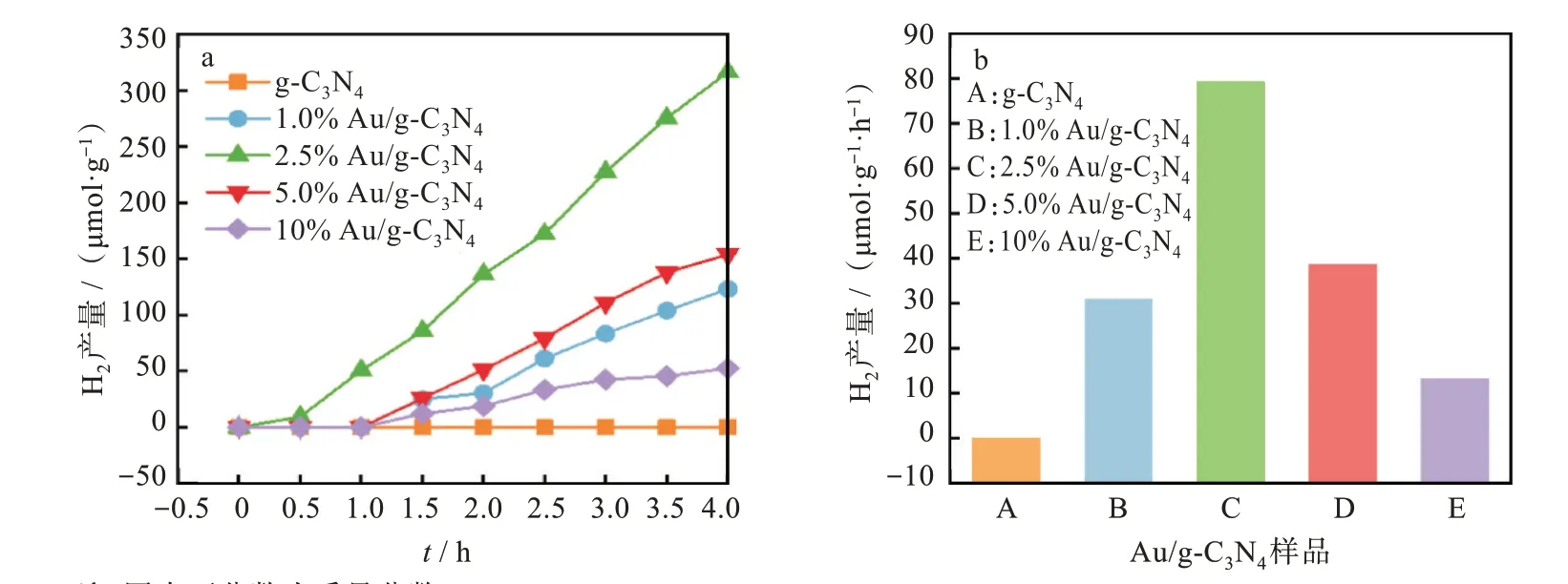
图6 不同Au NPs 负载量的Au/g-C3N4样品的可见光催化产氢性能:(a)产氢量随时间变化曲线,(b)光催化产氢速率Fig.6 Visible light photocatalytic hydrogen production of Au/g-C3N4 with different Au NPs loadings:(a)curves of hydrogen production amount versus time,(b)photocatalytic hydrogen production rates
2.3 光催化产氢活性增强原因
图7 为g-C3N4和质量分数2.5% Au/g-C3N4样品的荧光光谱、光电流响应谱以及电化学阻抗谱图。荧光强度能够反映样品中电子空穴对的复合效率,荧光强度越低,样品中载流子的复合效率越低;光电流强度能够反映样品产生光生载流子的能力,光电流强度越高,样品中载流子的生成能力越强;电化学阻抗谱能够反映光生载流子的迁移能力,谱图中的Nyquist 曲线圆弧直径与电荷转移的电阻相对应,直径越小电阻越小,电荷的迁移速率就越快。相较单纯g-C3N4样品,质量分数2.5%Au/g-C3N4样品具有更低的荧光强度、更高的光生电流密度以及更小的Nyquist 曲线圆弧直径,即通过负载Au NPs 能够有效增加光生载流子的产生能力、抑制载流子的复合能力、提高载流子的迁移能力,从而使得复合样品具有更高的光催化性能。

图7 样品的光电性质表征:(a)荧光光谱图,(b)光电流响应谱图,(c)电化学阻抗谱图Fig.7 Photoelectric properties of samples:(a)fluorescence spectra,(b)photocurrent response spectra,(c)electrochemical impedance spectra
3 结论
通过种子介导法合成尺寸均一的Au NPs 纳米颗粒,将其负载于单纯g-C3N4制得一系列不同Au NPs 负载量的Au/g-C3N4复合材料。通过XRD和SEM 对其物相和形貌进行表征,证明Au NPs 成功负载于g-C3N4表面。分别采用UV-Vis 和DRS对Au NPs、g-C3N4和Au/g-C3N4的光学性质进行表征,结果表明Au NPs 的引入能够有效拓宽复合材料的光响应范围。将所得Au/g-C3N4复合材料和g-C3N4用于光催化产氢活性测试,首先对光催化产氢体系中的牺牲剂种类和催化剂用量进行优化,确定最佳光催化产氢测试条件为:以体积分数为20%的TEOA为空穴牺牲剂,催化剂用量为10 mg。Au NPs 的引入能够有效提升复合材料的光催化产氢活性,全光下,随着Au NPs 负载量的增加,光催化产氢活性不断增加;可见光下,2.5%Au/g-C3N4样品具有最优的光催化产氢活性。光电测试结果表明Au NPs 负载能够增强复合材料的光吸收、增加光生载流子的产生和迁移能力,抑制载流子的复合,进而增强复合材料的光催化产氢活性。但过量的Au NPs 负载可能会成为载流子新的复合中心,使得其光催化活性反而降低。

