B等位基因新突变导致B抗原弱表达1例*
李小薇 李慧敏 宁义平 白晓莹 李翠莹
在人类血型系统中ABO血型系统的抗原性最强,是最复杂、最具多态性的血型系统之一,ABO 血型鉴定的准确性直接关系到患者输血治疗的安全[1]。除正常ABO血型外还存在着ABO亚型和受病理、生理等因素影响的ABO正反定型不符的血型表现,部分病例依靠血清学无法准确区分。基因检测方法能够克服以上血型血清学检测局限,结果判断更加客观,逐渐成为准确判断疑难血型必不可少的重要辅助手段[2]。本文分析了1例弱B抗原样本的血清学结果和基因检测结果,报告如下。
对象与方法
1对象 2021年12月就诊于本中心妇产与生殖医学科门诊患者1例。女性,41岁,乙肝患者,诊断阴道出血、贫血等,既往无输血史,送输血科进行血型和不规则抗体筛查。
2仪器与试剂 抗-A、抗-B单克隆抗体(批号:20200912,上海血液生物医药有限责任公司),抗-H抗体(批号:8000258203,荷兰Sanquin公司);ABO反定型细胞(批号:202108002,江苏力博医药生物技术股份有限公司);血型鉴定凝胶卡(批号:202108006,江苏力博医药生物技术股份有限公司);核酸提取试剂(批号:21072810T148,西安天隆科技有限公司)、人类红细胞ABO血型基因分型试剂盒(SSP荧光PCR染料法)(批号:K202106003)、人类红细胞ABO血型-B亚型基因分型试剂盒(SSP荧光PCR染料法)(批号:K210311001)(天津市秀鹏生物技术开发有限公司);dNTP-Buffer工作液(天津市秀鹏生物技术开发有限公司);Taq酶(美国Promage公司)。核酸提取仪NP968-C(西安天隆科技有限公司),基因扩增仪LifeECO(杭州博日科技有限公司),通用型电泳仪JY300C(北京君意东方电泳设备有限公司),测序仪ABI 3130xl(美国ABI公司)。
3方法
3.1ABO血型血清学鉴定:使用微柱凝集法及盐水试管法进行血清学方法的血型鉴定。
3.2DNA提取:按照试剂盒说明书提取血液标本DNA。调整DNA浓度至(30~50)ng/μL、A260/A280值为1.6~2.0。
3.3荧光定量PCR法检测ABO基因:进行ABO基因初筛和B亚型检测。严格按照试剂盒说明书操作。扩增条件如下,运行段:96℃ 2 min;96℃ 20 s,68℃60 s,5组循环;96℃ 20 s,65℃ 50 s,72℃ 45 s,10 组循环;96℃ 20 s,62℃ 50 s、72℃ 45 s,15组循环;72℃延伸 1 min。熔解段:95℃ 15 s,60℃ 1 min,95℃ 15 s,台阶温度1℃,台阶恒温时间20 s。
3.4ABO基因测序:对该例样本,分别进行ABO基因第1~7外显子测序和B基因单链测序,以确定突变位点以及突变点所在基因位置。委托天津秀鹏生物公司根据GENE BANK提供的ABO基因序列信息(NG_006669.1)设计ABO基因第1至第7外显子的扩增引物(表1)以及B等位基因第7外显子的扩增引物(表2),测序引物与扩增引物一致。采用Sanger测序法,将目的片段进行扩增后,测序仪进行测序并读取结果。

表1 ABO基因第1至第7外显子的扩增引物

表2 B等位基因第7外显子的扩增引物
按照以下反应体系对ABO基因的第1至第7外显子,以及B等位基因第7外显子进行单独扩增:dNTPBuffer工作液 43.5 μL,Taq酶(5 units/μL)0.5 μL,特异性引物对(300nM)1.0 μL,DNA 5 μL,总体积50 μL。
反应程序如下:96℃ 2 min;96℃ 20 s,68℃60 s,5组循环;96℃ 20 s,64℃ 50 s,72℃ 90 s,10 组循环;96℃ 20 s,61℃ 50 s、72℃ 90 s,25 组循环;72℃延伸 5 min。扩增产物4℃保存。将扩增完成的产物使用2.5%琼脂糖凝胶进行鉴定,确定产物条带均一且亮度足够后,进行测序。
使用chromespro软件以及DNAMAN8.0软件将测序的.ab1序列与ABO基因参考序列(NG_006669.1)进行人工对比,参比dbRBC数据库(更新日期2017年12月)以及ISBT数据库(Names for ABO(ISBT 001)blood group alleles v1.1 171023)确定基因型。
结果
1ABO血型血清学检测结果 患者红细胞B抗原弱表达,抗-H 4+,同时血清中存在抗-A抗体,无抗-B抗体。4℃加强半小时后检测B抗原3+,仍为弱表达(表3)。

表3 患者ABO血型血清学检测结果
2荧光定量PCR法检测B亚型基因 按照ABO基因初筛试剂盒读板纸判读结果为B/O型,进一步使用B亚型试剂盒检测,按照读板纸判读结果为B/O型。
3ABO基因测序 根据NCBI网站提供的The Blood Group Antigen Gene Mutation Database综合结果判定(以ABO*A1.01为参考序列):该样本ABO基因在ABO*B.01/ABO*O.01.01的基础上,存在外显子7的c.448 T>C的杂合突变(图1A)。结合血清学结果分析,推测该突变可能位于B基因上,导致B抗原减弱。
为了进一步确定杂合突变所在基因,进行B基因单链测序,结果发现该样本第7外显子突变点在ABO*B.01的基础上,多了c.448 T>C的突变,证明突变点位于B基因上,属新的未被数据库收录的B等位基因新突变(图1B)。
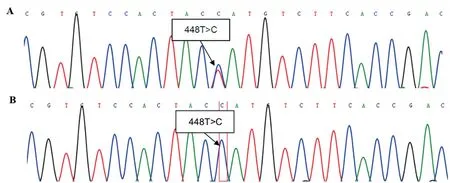
图1 新发现ABO血型等位基因的核苷酸突变
讨论
ABO血型系统中少数人群为ABO亚型,表现为抗原或抗体减弱,导致血清学ABO正反定型不一致,引起血型定型困难,影响临床输血的安全性和有效性。ABO基因编码区共有7个外显子,其中外显子6和外显子7分别编码45、230个氨基酸,是产生ABO亚型的主要基因突变区域,具有明确的血型血清学特点[3]。
本研究中患者血型血清学结果为ABO正定型检出弱B抗原,抗-H结果强凝集4+,反定型检出抗-A,无抗-B(表3),推测为B亚型,随后进行基因分型。B亚型基因分型结果显示患者为B/O型,但考虑到血型血清学检测结果为B抗原减弱,故怀疑存在试剂盒检测范围以外的罕见B亚型或者存在新的基因突变位点,导致B基因编码的氨基酸发生变化,从而使抗原表达减弱[4-6]。因此进行ABO基因外显子1-7测序,结果为ABO*O.01.01/ B-novel(c.448 T>C)(图1A);为进一步判断突变位点所在ABO基因,对B基因外显子7进行单链测序(图1B)。与ABO*B.01基因相比,患者B基因序列中第448位碱基发生了点突变T>C,提示第150号氨基酸由酪氨酸(Tyr)突变成组氨酸(His)。该突变并未被NCBI和dbRBC数据库收录,本文为首次报道;血清学结果导致了B抗原表达减弱,具体机理尚不明确。为了解患者该B变异等位基因的来源,进一步可对其父母及其父母系3代做家系调查。序列已提交NCBI 国际基因数据库(GeneBank),获得登录号“BankIt2613623 BSeq#1 OP254132”,等待确认序列号。
联用血清学和分子生物学检测技术对ABO亚型的准确鉴定具有重要作用[7-9]。本研究提示输血工作人员在进行患者输血前,对于ABO血型正反定型不符的患者有必要联合应用两种方法学进行ABO血型鉴定,最大程度地保障患者临床输血安全,并发现等位基因的新变异[10-12]。利用分子生物学技术可以明确区分ABO血型正反定型不符是ABO亚型,还是受病理、生理等因素影响,明确疑难血型产生的原因。如果患者ABO血型正反定型不符是受病理、生理等因素影响,排除干扰因素后,考虑输注ABO同型血液成分[13-15]。本研究中患者B抗原减弱是由于B等位基因的新突变造成,因同型红细胞获取困难,如需输血,首选自体输血,其次考虑输注交叉配血相合B型或O型红细胞。
利益冲突所有作者均声明不存在利益冲突

