磁共振成像诊断胎盘植入临床价值研究
戴 聪,杜 鑫,王 磊,戴云亮,李 博,刘文源
北部战区总医院 放射诊断科,辽宁 沈阳 110016
胎盘植入属于胎盘植入性疾病(placenta accreta spectrum disorders,PAS)的一种分型,是指分娩时胎盘部分或完全滞留的一种异常胎盘形态,包括胎盘粘连、胎盘植入以及穿透性胎盘植入等[1-4]。有研究显示,全球PAS 的发病率正逐年上升[1-2]。PAS 是妊娠期极度危险的情况之一,因其与孕产妇病死率密切相关[3]。然而大部分患PAS 的孕产妇在整个孕期无明显症状,其在分娩时存在较大的发病风险,有时会产生不可逆转的后果,特别是在无法立即提供相应临床所需条件及设施的地区[5-6]。因此,准确的诊断对于应对策略的选择至关重要[7]。但PAS 在大多数情况下无典型的临床症状和体征,实验室指标也相对缺乏特异性,因此其在产前诊断较困难[8]。目前,对PAS 的产前诊断主要依靠影像学检查,其中超声检查通常被作为主要方式,而产前MRI 检查作为超声检查的补充,特别是在超声不能确定的情况下,或需要评估胎盘对子宫侵犯深度和范围时[9]。本研究旨在探讨MRI 在PAS 诊治中的应用价值。现报道如下。
1 资料与方法
1.1 一般资料 选取北部战区总医院自2017 年8 月至2021 年12 月收治的4 例PI 患者为研究对象。本组患者年龄31~41 岁,平均年龄(35.00±4.32)岁;其中,2 例为第3 次怀孕,之前均经历人工流产及剖宫产(患者1,35 岁;患者2,41 岁);1 例无特殊病史(患者3,33 岁);另1 例在我院行一代试管,因胎膜早破、难免流产入院接受治疗,同时患有慢性高血压(患者4,31 岁)。所有患者均行MRI 检查。本研究经医院伦理委员会审批通过,所有患者及家属均签署知情同意书。
1.2 研究方法 患者入院后均接受常规检查及分娩后静脉血栓栓塞症的危险因素评分,未提示异常;同时MRI 检查结果提示胎盘植入(placenta increta,PI)。患者1 入院后静滴催产素并行人工破膜术,自然分娩,胎儿娩出后15 min,胎盘未娩出并无剥离征象,同时阴道大量活动性出血,于是给予按摩子宫,缩宫素10 U、卡贝缩宫素100 μg 静脉滴注,卡孕栓1 mg 口含,欣母沛2 ml、地塞米松10 mg 肌注,葡萄糖酸钙10 ml 静脉滴注。行手取胎盘术,发现胎盘与宫壁组织粘连致密,剥离出大部分破碎胎盘,并考虑胎盘残留约1/4;因阴道活动性出血多,行宫腔球囊压迫止血术及保守治疗(介入子宫动脉栓塞术)。其过程中输注红细胞悬液6.6 U、冰冻血浆1 000 ml。患者2 行剖宫取胎术,取耻骨上横切口,剔除瘢痕组织,逐层切开腹腔,见子宫右侧宫角呈紫蓝色改变,娩出胎儿后见胎盘致密粘连于子宫前壁及右侧壁,给予钝性分离胎盘。常规缝合子宫,查无活动性出血,逐层关腹。患者3 自然分娩,胎儿娩出后15 min,胎盘未娩出并无剥离征象,同时阴道持续流血,遂行手取胎盘术,探查宫腔可扪及胎盘,位于子宫宫底及子宫后壁,与宫壁致密粘连,手剥胎盘取出部分胎盘组织。患者4 因难免流产引产两完整死婴,胎盘胎膜未自然娩出,行手取胎盘术,其一胎盘组织剥离成功,另一胎盘完全残留,遂于超声引导下行清宫术,清宫术过程中见胎盘粘连严重,后行经皮子宫动脉造影、栓塞术,术后进行多次输血治疗,输注红细胞悬液6 U、冰冻血浆410 ml。
1.3 观察指标 记录各患者MRI 诊断结果,对所提示的PI 发生位置、病变范围、邻近子宫壁所发生的改变、对盆腔内周围组织的影响等与手术过程中子宫、胎盘及其他组织所见进行对比。
1.4 统计学方法 采用SPSS 26.0 软件对数据进行统计学分析。计量资料以均数±标准差()表示,组间比较采用t检验;计数资料以例(百分率)表示,组间比较采用χ2检验。以P<0.05 为差异有统计学意义。
2 结果
患者1 盆腔MRI 检查提示,子宫下段见斑片状不均匀稍长T2 信号胎盘影像,其内可见条状低信号及迂曲留空血管影,子宫与胎盘间低信号带显示不清,相应部位子宫壁变薄、浆膜未见侵袭,考虑PI。见图1。患者2 盆腔MRI 检查提示,胎盘呈等及稍长T2 信号,大部分覆盖于子宫右前壁,未达宫颈内口,其内可见条状低信号,子宫右侧壁及前壁局部胎盘-肌层交界面连续性中断、显示不清,考虑PI。见图2。患者3 盆腔MRI 检查提示,子宫后壁不均匀增厚、T2WI 呈稍高信号,部分区域接近于浆膜层,胎盘-肌层交界面连续性中断、显示不清,考虑PI。见图3。患者4 MRI 提示,子宫宫底、前壁及后壁上部T2WI 均可见片状稍高信号,与菲薄肌层分界不清,部分区域接近于浆膜层,前壁可见团块状混杂信号以及多发条状低信号影,宫腔及宫颈内见不规则低信号,子宫与盆腔周围结构分界尚清,考虑PI。见图4。4 例患者的PI 诊断均在手术过程中被证实,与MRI 诊断提示的位置、范围、邻近子宫壁改变等也有较高一致性;同时,根据MRI 显示的子宫损伤程度、周围组织是否受侵等,4 例患者均选择了保留子宫的保守治疗。

图1 患者1盆腔MRI图像[子宫下段见斑片状不均匀稍长T2信号胎盘影像,其内可见条状低信号(黑箭头)及迂曲留空血管影,子宫与胎盘间低信号带显示不清(白箭头),相应部位子宫壁变薄、浆膜未见侵袭,考虑PI]
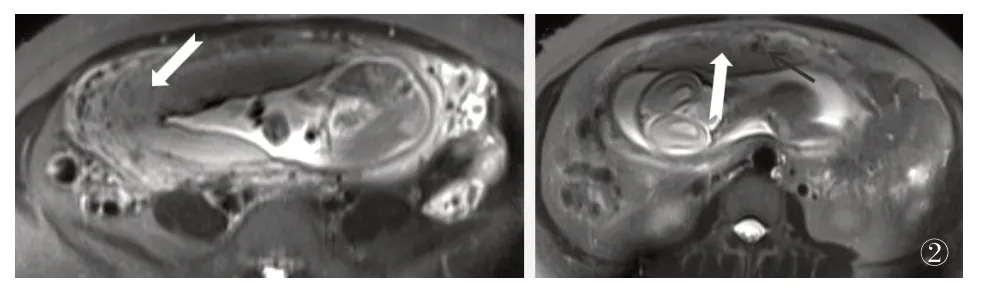
图2 患者2盆腔MRI图像[胎盘呈等及稍长T2信号,大部分覆盖于子宫右前壁,未达宫颈内口,其内可见条状低信号(黑箭),子宫右侧壁及前壁局部胎盘-肌层交界面连续性中断、显示不清(白箭),考虑PI]

图3 患者3盆腔MRI图像[子宫后壁不均匀增厚、T2WI呈稍高信号,部分区域接近于浆膜层,胎盘-肌层交界面连续性中断、显示不清(白箭),考虑PI]图4 患者4盆腔MRI图像[子宫宫底、前壁及后壁上部T2WI均可见片状稍高信号,与菲薄肌层分界不清(白箭),部分区域接近于浆膜层,前壁可见团块状混杂信号,并可见多发条状低信号影,宫腔及宫颈内可见不规则低信号,子宫与盆腔周围结构分界尚清,考虑PI]
3 讨论
PAS 的成因目前尚无定论,一般认为,侵入性胎盘与子宫内膜异常有关,通常是由剖腹产或其他子宫手术形成的瘢痕造成[1,3,10]。然而,这仅能提示该疾病的好发人群,并不能解释无子宫手术史或植入装置的未产妇PAS 的发生[10]。PAS 较常见的风险因素是既往剖宫产史,其发病率随剖宫产经历的增加而增加[10]。其次,前置胎盘是发生PAS 的另一重要危险因素[10]。其他危险因素还包括多胎次、体外受精、既往子宫手术或刮宫、Asherman 综合征和曾经确诊PAS 等[1,3]。尽管很多患者存在相关危险因素,但还会有部分患者未在产前确诊,致使PAS 的发病率和病死率大幅增加[2]。PAS 诊断主要依据高危因素、症状体征及辅助检查,但PI 患者的临床症状和体征在分娩前较少见,发生于子宫体部的患者产前常无明显临床表现,合并前置胎盘或子宫破裂的患者可有产前阴道流血或腹痛以及胎心率的变化[11]。因此,依靠影像学检查结果和病史是诊断PAS 的重要方法,确诊需根据术中或分娩时所见,亦或娩后的病理学诊断[2,11]。
超声可用于筛查和诊断PAS,也是诊断瘢痕妊娠和前置胎盘的主要方式[5,12]。较具提示性作用的征象是前置胎盘,常表现为胎盘内多个血管陷窝、胎盘与肌层之间正常低回声区缺失、胎盘下肌层厚度变薄(厚度<1 mm)等[10,13]。然而,有研究提示了PAS 不同超声征象相当大的可变性[3]。超声诊断的有效性取决于对临床危险因素、成像方式和质量、临床经验等的综合衡量,在准确评估PAS 类型和胎盘绒毛侵袭程度方面的价值也是有限的,这时需要MRI 检查进行补充[5,13-14]。MRI 已被推荐作为诊断PAS 的二线成像工具。在某些情况下,MRI 可以克服与超声诊断PAS 相关的技术局限[3]。MRI 检查多用于评估发生于子宫后壁的PAS、胎盘侵入子宫肌层深度及宫旁组织与膀胱受累程度[5,14-15]。MRI 在PAS 的诊断中具有较高的敏感性和特异性,允许不同医师离线重新评估[3]。PAS 相关的MRI 影像特征包括:T2 加权成像胎盘内出现低信号暗带、胎盘或子宫异常膨出、胎盘床血管异常、T2 加权成像子宫与胎盘间低信号带消失、胎盘植入部位子宫肌层变薄或缺失、局部外生团块以及侵及膀胱或周围脏器[2,10,14]。本研究中,患者MRI 检查图像呈现多个PAS 相关特征,并与后续的术中所见吻合。
产前对PAS 程度进行正确评估,可提供优化管理和结果的机会[10]。因为胎盘浸润深度是影响产妇预后的主要因素之一,PAS 处理不当可引起多种严重并发症[1]。目前,较普遍的处理方法是将胎盘在胎儿娩出后留在原位,再进行子宫切除术,手术方法的调整和预测围术期并发症需要MRI 来评估胎盘侵犯的深度和形态[9]。同时,PAS 的准确产前诊断也使保守治疗成为可替代方案,其中子宫动脉栓塞与甲氨蝶呤的适度使用现已受到医疗机构广泛认可。在本研究中,研究对象均选择了保守治疗,随访显示治疗效果及预后也令人满意。
综上所述,PAS 诊疗的关键在于产前的准确诊断,需要对具有危险因素的患者进行严密的影像学筛查。MRI作为超声检查的补充,可提供PI 发生位置、范围、邻近子宫壁的改变、对盆腔周围组织的影响等与手术结论有较高一致性的信息,对诊疗计划的制定和完善具有极高的应用价值。

