焙烧温度对Cu/SiO2纳米管催化剂催化草酸二甲酯加氢制乙醇酸甲酯性能的影响
王 征,武朦朦,宋有为,赵金仙,任 军
(太原理工大学 省部共建煤基能源清洁高效利用国家重点实验室,煤科学与技术教育部重点实验室,山西 太原 030024)
随着“禁塑令”的颁发,生物可降解材料聚乙醇酸的需求急剧上升,乙醇酸甲酯(MG)作为其生产原料备受关注[1]。目前制备MG的方法主要包括:氯乙酸水解法[2]、甲酸甲酯与甲醛偶联法[3]和甲醛与氢氰酸加成法[4]等,但这些方法存在污染严重和腐蚀性强等问题。与上述方法相比,草酸二甲酯(DMO)选择性加氢制备MG反应条件温和、原子利用率高且环境友好,是一条绿色经济的生产路线[5]。
在DMO选择性加氢制MG的反应中,常用催化剂为Ag基催化剂和Cu基催化剂[6]。然而Ag基催化剂的高成本限制了其工业化应用,Cu基催化剂由于其良好的C=O键加氢能力成为研究热点,但存在Cu粒子易发生聚集而导致其活性下降以及过度加氢生成乙二醇的问题[7-8],现有研究通过引入Ag[9]和Au[10]等贵金属助剂来提高其反应活性及稳定性。研究[11]表明,载体与活性金属间的强相互作用也能够稳定金属粒子,提高活性金属的分散度。页硅酸铜是一种具有特殊层状结构的Cu/SiO2前驱体,由CuO6和SiO4的三明治夹心结构组成,Si与Cu之间以Cu—O—Si键连接[12]。DING等[13]发现页硅酸铜中独特的Cu—O—Si能够形成强金属-载体相互作用,稳定结构中的Cu,防止其迁移聚集。TOUPANCE等[14]提出以页硅酸铜为前驱体制得的催化剂的Cu颗粒尺寸在3 nm左右,有利于提高反应活性。此外,Cu物种的价态是影响DMO选择性加氢反应产物分布的另一个重要因素。原位红外实验与密度泛函理论计算证实,对于DMO选择性加氢制MG反应,Cu0解离H2,Cu+解离DMO并稳定中间体甲氧基和酰基[15]。页硅酸铜经过焙烧后形成两种Cu物种:表面高度分散的CuO和页硅酸铜的Cu—O—Si结构。两种Cu物种经还原后分别得到Cu0和Cu+[16],是调节Cu物种价态的有效途径[17]。
本文以PEO-PPO-PEO三嵌段共聚物(P123)为结构导向剂,硝酸铜为铜源,硅溶胶为硅源,氨水为沉淀剂和络合剂,采用水热法制备了管状页硅酸铜前驱体,经还原后得到高度分散的Cu/SiO2纳米管催化剂,并将其用于催化DMO选择性加氢反应。通过实验与表征分析,系统研究了焙烧温度对催化剂结构和Cu物种分散度及价态分布的影响,探究了催化剂与DMO选择性加氢制MG反应的构效关系。
1 实验部分
1.1 实验试剂
硝酸铜、P123,AR,阿拉丁试剂有限公司;氨水,25%~28%,国药集团化学试剂有限公司;JN-30硅溶胶,青岛基亿达硅胶试剂有限公司。
1.2 催化剂制备
采用水热法合成Cu/SiO2纳米管催化剂。将1.00 g模板剂P123 溶解于 100 mL去离子水中,再加入 11.29 g Cu(NO3)2·3H2O,使用氨水调节pH值为10~11,加入30%(质量分数)的硅溶胶,室温下搅拌两小时后升温至90 ℃保持30 min,然后转移到水热釜中,密封后加热至200 ℃反应24 h。自然冷却至室温后,过滤,反复水洗得到固体,在100 ℃干燥12 h。在马弗炉中焙烧得到催化剂前驱体,记为CuPSNT-x(x代表焙烧温度)。催化剂前驱体在300 ℃纯H2气氛中还原4 h,得到Cu/SiO2纳米管催化剂,记为Cu/SNT-x。
1.3 催化剂表征
N2吸/脱附采用贝士德3H-2000PS2型物理吸附仪测定。取100 mg样品在氦气下180 ℃预处理3 h,在-196 ℃下测试其吸/脱附等温线。样品的比表面积和孔径分布分别采用BET和BJH法计算。
XRD采用D/Max-2500型X射线衍射仪测定,扫描速度为 8 (°)/min,电压为 40 kV,电流为 100 mA。
FT-IR谱图在Bruker vertex70型红外光谱仪上测定,扫描范围为 400~4000 cm-1。
样品的形貌结构及颗粒尺寸采用日本株式会社的JEM 2100F场发射透射电镜测定。将催化剂在乙醇中超声分散后滴在Cu网上,自然晾干后观察其形貌。
程序升温还原(H2-TPR)采用先权TP-5080型吸附仪测定。取50 mg催化剂前驱体装入管中,通入Ar预处理 30 min后,通入H2/Ar混合气,升温至
900 ℃进行还原。
H2-N2O滴定在先权TP-5080型吸附仪上测定。取50 mg催化剂前驱体装入管中,以10 ℃/min升温至350 ℃,在H2/Ar混合气下还原样品,此次H2消耗量记为X(mol)。降温至 50 ℃,通入N2O-Ar混合气进行氧化。随后再次切换至H2/Ar,升温至900oC,对样品进行还原,此次H2消耗量记为Y(mol)。Cu物种分散度(dCu,%)计算公式如式(1)。

Cu原子表面的平均面积为0.0711 nm2,相当于每平方米 1.4 × 1019个Cu原子,因此Cu活性比表面积计算公式如下:
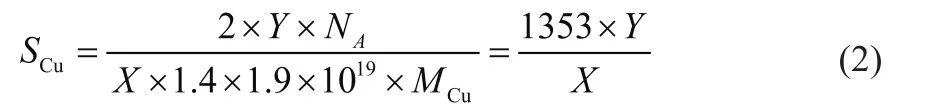
式中,SCu为Cu活性比表面积,m2/g;NA为阿伏伽德罗常数,6.02 × 1023;MCu为Cu相对原子质量,64.0 g/mol。
XPS谱图在AXIS ULTRA DLD型X射线光电子能谱仪上测定。以Al Kα为射线源,电子结合能采用C 1s峰(284.6 eV)进行校正,并采用XPS PEAK软件对数据进行分峰拟合。
1.4 催化剂活性评价
在固定床反应器中测试催化剂的DMO选择性加氢性能。将0.30 g催化剂与3.00 g石英砂均匀混合后装入长度为450 mm、管径为8 mm的反应管中。DMO溶液(质量分数为15%)经过预热汽化后与H2混合进入反应管,反应温度为210 ℃,n(H2)/n(DMO)为 100,压力为 2.0 MPa。产物经过冷凝后收集液体部分,使用DB-624毛细管柱和氢火焰离子化检测器进行分离检测。
DMO转化率、MG选择性、乙二醇(EG)选择性、乙醇(EtOH)选择性以及其他产物的选择性(包括甲酸甲酯、乙二醇甲醚、1,2-丙二醇和1,2-丁二醇)计算公式如下:
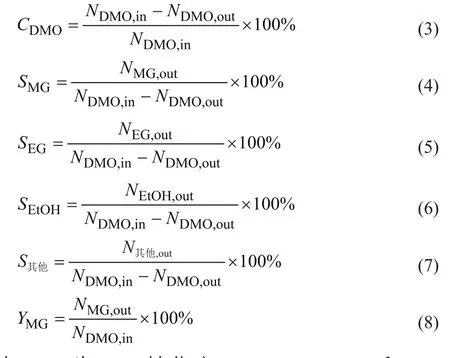
式中,CDMO为DMO转化率,%;SMG、SEG、SEtOH和S其他为MG、EG、EtOH和其他产物的选择性,%;YMG为MG的收率,%;NDMO,in和NDMO,out分别为进口和出口DMO的 物 质 的 量,mol;NMG,out、NEG,out、NEtOH,out和N其他,out分别为产物中MG、EG、EtOH和其他产物的物质的量,mol。
2 结果与讨论
2.1 催化剂织构性质分析
图1和图2分别为不同焙烧温度下CuPSNT-x和 Cu/SNT-x的N2吸/脱附等温线及孔径分布曲线。由图1(a)可知,所有样品均为典型的IV型等温线,在低压段(p/p0< 0.05),N2吸附量急剧增加,说明样品中存在微孔结构,随着p/p0增加到0.80~1.00时,出现典型的圆柱型孔回滞环,与催化剂的纳米管结构相对应。由图1(b)可知,所有样品均为双介孔分布,孔径主要分布在 2~4 nm和 9~17 nm,同时含有少量微孔和大孔结构。图2(a)显示Cu/SNT-x的等温线和回滞环与CuPSNT-x相似,说明催化剂保持了管状结构。图2(b)表明催化剂还原后孔径分布有所变化,主要分布在 2~3 nm和 9~16 nm,并且低孔径的比例明显降低。
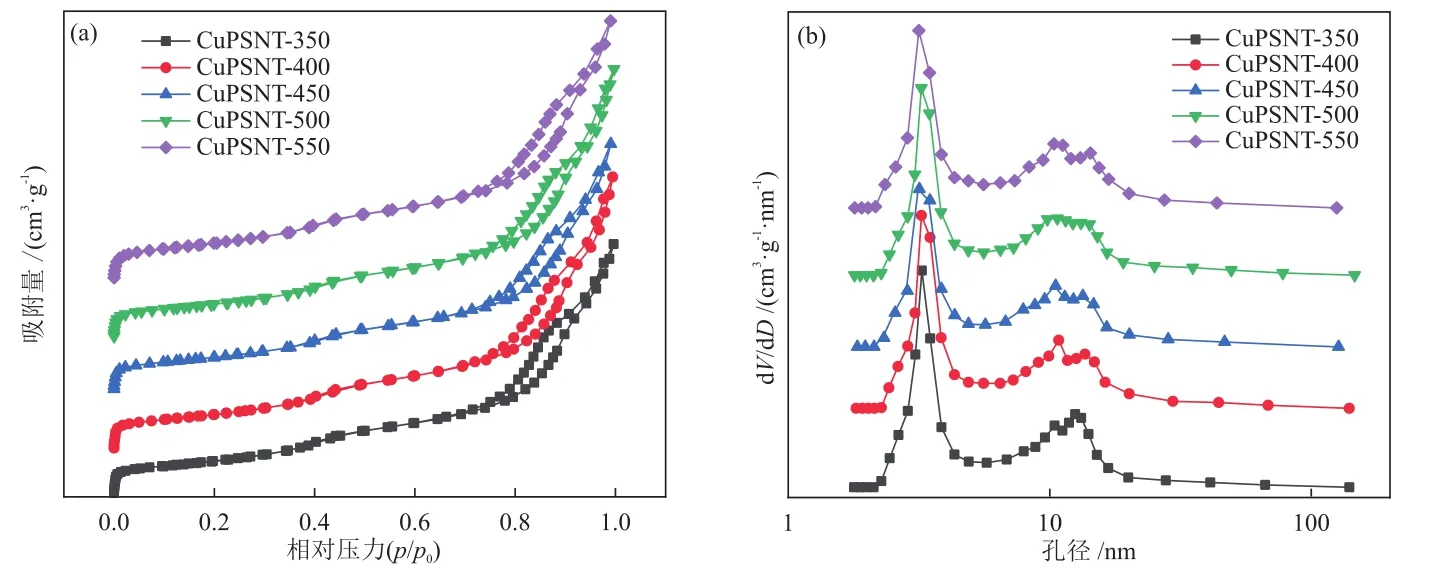
图1 CuPSNT-x的N2吸/脱附等温线(a)和孔径分布曲线(b)Fig.1 N2 adsorption/desorption isotherms (a) and pore-size distribution (b) of CuPSNT-x
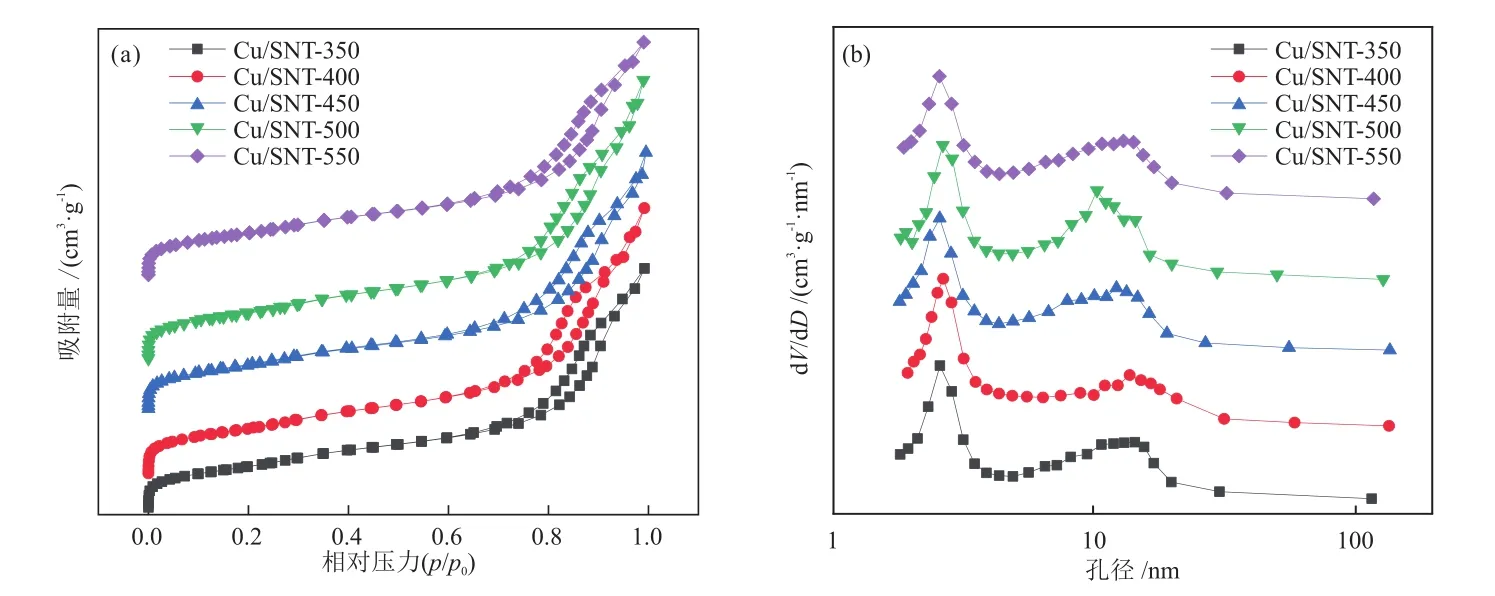
图2 Cu/SNT-x的N2吸/脱附等温线(a)和孔径分布曲线(b)Fig.2 N2 adsorption/desorption isotherms (a) and pore-size distribution (b) of Cu/SNT-x
表1展示了不同催化剂的比表面积、孔体积、孔径、Cu负载量(质量分数,下同)、Cu物种分散度、Cu活性比表面积、Cu0活性比表面积以及Cu+活性比表面积。由表1可知,Cu/SNT-x中Cu负载量接近于理论负载量35%。CuPSNT-x的比表面积随着焙烧温度的升高先升高后降低,还原后Cu/SNT-x的比表面积和孔径略微减小,可能是由于层间距的收缩导致[13],但变化趋势并未改变,Cu/SNT-450的比表面积最大为482.12 m2/g。随着焙烧温度的升高,Cu物种分散度先增加后减少。当焙烧温度为450 ℃时,Cu物种分散度和活性比表面积达到最高,分别为43.08%和291.46 m2/g,与比表面积的变化趋势相同。
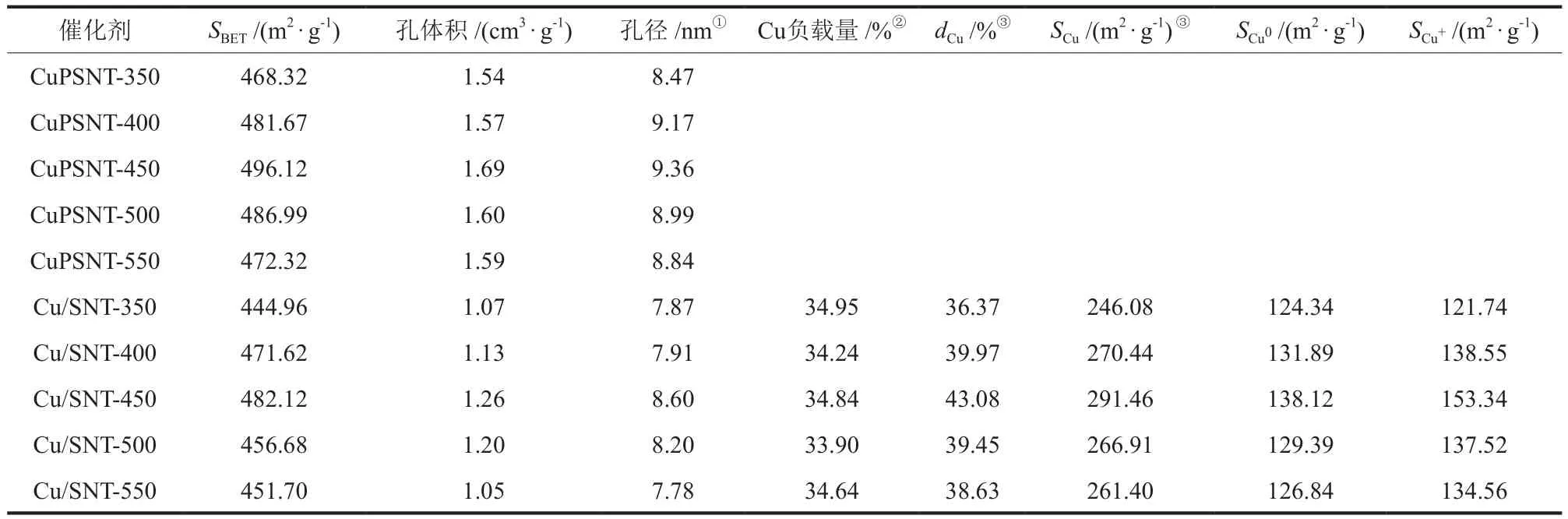
表1 不同催化剂的织构参数Table 1 Texture structure properties of different catalysts
2.2 催化剂物相分析
图3为CuPSNT-x和Cu/SNT-x的XRD谱图。CuPSNT-x在 2θ= 19.9°、21.8°、30.8°、35.0°、57.5°和62.4°的衍射峰归属于Cu2-aSi2O5(OH)3·aH2O (JCPDS No.27—0188)[18],2θ= 35.5°、38.7°、48.6°和 61.3°处衍 射 峰 则 归 属 于CuO(JCPDS No.48—1548)[16]。随着焙烧温度的升高,CuO的衍射峰增强,表明高的焙烧温度有利于CuO的形成,这可能是因为温度过高,导致Cu物种的聚集。Cu/SNT-x催化剂在2θ=21.6°有一个宽扁的包峰,归属于无定形SiO2的特征峰,2θ= 36.4°、42.3°和 61.3°处的衍射峰分别归属于Cu2O(JCPDS No.05—0667)的(111)、(200)和(220)晶面,2θ= 43.3°、50.4°和 74.1°处的衍射峰归属于Cu(JCPDS No.04—0836)的(111)、(200)和(220)晶面[19],表明还原后催化剂以Cu0和Cu+两种物种形式存在[20]。
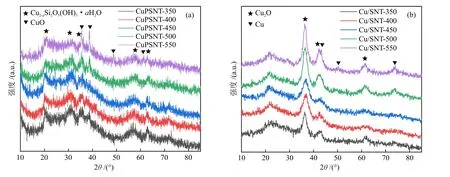
图3 CuPSNT-x (a)和Cu/SNT-x (b)的XRD谱图Fig.3 XRD patterns of CuPSNT-x (a) and Cu/SNT-x (b)
2.3 催化剂FT-IR表征
图4为CuPSNT-x的FT-IR谱图。位于470 cm-1和800 cm-1处的峰归属于SiO2中Si—O的弯曲振动和对称伸缩振动峰[21],1639 cm-1处的峰归属于吸附水的H—O—H的弯曲振动峰,3449 cm-1处的宽峰归属于水的—OH反对称伸缩振动[22]。670 cm-1和1040 cm-1处的峰分别属于页硅酸铜中的δOH振动峰和νSiO振动峰[23],表明催化剂前驱体中页硅酸铜的存在,这与XRD结果一致。页硅酸铜的形成表明Cu插入到硅载体的框架中,以Si—O—Cu的形式相互连接,形成了较强的金属-载体相互作用[24],提高了活性金属的分散度,减小了金属颗粒尺寸,进而提升了催化活性[25]。
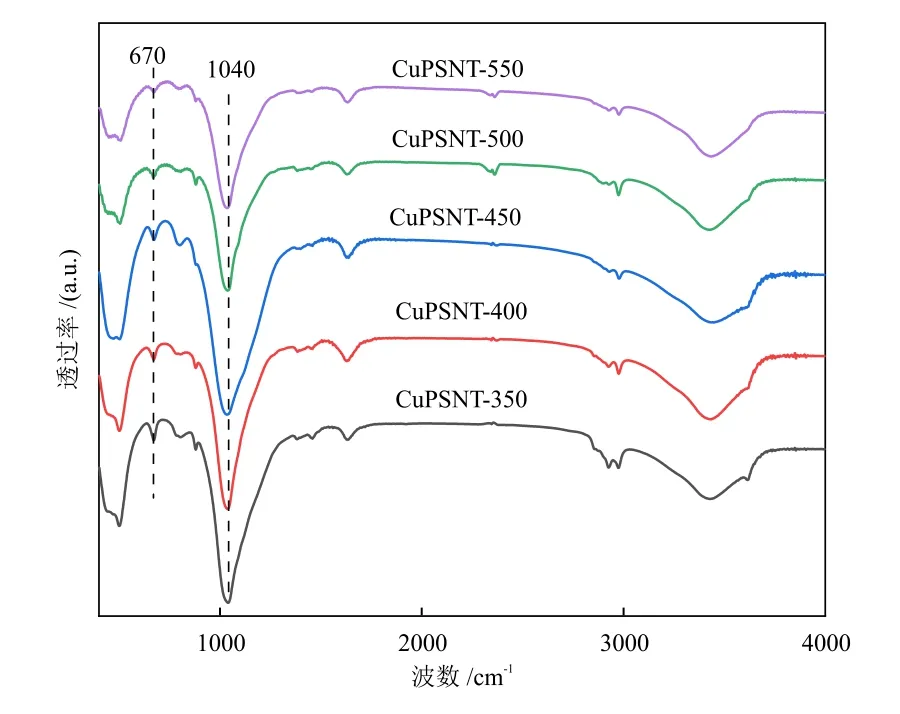
图4 CuPSNT-x的FT-IR谱图Fig.4 FT-IR spectra of CuPSNT-x
2.4 催化剂形貌分析
图5为Cu/SNT-x催化剂的TEM谱图和Cu粒径分布直方图。由图5可知,Cu/SNT-x催化剂为直径为10 nm左右的管状结构,Cu纳米颗粒均匀地分散在纳米管上。嵌在纳米管壁上的Cu纳米颗粒使纳米管直径变窄,这与还原后N2吸/脱附孔径变小一致[26]。通过随机测量200个Cu颗粒的尺寸,发现所有催化剂的平均Cu颗粒尺寸(Daverage)均小于5 nm,这得益于催化剂的大比表面积和金属-载体相互作用[14]。Cu颗粒尺寸随着焙烧温度的升高而增大,这可能是由于温度升高导致Cu颗粒聚集。
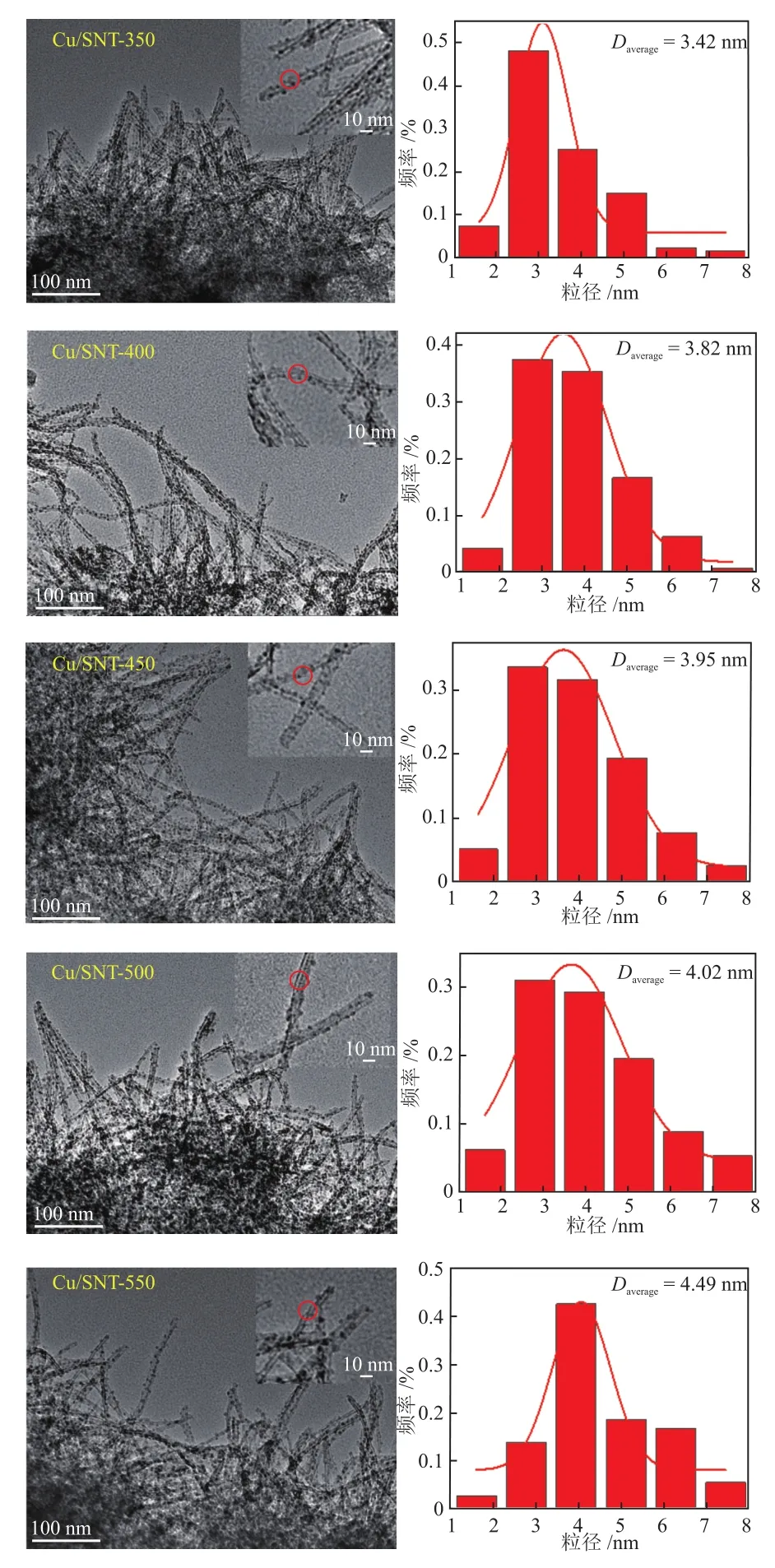
图5 Cu/SNT-x的TEM谱图和Cu粒径分布直方图Fig.5 TEM spectra and Cu particle size distribution histograms of Cu/SNT-x
2.5 催化剂H2-TPR表征
图6为CuPSNT-x的H2-TPR谱图。由图6可知,Cu物种的还原峰随着焙烧温度的升高向低温方向偏移。焙烧温度为350~500 ℃时,CuPSNT-x在300 ℃左右出现一个对称还原峰。分散良好的CuO还原为Cu0,与页硅酸铜还原为Cu+的还原峰位重合,表明催化剂中的Cu物种分散度较高[27]。而当焙烧温度上升到550 ℃时,还原峰变为双峰,主要的还原峰向低温方向移动至240 ℃处,在300 ℃左右出现一个肩峰,分别归因于CuO和页硅酸铜Cu—O—Si中Cu物种的还原。HUANG等[28]发现纯CuO的还原峰在233 ℃处,因此,CuPSNT-550催化剂中有大量与载体呈现弱相互作用的CuO存在,与XRD结果一致。
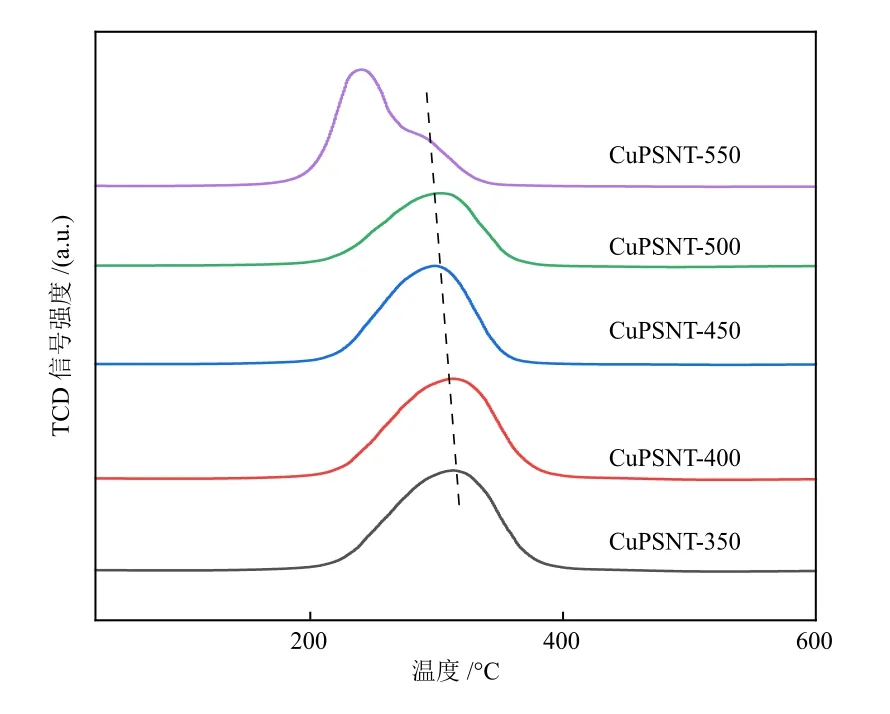
图6 CuPSNT-x的H2-TPR谱图Fig.6 H2-TPR patterns of CuPSNT-x
2.6 催化剂表面元素价态分析
采用XPS表征Cu/SNT-x表面的Cu物种的化学价态。由图7(a)可知,在932.43 eV处的强峰归属于Cu0+ Cu+,说明Cu/SNT-x催化剂中Cu物种主要以Cu0+ Cu+的形式存在。在结合能为 935.17 eV处出现了较弱的Cu2+峰,伴随着944.22 eV的Cu2+的卫星峰,表明催化剂中存在少量CuO,而还原后样品的XRD中未出现CuO的衍射峰,可能是由于CuO的含量太少。通过分峰拟合得出Cu2+含量(物质的量分数,下同)均小于15%(表2)。为了区分Cu0和Cu+,对Cu物种进行Cu LMM表征。由图7(b)可以观察到 3 个峰:916.36 eV处的峰归属于Cu0,912.24 eV处的峰归属于Cu+,914.08 eV处的峰归属于Cu2+[29-30]。从表2中可以看出,Cu/SNT-350中Cu0含量(物质的量分数,下同)最高,而Cu/SNT-450的Cu+含量最高。
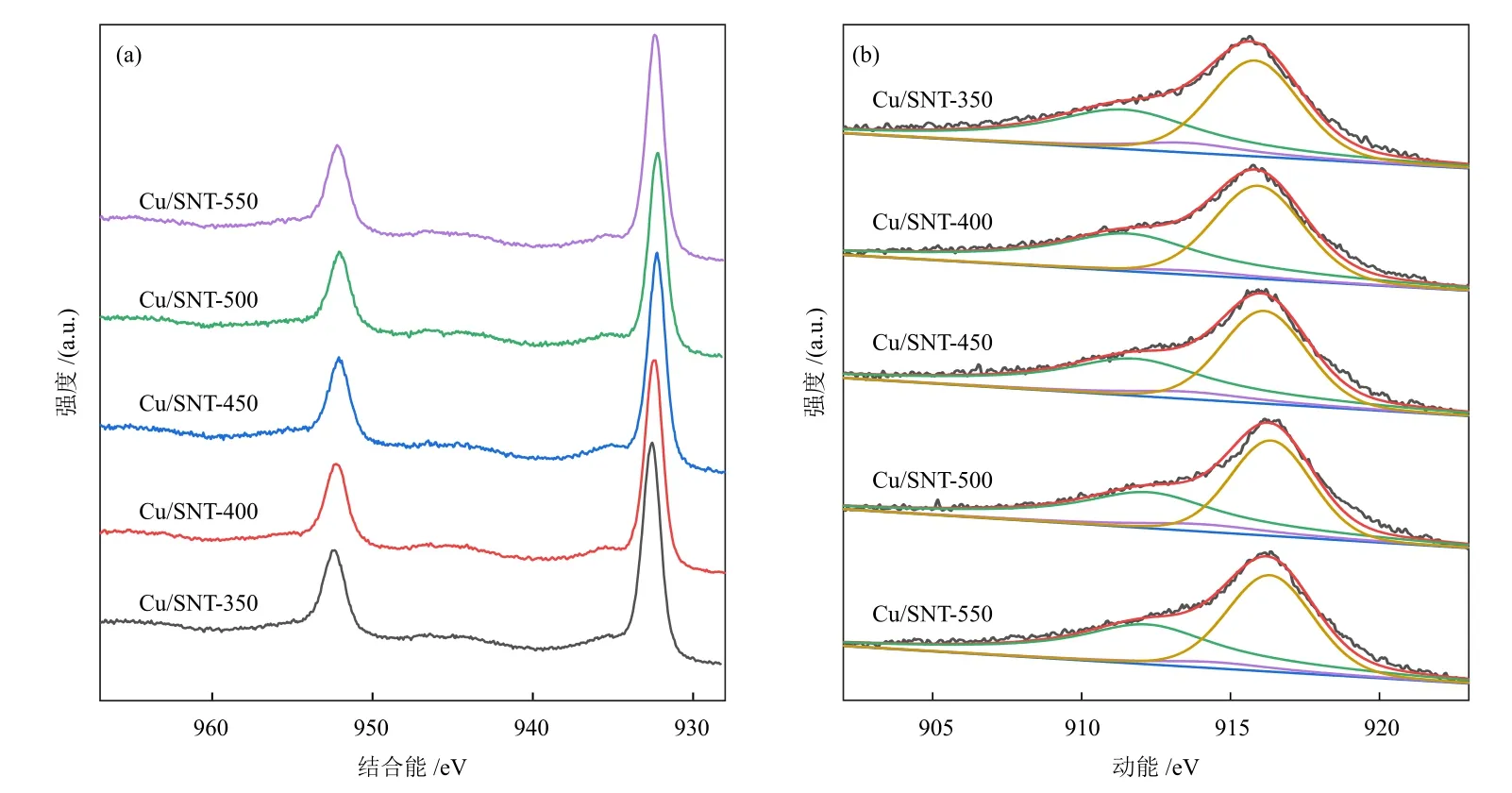
图7 Cu/SNT-x的Cu 2p XPS谱图(a)和Cu LMM Auger谱图(b)Fig.7 Cu 2p XPS spectra (a) and Cu LMM Auger spectra (b) of Cu/SNT-x
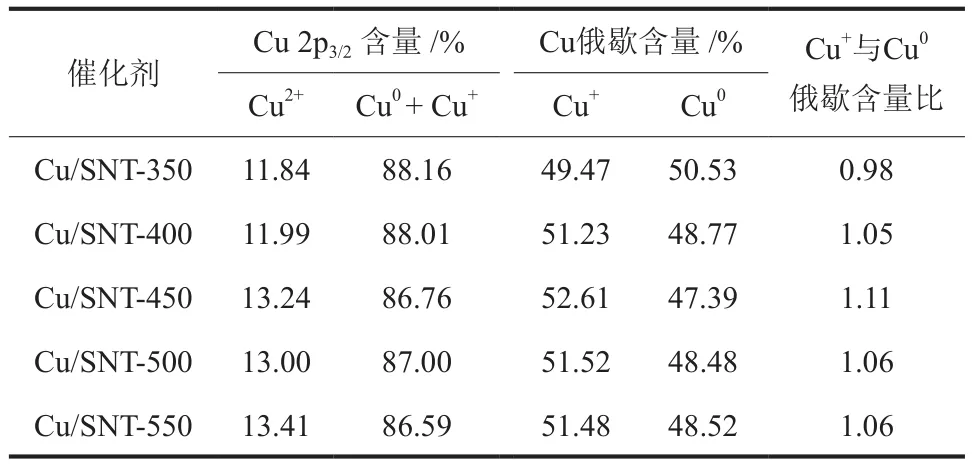
表2 Cu/SNT-x催化剂表面Cu物种含量Table 2 Content of Cu species on surface of Cu/SNT-x catalysts
2.7 催化剂活性及稳定性评价
在t= 210 ℃、p= 2 MPa、n(H2)/n(DMO) = 100,质量空速(WHSV) = 0.839 h-1的条件下,对不同焙烧温度下的催化剂进行了活性评价,结果如图8所示。DMO转化率与焙烧温度呈火山型曲线,随着焙烧温度的升高,DMO转化率先增加后降低,当焙烧温度为450 ℃时,DMO转化率最高为91.50%。MG选择性随着焙烧温度的上升呈下降趋势,Cu/SNT-350表现出最高的MG选择性,为82.24%,继续升高焙烧温度,MG选择性基本不变,约为62.00%。EG的选择性随焙烧温度的升高先升高后基本不变。乙醇的选择性稳定在1%左右,其它产物包括甲酸甲酯、碳酸二甲酯、乙二醇甲醚、1,2-丙二醇和1,2丁二醇,总选择性稳定在5%左右。MG收率与DMO转化率变化趋势类似,与焙烧温度呈现火山型曲线。
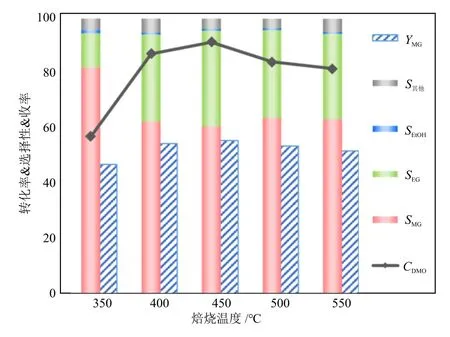
图8 Cu/SNT-x的活性评价Fig.8 Catalytic performance of Cu/SNT-x
结合表征结果发现,Cu的微观结构、理化性质和分散度受到了CuPSNT-x焙烧温度的影响。适宜的焙烧温度有利于提高催化剂的比表面积,进而提升Cu物种分散度及Cu+活性比表面积。研究[15]表明,DMO选择性加氢反应中,Cu0活性中心吸附解离H2,Cu+活性中心吸附解离DMO分子,并且DMO分子的活化是该反应的速控步骤。H2-N2O及XPS表征结果证实Cu/SNT-450具有最高的Cu+活性比表面积,因此,其MG收率最高,催化活性最好。但焙烧温度过高则会降低催化剂比表面积以及Cu+活性比表面积,导致催化活性降低。而Cu/SNT-350催化剂表现出最高的MG选择性,这可能是由于该催化剂中Cu物种活性比表面积小,活性中心较少[7]。
稳定性评价对于催化剂工业化应用至关重要。在t= 210 ℃、p= 2 MPa、n(H2)/n(DMO) =100,WHSV= 0.839 h-1的条件下,对Cu/SNT-450 进行了250 h的长期活性评价,实验结果如图9所示。在120 h之前DMO转化率稳定在90%左右,随着反应时间的延长,DMO转化率开始缓慢下降至80%左右,随后保持稳定。然而MG选择性则随着时间的延长缓慢上升至73%左右,然后保持稳定。MG收率则保持在58%左右,无明显降低,表明Cu/SNT-450具有优异的稳定性。
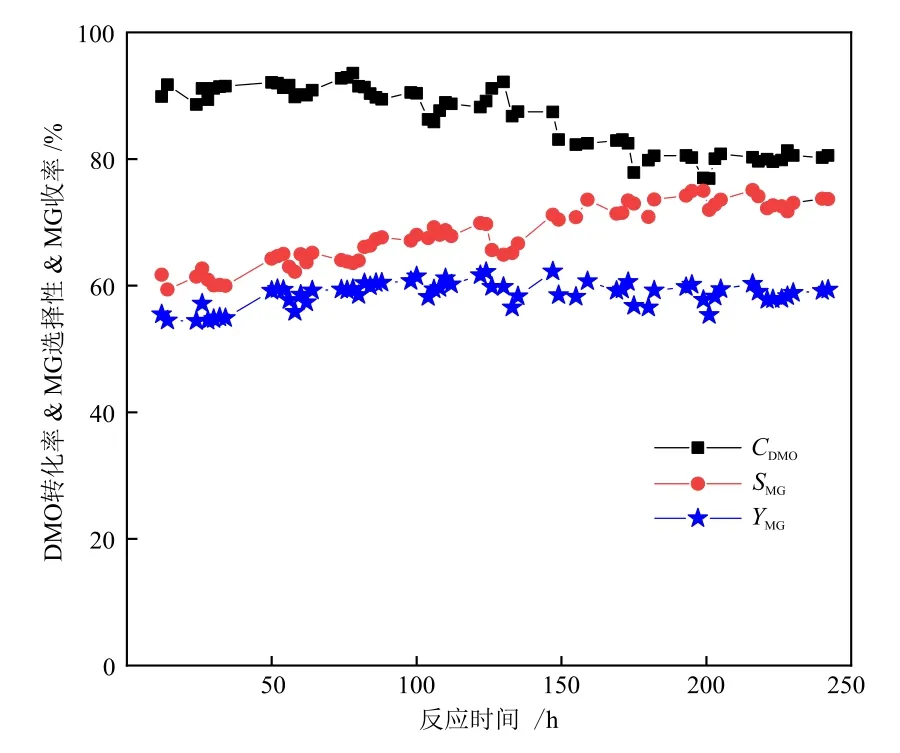
图9 Cu/SNT-450的稳定性评价Fig.9 Stability evaluation of Cu/SNT-450
3 结论
本文通过水热法合成了管状页硅酸铜前驱体,经还原得到高负载量的Cu/SiO2纳米管催化剂,探究了焙烧温度对Cu/SiO2纳米管催化剂的结构及性能的影响,得到如下结论。
(1)焙烧温度对Cu/SiO2纳米管催化剂的Cu物种分散度、活性比表面积和Cu颗粒尺寸有显著影响。随着焙烧温度的升高,Cu物种分散度及活性比表面积先升高后降低,Cu颗粒尺寸随着焙烧温度的升高逐渐增大。
(2)在t= 210 ℃、p= 2 MPa、n(H2)/n(DMO) = 100以及WHSV= 0.839 h-1的条件下,Cu/SNT-450 催化剂的活性最优,DMO转化率为91.50%,MG选择性为60.82%,且在250 h的长期评价中MG收率无明显降低,表现出优异的稳定性。
(3)催化剂的加氢活性主要与Cu物种分散度以及Cu+物种的活性比表面积相关。当焙烧温度为450 ℃时,催化剂的Cu物种分散度最高为43.08%,Cu+物种的活性比表面积最大为153.34 m2/g,使得Cu/SNT-450催化剂表现出最好的催化活性。

