产前HELLP 综合征并发可逆性后部白质脑病综合征一例
张巧妮,路会侠
HELLP 综合征以溶血、肝酶升高和血小板降低等为主要特点,典型症状包括全身不适、右上腹疼痛和体质量骤变等,妊娠期发生率为0.5%~0.9%,70%发生在产前,孕产妇为高危人群[1-2]。但也有因严重肾脏疾病、自身免疫性疾病、免疫抑制剂或细胞毒性药物等引发HELLP 综合征的报道[2-5]。可逆性后部白质脑病综合征(reversible posterior leukoencephalopathy syndrome,RPLS)1996 年由Hinchey 等[3]首次提出,发病率约为0.01%,是一种由多种病因引起的可逆、预后良好的临床影像学综合征,特征性临床表现为头痛、恶心呕吐、癫痫发作、意识及视力异常等,影像学多表现为大脑后部皮质和皮质下血管源性水肿。RPLS 与妊娠期高血压疾病密切相关。Mayama 等[4]的研究发现,RPLS 在子痫和子痫前期患者中发病率分别为92.3%和19.2%。子痫患者合并HELLP 综合征病情更危重,并发症发生率及死亡率更高[6]。回顾性分析1 例产前HELLP 综合征并发RPLS 患者的临床表现、诊疗过程及预后,以期引起产科医生的重视。
1 病例报告
患者 女,34 岁,因妊娠39+4周,头痛1 d,失明3 h,于2021年9 月30 日00∶42 就诊于大理大学第一附属医院(我院)急诊科。患者平素月经规律,末次月经:2020 年12 月26 日。23岁结婚,丈夫体健,孕4 产1,2014 年自然流产1 次,2017 年足月顺产一女活婴,2018 年人工流产1 次。本次预产期:2021年10 月2 日。否认特殊疾病及家族史,无内外科合并症史,“去痛片、芦荟”过敏。患者停经4 周出现早孕反应,持续至停经12 周消失。妊娠早期无阴道出血、流液,无毒物、药物及射线接触史。外院建档后未定期产检,停经18 周自感胎动,四维彩色超声、无创产前筛查及口服葡萄糖耐量试验均未见异常。2021 年9 月29 日患者无诱因出现头痛,双侧颞部持续性疼痛,无眩晕、黑矇、抽搐,无恶心、呕吐,未予重视;随后头痛加剧,伴视物模糊,直至视觉完全消失,无光感,遂至我院急诊科就诊。血压165/102 mmHg(1 mmHg=0.133 kPa),急查天冬氨酸转氨酶(aspartate aminotransferase,AST)、丙氨酸转氨酶(alanine aminotransferase,ALT)升高,血红蛋白和血小板正常,具体水平见表1。遂以①HELLP 综合征;②失明原因待查;③孕4 产1,妊娠39+4周头位先兆临产;④妊娠合并肝损伤;⑤高危孕产妇评分(50 分)于02:00 收住我院产科。
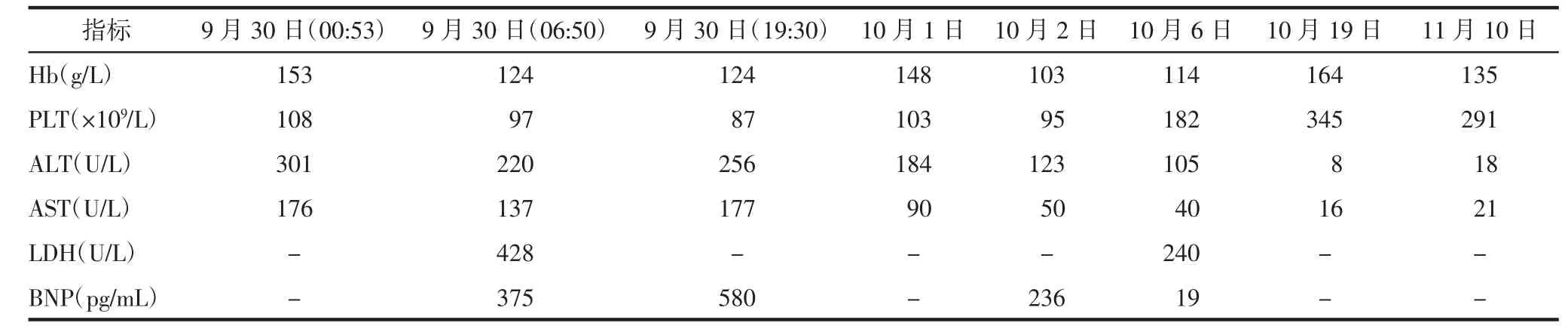
表1 患者主要临床指标检测结果
入院查体:血压163/107 mmHg,双眼仅有光感,双瞳孔等大等圆,对光反射稍迟钝。体质量55 kg,腹围95 cm,宫高30 cm,头先露,枕左前(left occiput anterior,LOA)位,胎心142 次/min;骨盆内外各径线均正常,宫颈长约3.0 cm,质中,宫口未开,先露部最低点在坐骨棘水平上2 cm(S-2),胎膜未破。入院后查ALT、AST、B 型脑钠肽(B-type natriuretic peptide,BNP)和乳酸脱氢酶(lactate dehydrogenase,LDH)升高,血小板降低;尿蛋白阳性(+++)。彩色超声检查示:宫内单活胎,胎儿大小相当于妊娠37 周,头位(LOA 位);胎儿妊娠晚期脐动脉收缩末期峰值与舒张末期峰值的比值(S/D)增高(3.88);脐绕颈1 周。头颅及眼眶CT 均未见明显异常。
2021 年9 月30 日04:40 全身麻醉下行紧急子宫下段剖宫产术,成功娩出一男活婴,脐绕颈一周,体质量2 360 g,新生儿1 min、5 min、10 min Apgar 评分分别为9 分、10 分、10分。因胎盘滞留,行徒手剥离术。术中出血600 mL,子宫体肌内注射卡前列素氨丁三醇250 μg 并按摩子宫后出血减少。术后给予缩宫素静脉滴注(20 U,1 次/d)促进子宫收缩;头孢美唑钠静脉滴注(2.0 g,每12 h 1 次)抗感染;因术前血小板明显降低且失血较多,术后输注同型红细胞悬液2.0 U、血浆500 mL 补充血容量;术后血压186/122 mmHg,给予硝酸甘油15 mg(5 mg/1 mL),以4 mL/h 微量泵静脉泵入降压;为预防产后子痫,给予硫酸镁60 mL(2.5 g/10 mL),以4 mL/h 静脉泵入解痉。头痛、失明症状请眼科、神经内科会诊,视力、眼底检查后考虑双眼视力骤降与颅内病变相关,建议根据病情尽快完善头颅磁共振成像(magnetic resonance imaging,MRI)、弥散加权成像、磁共振血管成像(magnetic resonance angiography,MRA)和磁共振静脉血管成像(magnetic resonance venography,MRV)。颅脑MRV 示:右侧横窦显影稍浅淡;上矢状窦内散在小斑片充盈缺损,蛛网膜颗粒与其他待鉴别。颈部、颅脑MRA-时间飞越法(time-of-flight,TOF)示:左侧椎动脉稍纤细,余未见明显异常。头颅MRI 示:脑实质内弥漫多发异常信号,考虑RPLS 可能;全组副鼻窦慢性炎症(见图1)。
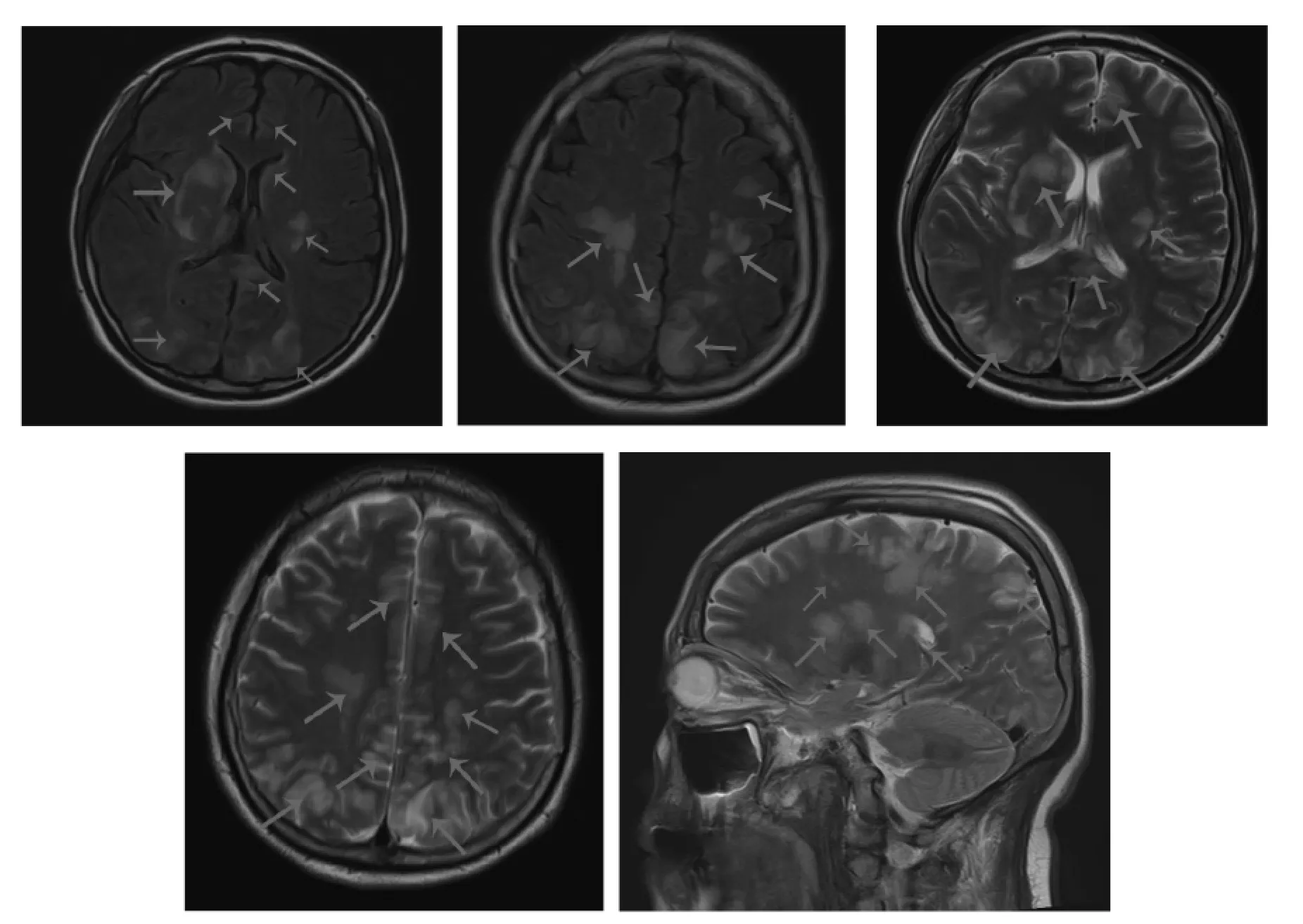
图1 患者入院头颅MRI 图像
患者于9 月30 日09:15 出现寒战,体温38.3 ℃,将头孢美唑钠更换为头孢他啶(2.0 g,每12 h 1 次),加强抗感染治疗。10:01 出现抽搐,血压187/115 mmHg,心率134 次/min,左侧卧位,清理呼吸道,5 L/min 氧流量鼻导管吸氧,缓慢静脉推注硫酸镁20 mL,硝酸甘油以6~8 mL/h 静脉泵入,随后抽搐缓解。留置胃管预防误吸,地塞米松10 mg 静脉推注抗炎、抗过敏治疗,吲哚美辛栓0.1 g 塞肛退热治疗后体温逐渐恢复正常。经心内科、重症医学科会诊后考虑患者生命体征不平稳,病情危重,与患者家属沟通后转入重症监护病房。患者双眼视力手动距离(hand motion,HM)20 cm,眼压正常,双眼眼前节未见明显异常。扩瞳行眼底镜检查示:视网膜血管走行迂曲。血压162/105 mmHg,继续静脉泵入硝酸甘油以降压,根据血压调节泵速,同时给予20%甘露醇静脉滴注(125 mL,每12 h 1 次),降低颅内压、保护脑部血管;还原型谷胱甘肽2.0 g 静脉滴注以保肝;地塞米松静脉滴注(10 mg,2 次/d),激素冲击治疗以改善肝肾功能,维持尿量;继续缩宫、抗感染、补液等对症支持治疗后病情好转。期间患者出现极度烦躁、大喊大叫、答非所问和胡言乱语等谵妄症状,予右美托咪定0.2 mg(0.2 mg/2 mL)以3~5 mL/h 静脉泵入镇静治疗;奥氮平经胃管注入(5 mg,2 次/d),抑制躁狂发作。10 月1 日拔除胃管,10 月2 日患者病情稳定后转回产科。时有烦躁不安,适度镇静、抑制躁狂发作治疗,格拉斯哥昏迷评分法(Glasgow Coma Scale,GCS)评分:13 分(轻度意识障碍)。查体:血压132/94 mmHg,双眼视物模糊,双侧瞳孔等大等圆,直径2.5 mm,对光反射迟钝。口服拉贝洛尔(100 mg,3 次/d)和硝苯地平控释片(30 mg,1 次/d)联合降压治疗后血压逐步稳定;继续给予缩宫、抗感染、保肝、激素逐步减量至停用、补液等对症支持治疗。10 月6 日患者血红蛋白、血小板、AST 和BNP 恢复正常水平,ALT、LDH 仍升高。10 月9 日患者病情稳定,视力恢复正常,血压控制平稳,办理出院。出院诊断:①HELLP 综合征;②RPLS;③孕4 产2,妊娠39+4周LOA 位剖宫产一男活婴;④胎盘植入;⑤脐绕颈1 周;⑥低体质量儿;⑦妊娠合并肝损伤;⑧谵妄查因;⑨全组副鼻窦慢性炎症;⑩高危孕产妇评分(50 分)。10 月19 日患者于我院门诊复查肝功能正常,产后42 d 于当地医院复查尿蛋白转阴。随访2 个月患者无明显不适,预后良好。
2 讨论
脑血管自身调节功能障碍及血管内皮细胞损伤是子痫及子痫前期引起RPLS 的主要机制[5]。HELLP综合征的机制较为复杂,除血管内皮细胞损伤外,还包括氧化应激异常、免疫炎症反应过度激活、脂质代谢异常及遗传等[6]。因此,了解两者并发时的临床特征可以为发病机制的研究提供依据。
本例患者未规律产检,出现头痛症状后未予重视,入院时血压明显升高,伴有尿蛋白,结合肝酶升高、血小板降低等辅助检查结果,符合HELLP 综合征的诊断。一经确诊应及时终止妊娠,按重度子痫前期给予解痉、降压、镇静、扩容等治疗,同时保护重要脏器系统、预防或治疗并发症,动态监测患者实验室指标变化。产后48 h 内HELLP 综合征患者的症状大多好转,部分产后病情反复甚至加重者需考虑糖皮质激素、血浆置换等治疗[1]。患者地处云贵山区,缺乏足够的产检意识,妊娠期未筛查是否存在妊娠期高血压疾病及胎儿生长受限的可能,入院时产科彩色超声提示孕周较实际小2 周。妊娠期患者若能定期产检,筛查妊娠期并发症,完善24 h 尿蛋白定量检测,早期识别妊娠期高血压疾病及胎儿生长受限等情况,可能会避免后续一系列并发症的发生。产检意识缺乏的病例,更要求临床医师重视对病史的采集,除加强对妊娠期重要疾病的筛查和胎儿生长发育的评估,还应加强对孕产妇的管理和联系。
RPLS 是一种表现为头痛、抽搐、视觉或意识障碍等,由血管内皮细胞功能障碍和高血压引起的血管源性脑水肿综合征,包括高血压引起的静水压升高、血-脑屏障完整性破坏导致的血管内皮细胞功能障碍[5,7]。本例患者病程中出现典型的精神、视觉症状,应与子痫、脑静脉窦血栓脑炎、肾上腺脑白质营养不良等疾病鉴别。RPLS 的症状一般在3 个月内完全消退,预后良好,少部分患者可发生不可逆性神经系统功能障碍。MRI 是RPLS 诊断的金标准,孕产妇RPLS 与非孕产妇表现无明显差异,多见双侧顶叶及枕叶的皮层下白质片状异常长T1 和T2 信号,弥散加权成像可见异常低信号,偶见于额颞叶皮层下白质、基底节区、脑干或小脑部[8]。本例患者头颅MRI检查示:双侧额顶枕颞叶、小脑半球及双侧基底节区、脑桥见多发大小不等斑片等/稍长T1 稍长T2 信号。妊娠相关RPLS 的治疗关键在于对症治疗及针对脑水肿、脑血管内皮细胞损伤的病因治疗,适当应用硫酸镁、抗癫痫药物(如地西泮、苯巴比妥)。本例患者给予脱水、降压、镇静等治疗后视力恢复。但在使用皮质类固醇激素与否的问题上仍存在争议[9-11],本例患者因肝肾功能损害、维持尿量等曾使用激素冲击治疗,但对于合并脑出血者应避免使用。
总之,目前HELLP 综合征及RPLS 的发病机制尚不清楚,均与子痫前期密切相关,且治疗缺乏临床指南统一指导。本例患者两种疾病合并的特点是“危、急、重”,且终止妊娠前后期间,两者均可相互重叠发生。产科医师不仅应重视提高孕产妇的妊娠期筛查意识和产前管理,还需要提高产后管理能力。对于妊娠期高血压疾病患者,出现神经、视觉障碍症状者需注意HELLP 综合征合并RPLS 的“警报”,及时进行MRI 检查,尽量早发现、早治疗,可避免遗留神经系统症状甚至死亡等不良结局。

