CdS/Sr2Bi2O5复合光催化剂的制备、表征及性能测试
周俊峰, 钟 燕, 黄 涛, 桑 湉, 胡朝浩
(桂林电子科技大学 材料科学与工程学院,广西 桂林 541004)
在工业生产过程中会有大量的工业废水产生,而其中有机染料废水比例较大,且随着新型工艺下对染料的改进,使得更多难以降解的有机污染物进入废水,因此增大了处理污染的难度[1]。在处理有机污染的研究过程中发现,相对传统处理方法,采用半导体光催化技术处理有机污染物更高效环保[2]。虽然CdS禁带宽度约2.0 eV,对可见光具有较好的响应,但CdS不稳定,易发生光腐蚀,光生电子和空穴易复合,造成单一CdS体系的光催化活性较低,限制了其实际应用[3]。而铋系光催化剂,如Bi2O3[4]、Bi2WO6[5]、BiVO4[6]等因其在可见光下(400~750 nm)具有良好的光催化活性而得到广泛关注。在众多铋系光催化剂中,Sr2Bi2O5的结晶度较好,颗粒粒径小且分布均匀,带隙在2.78 eV左右,易获得可见光光响应,是一种潜在的理想光催化剂[7]。通过将2种不同禁带宽度的半导体复合形成异质结复合光催化剂是改进单一半导体光催化性能的有效途径[8]。
鉴于此,通过在CdS体系中添加Sr2Bi2O5半导体来构筑异质结,研究2种半导体不同配比对复合光催化剂的结构、形貌、光生载流子及光催化活性的影响,以获得一种具有较好光催化性能的复合光催化剂。
1 CdS/Sr2Bi2O5复合光催化剂的制备
采用固相烧结法,将一定摩尔比的SrCO3和Bi2O3球磨2 h,混合均匀后,放入马弗炉中780 ℃下煅烧10 h,得到灰白色Sr2Bi2O5粉末。将一定量的Cd(NO3)2·4H2O和Na2S·9H2O分别溶解在30 mL去离子水中,搅拌15 min后分别形成溶液I和溶液II,再将溶液II缓慢加入溶液I中,加入过程中将一定量的Sr2Bi2O5加入溶液I,并持续搅拌30 min,形成橙黄色悬浊液。用去离子水和无水乙醇对悬浊液进行抽滤后,在60 ℃干燥12 h,得到一系列不同摩尔比的CdS/Sr2Bi2O5样品。
2 结果与讨论
2.1 CdS/Sr2Bi2O5晶体结构与组成
图1为单相CdS、Sr2Bi2O5和不同摩尔比合成的CdS/Sr2Bi2O5系列复合材料的XRD图谱。

图1 单相CdS,Sr2Bi2O5和CdS/Sr2Bi2O5复合光催化剂的XRD图谱
从图1可看出,单相的CdS属于闪锌矿结构,其三强峰位于2θ=26.980°、44.780°和53.059°处,分别对应于CdS(111)、(220)和(311)晶面,这与CdS的JCPDS标准卡片(JCPDS No.65-8873)完全吻合[9];单相的Sr2Bi2O5样品的三强峰则出现在2θ为24.860°、28.112°和28.814°,分别对应Sr2Bi2O5的(040)、(111)和(041)晶面,与具有正交结构的Sr2Bi2O5标准卡片(JCPDS No.81-0516)相一致[10];所有特征衍射峰均由CdS+Sr2Bi2O5两相组成,衍射峰的形状狭窄尖锐,且无其他杂质峰出现,表明成功合成了结晶度较高的CdS/Sr2Bi2O5复合光催化剂。
为了探讨合成的CdS/Sr2Bi2O5(1/1)复合光催化剂的化学成分和氧化状态,通过实验进一步研究其XPS光谱。图2(a)为CdS/Sr2Bi2O5(1/1)复合光催化剂的全光谱,检测到含有Cd、S、Sr、Bi、O和C六种元素,这些元素符合测试样品的元素组成,而C 1 s峰主要来自XPS仪器自带的含碳化合物。图2(b)中,结合能为405.1 eV的峰对应CdS中Cd2+的Cd 3d5/2电子轨道;结合能为411.8 eV的峰对应于CdS中Cd2+的Cd 3d3/2电子轨道。图2(c)中的S 2p光谱显示出在结合能分别为161.6、162.6 eV处存在2个峰,分别对应S 2p3/2、S 2p1/2电子轨道,表明S元素在复合光催化剂中以S2-的形式存在,这与文献[11]测试结果一致。图2(d)中,结合能为131.0 eV的峰对应于Sr2Bi2O5中Sr2+的Sr 3d5/2电子轨道,结合能为132.6 eV的峰对应于Sr2Bi2O5中Sr2+的Sr 3d3/2电子轨道,表明Sr在样品中的价态为Sr2+,这与SrCO3的测试结果完全一致[12]。图2(e)中,Bi 4f7/2电子轨道对应的结合能约为156.5、159.2 eV;Bi 4f5/2电子轨道对应的结合能为161.9、164.6 eV。图2(f)中O 1 s的XPS图谱由结合能为531.0、529.1 eV的2个峰组成,分别对应于化学吸附和晶格氧(Bi—O或Sr—O键),这与文献[13-14]的MgBi2O6和(Sr0.6Bi0.305)2Bi2O7的结论一致。
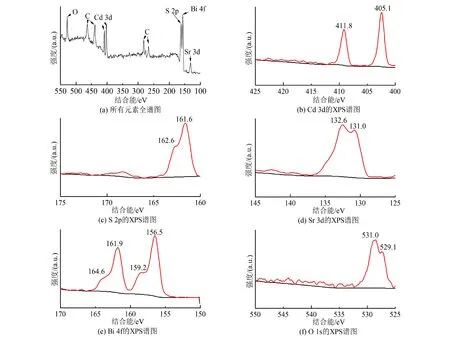
图2 CdS/Sr2Bi2O5(1/1)的XPS图谱
2.2 形貌分析
CdS/Sr2Bi2O5(1/1)复合光催化剂更为详细的微观形貌和相结构可采用透射电镜(TEM)和高分辨率透射电镜(HRTEM)来表征,其结果如图3、4所示。图3(a)~(b)表明Sr2Bi2O5是由大小约为300~700 nm的均匀小颗粒团聚成的不规则颗粒。如图3(c) SEM所示,CdS颗粒大小尺寸约为2 ~10 μm,表面粗糙,呈絮状分布,且结晶度较差。单相呈现的形貌结晶度与先前XRD分析结果一致。。对比图3(a)~(c)可看出 ,CdS/Sr2Bi2O5(1/1)复合光催化剂由CdS和Sr2Bi2O5两相颗粒组成,且CdS和Sr2Bi2O5颗粒的大小和形状基本保持不变,而CdS和Sr2Bi2O5颗粒的表面则相互耦合。

图3 单相的SEM图像以及CdS/Sr2Bi2O5(1/1)的SEM和EDS图像
从图4(a)可观察到不规则的Sr2Bi2O5颗粒与CdS颗粒紧密结合在一起,说明它们之间存在强烈的相互作用,在Sr2Bi2O5和CdS两相界面形成了异质结,使得复合体系颗粒的表面接触面积增加,从而产生比单相更多的活性位点,这将有利于促进复合光催化剂电荷的分离,提高其光催化性能。从图4(b)可看到Sr2Bi2O5和CdS的不同晶格条纹,晶面间距为0.337 nm的晶格条纹对应于CdS的(111)晶面,而晶面间距为0.317 nm的晶格条纹则与Sr2Bi2O5的(041)晶面相匹配,与XRD数据吻合。

图4 CdS/Sr2Bi2O5(1/1)的透射电镜图像
2.3 CdS/Sr2Bi2O5复合光催化剂的光学性质
为了确定复合光催化剂的禁带宽度,对半导体的光吸收特性进行了测试。图5为CdS、Sr2Bi2O5和CdS/Sr2Bi2O5(1/1)复合光催化剂的UV-vis漫反射光谱。图5(a)中 CdS、Sr2Bi2O5和CdS/Sr2Bi2O5复合光催化剂的光吸收波段均大于400 nm,表明这3种样品的光吸收区域在可见光范围内。图5(b)为样品的(ahv)2-hv曲线图。根据光吸收特性的结果,样品的带隙值Eg采用公式[15]
ahv=A(hv-Eg)n/2
(1)
进行计算,其中:a为光吸收系数;h为普朗克常量;v为频率;A为比例常数。n的取值与半导体的电子跃迁有关,间接半导体的n=4,直接半导体的n=1。由式(1)可算得CdS、CdS/Sr2Bi2O5(1/1)、Sr2Bi2O5的Eg分别为1.91、2.10、2.60 eV。根据图5(b)中x轴的截距也可估算出CdS、CdS/Sr2Bi2O5(1/1)和Sr2Bi2O5的Eg,与实验计算结果[16]一致。CdS有较小的Eg,因此对可见光响应区间较宽,但光生电子和空穴容易重组;Sr2Bi2O5的Eg较大,对可见光响应较弱,光催化效率较低;而当CdS和Sr2Bi2O5复合形成CdS/Sr2Bi2O5复光催化剂后,得益于复合材料中异质结的存在,其紫外可见漫反射光谱发生了红移,Eg相对于单相变大,有效抑制了光生电子和空穴的复合,有利于提高光催化活性。

图5 CdS,Sr2Bi2O5和CdS/Sr2Bi2O5(1/1)复合光催化剂的紫外可见漫反射光谱和带隙能谱图
2.4 CdS/Sr2Bi2O5复合光催化剂的光催化性能
图6为在模拟可见光光源下降解MB评价样品的光催化活性。先将0.05 g样品加入MB溶液,放入暗室中搅拌30 min,使混合溶液达到吸附脱附的平衡状态后进行可见光降解实验。图6(a)中,光照40 min后,CdS/Sr2Bi2O5(1/1)对MB的降解效率达95%,分别比CdS、CdS/Sr2Bi2O5(2/1)、CdS/Sr2Bi2O5(1/2)和Sr2Bi2O5提高38%、10%、7%和29%。另外,物理混合的CdS/Sr2Bi2O5(1/1)样品的光催化活性明显低于化学沉淀法制备的CdS/Sr2Bi2O5(1/1)异质结光催化剂,表明光催化活性的提高主要来自CdS与Sr2Bi2O5界面耦合产生异质结的作用。在图6(b)中,随着光照时间的变化,MB溶液的最强特征吸收峰强度逐渐降低,最终由蓝色变成透明溶液,说明染料被完全降解,这表明对MB的降解是由光催化驱动的,其中CdS/Sr2Bi2O5(1/1)的性能最好。图6(c)中MB的3次循环实验评价了CdS/Sr2Bi2O5(1/1)复合光催化剂的稳定性和可重复使用性,3次循环后降解率为80%,表明CdS/Sr2Bi2O5(1/1) 复合光催化剂具有良好的稳定性。通过捕获剂实验探究在光催化降解过程中是何种活性物质起主要作用。常见的捕获剂主要有EDTA-2Na、TEMPO和IPA,分别作为h+、·O2-和·OH的清除剂[17]。图6(d)为在添加不同捕获剂时CdS/Sr2Bi2O5(1/1)对MB的降解效果。使用EDTA-2Na可显著抑制MB的降解效率,而TEMPO和IPA的添加对降解MB几乎无影响,表明h+是主要的活性物质。
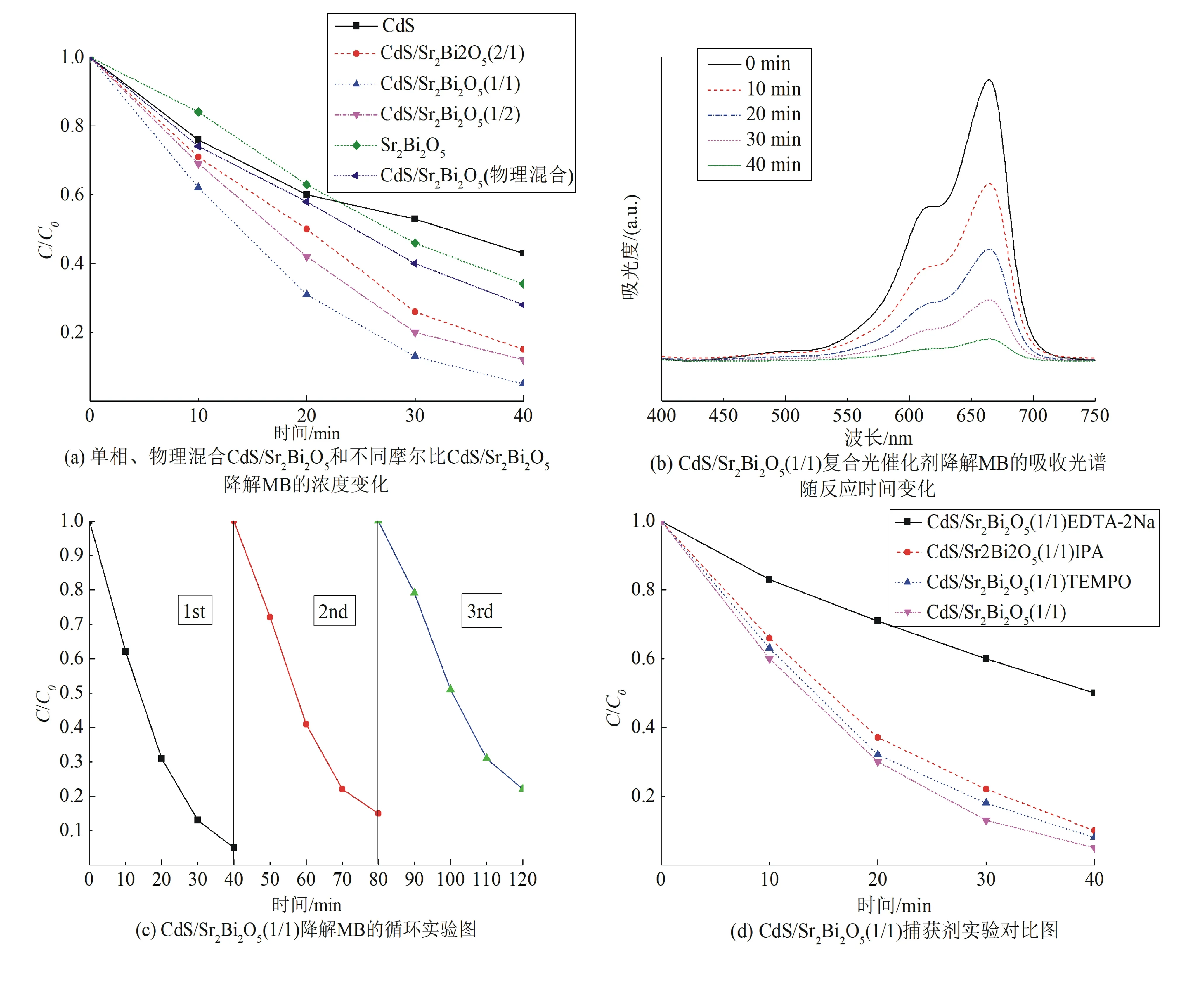
图6 CdS/Sr2Bi2O5光催化剂的光催化性能
2.5 CdS/Sr2Bi2O5复合光催化剂的光催化机理
为了研究复合光催化剂中光生电子和空穴的迁移过程,对具有良好光催化活性的CdS/Sr2Bi2O5(1/1)复合光催化剂进行了瞬态光电流和电化学阻抗测试。图7(a)为CdS、CdS/Sr2Bi2O5(1/1)和Sr2Bi2O5的瞬态光电流图谱,其中CdS的光电流最小,CdS/Sr2Bi2O5(1/1)复合光催化剂的光电流最大。瞬态光电流可间接反映电子空穴分离效率,光电流密度大的催化剂光生电子空穴对的分离效率通常较高。CdS/Sr2Bi2O5(1/1)具有更大的光电流密度,说明复合光催化剂中异质结发挥了作用,可有效分离光生载流子,所以其光催化性能比单相有大幅提升。同时,通过图7(b)的电化学阻抗谱图谱发现,CdS/Sr2Bi2O5(1/1)复合光催化剂的半圆半径比单相CdS和单相Sr2Bi2O5半圆半径小,说明复合材料的光诱导载流子重组率降低。
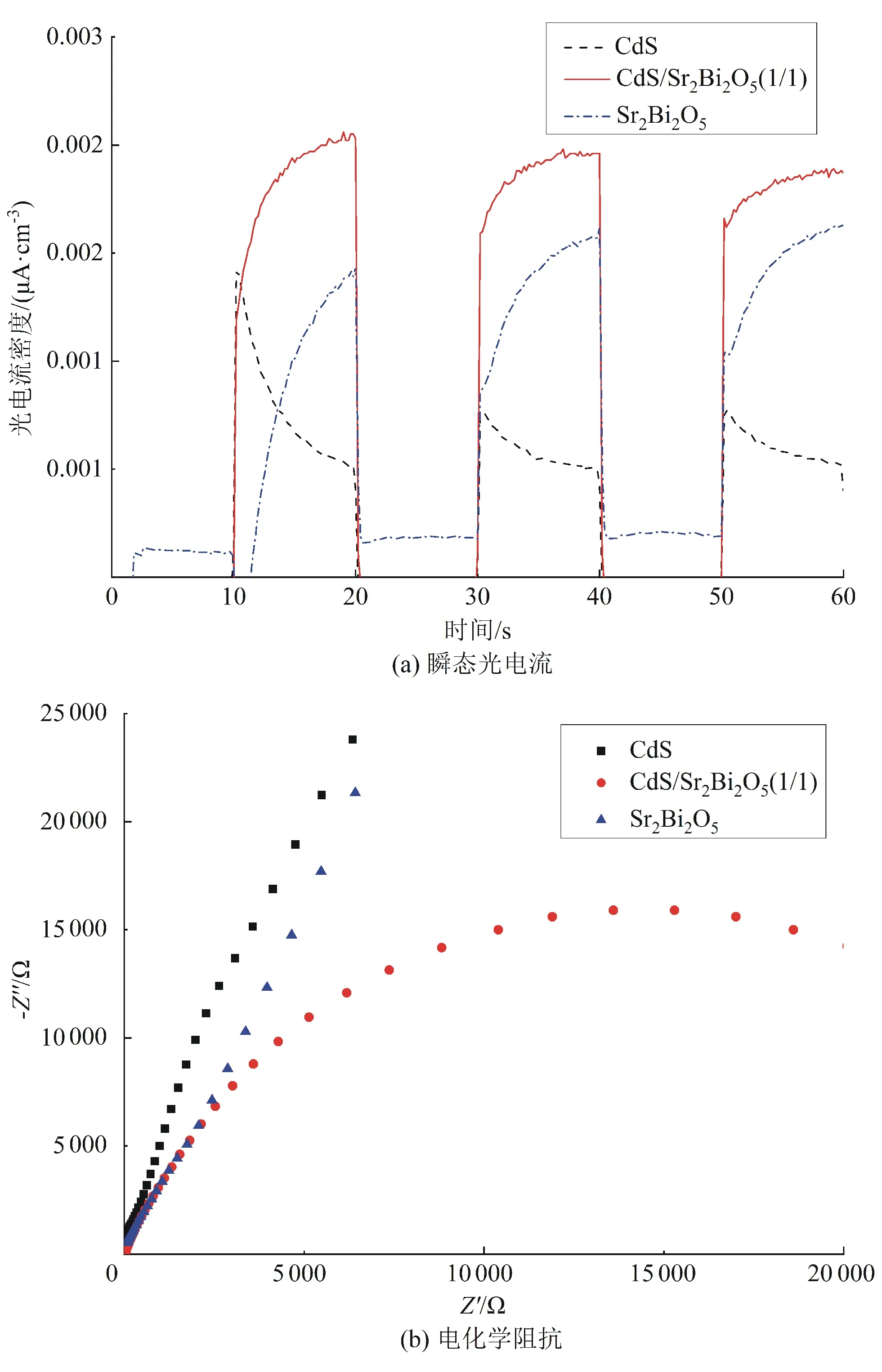
图7 单相及CdS/Sr2Bi2O5(1/1)的瞬态光电流和电化学阻抗
催化剂的带边位置在光生载流子分离过程中起关键作用[18]。Sr2Bi2O5和CdS的导带电势和价带电势分别为[19-20]
ECB=X-Ee-0.5Eg,
(2)
EVB=ECB+Eg,
(3)
其中:Ee为标准氢电极(4.5 eV)中自由电子的能量;X为半导体的绝对负电性。CdS、Sr2Bi2O5的X值分别为4.795、6.345 4 eV,测得CdS、Sr2Bi2O5的Eg分别为1.91、2.60 eV。根据式(2)、(3),CdS的ECB、EVB的计算值分别为-0.66、1.25 eV,Sr2Bi2O5的ECB、EVB分别为0.545 4、3.145 4 eV(见图8(a))。在图8(b)中,CdS和Sr2Bi2O5的费米能级电势都分别靠近各自的价带且费米能级电势有差异,复合后两者费米能级互相向对方移动,最终到达一个介于两者之间的位置,同时两者会发生电子空穴交换。在可见光的照射下,Sr2Bi2O5价带的电子从价带跃迁到导带产生光生电子,由于Sr2Bi2O5导带底层的电势高于CdS导带底层电势,光生电子由CdS和Sr2Bi2O5耦合的界面传向CdS的导带,而CdS价带顶层电势低于Sr2Bi2O5价带顶层电势,空穴经过两者耦合界面从CdS价带流向Sr2Bi2O5价带,从而能够快速分离电子空穴对,并有效抑制载流子复合,同时在表面流动过程中空穴可将MB降解。因此,实验过程中,主要的光催化活性物质是h+,这与图6(d)中的捕获实验分析结果一致。
3 结束语
在固相烧结法制备出单相Sr2Bi2O5的基础上,采用沉淀法成功合成出具有不同摩尔比的CdS/Sr2Bi2O5复合光催化剂。通过对所制样品进行结构表征和光催化性能测试发现:
1)CdS/Sr2Bi2O5复合光催化剂由CdS+Sr2Bi2O5两相组成,形貌为团聚状的Sr2Bi2O5颗粒附着在不规则的CdS颗粒上。两相表面紧密接触在一起,形成明显的界线,相互耦合形成异质结。
2)CdS和Sr2Bi2O5摩尔比为1∶1的复合体系具有最优的光催化性能,光照40 min对MB的降解效率为95%,3次循环试验后稳定性较好。显著改善的光催化性能主要归因于复合光催化剂中在CdS与Sr2Bi2O5两相之间形成了异质结,加快光生电子空穴对分离的同时,还能有效抑制光生电子空穴对的复合。

