原发性高血压患者血清RORγt mRNA、salusin-β水平及其与冠心病的相关性研究*
郭建霞,田 烁,徐 奕,俞 芳,肖红珍,李 莎,杨晓琳,刘阁玲
1.河北省唐山中心医院感染性疾病科,河北唐山 063000;2.河北省唐山市工人医院内分泌科,河北唐山 063000
原发性高血压是一种全球高疾病负担的慢性疾病,据统计,2012-2015年我国18岁及以上居民高血压患病率为27.9%,且呈升高趋势[1]。血压升高与心血管病发病和死亡密切相关,收缩压增高10 mm Hg可使无心血管疾病患者的冠状动脉事件风险增加20%[2]。合并冠心病(CHD)的高血压患者较未合并CHD的患者血压波动性更大[3],冠状动脉病变程度更严重,病变范围更广。早期识别原发性高血压合并CHD的风险有助于筛选高危人群,以便早期干预治疗,改善预后。高血压是一种慢性炎症性疾病,先天性和适应性免疫反应触发炎症过程,导致血压升高和器官损伤,辅助性T细胞17(Th17)参与和血压升高相关的炎症反应[4]。视黄酸相关孤儿受体(RORγt)是Th17发育必需及诱导白细胞介素(IL)-17表达的关键转录因子,RORγt表达异常可导致Th17分化异常,引起高血压及其相关并发症发生[5]。salusin-β是一种与血管平滑肌细胞增殖、血管纤维化和高血压有关的生物活性肽,salusin-β过表达可导致血管平滑肌细胞增殖和血管纤维化,导致高血压和心血管重塑[6]。RORγt、salusin-β是否与原发性高血压合并CHD的发生及严重程度有关尚不完全明确,为此本研究拟检测原发性高血压患者血清RORγt mRNA、salusin-β水平,分析其临床意义,以期为临床诊治提供借鉴,现报道如下。
1 资料与方法
1.1一般资料 本研究已获得唐山中心医院伦理委员会批准,选取2018年3月至2021年6月唐山中心医院收治的109例原发性高血压患者作为研究对象。纳入标准:(1)符合《中国高血压防治指南2018年修订版》[7]中原发性高血压诊断标准;(2)行冠状动脉造影检查,造影结果完整;(3)年龄18岁以上。排除标准:(1)肾动脉狭窄、皮质醇增多症、原发性醛固酮增多症等导致的继发性高血压;(2)急性冠脉综合征、风湿性心脏病、心脏瓣膜病、心肌病等;(3)严重肝肾功能障碍、急慢性感染、恶性肿瘤。根据冠状动脉造影检查结果分为CHD组(52例)和非CHD组(NCHD组,57例)。CHD组患者均经冠状动脉造影检查提示主支血管狭窄程度≥50%,符合《临床冠心病诊断与治疗指南》[8]相关标准。另选取同期于唐山中心医院门诊体检的61例志愿者作为对照组,均排除心血管疾病、原发或继发性高血压。所有受试者均知情同意并签署知情同意书。
1.2方法
1.2.1实验室检查 所有受试者入组当天早晨采集空腹静脉血3 mL注入干燥试管,血标本垂直放置30 min,待血液凝固后离心(3 000 r/min,半径15 cm,时间10 min)取上清液,以ML-dr3518酶标分析仪(上海酶联生物有限公司)采用酶联免疫吸附试验检测血清salusin-β水平,试剂盒购自上海酶联生物有限公司。采用BS-280全自动生化分析仪(深圳迈瑞医疗电子股份有限公司)检测甘油三酯(TG)、总胆固醇(TC)、尿酸(UA)、同型半胱氨酸(Hcy)水平;采用己糖激酶法检测空腹血糖(FPG)水平。采用实时荧光定量聚合酶链反应(qRT-PCR)检测血清RORγt mRNA表达水平,采用TRIzolTMplus RNA Purification Kit(美国Invitrogen公司)提取总RNA,Agilent 2100 生物分析仪(美国Agilent公司)评估RNA质量,M-MLV反转录酶(美国Promega公司)将RNA反转录为cDNA。在StepOnePlusTMqRT-PCR系统(美国赛默飞Applied Biosystems)上重复3次qRT-PCR,反应体系,DNA模板2 μL,上、下游引物各1 μL,Premix Ex Taq DNA聚合酶25 μL,RNase-Free ddH2O 21 μL。反应条件:95 ℃预变性3 min,98 ℃变性2 s,67 ℃退火15 s,72 ℃延伸20 s,循环30次。采用2-ΔΔCt的方法计算RORγt mRNA相对表达水平。引物设计由上海捷瑞公司合成,引物序列:RORγt mRNA上游5′-CATCTCCAGCCTCAGCTTTGA-3′;下游5′-TCCCCCAGAA GTCCTTAAATCC-3′,扩增长度102 bp。β-actin(内参)上游5′-TGTCCACCTTCCAGCAGATGT-3′;下游5′-GCTCAGTAACAGTCCGCCTAGA-3′,扩增长度96 bp。
1.2.2冠状动脉造影 采用标准Judkins法[9]进行冠状动脉造影,自网站www.syntaxscore.com计算SYNTAX积分。根据SYNTAX积分评价冠状动脉病变严重程度[10]并进行分组:轻度组(0~22分)15例,中度组(>22~32分)26例,重度组(>32分)11例。
2 结 果
2.1CHD组、NCHD和对照组基线资料和实验室指标水平比较 3组年龄、性别比较,差异均无统计学意义(P>0.05);CHD组和NCHD组吸烟史患者比例、饮酒史患者比例、体质量指数、高血压家族史患者比例、糖尿病患者比例、高脂血症患者比例、收缩压、舒张压、TG、TC、FPG、UA、Hcy、RORγt mRNA、salusin-β水平均高于对照组,差异均有统计学意义(P<0.05);CHD组体质量指数、高血压病程、糖尿病患者比例、高脂血症患者比例、收缩压、TG、FPG、Hcy、RORγt mRNA、salusin-β水平均高于NCHD组,降压药物治疗比例低于NCHD组,差异均有统计学意义(P<0.05);CHD组和NCHD组吸烟史患者比例、饮酒史患者比例、高血压家族史患者比例、舒张压、TC、UA及Ⅱ受体拮抗剂治疗比例比较,差异均无统计学意义(P>0.05)。见表1。
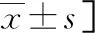
表1 CHD组、NCHD和对照组基线资料和实验室指标水平比较[n(%)或

组别n高血压病程(年)高血压家族史基础疾病糖尿病高脂血症收缩压(mm Hg)舒张压(mm Hg)CHD组5212.01±3.2615(28.85)*39(75.00)*#35(67.31)*#139.42±8.82*#82.13±6.15*NCHD组579.11±3.0117(29.82)*24(42.11)*26(45.61)*132.15±6.13*81.94±6.02*对照组61-5(8.20)6(9.84)8(13.11)112.03±5.1366.13±5.15χ2/F4.82910.30149.51335.086253.196148.796P<0.0010.006<0.001<0.001<0.001<0.001

组别nTC(mmol/L)TG(mmol/L)FPG(mmol/L)UA(μmol/L)Hcy(μmol/L)CHD组525.21±0.43*1.95±0.35*#8.12±1.23*#352.12±36.79*9.12±2.15*#NCHD组575.15±0.36*1.70±0.33*7.16±1.03*348.15±32.07*7.05±2.03*对照组614.21±0.401.55±0.244.71±0.68286.61±28.114.15±0.69χ2/F102.31895.16856.18432.16528.107P<0.001<0.001<0.001<0.001<0.001

注:与对照组比较,*P<0.05;与NCHD组比较,#P<0.05;-表示无数据。
2.2轻度组、中度组和重度组患者血清RORγt mRNA、salusin-β水平比较 重度组患者血清RORγt mRNA、salusin-β水平均高于中度组和轻度组,差异均有统计学意义(P<0.05);中度组患者血清RORγt mRNA、salusin-β水平均高于轻度组,差异均有统计学意义(P<0.05)。见表2。
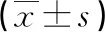
表2 轻度组、中度组和重度组患者血清RORγt mRNA、salusin-β水平比较
2.3影响原发性高血压发生CHD的多因素Logistic回归分析 将体质量指数、高血压病程、糖尿病(赋值:0=否,1=是)、高脂血症(赋值:0=否,1=是)、收缩压、TG、FPG、Hcy、RORγt mRNA、salusin-β作为自变量(连续性变量原值代入),将原发性高血压是否发生CHD作为因变量(赋值:0=否,1=是),采用ENTER法筛选变量,结果显示,高表达RORγt mRNA、高水平salusin-β、高水平Hcy、糖尿病是原发性高血压发生CHD的危险因素(P<0.05)。见表3。

表3 影响原发性高血压发生CHD的多因素Logistic回归分析
2.4RORγt mRNA、salusin-β诊断原发性高血压患者发生CHD的价值 RORγt mRNA、salusin-β诊断原发性高血压患者发生CHD的截断值分别为0.752、4.02 nmol/L,灵敏度分别为61.54%、67.31%,特异度分别为73.68%、77.19%,曲线下面积(AUC)分别为0.628、0.693,基于多因素Logistic回归计算RORγt mRNA、salusin-β水平联合检测诊断原发性高血压患者发生CHD的AUC为0.910,二者联合检测诊断原发性高血压患者发生CHD的AUC高于RORγt mRNA、salusin-β单项检测(Z=5.056、4.231,P<0.001)。见图1、表4。

图1 RORγt mRNA、salusin-β检测诊断原发性高血压患者发生CHD的ROC曲线

表4 RORγt mRNA、salusin-β检测对原发性高血压患者发生CHD的诊断效能
3 讨 论
长期高血压可导致血流剪切力变化,损伤血管内皮细胞,导致血小板激活、聚集黏附,巨噬细胞释放炎症因子,最终引起平滑肌细胞增殖和动脉粥样硬化斑块形成[11]。免疫炎症反应和高血压发病密切相关,Th17活化导致动脉巨噬细胞和T细胞浸润,外周循环血中促炎因子水平升高,长期炎症反应过程会增加活性氧的产生,引起氧化应激,导致内皮功能障碍,对一氧化氮生物利用度降低,使血管松弛和血管舒张作用减弱[12],最终引起血压升高及心血管损伤。
RORγ是人类基因组中核受体超家族的成员,RORγt是RORγ的亚型,RORγt可促使T细胞分化为Th17,并调节Th17的细胞因子IL-17基因转录,参与免疫应答和调节过程[13]。有研究发现,过表达IL-17可诱导全身内皮功能障碍、血管氧化应激及动脉高血压[14],而RORγt可通过促使IL-17表达驱动炎症反应,参与高血压的发病机制[15]。RORγt是否与原发性高血压及合并CHD有关尚不清楚,本研究发现,CHD组患者血清RORγt mRNA表达水平明显增高,高于NCHD组和对照组,且RORγt mRNA表达水平随冠状动脉病变加重而增高。多因素Logistic回归分析结果显示,高表达RORγt mRNA是原发性高血压患者发生CHD的危险因素之一,说明RORγt可能与原发性高血压及高血压介导的冠状动脉病变发生有关。有研究显示,RORγt参与Th17发育分化及IL-23R产生,IL-23R和IL-23结合促使Th17分泌IL-17并维持病理形态,RORγt/IL-23R信号通路通过诱导病理性Th17分化参与高血压的发病过程[16]。Th17过度活化及IL-17过量合成可加速动脉粥样硬化进程,CHD患者外周血Th17占比、IL-17mRNA表达水平均明显增加[17],提示RORγt可能通过诱导Th17活化及其特征性细胞因子IL-17合成,参与原发性高血压合并CHD的发病过程。
salusin-β是具有血流动力学和促有丝分裂作用的生物活性肽,由20个氨基酸组成,在中枢及外周组织中广泛表达,中枢salusin-β参与交感神经激活、精氨酸加压素释放和高血压调节[18]。临床研究显示,原发性高血压患者血清salusin-β水平明显升高,salusin-β水平与颈动脉病变严重程度有关[19]。本研究结果显示,原发性高血压患者血清salusin-β水平较对照者升高,且CHD组患者血清salusin-β水平高于NCHD组患者,说明salusin-β与原发性高血压患者冠状动脉病变有关。分析可能的原因为salusin-β在人血管平滑肌细胞中也有表达,salusin-β可通过激活烟酰胺腺嘌呤二核苷酸磷酸,促使活性氧产生,下调抗衰老基因Klotho表达,促使血管钙化[20]。salusin-β还可上调miR155表达水平,促使p65-核因子-κB核易位,增加胆固醇酰基转移酶-1和血管细胞黏附分子-1的表达和活性,促使脂质在血管平滑肌细胞中积累,单核细胞黏附,泡沫细胞形成[21],导致动脉粥样硬化形成。本研究多因素Logistic回归分析结果显示,高水平salusin-β是原发性高血压患者发生CHD的危险因素,说明salusin-β可作为诊断原发性高血压合并CHD的生物学标志物。WANG等[22]报道指出,salusin-β水平与冠状动脉狭窄有关,是评估冠状动脉疾病的潜在标志物。
本研究ROC曲线分析结果显示,RORγt mRNA、salusin-β鉴别原发性高血压患者发生CHD均具有一定价值,RORγt mRNA、salusin-β联合检测鉴别原发性高血压患者发生CHD的效能明显提高,说明RORγt mRNA、salusin-β水平均升高可能警示更高的冠状动脉病变风险,联合检测对临床识别冠状动脉病变风险更有价值。多因素Logistic回归分析结果显示,糖尿病、高水平Hcy也与原发性高血压患者发生CHD有关。王哲辉等[23]报道指出,高血压合并糖尿病患者并发CHD的风险高于单独高血压和糖尿病,提示高血压、糖尿病并存可加速冠状动脉病变。阴淑莹等[24]研究指出,Hcy水平与冠状动脉病变程度呈正相关,Hcy水平升高是原发性高血压合并冠心病的危险因素。
综上所述,原发性高血压合并CHD患者血清RORγt mRNA、salusin-β水平均升高,RORγt mRNA、salusin-β水平升高与冠状动脉病变及病变程度均有关,是原发性高血压合并CHD的危险因素。RORγt mRNA、salusin-β可作为诊断原发性高血压合并CHD的生物学指标。

