膜法去除海上气田乙二醇富液中二价阳离子的研究*
尤学刚,胡 凯,盛春光,吴 巍,臧毅华
(1.中海石油(中国)有限公司 海南分公司,海南 海口 570125;2.中海油 天津化工研究设计院有限公司,天津 300131)
海上气田生产平台开采的天然气需要通过海底管线运送至陆地生产终端。由于海底温度低、海管管线长造成管内气体温度降低、压力升高,极易形成水合物堵塞管线。为了有效抑制天然气水合物的生成,常用的方法是将大量乙二醇注入海管中。但乙二醇经过海管后,会含有大量的Ca2+、Mg2+、CO2、水和轻烃,循环使用会产生严重的结垢现象[1-3]。目前,乙二醇再生系统中脱除二价盐的方法是向高含盐乙二醇中加入Na2CO3、NaOH形成悬浊液,在通过固液分离装置去除二价盐沉淀。固液分离装置主要有即颗粒过滤器和高速离心机[4-6]。但上述装备都存在过滤精度低、运行周期短、自动化程度低等缺点。本文使用陶瓷无机超滤膜对加碱后的乙二醇富液进行分离,考察膜对高含盐乙二醇富液的处理效果。
1 实验部分
1.1 器材、仪器及药品
陶瓷无机超滤膜(膜外径30mm,61通道,通道直径2.5mm,膜管长度1100mm,膜面积0.5m2,膜表面平均孔径50nm,中海油天津化工研究设计院有限公司)。
乙二醇富液(水含量50.4%,Na+浓度11340mg·L-1,Ca2+浓度180mg·L-1,Mg2+含量127mg·L-1,轻烃浓度523mg·L-1,取自南海气田某生产平台);NaOH、Na2CO3,均为分析纯,天津光复精细化工研究所。
UFE500ZX21型强制对流烘箱(德国美而特);Mastersizer 3000型激光粒度仪(英国马尔文);7890B型气相色谱仪(美国安捷伦);ICS-600型离子色谱仪(美国赛默飞)。
1.2 富乙二醇化学除Ca2+、Mg2+原理及方法
根据溶度积原理,采用化学法除Ca2+、Mg2+。通过向乙二醇富液加入适量的NaOH和Na2CO3,使乙二醇溶液中Ca2+、Mg2+形成难溶化合物。取待处理的乙二醇富液5L置于水桶中,在电动搅拌下缓慢加入药品,加入后持续搅拌15min,形成富乙二醇悬浊液。
1.3 膜法处理富乙二醇悬浊液实验方法[7,8]
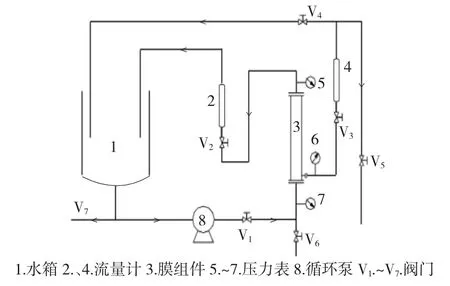
图1 膜分离评价装置工艺流程图Fig.1 Process flow chart of membrane separation evaluation device
自制的膜分离评价装置,采用单根膜管组件,设计处理量0.01~1m3·h-1,膜面积为0.5m2。实验开始先打开V1、V2、V3、V4,关闭V5、V6、V7,向水箱加入富乙二醇悬浊液,开启加热,打开循环泵至温度、压力及流量稳定,进行试验检测及数据记录;7-压力表记录进膜压力P1,5-压力表记录出膜压力P2,6-压力表记录渗透侧压力P3,跨膜压差ΔP由ΔP=(P1+P2)/2-P3公式得到;2-流量计记录系统循环流量Q1,4-流量计记录膜组件渗透液流量Q2,膜通量J由J=Q2/S2得到,S2为膜组件有效过滤面积;膜面流速u由u=(Q1+Q2)/S1得到,S1为膜组件进液截面积;通过控制阀门开度,加热温度以及循环泵流量,将跨膜压差、膜面流速及温度3个影响因素中的两个因素固定,考察剩下的一个因素的变化对膜性能的影响。
盐颗粒悬浮物固含量使用0.22μm的滤膜对膜产水进行过滤,将截留物和过滤膜置于烘箱内105℃减压干燥至恒重,称量结果减去滤膜重量即为盐颗粒悬浮物固含量;悬浮物粒径中值采用粒度分析仪进行检测。
2 结果与讨论
2.1 除盐药剂投加量对二价盐沉降效果的影响
向富乙二醇中分别加入一定量的NaOH和Na2CO3,考察加药量对二价盐沉降效果的影响。图2为NaOH投加量对富乙二醇中Ca2+、Mg2+浓度的影响。

图2 NaOH投加量对Ca2+、Mg2+浓度的影响Fig.2 Effect of sodium hydroxide dosage on calcium and magnesium ions
由图2可知,NaOH投加浓度从40mg·L-1上升至80mg·L-1的过程中,富乙二醇中的Ca2+、Mg2+浓度没有明显下降;NaOH投加浓度从80mg·L-1增加至120mg·L-1,Mg2+浓度开始明显下降,而Ca2+下降趋势比较缓慢,这是由于Mg(OH)2溶解度本身就小于Ca(OH)2,Mg2+优先沉淀下来;NaOH投加浓度从120mg·L-1继续增加,富乙二醇中的Ca2+开始明显下降,这是由于富乙二醇中的Ca(OH)2到达了饱和,继续加入OH-,新生成的Ca(OH)2开始析出沉淀,另一方面,富乙二醇的Ca(OH)2会与空气中的CO2反应生成CaCO3,也会使富乙二醇中的Ca2+浓度降低;当NaOH浓投加浓度增加至320mg·L-1以上,Mg2+的浓度稳定在0.60mg·L-1左右,可能在富乙二醇剩余的Mg(OH)2已经达到溶解平衡,不能继续沉淀析出。综合考虑,如果继续增加NaOH,一方面,不能继续去除Mg2+,另一方面,碱度过大会对设备造成严重的腐蚀,鉴于此,NaOH投加浓度为320mg·L-1,此时富乙二醇中的Mg2+浓度为0.62mg·L-1,Ca2+浓度为87.13mg·L-1。由于Ca2+浓度仍然很高,需要继续投加Na2CO3。
图3为Na2CO3投加量对富乙二醇中Ca2+、Mg2+浓度的影响。
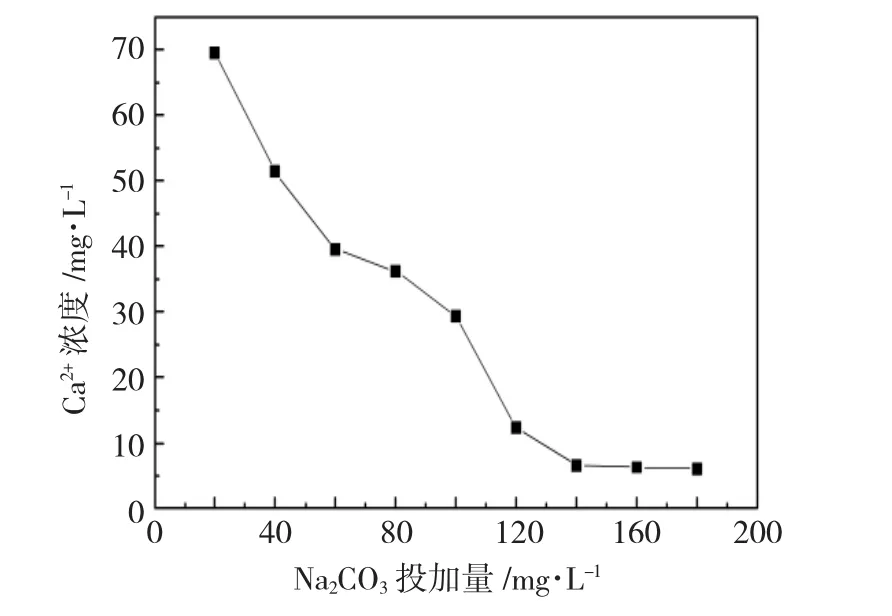
图3 Na2CO3投加量对Ca2+浓度的影响Fig.3 Effect of sodium carbonate dosage on calcium ion
由图3可知,Na2CO3投加量从20mg·L-1至140mg·L-1,Ca2+浓度从69.58mg·L-1下降至6.55mg·L-1;其中,Na2CO3投加量从60mg·L-1增加到100mg·L-1这个区间,Ca2+浓度下降趋势减缓,可能是由于CO2-3和一些已沉淀的Ca(OH)2生成了CaCO3;在Na2CO3投加浓度超过140mg·L-1时,溶液中Ca2+浓度基本不变。
2.2 跨膜压差对膜性能的影响
向富乙二醇分别加入NaOH(浓度320mg·L-1)、Na2CO3(浓度140mg·L-1)之后生成黄色悬浊液,悬浮物固含量为863.89mg·L-1,粒径中值50.224μm。将药剂处理后的富乙二醇通过膜处理装置,在温度80℃,膜面流速为5.6m·s-1的条件下,考察跨膜压差对膜过滤效果的影响。
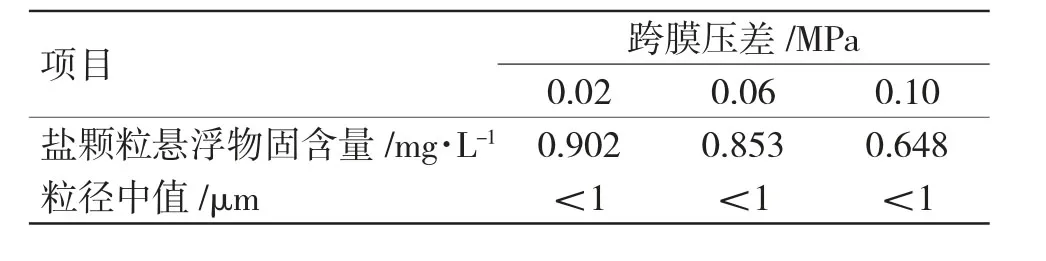
表1 不同跨膜压差条件下稳定产品质量分析Tab.1 Analysis of product under different transmembrane pressure difference
跨膜压差(TMP)是驱动液体透过膜所需压力,从图4中可以看到,3组对比实验都有3个阶段:第一阶段,膜通量较大,但衰减较快;第二阶段,膜通量缓慢下降;第三阶段,膜通量保持平稳。TMP越大,膜初始通量也越大。在TMP为0.10MPa时,膜初始通量达到538L·(m2·h)-1,但运行至150min,膜通量已经下降至121L·(m2·h)-1,相比于低跨膜压差的两组实验,膜通量衰减的更快。这是因为TMP过高,透过膜层的乙二醇增加,相应的更多的盐颗粒被截留在膜表面上,并且由于膜面流速是一定的,大量的盐颗粒不能被及时冲走,这样膜表面的污染层就越来越厚,导致膜通量快速下降;并且,跨膜压差过大会将污染层挤压的更加紧实,使污染物进入孔道内部,导致清洗恢复更加困难[7]。而TMP为0.02、0.06MPa,在操作时间超过120min膜通量趋于稳定,分别稳定在104、210L·(m2·h)-1。过滤后的富乙二醇,在0.02和0.06MPa的条件下,悬浮物固含量基本在0.853~0.902mg·L-1,粒径中值小于1μm;而在0.10MPa的条件下,粒径中值小于1μm,但悬浮物固含量下降至0.648mg·L-1左右,这是因为,由于膜表面污染层更厚,小粒径的盐颗粒更难通过膜层,所以造成富乙二醇过滤液固含量下降。
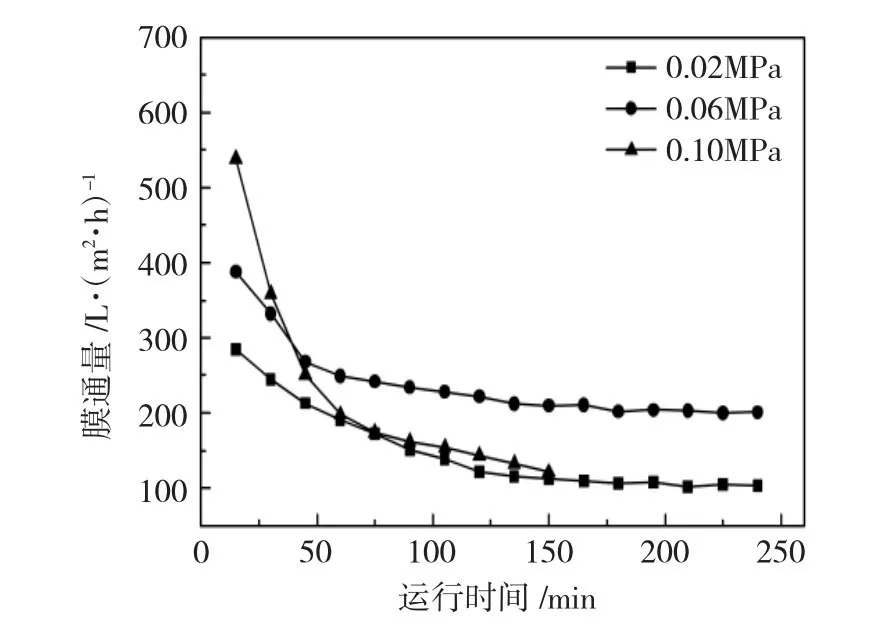
图4 不同跨膜压差条件下膜通量随时间的变化Fig.44Variation of membrane flux with time under different transmembrane pressure difference
2.3 膜面流速对膜性能的影响
膜面流速等于进料量除以膜截面面积,因为膜截面面积是一定的,所以膜面流速对膜过滤效果的影响可以看做进料量对膜过滤效果的影响。图5和表2是温度为80℃,TMP为0.06MPa的条件下,考察膜面流速对膜过滤加药后的富乙二醇悬浊液的影响。

图5 不同膜面流速的条件下膜通量随时间的变化Fig.5 Variation of membrane flux with time under different membrane velocity

表2 不同膜面流速的条件下稳定产品质量分析Tab.2 Analysis of product under different membrane velocity
从图5中可以看到,在操作时间100min以内,随着膜面流速越大,膜通量也越大。这是因为在膜面积和TMP一定的情况下,膜面流速越大,膜表面的污染物更容易被冲刷掉,使膜表面的污染情况降低,富乙二醇更容易穿过膜层进入渗透侧。随着操作时间超过100min,在膜面流速3.2和5.6m·s-1的条件下,膜通量基本一致,为211L·(m2·h)-1左右,这说明虽然提高流速有利于降低膜表面的污染,但膜表面的污染是不可避免的,继续通过提高进料量不能明显增加膜的处理量,反而会增加大量的能耗。所以,膜面流速5.6m·s-1是比较合适的操作条件。
2.4 温度对膜性能的影响
图6和表3为跨膜压差为0.06MPa,膜面流速为5.6m·s-1,运行150min的条件下,考察温度对膜过滤加药后的富乙二醇悬浊液的影响。
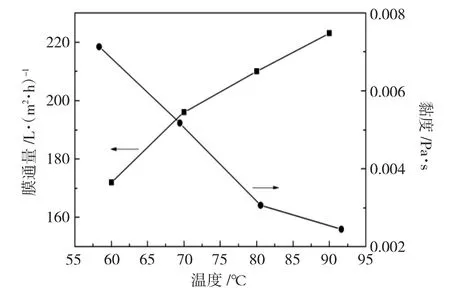
图6 不同温度条件下稳定膜通量随时间的变化Fig.6 Variation of stable membrane flux with time at different temperatures

表3 不同温度条件下稳定产品分析Tab.3 Analysis of product under different membrane velocity
从图6中可以看到,随着温度从60℃上升至90℃,富乙二醇黏度从0.00713Pa·s下降至0.00245Pa·s,膜通量从172L·(m2·h)-1上升至223L·(m2·h)-1。温度的升高可以降低富乙二醇的黏度,并且可以使膜表面液体从层流变为湍流,这既减少了膜表面浓差极化的现象,又增大了富乙二醇透过膜的传质系数,从而增大了膜通量[7]。同时,从表3中可以看到,随着温度的上升,产品的盐颗粒悬浮物固含量逐渐升高,在90℃的条件下,产液悬浮物固含量达到0.985mg·L-1。这是由于温度的上升,小粒径的悬浮物布朗运动更加剧烈,使得盐颗粒更容易穿过膜层进入渗透侧。在实际工况下,富乙二醇悬浊液温度为80℃,此时膜通量为210L·(m2·h)-1与90℃下的膜通量差别不大,提高温度会增加设备投资和工艺设备的复杂性,所以选择80℃为适合的工艺条件。
2.5 膜的抗污染性能的研究
在确定最佳工艺条件后,需要进一步考察膜的抗污染性和长周期的稳定性。在跨膜压差为0.06MPa,膜面流速为5.6m·s-1,温度为80℃的运行条件下,进行膜过滤富乙二醇悬浊液长周期运行试验,结果见图7。

图7 陶瓷无机超滤膜过滤富乙二醇长周期稳定性实验Fig.7 Stability experiment of rich MEG filtered by ceramic inorganic ultrafiltration membrane
由图7可见,在运行的前15min,膜通量达到388L·(m2·h)-1,持续运行2h后,膜通量急剧下降至222L·(m2·h)-1;之后运行120h内,膜通量稳定在200L·(m2·h)-1以上;当运行时间在120~192h,膜通量继续下降,从200L·(m2·h)-1下降173L·(m2·h)-1。从长周期试验可以看出,陶瓷超滤膜分离的整体过程:在初始阶段,由于膜表面没有污染物的沉积,膜表面孔道比较干净,乙二醇可以轻易通过膜进入渗透侧,所以膜初始通量很高,但污染物很快会进入膜孔道,并堆积在膜表面,导致膜通量迅速下降;随着试验继续进行,由于陶瓷膜表面具有一定的膜面流速,可以将堆积在表面的污染物冲掉,使污染层保持一定的厚度,达到动态平衡,所以膜通量稳定200L·(m2·h)-1以上,出现平台期;随着试验进入后期,一些小颗粒的污染物会进入孔道内部,导致孔道内部,造成膜通量进一步下降,这时需要对膜管进行清洗再生,否则会对膜造成不可逆的损伤。
图8为富乙二醇膜过滤液的悬浮物含量和Ca2+、Mg2+含量。
由图8可以看到,膜过滤液Ca2+、Mg2+含量小于0.19mmol·L-1,悬浮物固含量小于0.829mg·L-1,悬浮物粒径中值小于1μm,Ca2+、Mg2+脱除率大于99.8%。

图8 富乙二醇膜过滤液的悬浮物含量和Ca2+、Mg2+含量Fig.8 Suspended solids content and calcium and magnesium content of rich MEG filtrated
2.6 膜清洗再生试验研究
图9 为陶瓷无机超滤膜污染后的清洗效果图。

图9 酸性药剂清洗对膜通量恢复率的影响Fig.9 Effect of acid agent cleaning on membrane flux recovery rate
使用的酸性复配药剂为HCl、EDTA、水的混合溶液(混合比例为mHCl∶mEDTA∶m水=10∶1∶1000)。从图9中可以看到,膜污染后先使用清水进行清洗,将膜面附着不紧的污染物冲掉,膜通量恢复了25.9%左右;之后使用酸性复配药剂清洗,将膜表面及孔道内部的CaCO3、MgCO3、NaOH等污染物去除,膜通量恢复了99.1%;最后再次使用水洗,最终膜通量恢复到初始通量的99.9%。
3 结论
(1)实验表明,跨膜压差为0.06MPa,膜面流速为5.6m·s-1,温度为80℃为陶瓷基功能膜过滤MEG富液的最佳工艺条件;在该工艺条件下,通过长周期稳定性试验,在120h内,膜通量大于200L·(m2·h)-1,膜过滤液悬浮物固含量小于0.829mg·L-1,悬浮物粒径中值小于1μm,富乙二醇过滤液Ca2+、Mg2+含量小于等于0.19mmol·L-1,Ca2+、Mg2+脱除率大于等于99.8%;
(2)酸性药剂清洗,可以有效去除陶瓷无机膜表面的污染层,降低表面浓差极化的现象,并且将附着在膜表面和孔道内部的碳酸盐垢完全清除,使陶瓷无机超滤膜基本实现再生,膜通量恢复率在99%以上;
(3)陶瓷无机超滤膜在处理高含盐乙二醇富液表现出优异的分离过滤性能、抗污染性能以及稳定性,该膜材料在乙二醇再生领域具有巨大的应用潜力。

