颅内多中心性胶质母细胞瘤1例
齐洪武 刘岩松 张立钊 乔 民 曾维俊 刘清石
1 病例资料
60 岁男性,因左侧肢体力弱、右手指麻木2 个月伴右侧面部麻木1 d入院。入院体格检查:神志清楚;右侧上肢及右侧面部浅感觉减退,右侧肢体肌力5级,左侧鼻唇沟稍浅,左侧肢体肌力4级。颅脑MRI 检查示:双侧顶叶可见结节状T2稍高信号影,增强后呈边缘强化或结节样强化,边界清楚,最大病变位于右侧顶叶(2.2 cm×3.2 cm×2.5 cm),左侧顶叶病变大小约2.1 cm×1.3 cm×2.2 cm;周围可见片状水肿信号;右侧侧脑室受压变扁,中线结构稍左偏(图1A)。完善术前准备后,先行右侧顶叶占位病变切除术,术后病理示右顶胶质母细胞瘤(WHO 分级Ⅳ级)。术后恢复良好,未出现左侧肢体肌力及感觉改变。2 周后再次行左侧顶叶占位病变切除术,术后病理左顶胶质母细胞瘤(WHO分级Ⅳ级)。术后恢复良好,未出现右侧肢体肌力及感觉改变。术后11 d 复查颅脑MRI示左侧顶叶肿瘤残留(图1B),行头部伽玛刀治疗(共设4个靶区、计13 个靶点,给予50%等剂量曲线、周边剂量为1 500 cGy、中心最大剂量为3 000 cGy);并同步化疗(替莫唑胺,300 mg/d),每28 d为一周期,用药时间为连续5 d,1次/d,间隔23 d。术后5 个月复查颅脑MRI 示肿瘤控制良好(图1C)。术后11个月出现继发性癫痫,复查颅脑MRI示右侧顶肿瘤复发并侵及右侧脑室壁(图1D)。病人及家属拒绝手术治疗,口服卡马西平(0.2g,3次/d)控制癫痫,继续替莫唑胺化疗。术后13 个月,突发意识不清,急查头颅CT 示脑室出血,第三脑室、第四脑室均已堵塞,考虑为右侧顶叶胶质母细胞瘤卒中(图1E)。急诊在全麻下行颅骨钻孔脑室外引流术,对症治疗3周,复查头颅CT示脑室内出血已吸收(图1F),恢复良好出院。此后,病人未再行替莫唑胺化疗。术后17个月因肿瘤快速生长导致中枢性呼吸循环衰竭死亡。
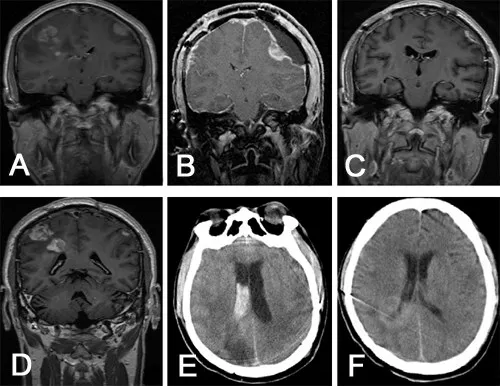
图1 颅内多发性胶质母细胞瘤显微手术治疗前后影像
2 讨论
多灶性胶质瘤占胶质瘤的11%,而多中心性胶质瘤占6%。多灶性胶质瘤的病灶之间相邻较近,播散途径较为明确,譬如脑脊液通道、白质传导束(胼胝体、前后联合、穹窿、锥体束)等。多中心性胶质瘤的病灶之间相邻较远,肿瘤病灶分别位居两个脑叶,甚至位于两侧大脑半球,无明显肿瘤细胞播散途径。多灶性胶质瘤病理等级往往比多中心性胶质瘤高,多灶性胶质瘤以胶质母细胞瘤最常见,而多中心性胶质瘤以级别较低的星形细胞瘤常见。少数多中心性胶质瘤的不同病灶可表现为不同的病理性质,多为胶质母细胞瘤合并其他类型肿瘤,如少突胶质细胞瘤、单纯星形细胞瘤、室管膜瘤等。胶质母细胞瘤中位生存期较短。目前,胶质母细胞瘤的标准治疗方法是手术切除,术后行放疗结合替莫唑胺化疗。对多发性高级别胶质瘤,多病灶切除可以改善病人的预后;而多发性胶质母细胞瘤切除所有病灶后的生存期,与单发性胶质母细胞瘤术后生存期接近,且不增加术后并发症。本文病例为多中心性胶质母细胞瘤,均位于脑功能区,一次性切除可能致病人全瘫,故采取分期手术。对肿瘤位置较深、无明显颅内压增高症状的病人,可采取立体定向活检术,根据术后病理结果进行后续综合治疗。

