运动调控肌肉、肝脏、脂肪的运动因子的文献计量学分析
唐韶慨,耿元文,林琴琴,李若明,王柏慧,余一荣,李 浩
体力活动缺乏是当今社会存在的普遍问题,世界卫生组织早在2002年已将其列为导致发达国家人口死亡的主要原因之一[1]。运动作为一种疾病非药物干预手段,具有便捷、经济、安全及高效等优势,其健康促进效应已得到广泛认可,但具体机制尚未阐明。运动健康促进效应是一种涉及神经—内分泌—代谢—免疫等多个系统的全身性保护效应,其核心是通过运动产生的缺氧、氧化应激和机械力刺激(例如血流加速)等激活机体内源性保护机制[2]。新兴研究表明,运动可诱导多种组织和器官分泌“运动因子(Exerkine)”参与代谢保护,展示出组织器官间“相互作用”在运动健康促进效应中的重要性与可能性[3]。
Pedersen等于2004年正式提出“运动因子”一词,肌肉收缩时产生的白细胞介素-6(Interleukin 6,IL-6)为首个被人们确定的运动因子[4]。Safdar等于2016年提出此概念,即运动可诱导骨骼肌和其他器官释放的抗凝血肽、核酸及代谢物等物质可进入细胞外液或血液中,以自分泌信号实现细胞自身“自我对话”,也可以旁分泌信号和内分泌信号分别与邻近和远处器官(组织)的细胞进行交互作用,其中肌肉、肝脏、脂肪的运动因子研究较为广泛[5]。近年来,运动调控肌肉、肝脏、脂肪的运动因子的相关研究以药物靶点筛选和疾病诊断及预防为研究导向,取得了长足的进步与发展。研究证实,肌肉运动因子卵泡抑素样蛋白1可以抑制细胞凋亡和炎症反应[6];脂肪运动因子爱帕琳肽可以促进血管生成[7];肝脏运动因子胰岛素样生长因子-1(Insulin-like growth factor 1,IGF-1)可以提高能量代谢[8]和降低血糖[9],说明肌肉、肝脏、脂肪的运动因子可能作为疾病的潜在治疗靶点,对机体发挥保护效应。此外,运动可调控肌肉、肝脏、脂肪的运动因子水平,预防多种代谢性疾病或延缓其过程。运动可显著增加1型糖尿病儿童血液中脂联素(Adiponectin,ADPN)水平,下调糖化血红蛋白(Glycated hemoglobin,HbA1C)水平,明显增强下肢肌力,增加胰岛素敏感性[10];可刺激骨骼肌分泌IL-6、鸢尾素、IGF-1和成纤维细胞生长因子2(Fibroblast growth factor,FGF2),能够对抗由于感染引起的急性炎症和由于缺乏运动、衰老或代谢紊乱引起的慢性低度炎症,延缓肌肉减少症[11]。鉴于此,本研究对国内外关于运动调控肌肉、肝脏、脂肪的运动因子的相关研究现状及热点进行文献计量学研究,以期为今后开展运动调控肌肉、肝脏、脂肪的运动因子的相关研究提供参考。
1 研究方法
1.1 文献来源
关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的文献资料来源于国内“CNKI”中文期刊数据库(166篇)和国外“Web of Science(WoS)”核心合集数据库(632篇)。由于Pedersen于2004年正式提出“Exerkine”概念[4],因此检索时间均设置为2004年1月1日至2020年12月25日。在“CNKI”中文核心期刊数据库的检索词为“运动”或“身体活动”,并在上述检索结果中增加检索词“肝脏运动因子”或“肌肉运动因子”或“脂肪运动因子”或“运动因子”进行检索,检索范围为北大核心期刊。在“WoS”的核心合集数据库的检索词为“ExerciseOR TrainingOR Sport”AND“Myokines OR Adipokines OR Hepatokines OR Exerkines”,检索范围为SCI-E和SSCI期刊。
1.2 分析工具
本研究对中文文献采用“CNKI”期刊检索系统中“可视化分析”功能进行计量分析;对外文文献以“纯文本”格式导出并保存,采用“Cite Space V5.7.R4.64bit”软件对保存文献进行图谱绘制与分析[12]。
1.3 知识图谱分析指标
阅读“CNKI”图谱时,“圆点”代表关键词,“圆点”间连线越粗表示各关键词之间共现次数越多,“圆点”面积越大代表关键词出现频次越高。阅读“Cite Space V”图谱时,时间分区为1,图谱中节点表示每个国家(地区)或关键词,节点面积越大代表每个国家(地区)发文频次或关键词出现频次越高,节点间连线的粗细表示合作关系或共现关系强弱。中心性是衡量节点在图谱网络中重要性的关键指标,其数值大小表示与其他节点联系的紧密程度[13]。
2 研究结果与分析
2.1 国内关于运动调控肌肉、肝脏、脂肪的运动因子的研究进展
2.1.1 国内关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的发文量分布
在“CKNI”数据库中分析检索结果,得到出版年发文情况如图1所示。我国在运动调控肌肉、肝脏、脂肪的运动因子相关研究中的首篇文献为孙佛晓等于2004年在《中国临床康复》杂志发表的《运动和细胞因子》。该文综述了细胞因子的分子生物学特性、运动中细胞因子的变化特点及运动调控细胞因子水平变化的可能机制,证实单核细胞、氧自由基、内毒素血症及肌肉损伤与运动中及运动后细胞因子水平变化密切相关[14]。2004—2020年间运动调控肌肉、肝脏、脂肪的运动因子的相关研究共发文166篇,年发文总体呈缓慢上升趋势,其中2020年发文量最多(19篇)。

图1 国内关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的发文量统计结果
2.1.2 国内关于运动调控肌肉、肝脏、脂肪的运动因子的研究热点
关键词是研究内容的核心及凝练,其出现频次越多表示相关研究内容为此领域的研究热点[15]。在“CNKI”可视化分析功能中设置出现频次为“10”,得到国内关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的关键词共现图谱(见图2)。由图2可知,在共现强度方面“胰岛素抵抗(Insulin resistance,IR)”与“脂肪组织”之间共现强度最强,共现次数为13次。其他关键词共现强度相对较弱,共现次数均小于10次。在出现频次方面IR“圆点”面积最大,出现频次为36次;有氧运动出现频次位列第2(26次);脂肪组织(20次)、运动训练(19次)、跑台运动(18次)和大鼠骨骼肌(17次)等关键词“圆点”面积相当,出现频次次之。由图2可知,当前国内运动调控肌肉、肝脏、脂肪的运动因子的相关研究范畴较广,研究热点主要集中在以下3方面。
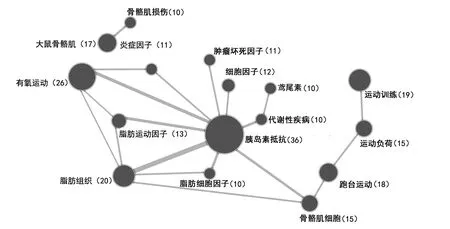
图2 国内关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的关键词共现图
2.1.2.1 热点Ⅰ:有氧运动调控脂肪运动因子改善IR
IR是指正常剂量的胰岛素产生低于其正常生物学效应的一种状态,主要表现为胰岛素作用的靶组织和靶器官葡萄糖摄取能力下降,IR通常与心血管疾病(Cardiovascular disease,CVD)、肥胖、癌症和2型糖尿病(Type 2 diabetes mellitus,T2DM)等疾病的发生发展密切相关[16]。有研究发现,有氧运动可显著降低肥胖青少年血清IL-1、IL-6及肿瘤坏死因子-α(Tumor necrosis factor,TNF-α)水平,改善肥胖青少年脂肪堆积及IR[17]。动物实验证实,有氧运动可显著上调高脂饮食诱导的IR大鼠肝脏锌-α2-糖蛋白和过氧化物酶体增殖物激活受体γ辅激活因子-1α(Peroxisome proliferator-ac-tivated receptor gamma coactivator,PGC-1α)表达,刺激脂肪分解,改善大鼠血脂代谢和IR状态[18]。有氧运动可显著降低老年肥胖IR大鼠血清及脂肪组织中内脏脂肪组织源性丝氨酸蛋白酶抑制剂(Visceral adipose tissue-derived serine proteaseinhibitor,VASPIN)基因及蛋白表达,改善老年肥胖大鼠IR并降低血糖[19]。此外,长期有氧运动可显著下调IR小鼠脂肪组织中TNF-α活性并上调ADPN基因表达,显著改善IR小鼠胰岛素敏感性[20]。综上可见,有氧运动可通过调控脂肪运动因子表达水平改善胰岛素敏感性。
2.1.2.2 热点Ⅱ:不同运动方式及运动负荷对肌肉、肝脏、脂肪的运动因子表达的影响
有研究证实,8周20 m/min速度的跑台运动显著升高T2DM大鼠骨骼肌脑源性神经营养因子(Brainderived neurotrophic factor,BDNF)表达,促进大鼠骨骼肌脂肪代谢,改善血脂水平;50%1RM、75%1RM、90%1RM及1RM强度负重爬梯训练可使T2DM大鼠骨骼肌核因子-κB和TNF-α表达显著下调,骨骼肌代谢提高,大鼠血糖水平明显改善[21]。与高脂安静大鼠相比,高脂饮食大鼠进行8周跑台运动干预(60%~70%VO2max)后,皮下脂肪组织中血管内皮生长因子受体2(Vascularendothelialgrowthfactorreceptor2,VEGFR2)表达显著升高,解偶联蛋白1(Uncoupling protein 1,UCP-1)表达降低,睾周脂肪组织中VEGF、VEGFR2、血小板内皮细胞黏附分子及UCP-1表达均显著降低,肾周脂肪组织中VEGF、VEGFR2及内皮细胞黏附分子表达均显著升高[22]。8周跑台运动(40 min/d,前5 d跑台速度逐渐从5 m/min增加到15 m/min;第2周,跑台速度从16 m/min增加到22 m/min,以后每周跑速增加2 m/min)显著提高T1DM大鼠海马神经生长因子表达,下调TNF-α表达,提高T1DM大鼠学习记忆能力[23]。此外,对小鼠进行8周50 min/d游泳运动或下坡跑运动干预研究,结果显示,游泳运动可显著下调T2DM小鼠股骨FGF23表达,上调脂质蛋白2(Lipocalin 2,LCN2)表达,T2DM小鼠股骨湿重显著下降;而下坡跑可显著升高小鼠股骨骨钙素、FGF23和LCN2表达,明显提高小鼠股骨和胫腓骨湿重及骨质量[24]。由此可知,不同运动方案可调控肌肉、肝脏、脂肪的运动因子差异性表达。
2.1.2.3 热点Ⅲ:肌肉、肝脏、脂肪的运动因子对代谢性疾病的调控作用
代谢性疾病包括T2DM、肥胖、CVD及代谢相关癌症等,其发病机制复杂,与遗传、环境、缺乏运动等因素有关。运动促进健康是一种系统、综合性效应,其可通过肌肉、肝脏、脂肪的运动因子实现组织器官之间相互作用,发挥健康促进效益。有研究证实,作为运动诱导分泌的细胞因子,鸢尾素可在骨骼肌、脂肪组织中广泛表达,可通过促进白色脂肪组织棕化、改善IR、提高认知功能等作用降低肥胖、T2DM、CVD和神经认知性疾病患病风险[25]。IGF-1是与胰岛素分子结构类似的多肽类物质,主要由肝脏和骨骼肌分泌,其可通过抑制氧化应激、细胞凋亡、炎症反应等病理生理过程,延缓肌肉减少症等代谢性疾病的发生发展[26]。瘦素和ADPN是白色脂肪组织分泌的脂肪运动因子,可通过调节血管稳态、降低内脏脂肪积累、改善IR、促进血管生成等功能改善CVD[27]。此外,IL-6、IL-8、IL-15、BDNF、促红细胞生成素、白血病抑制因子等运动因子在肌骨代谢异常中同样发挥关键作用[28]。综上分析,肌肉、肝脏、脂肪的运动因子与代谢性疾病发病进程密切相关。
2.2 国外关于运动调控肌肉、肝脏、脂肪的运动因子的研究进展
2.2.1 国外关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的发文量分布
通过“WoS”的分析检索结果功能得到出版年发文情况如图3所示。在纳入的相关文献中,国外关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的首篇文献为Pedersen等于2004年发表在Proceedings of the Nutrition Society。该文综述肌肉收缩时产生的肌肉运动因子IL-6具有多种生物学作用,运动中补充碳水化合物可抑制肌肉收缩时IL-6的释放,认为肌肉来源的IL-6符合运动因子的标准[4]。运动调控肌肉、肝脏、脂肪的运动因子相关研究的16年间年平均发文为39.5篇,最多为2019年(83篇)。图4显示,根据普赖斯文献增长规律的4个阶段[29],2017年应为研究的快速发展阶段,但实际并不相符,未出现文献累计数量“爆发式”增长,与文献指数增长规律有极大的差距,说明国外关于运动调控肌肉、肝脏、脂肪的运动因子的相关研究处于初始发展阶段。
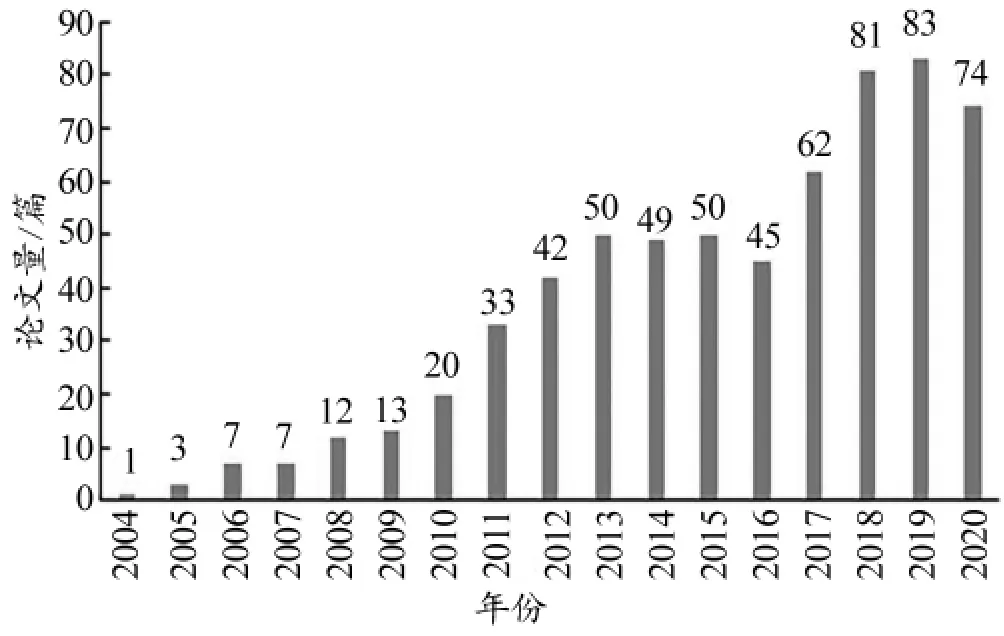
图3 国外关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的发文量统计结果
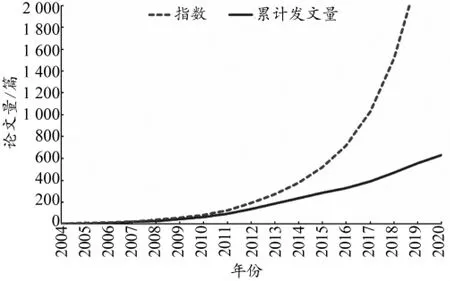
图4 文献年度累计与文献增长规律指数的拟合曲线比较
2.2.2 国外关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的国家(地区)分布
通过“Cite Space V”析出的合作网络图谱(见图5)可知,参与研究的国家(地区)有58个,但不同国家(地区)的发文量差距较大。表1所示的发文量和中心性前10位国家(地区)中,美国是图谱中最大的节点,以156篇发文量位居首位。来自美国杜克大学的Farshid发现[30],运动可上调肌肉运动因子C1q肿瘤坏死因子相关蛋白15(Complement C1q/tumor necrosis factor-related protein15,CTRP15)表达,CTRP15可将骨骼肌与肝脏、脂肪组织中的脂质稳态联系起来,以响应能量状态的改变,协调全身代谢。其次是德国、巴西发文量分列第2位、第3位。澳大利亚中心性最高,高达0.95,在整个网络结构中占据关键位置,其中澳大利亚加文医学研究所的Hjorth发现,耐力和力量联合训练可显著增加中年男性骨骼肌和血浆中巨噬细胞集落刺激因子1(Macrophage-colony stimulating factor,CSF1)基因表达,升高循环CSF1水平,并进一步鉴定CSF1是新的肌肉运动因子[31]。其次是意大利和新西兰的中心性排名分别为第2位、第3位。图5结果显示,国家(地区)间合作以澳大利亚为主导的合作相对密切,以意大利、挪威、法国等为主导的合作次之。其中,我国与意大利、芬兰、瑞典建立合作交流较多,但国家(地区)之间总体合作关系较为单一。

图5 国外关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的国家(地区)合作图
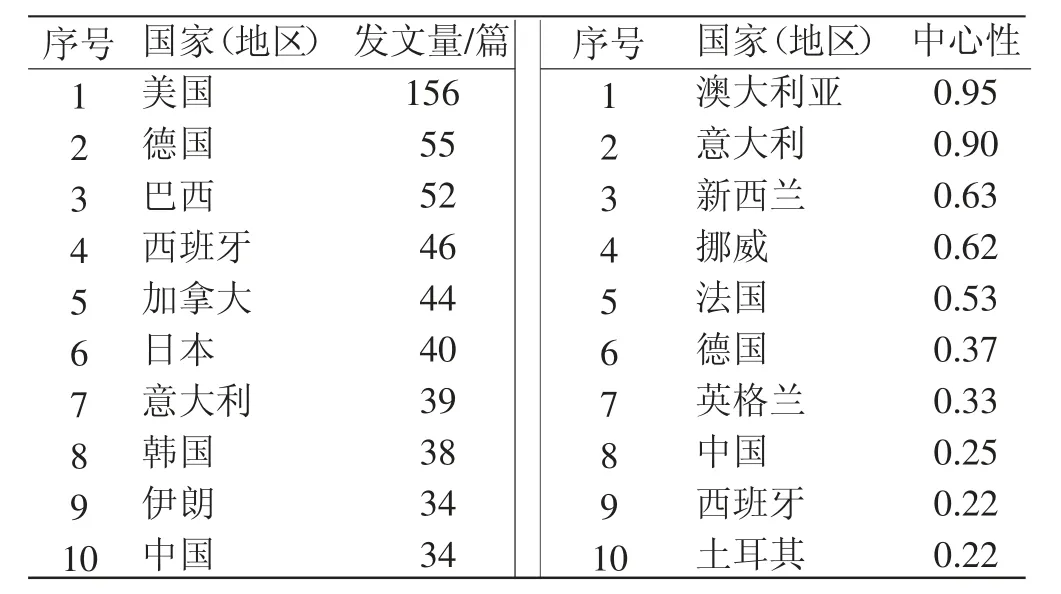
表1 国外关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的国家(地区)发文量及中心性统计结果(前10位)
2.2.3 国外关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的来源期刊分析
学术期刊是呈现研究成果的载体。通过“WoS”统计可知,运动调控肌肉、肝脏、脂肪的运动因子相关研究的632篇文献共来源于320种期刊。从发文量位居前10位的期刊可知(见表2),期刊发文量排名第1位的是Frontiers in Physiology(19篇)。该期刊影响因子为4.566(2020年)。其中,来自巴西圣卡洛斯联邦大学的Costa发现:间歇运动可显著降低肥胖大鼠血清ADPN、IL-10水平,网膜素和VASPIN水平无变化,间歇运动显著抑制肥胖大鼠体脂增加[32]。PLoS One(17篇)发文量排名第2位,影响因子为3.240(2020年)。其中,来自匈牙利佩奇大学医学院Rostás的一项关于训练干预对中年或老年肥胖患者外周瘦素水平影响的Meta分析发现,训练干预可显著降低中年或老年超重及肥胖患者的血液瘦素水平,且抗阻训练相较有氧运动更有效[33]。发文量分列第3位、第4位的期刊为American Journal of Physiology Endocrinology and Metabolism(13篇)、Archives of Physiology and Biochemistry(11篇),发文量前4位的期刊共刊载约9.66%的英文文献。

表2 国外关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的来源期刊发文量统计结果(前10位)
根据布拉德福定律,将期刊刊载的关于运动调控肌肉、肝脏、脂肪的运动因子相关研究领域的文章按数量递减顺序排列,可将该领域的期刊分为3种类型(核心区期刊、相关区期刊和非相关区期刊)[34]。计算公式为:K=2ln(eE×Y),K为核心区期刊,E为欧拉系数(E=0.577 2),Y为本领域期刊最大刊文量。本研究中Y=19,计算得出K≈7.043,按照四舍五入原则,取K值为7,即Frontiers in Physiology、PloS One等发文量排名前7位的期刊为目前运动调控肌肉、肝脏、脂肪的运动因子相关研究领域的核心区期刊。
2.2.4 国外关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的作者分析
作者发文量可衡量其学术影响力。运动调控肌肉、肝脏、脂肪的运动因子相关研究领域的作者共3 639名,发文量位居前5位的作者分别是Tufik(8篇)、Tock(7篇)、Piano(6篇)、Carnier(6篇)、Damaso(6篇),均来自巴西圣保罗联邦大学,说明该机构是此领域研究的“主力军”。Damaso是中心性(0.02)最高的作者,其于2012年发表的“Long-Term Effects of Aerobic Plus Resistance Training on the Adipokines and Neuropeptides in Nonalcoholic Fatty Liver Disease Obese Adolescents”被引频次(43次)最高。该研究发现,与有氧运动相比,有氧联合抗阻运动可显著增加非酒精性脂肪性肝病(Nonalcoholic fatty liver disease,NAFLD)肥胖青少年血液中ADPN、瘦素水平,并显著下调黑色素浓缩激素浓度,改善炎症生物标志物并降低NAFLD肥胖青少年的促食欲神经肽浓度,并首次展示了有氧联合抗阻运动方案在长期跨学科治疗中的积极作用[35]。同时,作者间注重团体合作研究,以巴西圣保罗联邦大学Tufik和Tock为核心的研究团体,主要研究方向为多学科联合干预对青少年肥胖生物标志物及细胞因子指标影响。以不列颠哥伦比亚大学的Campbell为核心的研究团体主要开展运动对绝经妇女生理指标、运动因子和激素调节等研究。以德国糖尿病研究中心Eckardt为核心的团队致力于人体骨骼肌原代细胞释放的新型运动因子鉴定、验证及应用研究。同时,以丹麦哥本哈根医院的Pedersen为代表的高发文量独立作者也广泛存在。分析结果显示,运动调控肌肉、肝脏、脂肪的运动因子的相关研究呈现大集中、小分散的合作关系。
2.2.5 国外关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的前沿分析
突现词是指某一时间段内频率变化显著的关键词,突现词分析可反映出该领域的研究前沿[36]。利用“Cite Space V”软件关键词突发性探测功能分析出运动调控肌肉、肝脏、脂肪的运动因子相关研究的突现词共有18个(见表3),其中,2018—2020年突现强度前3位的突现词分别为:激活(4.9293)、鸢尾素(4.6965)、生物标志物(4.207 6),本研究对该3个激增显著的突现词进行分析。
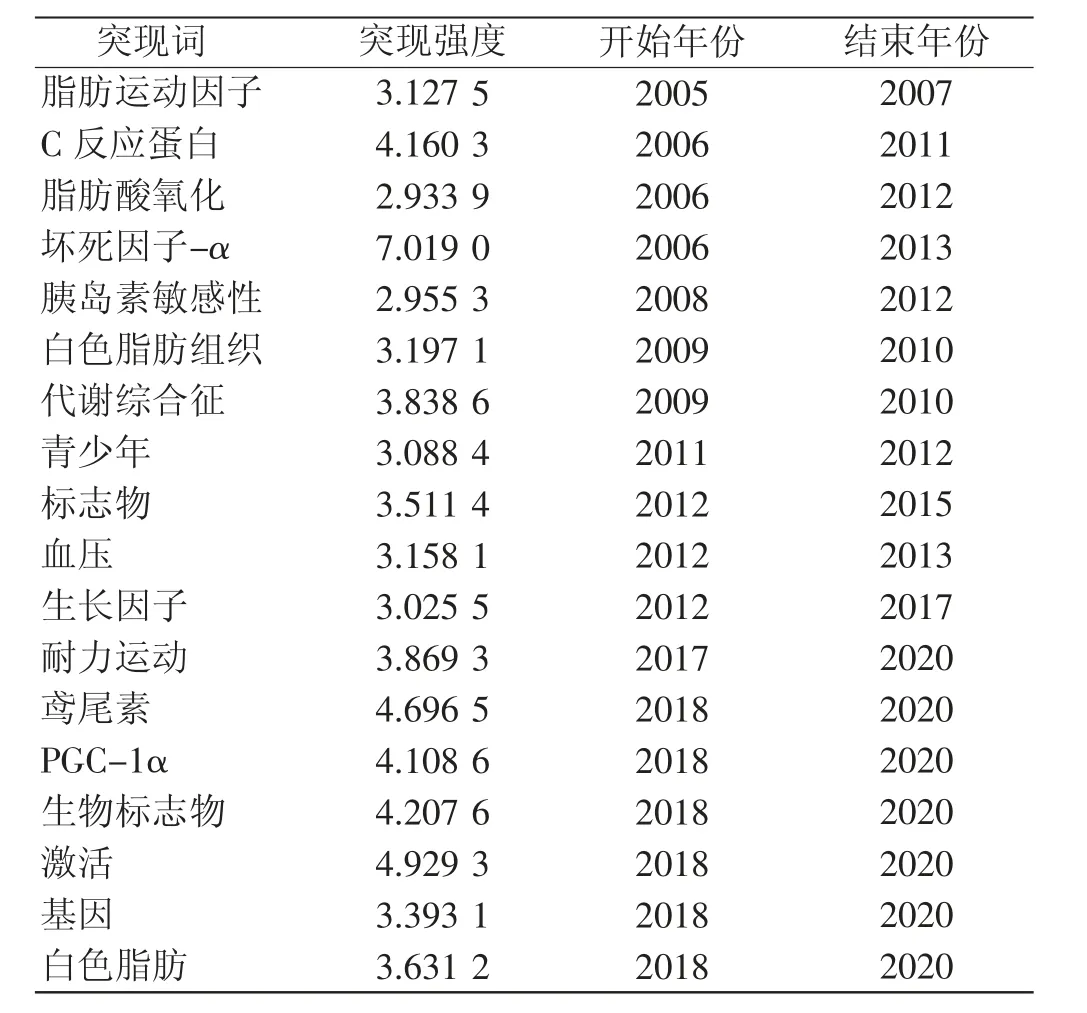
表3 国外关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的突现词统计结果
2.2.5.1 激活
研究证实,肌肉、肝脏、脂肪的运动因子可通过激活信号通路与疾病发生关联,进而发挥关键作用[37]。研究发现,脂肪运动因子CTRP3通过激活腺苷酸活化蛋白激酶(AMP-activatedproteinkinase,AMPK)/PGC-1α通路和转化生长因子-β激活激酶1/c-Jun氨基末端激酶轴,提高沉默信息调节因子1(Silent information regulator 1,SIRT1)表达水平,改善心肌功能,抑制心脏发生病变[38]。肝脏运动因子FGF21能够激活Ca2+/Ca2+调蛋白依赖性蛋白激酶/AMPKα和细胞外信号调节激酶/p38丝裂原活化蛋白激酶/AMPK信号通路,显著抑制氧化应激,增强主动脉内皮依赖性血管舒张,进而改善小鼠主动脉内皮功能障碍[39]。另有研究证实,运动可介导肌肉、肝脏、脂肪的运动因子相关信号通路干预疾病进程。运动训练可显著增加与长寿相关的AMPK/SIRT1/PGC-1α信号通路和脑IGF-1/磷酸化磷脂酰肌醇3-激酶(phosphatidylino-sitol 3-kinase,PI3K)/蛋白激酶B(protein kinase B,Akt)的存活通路,减少衰老引起的脑细胞凋亡和炎症信号活动,还可增强海马体的存活通路,为衰老大鼠改善认知障碍提供新的干预方式[40]。有氧运动可显著增加自发性高血压大鼠主动脉中胰岛素受体、IGF-1R、胰岛素受体底物-1(Insulin receptor substrate-1,IRS-1)和内皮型一氧化氮合酶(Endothelial NOS,eNOS)的蛋白水平,改善内皮依赖性胰岛素/IGF-1介导的血管舒张,表明其部分机制是通过有氧训练促进PI3K和eNOS激活及提高IGF-1R、IRS-1和eNOS的蛋白水平[41]。综上可见,运动可激活肌肉、肝脏、脂肪的运动因子相关信号通路,发挥远端调节作用。
2.2.5.2 鸢尾素
Boström等于2012年发现并报道:小鼠长期运动训练可使肌肉中的PGC-1α表达显著升高,PGC-1α可刺激靶基因Ⅲ型纤维蛋白结构域结合蛋白5(Fibronectin typeⅢdomain containing 5,FNDC5)表达增加,生成FNDC5代谢物Ⅲ型纤连蛋白水解后的多肽片段,该运动因子被称为鸢尾素[42]。鸢尾素由肌肉、脂肪等组织合成与分泌,可使白色脂肪组织转化成棕色脂肪,增加产热,促进能量代谢、改善IR、参与骨代谢、改善脑功能和提高认知能力[42-48]。研究表明,通过对心肌梗死小鼠进行抗阻运动、有氧运动、振动运动及电刺激干预,发现不同类型的运动和骨骼肌电刺激干预均能显著上调心肌梗死小鼠心肌鸢尾素/FNDC5表达,促进线粒体自噬,改善心功能。其中,抗阻运动通过激活FNDC5/鸢尾素-PTEN诱导推定激酶1/人帕金森蛋白2-微管相关蛋白1轻链3-Ⅱ/核孔蛋白62通路,可调节线粒体自噬和抑制氧化应激,改善心脏功能[49]。游泳运动可显著增加高脂饮食大鼠血清鸢尾素水平,减少高脂饮食大鼠体脂量[50]。此外,有氧运动可上调阿尔兹海默症小鼠大脑鸢尾素水平,降低小鼠焦虑水平[51]。综上可知,不同运动方式可调控鸢尾素水平,降低疾病危险因素。
2.2.5.3生物标志物
生物标志物是指揭示疾病特征、状态或进展的物质,划分为前因型、筛选型、诊断型、分期型和预后型5种[52]。临床研究证实,获得性、部分性脂肪营养不良(Barraquer-Simons syndrome,BSS)患者血清及萎缩脂肪组织中降脂蛋白水平显著升高,且与患者年龄密切相关。研究表明,降脂蛋白通过促进脂肪组织环境中不受限制的局部补体系统激活,成为参与BSS病理生理学的可靠诊断生物标志物[53]。与健康者相比,乳腺癌和胃癌患者血清趋化素水平显著增加,证实趋化素可作为癌症患者预后不良的独立预测因子[54-55]。T2DM受试者的血浆肌连接蛋白浓度显著升高,与受试者腰臀比、体脂百分比、甘油三酯、空腹血糖、葡萄糖超负荷后2 h血糖、空腹胰岛素、HbA1C和IR指数呈正相关,与胰岛素敏感性指数呈负相关,由此推断,肌连接蛋白可能是预测糖尿病前期和糖尿病发展的预测指标[56]。T2DM患者血浆脂肪酸结合蛋白1(Fattyacid-bindingprotein 1,FABP1)和FABP2浓度升高与糖尿病肾病独立且显著相关,证实肝脏运动因子FABP1和FABP2可能是糖尿病肾病的新型生物标志物[57]。综上可知,肌肉、肝脏、脂肪的运动因子可作为判断疾病发生发展的生物标志物。
2.2.6 国外运动调控肌肉、肝脏、脂肪的运动因子相关研究的热点分析
利用“CiteSpace V”软件时间线功能可分析出运动调控肌肉、肝脏、脂肪的运动因子相关研究领域的聚类演变及研究热点[58](见图6)。根据包含关键词多少划分,时间线视图中共生成10个聚类标签,此聚类模块值(Q=0.203 3,S=0.851 6>0.7)表明聚类具有较高的可信性[12]。由于聚类标签不能直观展示出各个聚类节点数、研究关键词、覆盖值等重要信息,本研究对相关信息进行了简要归纳(见表4)。根据聚类名称及聚类内容的不同,本研究将关键词分为3大聚类研究群进行分析。

表4 国外关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的关键词聚类结果

图6 国外关于运动调控肌肉、肝脏、脂肪的运动因子相关研究的时间线视图
2.2.6.1 聚类群Ⅰ:运动调控肌肉、肝脏、脂肪的运动因子对肥胖的影响研究
聚类群Ⅰ包括:聚类#0、#6和#8。肥胖是由遗传、环境等多种因素引起人体脂肪过量堆积、脂肪组织增多、脂肪比例异常的一种不健康状态。瘦素主要是由脂肪细胞合成分泌的一种肽类激素,作用于下丘脑弓状核,通过神经—内分泌轴对免疫、神经、生殖等系统发挥重要保护作用[59]。研究证实,肥胖患者常常伴有瘦素抵抗现象[60]。综上可知,减轻瘦素抵抗对治疗肥胖及其相关疾病具有重要意义。研究发现,有氧结合抗阻运动可显著上调肥胖女性血液瘦素和ADPN水平,明显改善血糖水平和胰岛素敏感性,降低肥胖女性体脂率、体重和腰围[61]。运动结合饮食干预可显著降低肥胖儿童血清瘦素水平,缓解瘦素抵抗,显著升高鸢尾素水平,降低体脂及体重,改善相关人体测量参数和代谢参数[62]。这说明运动可显著提高瘦素的表达水平,改善肥胖。
TNF-α是肿瘤坏死因子家族的一员,主要由激活的单核细胞与巨噬细胞分泌,在中枢神经系统中由小胶质细胞、星形细胞、神经元等产生[63-64]。TNF-α可以通过自分泌或旁分泌方式作用于脂肪细胞,具有防止脂肪堆积和提高脂肪代谢等作用[65]。研究证实,运动可显著下调超重或肥胖女性血清TNF-α、TNF-RI和TNF-RII水平,改善肥胖引起的IR,降低肥胖受试者体重[66]。运动加饮食干预可降低肥胖患者体内TNF-α水平,减轻肥胖患者体重[67]。有氧运动显著上调超重女性血清TNF-α、IL-15、IL-18和瘦素水平,降低超重女性体重和脂肪含量[68]。上述说明,运动可通过调控TNF-α表达提高脂肪代谢。
2.2.6.2 聚类群Ⅱ:运动调控肌肉、肝脏、脂肪的运动因子对CVD的影响研究
聚类群Ⅱ包括:聚类#3、#4和#7。《中国心血管健康与疾病报告2020概要》显示,我国CVD患病人数高达3亿3000万,且预计未来10年患病率持续上升[69]。心血管代谢风险疾病包括高血压、高血脂、超重肥胖等[70]。研究证实,有氧结合抗阻运动可显著降低肥胖女性血清CTRP-3水平、视黄醇结合蛋白4水平,轻度增加CTRP-5水平,改善肥胖女性代谢综合征和IR等心脏代谢危险因素[71]。有氧运动可显著下调CVD高危人群血清细胞间黏附分子-1水平,有效预防血管内皮损伤[72]。此外,有氧运动还可提高人体组织中IGF-1水平,通过激活IGF-1R/Akt通路,降低血液胆固醇水平,降低心血管代谢危险因素[73-74]。可见运动可介导肌肉、肝脏、脂肪的运动因子改善CVD。
细胞凋亡由Kerr等于1972年首次发现,且一直是近些年的研究热点[75]。细胞凋亡是细胞特殊的死亡方式,是一种自身调控下的主动死亡过程,多种CVD发生发展过程涉及细胞凋亡。研究证实,有氧可显著增强心肌梗死小鼠FGF-21蛋白表达,致使转化生长因子β1-Smad同源物2/3-基质金属蛋白酶2/9信号通路失活,缓解心脏纤维化、氧化应激和细胞凋亡,进而改善心肌梗死小鼠心功能障碍[76]。有氧运动可提高心肌梗死小鼠肾脏中鸢尾素水平,降低心磷脂酰基转移酶1水平,激活FNDC5/鸢尾素/-AMPK-SIRT1-PG C-1α信号通路,抑制细胞凋亡,减轻心肌梗死后受损肾组织的氧化应激水平,改善心肌梗死小鼠肾功能损伤[77]。综上可知,运动可显著抑制细胞凋亡,缓解CVD进程。
2.2.6.3 聚类群Ⅲ:有氧运动调控肌肉运动因子对脑功能的影响研究
聚类群Ⅲ包括:聚类#1、#2、#5和#9。BDNF是由人类11号染色体短臂1区3带(11p13)上的BDNF基因编码的一种碱性蛋白质,是目前研究最多的参与调节成年人神经元生长和突触可塑性的肌肉运动因子[78]。研究证实,有氧运动显著增加帕金森病(Parkinson’s disease,PD)小鼠黑质纹状体中BDNF基因水平,促进慢性PD小鼠模型中黑质纹状体神经元的神经营养活性,能明显改善小鼠运动能力、平衡功能及脑细胞线粒体功能[79]。有氧运动训练能显著提高小鼠海马细胞再生率,增强BDNF基因表达水平,改善小鼠空间记忆能力,适度提高小鼠的运动表现,保护小鼠的脑功能[80]。此外,有氧运动能显著上调小鼠海马BDNF基因水平,有效增强年轻(3个月)、中年(9~12个月)和老年(18个月)小鼠海马神经可塑性和记忆功能,甚至在记忆障碍发展到晚期时也能有效地增强海马神经可塑性和记忆功能[81]。另有研究证实,有氧运动可调控肌肉运动因子表达,改善脑功能。有氧运动过程中肌肉运动因子组织蛋白酶B蛋白可通过多功能蛋白P11依赖性机制上调健康成年人海马中BDNF和双皮质素表达,改善成年人记忆功能[82]。此外,有氧运动促进神经损伤小鼠海马中的IL-6表达,导致神经元促炎细胞因子下调并抑制炎症反应,能保护小鼠的脑功能[83]。可见,有氧运动可介导肌肉运动因子改善脑功能。
3 结论
综上所述,本文借助“CNKI”可视化分析功能及“Cite Space V”软件的共现分析、突现词分析及时间线分析等知识图谱绘制功能,对2004—2020年间国内外关于运动调控肌肉、肝脏、脂肪的运动因子相关研究进行了综述,直观呈现该领域的研究现状、研究热点和研究前沿。有氧运动可调控脂肪运动因子表达改善胰岛素敏感性;不同运动方案可调控肌肉、肝脏、脂肪的运动因子差异性表达;肌肉、肝脏、脂肪的运动因子可降低代谢性疾病危险因素。运动可上调瘦素表达,调控肿瘤坏死因子-α水平,改善肥胖;介导肌肉、肝脏、脂肪的运动因子能抑制细胞凋亡,缓解CVD进程;且提高肌肉运动因子表达改善脑功能。提示:1)未来应增强运动调控肌肉、肝脏、脂肪的运动因子相关研究的深度与合作力度;2)加强肌肉、肝脏、脂肪的运动因子防治糖尿病、肥胖、心血管疾病及脑部疾病等代谢性疾病的机制研究,探索肌肉、肝脏、脂肪的运动因子最佳作用效果的确切运动方案及其作为疾病检测与预后判断的新型生物标志物,系统梳理运动调控肌肉、肝脏、脂肪的运动因子与疾病关联的相关信号通路,为今后相关研究提供崭新的视角。

