用硝酸从电解质废渣中浸出锂试验研究
马兴娟,费发源,雷占昌,马福宝,李学莲
(青海省核工业检测试验中心 青海省核工业核地质研究院,青海西宁 810016)
工业上,铝是通过冶金级氧化铝和冰晶石在电解槽内熔融电解得到的[1-4]。为提高铝电解电流效率,降低能耗,电解体系内通常需要添加氟化锂等盐[5-6],由此会产生含锂的电解质废渣,其中锂质量分数在2%左右,具有回收价值。
目前,从电解质废渣中浸出锂,通常采用硫酸[7-8],但锂回收率相对较低。试验针对某电解铝企业的电解质废渣,研究了用硝酸浸出锂,并探讨了浸出动力学,以期为电解铝企业电解质废渣中锂的综合回收提供可行方法。
1 试验部分
1.1 试验原料、试剂及仪器
电解质废渣:取自国内某铝厂,其中锂质量分数1.96%,化学组成见表1,物相组成如图1所示。电解质废渣的主要物相为氟化锂、冰晶石及氟化钙。氟化锂难溶于水,但可溶于酸。

表1 电解质废渣的化学组成 %

图1 电解质废渣的物相分析结果
主要试剂:硝酸,分析纯。
主要仪器:X射线衍射仪(X’Pert MPD型,荷兰帕纳科公司),电感耦合等离子发射光谱仪(6300型,赛默飞世尔科技公司)。
1.2 试验原理与方法
氟化锂在硝酸溶液中可以溶解,化学反应为

(1)
冰晶石也会与硝酸反应生成硝酸铝,但冰晶石与酸之间的反应不影响锂的浸出,只增加硝酸耗量。
浸出试验在玻璃三口烧瓶中进行,温度由恒温水浴控制。将电解质废渣与不同浓度硝酸溶液按一定液固体积质量比混合后,搅拌同时加热,在40~80 ℃条件下反应一段时间后,悬浮液降温并过滤。滤液稀释后采用电感耦合等离子体发射光谱仪测定锂质量浓度,计算锂浸出率。
2 试验结果与讨论
2.1 硝酸浓度对锂浸出率的影响
在温度40 ℃、液固体积质量比10 L/1 kg、浸出时间2 h条件下,用硝酸浸出锂,硝酸浓度对锂浸出率的影响试验结果如图2所示。
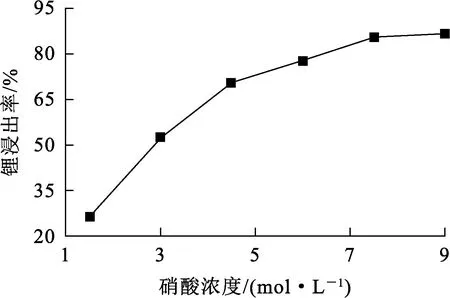
图2 硝酸浓度对锂浸出率的影响
由图2看出:随硝酸浓度增大,锂浸出率升高;硝酸浓度增大至7.5 mol/L时,锂浸出率达85.27%;之后继续增大硝酸浓度,锂浸出率略有升高,变化不大。考虑到硝酸浓度增大会增加生产成本,所以,确定硝酸浓度以7.5 mol/L为宜。
2.2 液固体积质量比对锂浸出率的影响
在温度40 ℃、硝酸浓度7.5 mol/L、浸出时间2 h条件下,液固体积质量比对锂浸出率的影响试验结果如图3所示。

图3 液固体积质量比对锂浸出率的影响
由图3看出:随液固体积质量比增大至8 L/1 kg,锂浸出率提高至84.27%;液固体积质量比继续增大,锂浸出率提高幅度不大。随液固体积质量比增大,体系黏度降低,有利于反应传质;但液固体积质量比增大会增加后续液固处理成本:综合考虑,确定液固体积质量比以8 L/1 kg为宜。
2.3 浸出温度与时间对锂浸出率的影响
在硝酸浓度7.5 mol/L、液固体积质量比8 L/1 kg 条件下,浸出温度与时间对锂浸出率的影响试验结果如图4所示。
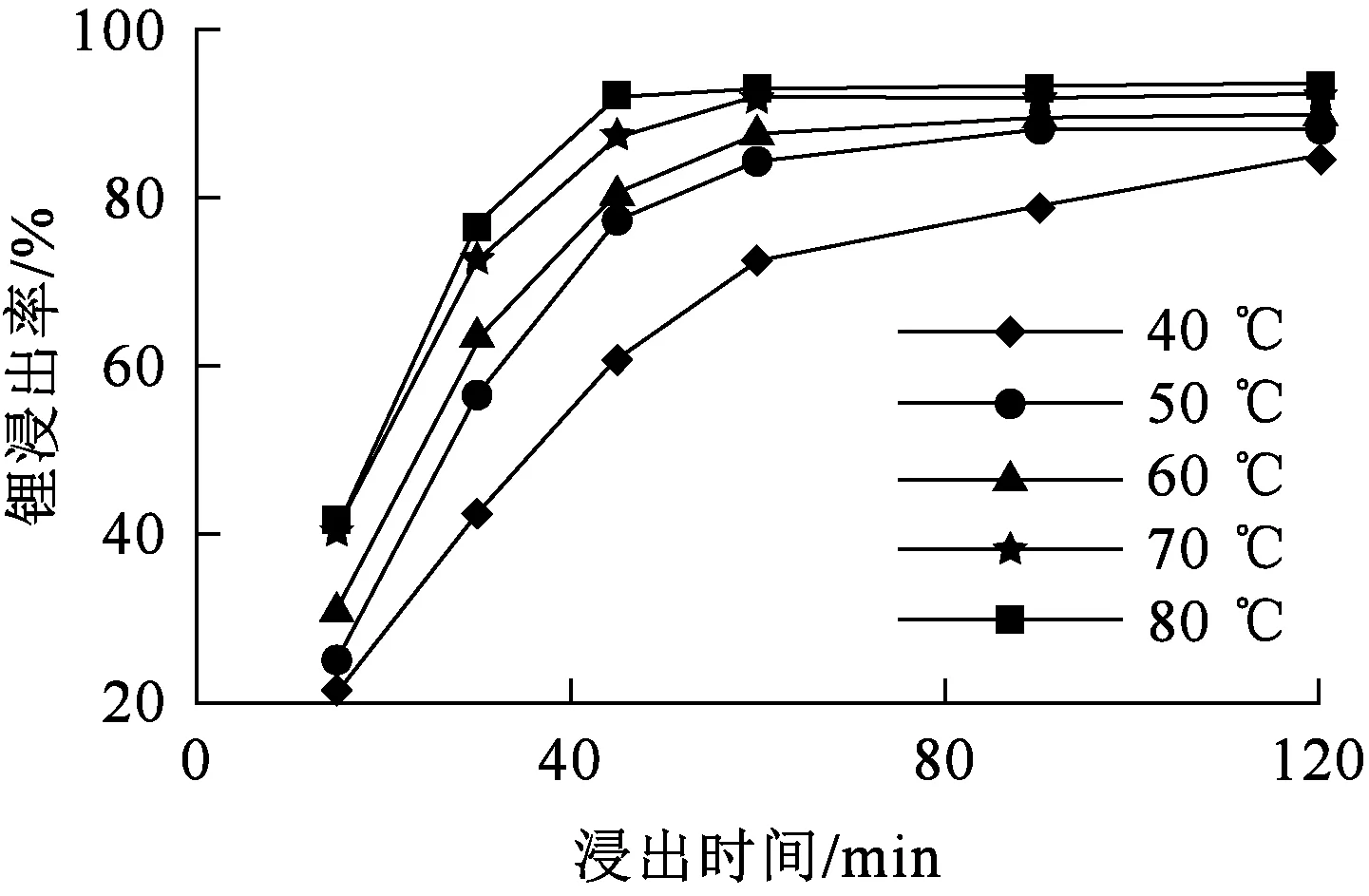
图4 浸出温度与时间对锂浸出率的影响
由图4看出:锂浸出率随反应时间延长、温度升高而升高;在反应前45 min内,随温度升高,锂浸出率迅速升高;反应60 min后,锂浸出率变化不大;而随温度升高,锂浸出率有所提高。升温有利于分子扩散,加快反应速率;但温度过高,硝酸会挥发,会增大能耗:综合考虑,确定适宜温度和浸出时间分别为70 ℃和60 min,此时锂浸出率为91.90%,浸出效果较好。
2.4 浸出动力学
硝酸浸出锂的反应属于液-固相反应,适于采用缩芯模型解释。液-固反应通常受表面化学反应控制或内扩散控制。当反应过程受内扩散控制或表面化学反应控制时,其浸出率x与反应时间t之间的关系分别见式(2)、(3)[9-13]:
(2)
(3)
反应温度为40 ℃时,对不同浸出时间条件下锂的浸出率分别用式(2)、(3)拟合,得到拟合曲线如图5所示。
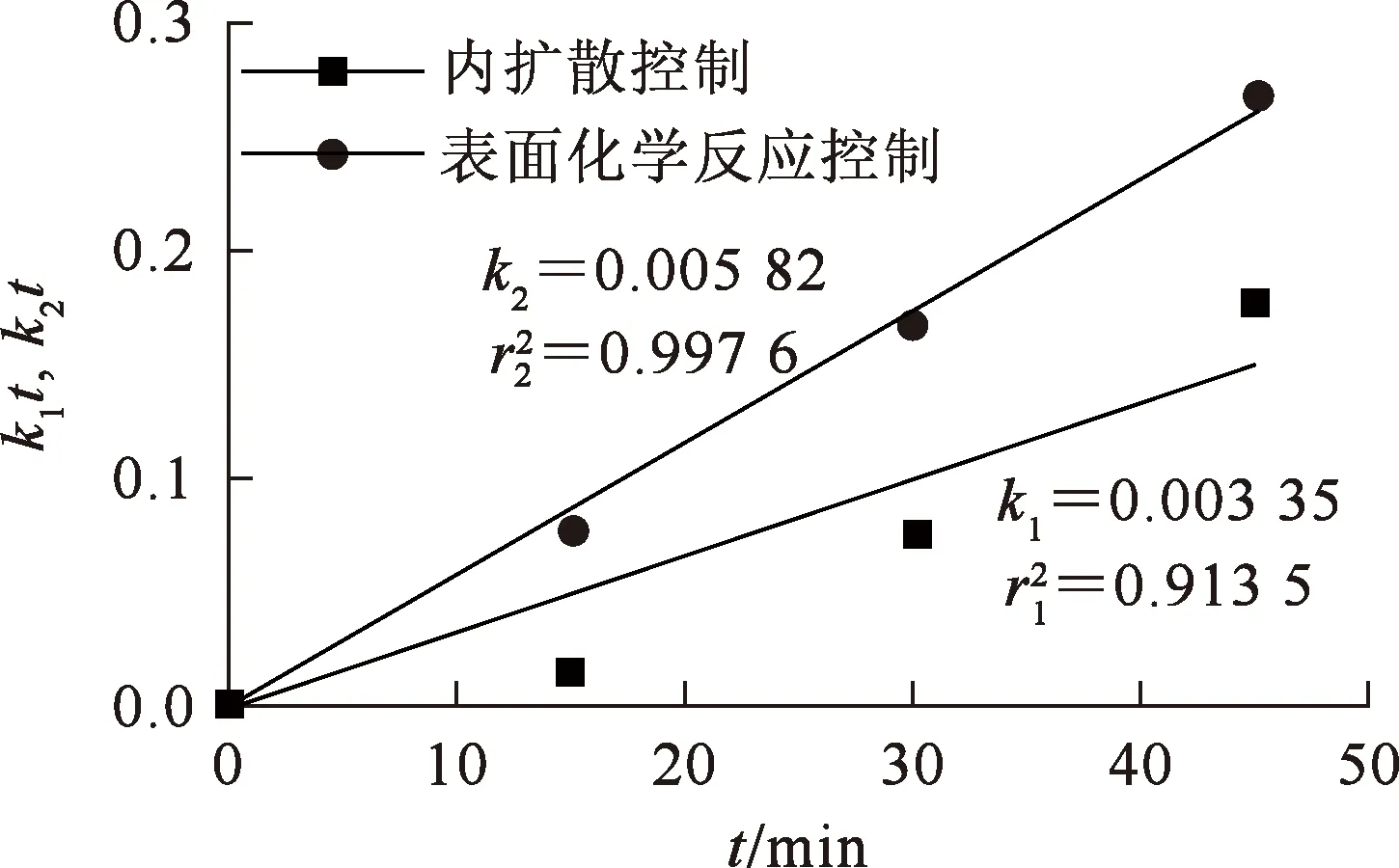
图5 表面化学反应控制和内扩散控制动力学拟合曲线
由图5看出:式(3)曲线的拟合度为0.997 6,明显高于式(2)曲线的拟合度,可以初步判定浸出反应过程受表面化学反应控制。根据Arrehenius方程:
(4)
(5)
由反应速率常数k与热力学温度T之间的关系,可以计算反应活化能Ea。根据式(3),不同温度下浸出率x与浸出时间t的拟合曲线如图6所示,图中曲线斜率为反应速率常数k。lnk与1/T的拟合曲线如图7所示。

图6 不同温度下与t之间的拟合曲线

图7 ln k与1/T之间的拟合曲线
根据曲线斜率和截距,Ea=50.3 kJ/mol,A= 0.026 8;Ea>40 kJ/mol[14],可以推断浸出过程受表面化学反应控制。因此,硝酸浸出锂的动力学方程为
(6)
3 结论
用硝酸从电解铝中产生的电解质废渣中浸出锂是可行的,适宜条件下,锂浸出率可达91.90%,浸出反应受表面化学反应控制,反应活化能为50.3 kJ/mol。

