硫酸镁型光卤石转化钾盐镁矾的过程机制与动态规律
周桓,张梦丽,郝晴,吴思,李杰,徐存兵
(1 天津科技大学化工与材料学院,天津 300457; 2 天津科技大学海洋与环境学院,天津 300457; 3 天津市卤水资源与生态化利用重点实验室,天津 300457)
引 言
新疆的罗布泊,青海的(东、西)台吉乃尔、一里坪、大浪滩、大柴旦等都属于硫酸镁亚型盐湖,是我国盐湖硫酸钾的主要生产基地[1]。硫酸镁亚型盐湖钾肥生产,包括三段式盐田成矿过程,即钠盐矿、钾混盐矿、光卤石矿,和钾矿加工过程[2]。盐田钾混矿主要由软钾镁矾(Pic)、氯化钾、七水硫酸镁(Eps)和氯化钠构成;光卤石矿主要由光卤石(Car)、氯化钾、七水硫酸镁和氯化钠构成;钾矿加工则包括钾混矿转化并浮选软钾镁矾,光卤石矿分解并浮选氯化钾,以及软钾镁矾和氯化钾合成硫酸钾等过程。硫酸镁亚型盐湖卤水成盐种类多,盐田钾矿成分复杂,导致钾矿加工存在钾盐收率低[3]和质量波动,是亟待解决的问题。
水盐体系相图是卤水化工过程分析与开发的依据[4],而硫酸镁亚型盐湖的三段式盐田过程主要是依据蒸发析盐规律[5-9]来确定的;盐田钾矿加工生产软钾镁矾工艺也通常由实验确定[10-13]。这主要是因为硫酸镁亚型盐湖卤水的蒸发析盐规律[5-9]与稳态相图[14]存在着明显差异,如钾盐析出顺序是Pic、KCl和Car,没有出现van’t Hof 平衡相图[14]上的钾盐镁矾(Kai)。这一现象早在1938 年由Kurnakov 等[15]发现,并绘制了蒸发相图(“介稳相图”),Danilov[16]在此基础上研究了俄罗斯南部盐湖的析盐规律;金作美等[17-19]采用等温蒸发法测定了15、25、35℃三套“介稳相图”数据,图1 是25℃“介稳相图”与平衡相图的比较,安东等[20]用“介稳相图”的方法研究了25℃钾盐镁矾相区特征。因蒸发析盐规律与“介稳相图”相符,而被盐湖企业和广大学者广泛认同和使用。

图1 五元体系25℃平衡相图[14]与“介稳相图”[17]比较Fig.1 Comparison between the 25℃equilibrium phase diagram[14]and“metastable phase diagram”[17]of quinary system
但事实上,尽管蒸发析盐过程没有复盐Kai,可盐田光卤石矿的XRD 显示有Kai 复盐存在。Choudhari[21]也曾研究过日晒蒸发海水苦卤生产Kai的过程。关于介稳相图的科学性Steiger 等[22]提出质疑,并指出等温蒸发实验法不能获得稳态的和严格意义上介稳态的溶解度数据;Autenrieth 等[23-27]特别研究了海水体系的介稳平衡,以更好地了解钾盐的结晶过程;Zhou 等[28-30]对蒸发成盐相区不同于平衡相图的机制进行过阐述:成盐所需推动力的差异是造成成盐相区偏离平衡相区的原因。
对于盐湖钾矿加工转化过程,因不存在蒸发推动力,其固液相平衡规律应满足平衡相图特征。但令人费解的是:硫酸镁型光卤石的分解液组成点,恰好位于“介稳相图”的KCl、Car、Eps、NaCl 四盐共存 的 液 相 点,而 不 是 平 衡 相 图 上KCl、Car、Kai、NaCl,或Car、Kai、Eps、NaCl 四盐共饱点。对于钾镁混盐转化的复杂过程,海擎宇[31]、时历杰等[32]做过硫酸镁亚型盐湖钾镁混盐成矿及转化行为的研究,但尚不足以说明上述过程。因此,为了澄清理论上的混乱,进一步开展过程机制和动力学特征的研究非常必要。
为此,本研究关注硫酸镁亚型卤水体系介稳态到平衡态转化的热力学机制和动力学特征,以一里坪盐湖盐田光卤石矿为原料,以少量加水保证光卤石不完全分解的方式,考察硫酸镁型光卤石在全混状态下的分解和转化规律,进而提出过程机制,建立预测固液系统状态及其随时间变化的动态模型,为认识盐湖钾盐转化机制、表达固相转化过程动态,改善盐湖资源利用过程提供依据。
1 实验材料和方法
为考察硫酸镁型光卤石分解及转化机制和动力学特征。本研究以一里坪盐田光卤石矿为原料,做恒温全混的不完全分解实验,检测分解与转化过程的固液相变化。
反应装置:容积2 L 的三层玻璃反应釜,黑道夫锚式搅拌桨器,使过程从加水开始就处于全混状态;温度控制:由导热油控制反应釜夹套层的温度为(25±0.5)℃。
加水量:1000 g 光卤石矿,研磨到全部通过0.3 mm 筛。按E′和A点液相组成,核算加水量分别为292 g 和234.6 g。为确保整个过程始终有未分解的光卤石,加水量为最低水量的95%,即实际加水量仅为222 g。
取样:考虑到开始时变化较快,取样时间做近似指数型递增安排,详见3.1 节;移液管抽取的浆料做等温过滤,湿固相用滤纸吸干;测定固液相组成,鉴定固相盐类物种。
分析检测[33]:测定离子K+、Mg2+、Cl-和SO2-4浓度,其中K+采用四苯硼酸钠法,Mg2+采用EDTA 法,Cl-采用硝酸银法,METTLER TOLEDO-T70 型电位滴定仪;SO2-4采用BaSO4重量法;Na+由离子电中性核算,H2O用归一法计算。根据固相样的XRD谱图确定盐类构成,设备为日本岛津-6100型X射线衍射仪。
2 过程机理与模型
2.1 硫酸镁型光卤石的成矿组成
硫酸镁亚型盐湖卤水钾盐生产的光卤石析出阶段,卤水组成变化与Na+, K+, Mg2+//Cl-, SO2-4-H2O五元体系“介稳相图”相符,伴有氯化钠和硫酸镁水合物的析出。从光卤石开始析出的(KCl、Car、Eps、NaCl)共析点,到(Car、Eps、Kai、NaCl)共析点的所析出盐类,按15~25℃的“介稳相图”数据核算光卤石矿的盐类构成:Car 63%~68%、Eps 23%~33%、NaCl 3%~8%,例如一里坪盐田光卤石矿见表1 和图2。因此,含大量硫酸镁水合物和较少氯化钠是硫酸镁亚型盐湖卤水光卤石矿(简称:硫酸镁型光卤石)的基本特征。

表1 硫酸镁型光卤石矿组成Table 1 Composition of magnesium sulfate type carnallite
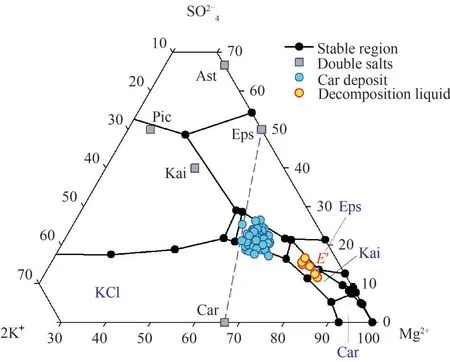
图2 硫酸镁型盐田光卤石矿组成点与分解液相点Fig.2 Composition points of magnesium sulfate type carnallite ore points and decomposition liquid
2.2 过程机理
2.2.1 光卤石分解 光卤石加适量水,氯化镁全部溶于水,氯化钾则部分溶解并形成固相,即:

硫酸镁型光卤石分解的同时,硫酸镁水合物部分溶解,分解液满足NaCl、KCl、Car 和Eps 四盐共饱和,这一液相点在五元体系平衡相图上并不存在,但在“介稳相图”上为E′点,见图1。
2.2.2 钾盐镁矾的生成机制E′点处于五元相图的钾盐镁矾相区,存在转化生成钾盐镁矾的可能。如
果出现转化,会有三种可能的转化机制,如图3 和图4。

图3 硫酸镁型光卤石转化钾盐镁矾的反应机制Fig.3 Conversion mechanism of magnesium sulfate type carnallite convert to kainite

图4 硫酸镁型光卤石转化钾盐镁矾的相图分析Fig.4 Phase diagram analysis of magnesium sulfate type carnallite convert into kainite
机制一:光卤石分解产生的氯化钾和七水硫酸镁转化为钾盐镁矾,如图3(a),该过程反应物与产物的氯化钾和硫酸镁是等量的,因此反应前后的液相和固相的干基组成不变。释放4.25 当量的水可使母液量增加。
机制二:如果固相氯化钾过量,但七水硫酸镁不足,如图3(b),液相硫酸镁与氯化钾结合形成钾盐镁矾。如图4,液相点向Kai、Car、KCl、NaCl 共饱和的稳定平衡点A移动。
机制三:硫酸镁水合物和光卤石共存,并转化为钾盐镁矾,如图3(c),释放氯化镁和水,使液相点向图4中B点方向移动,B点为Kai、Car、Eps、NaCl共饱和点。
2.3 动力学方程
根据钾盐镁矾形成的过程机制,Eps与Car共存时,液相点不动;Eps 消失后,液相点从“介稳”点E′向平衡点A转移。两个阶段钾盐镁矾生成的反应方程均为:

与反应式伴随的还有Eps、Car、KCl 的溶解,但溶解速率受限于反应式(2)的反应速率。考虑到钾盐镁矾的生成也是结晶过程,设定结晶速率的影响因素为2 个:液相离子浓度与平衡状态的差异和钾盐镁矾晶种的表面积。为此提出反应动力学方程:
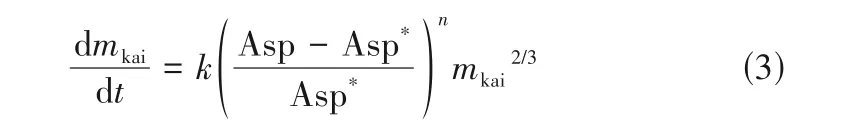

2.4 物料衡算方程
通过取样点与初始配料的物料衡算,可以确定取样时刻,液相量和固相中各盐的量。衡算方程为:
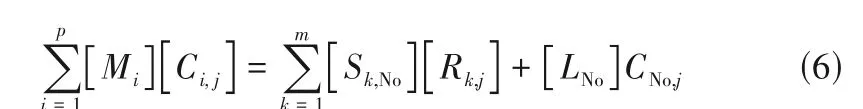
其中,j= 1~6 是组分数(5 个离子和1 个水);Mi是光卤石矿、水、底液、晶种(i=1~4)的配料量;No 为取样点序号;Ci,j,CNo,j为配料和取样点No 的液相浓度;S1~m是固相中盐(Car, Kai, Eps, KCl, NaCl)的质量;Rk,j是盐的离子计量系数;LNo是第No 点的液相质量。
3 结果与讨论
3.1 转化过程
从固液混合开始计时(t0),到确认系统达到平衡状态,共持续50 h(t4),过程取样22 组。取样点的固液相离子浓度见表2 和表3。液相离子浓度随时间的变化见图5(a),固液组成在五元相图上的位置见图5(b)。从表2数据和图5可见:t0~t1时段,液相数据波动较大;t1~t3时段,固液相离子浓度没有明显的和规律性的变化,如图5(b)液相点在E′附近几乎不动;t3~t4时段,图5(b)液相点移动并趋近KCl、Car、Kai、NaCl四盐共饱和点A。

表3 25℃光卤石矿加水转化钾盐镁矾过程的盐类组成和母液量Table 3 Salt composition and mother liquor amount in the process of kainite converted from carnallite ore at 25℃
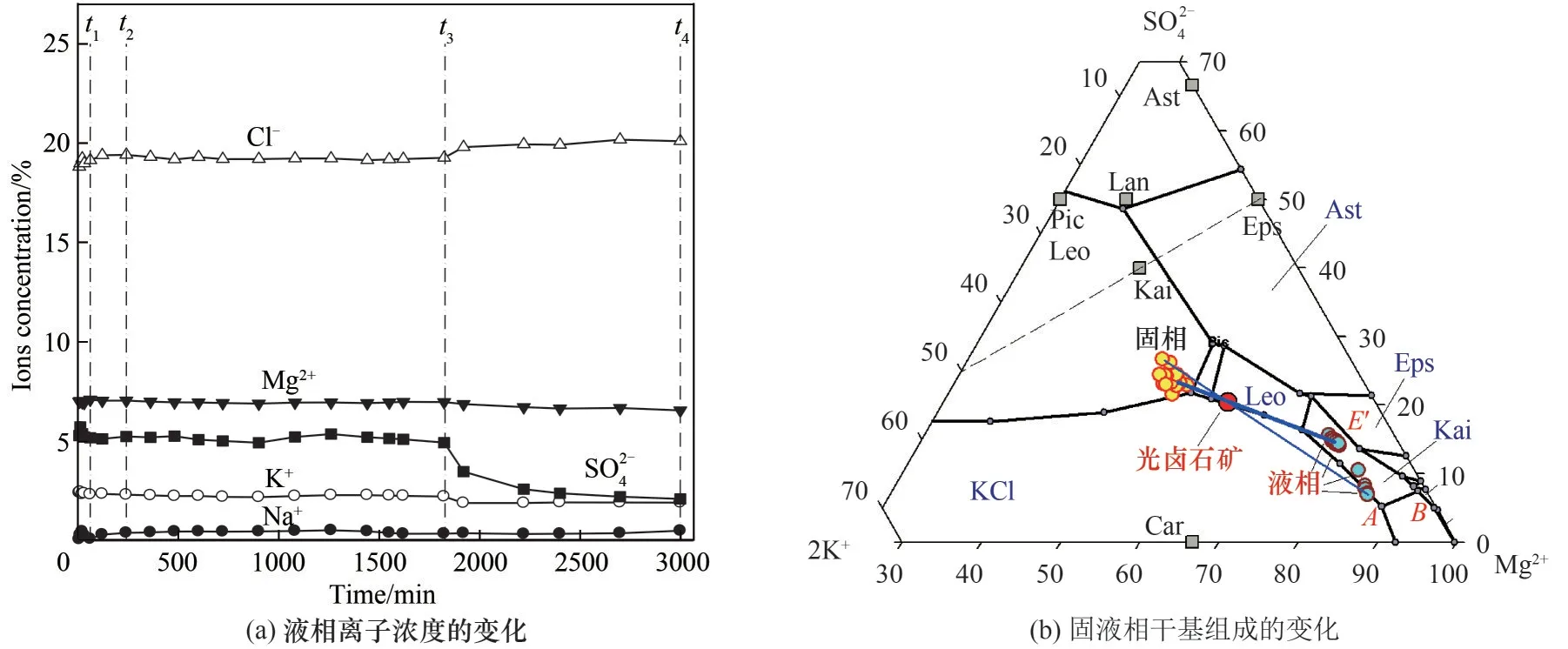
图5 硫酸镁型光卤石矿加水转化过程液相组成变化Fig.5 The liquid composition change in magnesium sulfate type carnallite ore decompose process
固液相点在t1~t3时段的不动和在t3~t4时段的移动说明:(1)KCl、Eps 和Car 共存时,液相点不变;(2)t1~t4过程有Kai 生成;(3)存在t3时刻,固相中Eps刚好全部溶解。也就是t1~t3时段符合机制一的特征;t3~t4时段符合机制二的反应特征。t3无法用实验方法准确测定,也就无法确定t1~t3时段反应的程度。
为确定t1~t3时段钾盐镁矾出现的时刻,比对时间点720、1260、1440、3000 min 的固相样品XRD 谱图(图6),判断钾盐镁矾的存在属性分别为:(a)不排除,(b)可确定,(c)很明显和(d)肯定是。如果就此判定720 min 就是钾盐镁矾出现的时刻,还是很勉强的,因为钾盐镁矾复盐的结晶度很差,尤其与氯化钠、氯化钾、七(六)水硫酸镁XRD 特征峰很强的物质共存,钾盐镁矾的XRD特征峰非常弱。
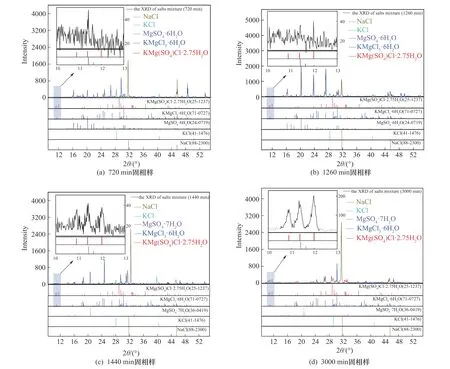
图6 光卤石矿加水转化钾盐镁矾过程的固相XRD谱图Fig.6 XRD pattern of solid phase during carnallite ore decompose process
盐量变化:在t1~t3阶段,5 个盐和液相共6 个变量,物料衡算只有5个独立方程,只能结合动力学方程,求解各点的物料衡算方程,获得每个盐的质量,进而分析盐类转化规律。t3时刻之后,各点的Eps量为零,固相盐和液相量可以直接衡算得到:如1920 min,Kai 量为215.93 g,占总固相量的44.4%,占Kai 全过程析出量的89.0%。下面的动力学研究确定t3时刻为1823.5 min,t1~t3时段钾盐镁矾析出量占总量的84.9%。
用表2数据和相图数据计算钾盐镁矾的浓度积Asp和平衡态浓度积Asp*,得到图7的Asp、Asp*随时间的变化,其中虚线是t1~t3时段离子平均浓度计算的Asp。总体特征为:t1~t3时段Asp 在均值上下呈现明显的波动,但其均值是Asp*的3.5倍;在t3之后Asp逐渐趋近于Asp*。这一结果表明,当硫酸镁固相存在时,钾盐镁矾的成盐推动力(Asp-Asp*)大体恒定,反之则消耗液相的硫酸镁直至推动力减为零。

图7 钾盐镁矾析出的过程推动力随时间的变化Fig.7 Driving force changes of potassium magnesium alum precipitation process with time

表2 25℃光卤石矿加水转化钾盐镁矾过程的固液相离子浓度Table 2 Solid and liquid ion concentrations of kainite converted from carnallite ore with water at 25℃
3.2 动态模拟
过程模型:动力学方程式(3)和物料衡算方程式(6)构成了过程的动态模型。给定配料量,积分求解过程模型,可以确定体系状态(液相量和各盐量)随时间的变化;模拟结果与实验结果的匹配可以验证动力学方程的合理性,并确定反应级数n和反应速度常数k。
约束条件:这是一个动态过程模拟的边值问题。求解两个待定参数应满足两个约束条件:(1)硫酸镁水合物消失时刻t3的预测值,应在1620~1920 min 之间;(2)钾盐镁矾累积量预测值在t3之后应与物料衡算结果相匹配。


3.3 过程分析
经过上述模拟,确定Kai生成的反应级数n和速度常数k分别为1.5和3.907×10-4mol1/3·min-1;硫酸镁水合物的消失时刻t3为第1823.5 min;t3~t4时段的钾盐镁矾析出量,预测值与测定值偏差为±1.2%。
用t2~t3时段各离子的平均浓度预测每个时间点Kai 的析出量;用离子平均浓度和实测浓度,分别对每个时间点的Car、Eps、KCl、NaCl 的盐量进行衡算;所得两组数据绘成图8。曲线为基于平均浓度的预测值,散点为实测浓度衡算值,两组的偏差分别为Kai±1.2%,Eps±2.5%,KCl±1.96%,Car±2.08%。结合图8 可见,预测值基本反映了系统状态(每个盐的量、液相量)随时间的变化规律。过程分析具体如下。
(1)加水时段(t0~t1),Car、Eps 分解和溶解量分别为330.39 g 和79.58 g,析出和溶解的KCl 分别占总钾量的45.2%和15.3%。t1~t2固液稳定时段,大体为钾盐镁矾的结晶诱导期。
(2)在t2~t3时段,硫酸镁型光卤石矿转化,但液相组成大体不变,见图5,此时固相发生着氯化钾和Eps 转化为钾盐镁矾的过程,见图8,此阶段Kai析出并逐步增加,在720 min 的固相XRD 不排除Kai 存在,Kai 析出量占全部固相量的1.05%,由于含量较低和Kai 的XRD 特征峰并不明显,到1260 min 时,Kai 量占总固相量的8.8%,XRD 可以判定其存在。
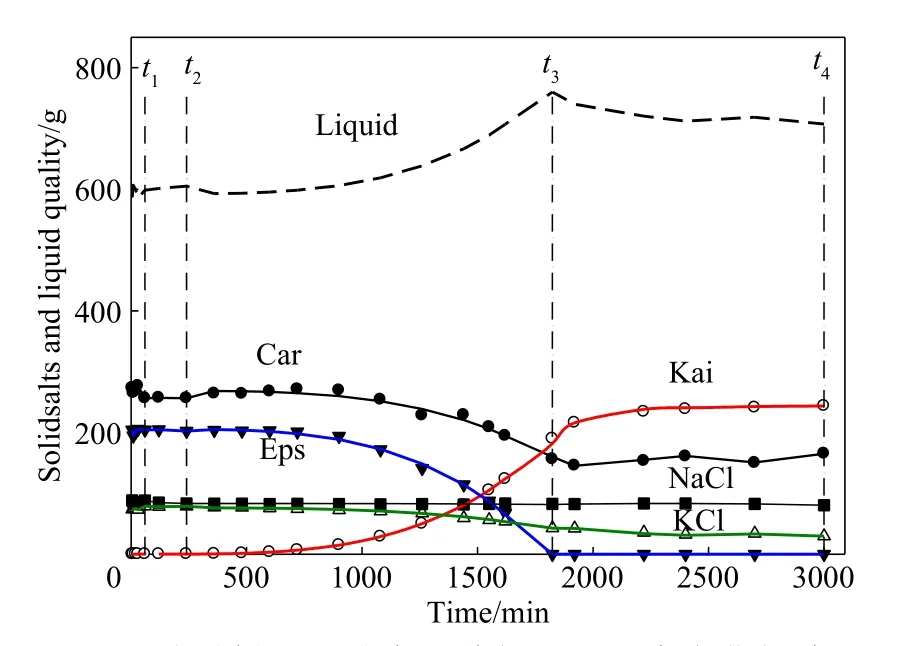
图8 硫酸镁亚型光卤石分解过程盐类变化规律Fig.8 Salts conversion behaviors in carnallite decomposition process
t2~t3时段,固液组成看似处于所谓的“介稳状态”,实则是固相转化的动态和液相的非平衡定态。
(3)Eps 消 失 的t3时 刻:Kai 已 析 出 总 量 的74.6%,Car 和KCl 固相存量分别降低到t2时刻的57.9% 和54.4%;此时光卤石分解的氯化钾,有32.6%为氯化钾结晶,42.3%转化为钾盐镁矾,其余25.1%溶于液相;硫酸镁的64.5%转化为钾盐镁矾,35.5%溶于液相。
(4)液相点移动时段(t3~t4);光卤石存量大致不动,但氯化钾降低到t2时刻的37.5%。
也就是整个转化过程,光卤石分解释放的氯化钾,仅有25.4%为氯化钾结晶态,54.9%转化为钾盐镁矾,其余19.7%溶于液相;原矿中的硫酸镁的85.6%转化为钾盐镁矾,14.4%溶于液相。
4 结 论
为了高效利用硫酸镁亚型盐湖钾资源,弄清硫酸镁型光卤石加工钾盐收率低的原因,对硫酸镁型光卤石的分解转化机制、动态规律进行了25℃不完全分解实验和过程模型化研究,得到如下结论。
(1)硫酸镁型光卤石矿特点和转化机制:硫酸镁型光卤石矿通常含有20%~33%硫酸镁水合物;在光卤石加水分解过程,硫酸镁水合物具有与氯化钾形成钾盐镁矾的热力学条件,经过3~4 h 的诱导期,钾盐镁矾会逐渐形成,在达到系统平衡后,光卤石分解的氯化钾,仅有约25%处于氯化钾结晶态,近55%转化为钾盐镁矾,其余20%则溶于分解液。
(2)对硫酸镁型光卤石矿在加水分解时所呈现的状态有了新的认知:光卤石与硫酸镁水合物共存时,固液混合物中固相和液相组成大体不变,看似处于所谓的“介稳状态”,但实际上处于氯化钾和硫酸镁水合物转化为钾盐镁矾的过程中,直到硫酸镁水合物缺失,液相点的化学组成才开始变化。
(3)钾盐镁矾的离子活度积与共饱和点活度积之差是钾盐镁矾生成的推动力,反应级数为1.5,产物存量对生成速率的影响指数为2/3,反应速率常数为3.907×10-4mol1/3·min-1。动力学方程与全组分物料方程构成了动态模型,可量化表达转化过程中任意时刻固液混合体系的状态。
这一研究掌握了硫酸镁型光卤石特性、过程机制和动态规律,在理论上澄清了关于介稳现象的认知,对盐湖钾资源利用过程的改善具有指导意义。

