不同条件下甘露醇注射液中不溶性微粒的观察研究
高小焕,何光照,张程亮
1.常州市第四人民医院,江苏213032;2.华中科技大学同济医学院附属同济医院
20%甘露醇注射液为高渗透压性组织脱水剂,经静脉输注可减轻脑水肿,降低颅内压,并可产生渗透性利尿作用[1-2]。然而,20%甘露醇注射液常可见结晶现象,在天气寒冷时尤其明显[3-8],存在结晶的注射液如果被输注到人体内,容易导致静脉炎、静脉硬化及闭塞,甚至堵塞肾小管,引起血尿或无尿,进而导致急性肾衰竭[7-11]。此外,地塞米松主要用于过敏性与自身免疫性炎症疾病,临床也常与20%甘露醇注射液配伍,起到协同增效降低颅内压的作用[7-9]。尽管笔者工作实践中未发现20%甘露醇注射液与地塞米松配伍液有析出结晶的情况,然而,有文献报道这属于配伍禁忌[5-6]。基于此,本研究观察了不同条件下20%甘露醇注射液以及其与地塞米松配伍后的不溶性微粒,为临床护理规范使用甘露醇注射液提供参考。
1 材料与方法
1.1 材料
20%甘露醇注射液(华润双鹤药业股份有限公司,规格:100 g∶500 mL,批号:Y2011281)90瓶,常温保存。地塞米松磷酸钠注射液(天津金耀集团湖北天药药业股份有限公司,规格:5 mg∶1 mL,批号:201203)30支;一次性使用无菌注射器(常州医疗器材总厂有限公司,规格:每支10 mL)120支;一次性使用精密过滤输液器(武汉智迅创源科技发展股份有限公司,规格:0.7 mm×25 mm,批号:21011010)30支;不溶性微粒检测仪(天津天河分析仪器厂,GWF-8JA型);恒温水浴锅(常州万科仪器科技有限公司,HH-S-4型)。
1.2 方法
1.2.1 判定标准
参照中华人民共和国药典可见异物检测法(通则0904)和不溶性微粒检测法(通则0903)进行可见异物检测[12],未检出可见异物视为符合质量标准。不溶性微粒检测,若每1 mL中含10 μm及10 μm以上的微粒数不超过25粒,含25 μm及25 μm以上的微粒数不超过3粒,视为符合质量标准。
1.2.2 不同温度下的20%甘露醇注射液微粒检测
取20瓶20%甘露醇注射液,先经肉眼仔细检查,确认未见明显结晶。各取10瓶分别置于25 ℃和4 ℃恒温水浴锅中静置30 min,轻轻摇匀,经75%乙醇消毒胶塞后,以10 mL一次性使用无菌注射器穿刺胶塞并抽取药液5 mL,在6 min内使用不溶性微粒检测仪测定药液不溶性微粒,每瓶在6 min内连续测4次,取第2次~第4次数值的平均值为该瓶20%甘露醇的不溶性微粒值。上述药液平行配制和测定3次,共用20%甘露醇注射液60瓶。根据测定值,分别判断是否存在25 ℃和4 ℃温度下的20%甘露醇不溶性微粒不符合药典标准,另计算每组10瓶20%甘露醇不溶性微粒值的平均值。
1.2.3 20%甘露醇与地塞米松配伍液的微粒检测
任意取10瓶20%甘露醇注射液,先经肉眼仔细检查,确认未见明显结晶,再经不溶性微粒检测仪检测符合药典标准后,再置于25 ℃恒温水浴锅中静置30 min。轻轻摇匀,经75%乙醇消毒胶塞后,以10 mL一次性使用无菌注射器抽取地塞米松磷酸钠注射液1 mL,穿刺经75%乙醇消毒的胶塞后,注入20%甘露醇注射液中得到配伍液。配伍液先经肉眼仔细检查,确认未见明显结晶,以10 mL一次性使用无菌注射器穿刺胶塞并抽取药液5 mL得到过滤前配伍液。再连接一次性精密过滤输液器,在经过滤膜过滤后的针头处取出并得到过滤后配伍液,约50 mL。各取过滤前和过滤后配伍液5 mL,在6 min内使用不溶性微粒检测仪测定配伍液不溶性微粒,每瓶在6 min内连续测4次,取第2次~第4次数值的平均值为该瓶配伍液的不溶性微粒值。上述药液平行配制和测定3次,共用20%甘露醇注射液30瓶、地塞米松磷酸钠注射液30支。根据测定值,分别判断是否存在过滤前和过滤后配伍液不溶性微粒不符合药典标准,另计算每组配伍液不溶性微粒值的平均值。
2 结果
2.1 20%甘露醇注射液在不同温度下的不溶性微粒
25 ℃时的10瓶20%甘露醇注射液肉眼检查未见明显结晶,提示20%甘露醇注射液可见异物符合质量标准;4 ℃时不符合质量标准。微粒检测显示:2种温度下20%甘露醇注射液不溶性微粒平均值见表1,数据提示20%甘露醇注射液在25 ℃时不溶性微粒符合质量标准,4 ℃时不符合质量标准。

表1 不同温度下20%甘露醇注射液中不溶性微粒平均值 单位:粒/mL
2.2 20%甘露醇注射液与地塞米松配伍液的不溶性微粒
10瓶20%甘露醇注射液肉眼检查均未见明显结晶,提示可见异物均符合质量标准。配伍液在过滤前和过滤后,肉眼均未见明显结晶,提示配伍液可见异物符合质量标准。地塞米松和20%甘露醇注射液不溶性微粒平均值见表2,数据提示20%甘露醇注射液与地塞米松配伍液在25 ℃时过滤前不符合质量标准,过滤后符合质量标准。
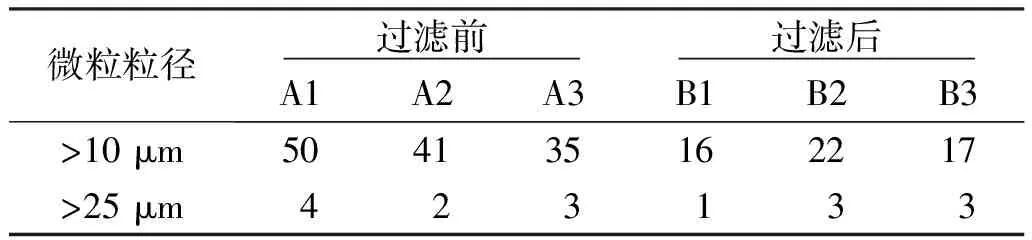
表2 20%甘露醇注射液与地塞米松配伍液在25 ℃时不溶性微粒情况 单位:粒/mL
3 讨论
3.1 不同温度下20%甘露醇注射液不溶性微粒
护士在工作中常接收到药房配送的20%甘露醇注射液药瓶内有明显的白色结晶,在病区抢救车上也有类似情况。此种情况多出现在冬季。此时,护士常将20%甘露醇注射液退回药房,或者置于热水中,直至白色结晶完全溶解后,再降至常温后给病人使用。
甘露醇是一种糖醇,易溶于水。甘露醇同多数化学物质一样,其溶解度随着温度的降低而降低。25 ℃时甘露醇饱和溶液浓度超过20%,15 ℃时,甘露醇溶液饱和浓度低于20%[7-9]。本研究中20%甘露醇注射液在25 ℃时均无色透明,药液不溶性微粒计数符合静脉输液的质量标准,提示25 ℃时的20%甘露醇注射液并非饱和溶液。4 ℃时出现少量结晶,不溶性微粒明显增加,不符合直接静脉输液的质量标准(标示装量为100 mL或以上的静脉用注射液除另有规定外,每1 mL中含≥10 μm以上的微粒数不超过25粒,含≥25 μm以上的微粒数不得超过3粒)[12]。本研究团队人员在临床工作中未发现20%甘露醇注射液有结晶情况,主要原因可能是药品的实际贮藏温度时药液并未达到过饱和状态。
甘露醇溶液化学稳定性良好,在20%甘露醇注射液生产过程中需要加热直至煮沸[13]。将有结晶析出的20%甘露醇注射液在温水中加热,不会破坏其输液稳定性。有研究显示,通过对已经析出结晶的20%甘露醇注射液采取加热促进结晶溶解方法,已经应用于临床实践[14-15]。这种方法虽然理论上可行,但这明显会影响抢救治疗的及时性,增加了护士的工作量,同时也存在安全隐患。
除了常规使用精密过滤器外,如何防止20%甘露醇注射液出现结晶应引起重视。临床发现经注射器抽吸或者输液器排液后的半量甘露醇相比于全量甘露醇更易出现结晶,在临床应用半量(125 mL)20%甘露醇注射液时不建议使用注射器以及输液器抽吸排液的方法[3]。有研究采用泡沫盒内放丝绵包裹甘露醇全封闭储存甘露醇注射液的方法降低了20%甘露醇注射液结晶发生率[4]。实际护理工作中,20%甘露醇注射液与其他输液先后序贯使用在注射器滴壶中有结晶的情况。建议20%甘露醇注射液在输注前后使用生理盐水冲管,待输液管中前一种药物排净后再输入[9]。
3.2 地塞米松和20%甘露醇配伍液不溶性微粒
开展配伍相溶性试验,可以客观反映药物配伍相溶性,为临床配伍用药提供参考依据[16]。医生习惯性将地塞米松注射液和20%甘露醇注射液配伍使用,文献中偶有报道2种药配伍后出现沉淀[5-6]。但在实际工作中,较少见到输液中析出结晶的情况,护士遵照医生医嘱执行过程中,将地塞米松注射液加入20%甘露醇注射液后常规检查确保无析出结晶的情况,再给病人用药。
本研究未发现25 ℃时20%甘露醇注射液中加入5 mg地塞米松注射液出现明显结晶的情况,与文献报道一致[7-8]。未发现文献中报道的20%甘露醇注射液和地塞米松配伍禁忌情况[5-6]。本试验中20%甘露醇注射液和地塞米松配伍液在25 ℃时均无色透明,但是,药液不溶性微粒计数并不符合药典中静脉输液的质量标准[12],提示25 ℃时加入5 mg地塞米松注射液的20%甘露醇注射液可能存在析出肉眼不能发现的细微结晶的情况。同时,输液中的不溶性微粒经过滤器后,不溶性微粒明显减少,并且符合药典中静脉输液的质量标准[12],提示20%甘露醇注射液配套使用带精密过滤器的输液器,可以很好地过滤药液中的不溶性微粒,提高了输液用药的安全性。
4 小结
使用20%甘露醇注射液前,需要肉眼观察是否有晶体产生,为避免析出结晶,建议贮存于15 ℃以上的温度环境中。为避免配伍禁忌的潜在风险,建议不要将地塞米松和20%甘露醇配伍用药。不管何种情况,护士在执行20%甘露醇输液操作时,除了加强巡视,注意观察病人的液体输液情况外,可配套使用带有精密过滤器的输液器[17],以保证输入病人体内的药液符合静脉输液质量标准。

