Al/Fe3O4/Fe2O3原位复合铝热剂的制备
石强,秦明娜,郑晓东,唐望,张彦,邱少君
(1.西安近代化学研究所,陕西 西安 710065;2.福建技术师范学院,福建 福清 350300)
随着材料制备技术的发展,纳米铝热剂的研究成为了热点。在传统铝热剂中,氧化剂与还原剂内在颗粒的分离,导致其燃爆速度慢,缓慢的能量释放速率限制了铝热剂的应用[1]。与传统铝热剂相比,纳米铝热剂的反应性是基于纳米级分子间的相互作用,不再受氧化剂和还原剂质量传递的制约[2],混合物之间的接触更加紧密,大大提高了体积能量密度[3-4]。纳米铝热剂的制备包括物理法和化学法,广泛应用的主要有超声共混法、机械球磨法和溶胶-凝胶法,其中溶胶-凝胶法是制备纳米铝热剂的优秀方法[1,5-8]。王毅等利用溶胶-凝胶法,通过引入1,2-环氧丙烷作为Fe(Ⅲ)离子的水解促进剂,实现纳米Al和无定型铁氧化物的复合,得到Fe2O3/Al纳米复合铝热剂,Fe2O3干凝胶粒子紧密地包裹着纳米Al粒子,其性能明显优于传统铝热剂[9]。高坤等也采用溶胶-凝胶法制备了Al/Fe2O3纳米铝热剂,并研究了煅烧条件对铝热剂性能的影响,经过煅烧,无定型的Fe2O3转变为γ-Fe2O3晶粒,铝热剂固-固反应的放热量提高30%,经热处理得到的Al/Fe2O3纳米铝热剂,其最高热值为1 209 J/g[2]。氧化剂和还原剂紧密结合,有利于传质,使得反应更加充分,提高铝热反应的效能,结晶态氧化剂可进一步提高铝热反应的放热量。本研究采用硫酸亚铁氨与三氯化铁,在水合肼水溶液作用下,形成羟基氧化铁。以羟基氧化铁作为前驱体,通过溶剂热反应在铝颗粒表面及铝颗粒之间原位形成结晶态的Fe3O4/Fe2O3颗粒及颗粒团聚体,与Al粒子紧密结合,得到了Al/Fe3O4/Fe2O3复合铝热剂,并研究了复合铝热剂的热性能。
1 实验部分
1.1 试剂与仪器
水合硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]、水合三氯化铁(FeCl3·6H2O)、水合肼(H2NNH2·H2O)、乙二醇(HOCH2CH2OH)均为分析纯;超细铝粉(平均粒径175 nm) 活性铝含量≥85.0%。
D/max-3A型X射线衍射仪;Quanta600FEG型场发射扫描电镜;DSC-TG热分析仪。
1.2 Al/Fe3O4/Fe2O3复合铝热剂的制备
将4 g水合肼与蒸馏水配制成50 mL水合肼溶液,得到A液。称取0.941 g FeSO4·(NH4)2SO4· 6H2O及1.081 g FeCl3·6H2O溶解于100 mL蒸馏水中,得到B液。搅拌下,将A液缓慢滴加到B液中,离心分离生成的固体,分别用蒸馏水及乙醇洗涤固体,干燥,得到FeO(OH)。
将0.25 g FeO(OH)及0.2 g铝粉加入水热釜中,并加入18 mL乙二醇,200 ℃反应24 h,冷却后,离心分离出固体,分别用蒸馏水及乙醇洗涤固体,干燥,得到Al/Fe3O4/Fe2O3铝热剂。
2 结果与讨论
2.1 FeO(OH)的XRD分析及SEM表征
由硫酸亚铁氨产生的Fe2+与三氯化铁产生的Fe3+,在碱性水合肼水溶液作用下,发生共沉淀反应,从溶液中析出固体,经分离、洗涤、干燥后,所得样品进行XRD分析,结果见图1。

图1 样品的XRD图谱Fig.1 XRD pattern of the sample
由图1可知,与PDF卡片上的数据相对比,样品衍射峰同两种晶型FeO(OH)的特征衍射峰相一致,标准卡号分别为:08-0098、29-0713,表明得到的固体样品为两种晶型FeO(OH)复合物。
采用场发射扫描电镜对得到的FeO(OH)进行了微观形貌表征,结果见图2,FeO(OH)为片状。

图2 FeO(OH)的SEM照片Fig.2 SEM photo of the FeO(OH)
2.2 Al/Fe3O4/Fe2O3复合铝热剂的表征
2.2.1 Al/Fe3O4/Fe2O3复合铝热剂的XRD分析 将羟基氧化铁[FeO(OH)]、铝粉与乙二醇加入水热釜中,经高温反应,冷却后,分离出的固体经洗涤、干燥后,进行XRD分析,结果见图3。
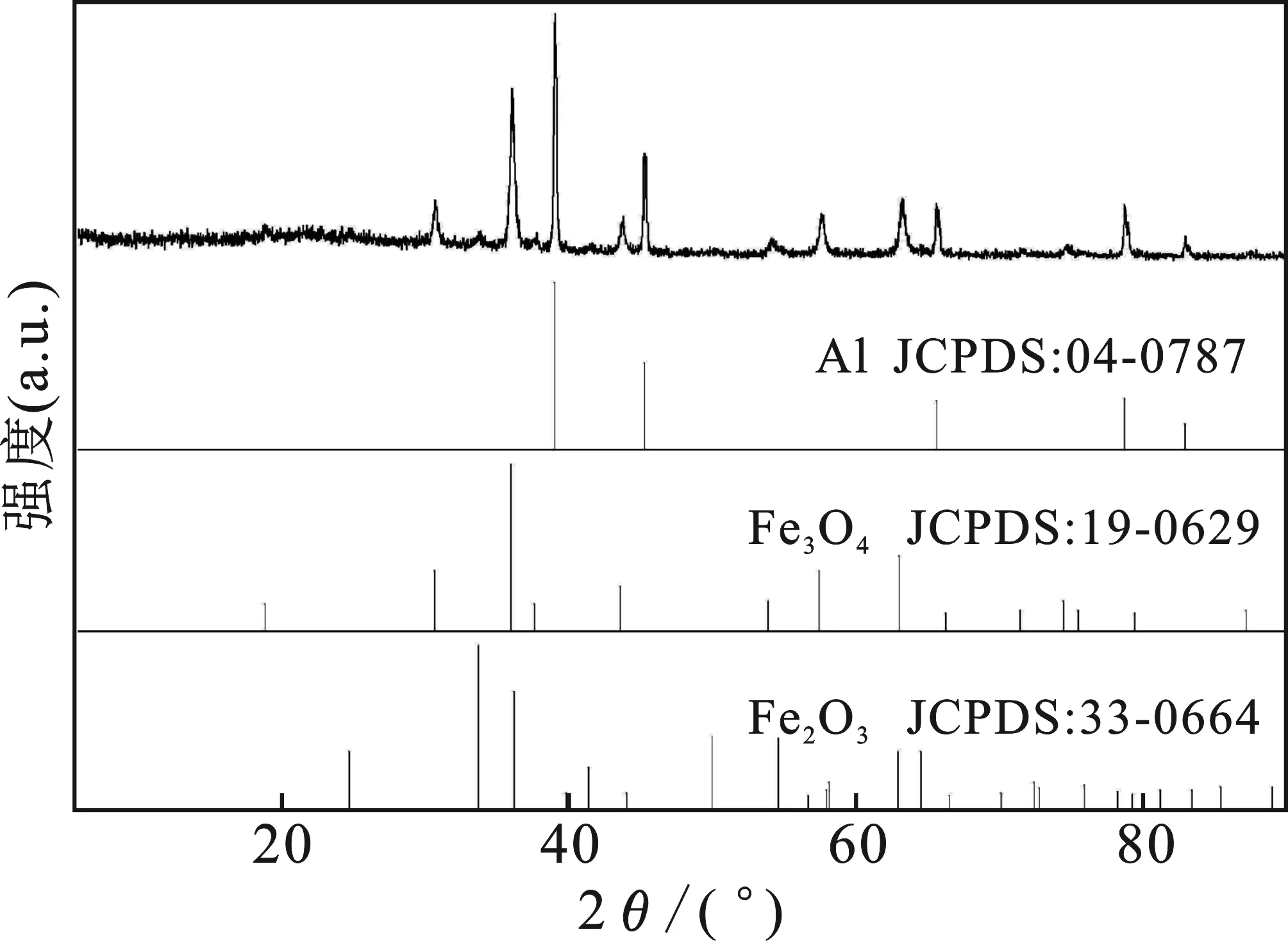
图3 复合铝热剂的XRD图谱Fig.3 XRD pattern of the thermite
由图3可知,与PDF卡片上的数据相对比,所得固体的衍射峰同Al(标准卡号为:04-0787)、 Fe3O4(标准卡号为:19-0629)及Fe203(标准卡号为:33-0664)的特征衍射峰相一致,说明所得到的固体为Al/Fe3O4/Fe2O3复合材料。
2.2.2 Al/Fe3O4/Fe2O3复合铝热剂的SEM表征及EDS分析 采用场发射扫描电镜对Al/Fe3O4/Fe2O3复合材料的微观形貌进行表征,结果见图4 。
由图4可知,有许多球状的Fe3O4/Fe2O3粒子(约40~60 nm)及其团聚体(约80~260 nm)位于Al球的表面及Al球之间,与Al球紧密结合,Al球粒子镶嵌在Fe3O4/Fe2O3颗粒之中。

图4 Al/Fe3O4/Fe2O3复合铝热剂的SEM照片Fig.4 SEM photo of Al/Fe3O4/Fe2O3 thermite
为了进一步确证复合材料的元素组成,对样品进行了EDS分析,结果见图5。
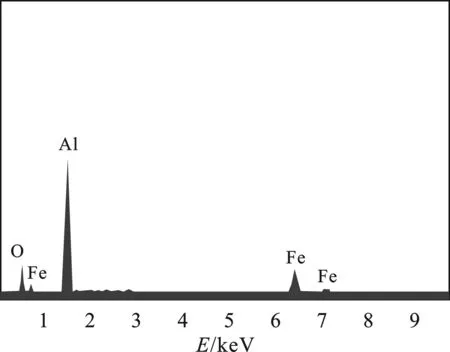
图5 复合铝热剂的EDS谱图Fig.5 EDS spectrum of the thermite
图5中的分析结果表明,复合材料中主要含有O、Fe、Al三种元素,这与XRD分析结果相一致。
2.3 Al/Fe3O4/Fe2O3复合铝热剂的热反应性能
利用DSC-TG热分析仪对Al/Fe3O4/Fe2O3复合铝热剂的热反应性能进行研究,结果见图6。

图6 复合铝热剂的DSC-TG曲线Fig.6 DSC-TG curves of the thermite
图6为Al/Fe3O4/Fe2O3在空气气氛中,以10 ℃/min 升温速率下加热的DSC-TG曲线。图6中的DSC曲线表明,在565.67 ℃和777.33 ℃分别出现两个放热峰,对应Al和氧化剂之间的反应热,总放热量为1 345.2 J/g,DSC曲线两峰之间最低点所对应的温度为658.33 ℃,与Al粉的理论熔化温度(660 ℃)基本一致。因此,可以大致判断,第1个放热峰对应固态Al与固态Fe3O4/Fe2O3发生的固-固相反应,而第2个放热峰对应液态Al与固态Fe3O4/Fe2O3发生的液-固相反应,并且固-固相反应放热峰面积明显大于液-固相反应放热峰面积,说明铝热反应以固-固相反应为主。TG曲线表明,在发生固-固相反应及液-固相反应的过程中,增重明显,可能在发生铝热反应的同时,还伴随着铝与空气气氛中的氧气及氮气反应,生成氧化铝及氮化铝。
3 结论
本文采用共沉淀法,制备出了FeO(OH)。以FeO(OH)作为前驱体,乙二醇为溶剂,通过溶剂热法,在铝粒子表面及铝粒子之间生成了结晶态纳米Fe3O4/Fe2O3复合物,Fe3O4/Fe2O3与铝粒子紧密结合,形成Al/Fe3O4/Fe2O3复合铝热剂。考察了Al/Fe3O4/Fe2O3复合铝热剂的热性能,结果表明,DSC曲线在565.67 ℃和777.33 ℃出现了两个明显的放热峰,总放热量达到1 345.2 J/g。

