异基因造血干细胞移植患者环孢素血药浓度及影响因素分析
张 潇, 回广飞, 任天舒, 许子华, 周春娟, 王艳帅, 赵 俭
1.北部战区总医院 药剂科,辽宁 沈阳 110016;2.沈阳药科大学 生命科学与生物制药学院,辽宁 沈阳 110016;3.联勤保障部队第九六八医院 呼吸消化科,辽宁 锦州 121001
异基因造血干细胞移植在治疗多种血液系统疾病方面具有显著的临床疗效,而移植物抗宿主病(graft-versus-host disease,GVHD)是异基因造血干细胞移植的并发症之一,也是患者死亡的主要原因[1]。环孢素是临床常用的免疫抑制剂,在异基因造血干细胞移植中预防GVHD具有确切的临床疗效[2]。环孢素为脂溶性药物,分子量大,其吸收受胆汁、食物和食物中脂肪含量的影响,浓度太低达不到预防作用,浓度太高易导致不良反应发生。环孢素治疗个体差异大,治疗窗窄,药物相互作用常见,移植器官、肝功能、胃肠道功能、血红细胞数量、术后时间、饮食、给药方法、药物剂型和质量、合并用药等均为影响环孢素血药浓度的因素。因此,在使用过程中密切监测环孢素血药浓度具有重要意义[3]。环孢素血药浓度监测在肝、肾移植术后的抗排异反应中已经广泛开展,全血中环孢素谷浓度和服药后2 h血药浓度的最佳范围也已达成了一定的共识[4]。然而,异基因造血干细胞移植术后环孢素治疗的目标血药浓度尚待进一步分析。本研究旨在探讨异基因造血干细胞移植患者环孢素的血药浓度及其影响因素。现报道如下。
1 资料与方法
1.1 一般资料 回顾性分析2008—2016年某医院收治的17例造血干细胞移植患者的临床资料。纳入标准:进行异基因造血干细胞移植者;移植10 d内未死亡者;预处理前无感染病灶,肝、肾功能正常者。排除标准:处于疾病危险期进行骨髓移植者;使用非清髓性预处理方案者;未进行环孢素血药浓度监测者。
1.2 治疗方法 17例患者中,7例为半相合同胞异基因移植患者,采用ATG、CD25单抗、环孢素、MMF及短疗程MTX标准五联方案预防GVHD;10例为全相合同胞异基因移植患者,采用环孢素、MMF及短疗程MTX标准三联方案预防GVHD。起始剂量均为2.5 mg/(kg·d),治疗期间根据患者血药浓度、临床缓解情况及患者耐受情况适当调整药物剂量。
1.3 环孢素浓度监测方法 取样方式:再次给药前,采静脉血2 ml,测量谷浓度。监测方法:用酶放大免疫法进行环孢素浓度监测。监测频率:初始服用环孢素时,每隔5 d监测一次环孢素血药浓度,当血药浓度异常时,更改用药剂量,随时监测血药浓度。
1.4 观察指标 观察红细胞计数、肾功能指标、肝功能指标、不良反应发生情况[5]等。按改良 Glucksberg 标准(表1)将GVHD分为Ⅰ~Ⅳ共4度,通过急性GVHD发生情况及其分级判断环孢素的临床疗效。
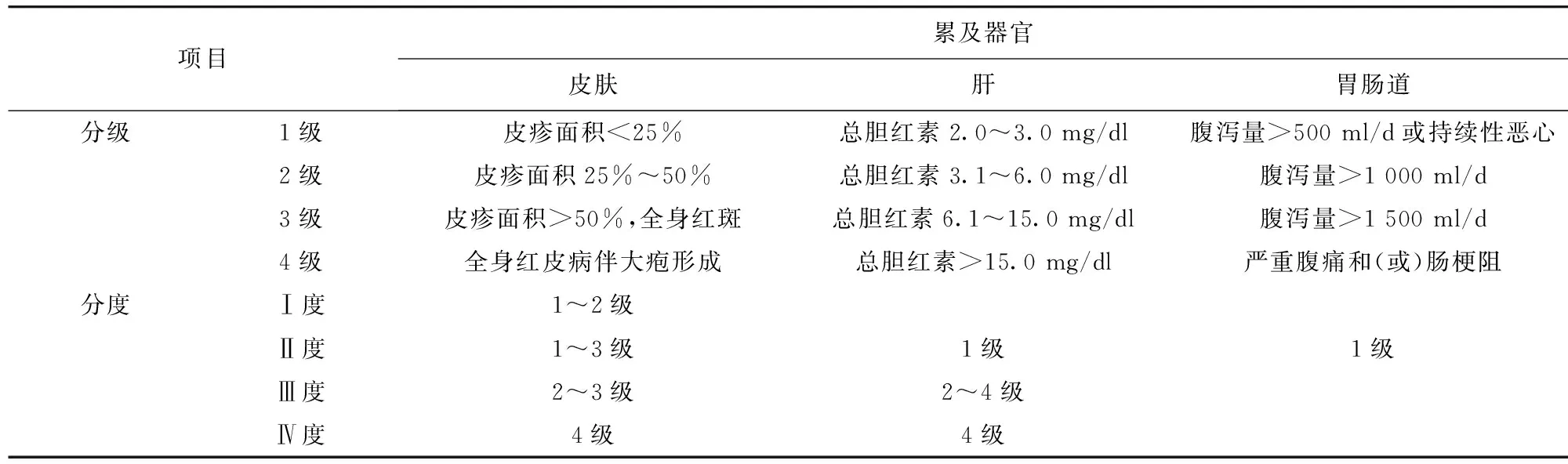
表1 急性GVHD分级
1.5 统计学方法 采用SPSS 22.0统计学软件对数据进行处理。环孢素血药浓度与不良反应发生率的相关性采用Spearman等级相关系数分析。环孢素血药浓度与红细胞、肝功等指标的相关性采用Pearson相关性分析。以P<0.05为差异有统计学意义。
2 结果
2.1 不同环孢素血药浓度患者急性GVHD发生情况 10例患者发生急性GVHD,发生率为58.8%(10/17)。血药浓度50~150 ng/ml者发生急性GVHD Ⅳ期2例(11.8%);血药浓度150~250 ng/ml者未发生急性GVHD 1例(5.9%),急性GVHD Ⅰ期2例(11.8%),急性GVHD Ⅱ期2例(11.8%),急性GVHD Ⅲ期2例(11.8%);血药浓度250~400 ng/ml者未发生急性GVHD 6例(35.3%),急性GVHD Ⅰ期1例(5.9%),急性GVHD Ⅱ期1例(5.9%)。
2.2 不同环孢素血药浓度患者不良反应发生情况 Spearmen等级相关分析结果显示,随着环孢素血药浓度的升高,不良反应发生率明显上升(P<0.05)。见表2。
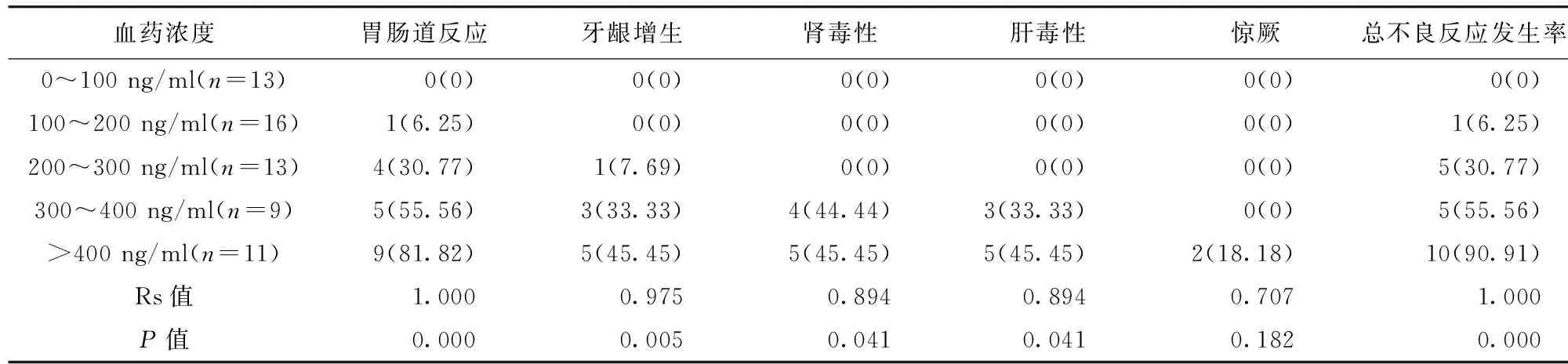
表2 不同环孢素血药浓度患者不良反应发生情况/例(百分率/%)
2.3 环孢素血药浓度影响因素分析 Pearson相关性分析结果显示,环孢素血药浓度与红细胞计数呈正相关(r=0.787,P<0.05);环孢素血药浓度与血清肌酐清除率、丙氨酸氨基转移酶、天冬氨酸转氨酶、谷氨酰转肽酶无相关性(r=0.060、-0.236、-0.076、0.006,P>0.05)。见图1。
2.4 合并用药对环孢素血药浓度的影响 甲泼尼龙、熊去氧胆酸、伊曲康唑、氟康唑、左氧氟沙星均可以使环孢素血药浓度上升。其中,氟康唑、伊曲康唑对环孢素血药浓度的影响较大(P<0.05)。见表3。
3 讨论
环孢素血药浓度监测在20世纪80年代初于临床实践中首次应用[6]。环孢素作为一种临床常用的钙调神经磷酸酶抑制剂,具有良好的免疫抑制作用,被广泛应用于异基因造血干细胞移植术后预防GVHD[7-8]。本研究纳入17例患者,共计监测血药浓度136次。其中,10例发生急性GVHD,7例未发生急性GVHD,患者血药浓度均保持在150~400 ng/ml,1例患者因GVHD死亡,1例患者出院后未进行系统监测发生严重的急性GVHD,2例发生Ⅳ期GVHD的患者血药浓度低于有效范围,血药浓度在50~150 ng/ml。王亚妮等[9]研究发现,当环孢素血药浓度<200 ng/ml时,急性GVHD的发生率高;当环孢素血药浓度>400 ng/ml时,肝肾毒性增加。本研究发现,当环孢素血药浓度在150~250 ng/ml,急性GVHD的发病率高;Spearmen等级相关分析发现,环孢素血药浓度范围在200~300 ng/ml时,不良反应的发生率较高浓度时低,可考虑将血药浓度控制在此范围内。
为减少不良反应的发生,除密切监测相关指标外,还应对不良反应做出及时的判断和处理,根据血药浓度及合并用药情况调整剂量[10]。本研究中,环孢素血药浓度与红细胞计数呈正相关。有研究报道,红细胞计数可能通过影响环孢素体内分布及其与蛋白的结合升高环孢素的血药浓度[11]。本研究中,环孢素血药浓度与其他指标变化无显著相关性,考虑可能与本研究样本量较少有关。本研究中,甲泼尼龙激素类药物和熊去氧胆酸及其衍生物类药物可以使环孢素血药浓度升高,左氧氟沙星和诺氟沙星等喹诺酮类抗菌药对环孢素血药浓度影响较小。伊曲康唑、氟康唑为三唑类抗真菌药,可以使环孢素血药浓度上升,两者对环孢素血药浓度影响均较大。有研究报道,氟康唑与环孢素联用导致重度免疫抑制致患者死亡[12]。因此,在环孢素与氟康唑联用过程中应密切监测环孢素血药浓度,一旦发现升高应立即下调剂量。伊曲康唑是通过人工合成的三唑类抗真菌药,可用于治疗侵袭性曲霉菌病,因其具有广谱抗真菌活性和良好的耐受性,在临床上被广泛使用[13]。陈苗等[14]研究表明,环孢素主要由肝、肠细胞色素酶P450(CYP3A4)和肠P-糖蛋白代谢,而三唑类抗真菌药物,包括伊曲康唑、氟康唑,可不同程度地抑制CYP3A4,导致环孢素的血浆浓度升高。此外,伊曲康唑还会抑制P-糖蛋白。本研究中,3例同时服用环孢素和伊曲康唑患者的环孢素血药浓度最高达到了600 ng/ml以上。由于伊曲康唑能使环孢素血药浓度快速升高,可考虑在环孢素与伊曲康唑同时服用时,将环孢素用药减半。
综上所述,临床治疗中可考虑将环孢素血药浓度控制在200~300 ng/ml,患者的GVHD发生率、不良反应发生率较低。本研究存在不足:本研究为回顾性研究,由于患者住院时间及住院频率不同,环孢素血药浓度监测不完全,部分患者遗漏或监测时间不准确;未能分析环孢素给药剂量与血药浓度的相关性,纳入的样本较少,随访时间较短,未完全排除一些混杂因素的影响,监测指标不全面,仍需进一步大样本、长随访时间、全面、前瞻性研究分析。

