陌上菅浸提液对斜生栅藻化感效应研究
刘汝梦,杜勇,张剑波,叶晓馨,*
1.安徽大学资源与环境工程学院,合肥 230000
2.浙江大学生命科学学院,杭州 310000
化感作用(allelopathy)是植物或微生物通过向环境中释放化学物质对其他植物或微生物生长产生促进或抑制的现象[1]。植物或微生物释放的这些化学物质被称为化感物质,由于其来源天然,具有生物降解性好、生态安全性高等特点,近年来植物释放化感物质抑制藻类生长的研究引起了国内外的广泛关注[2-3]。目前化感抑藻研究关注最多的是水生植物,包括苦草(Vallisneriaspiralis)、穗花狐尾藻(Myriophyllumverticillatum)和微眼子菜(Potamogetonmaackianus)等[4-6]。水生植物对藻类的化感效应存在强烈的种间差异性和季节性,且在同一生境中的生物有机体已经适应了该系统内的化感物质,所以在抑藻方面有一定的局限性[7]。部分陆生植物也被证实具有一定的化感抑藻效果,如大麦(Hordeumvulgare)、小麦(Triticumaestivum)等[8-10]。王家春等[11]研究了加拿大一枝黄花(Solidagocanadensis)根、茎、叶和花4种器官的水浸提液对东海原甲藻(Prorocentrundonghaiense)生长的影响,结果显示4种器官水浸提液对东海原甲藻的生长抑制率均达到90%左右。水稻分蘖枝发酵液对蛋白核小球藻(Chlorellapyrenoidosa)和斜生栅藻(Scenedesmusobliquus)的抑制率分别达到83.68%和50.90%[12]。利用大麦秸秆治理藻华是目前实际运用最为成功的陆生植物抑藻的实例。经Ball等[13]测定,大麦秸秆浸提液对铜绿微囊藻有明显抑制效果,腐烂的大麦秸秆浸提液可以显著抑制铜绿微囊藻的生长,浸提液处理后铜绿微囊藻叶绿素a(Chla)的含量仅为对照组的10%。作为陆生和水生植物过渡带的部分湿生植物既能够分泌化感物质又可对其他植物产生强烈的化感作用[14],如添加50 g·L-1香蒲(Typhaorientalis)叶浸提液12 d后,铜绿微囊藻生长抑制率高达91.37%[15]。探讨湿生植物的化感抑藻作用具有重要的研究意义。
植物化感物质作用于藻细胞的机制主要包括:抑制细胞酶活性、影响藻类光合作用、损坏细胞膜结构以及其他生理方面影响如改变细胞的呼吸作用、蛋白质合成和基因表达等[16]。酶在生物体中起着至关重要的作用,部分酶活性及功能受到化感物质的影响从而直接或间接影响生物体的生长和生理特性。Yang等[17]研究发现化感物质2-甲基乙酰乙酸乙酯(eathyl-2-methyl acetoacetate,EMA)处理三角褐指(Phaeodactylumtricornutum)6 d后,藻细胞内的抗氧化酶活性显著下降。在化感物质的作用下,藻类的光合色素也会受到影响,光合速率降低是化感物质对光合作用造成影响的重要表现。经0.65% (V∶V)水稻分蘖枝发酵液处理5 d的铜绿微囊藻Chla含量降至对照组的14.6%[12]。化感物质还可以破坏藻细胞质膜上离子通道,导致细胞内含物渗出率增加,造成细胞膜结构损伤,破坏细胞膜完整性[7]。蛋白核小球藻藻液中加入从芦苇(Phragmitescommunis)中分离的化感物质EMA后,藻细胞的离子渗出率达到细胞膜完全破坏时离子渗出率的95%以上[18]。探讨化感植物对不同藻类的选择性抑制机理有助于将化感作用有效应用于富营养化水体中的藻类控制。
陌上菅(Carexthunbergii)为莎草科苔草属多年生草本植物,是湿地消落带的常见种和优势种,在湿地植物群落构建和演替过程中起重要作用[19]。近年升金湖湿地陌上菅迅速扩增,造成湿地结构简单化,生物多样性降低。张金羽等[20]研究认为陌上菅对其他伴生禾本科植物强烈的化感作用可能是陌上菅成为升金湖消落带优势种的重要原因。探讨陌上菅的化感抑藻效应,不仅是对陌上菅的资源化利用,且扩宽了化感抑藻植物的筛选范围。斜生栅藻是淡水中极为常见的浮游绿藻,对污染物的耐性较强且繁殖快,常作为淡水水体生态常用指示物种,同时斜生栅藻也是淡水水体污染指示种之一,在水生生态系统中占有重要地位[21]。因此本文以指示物种斜生栅藻为受体,探讨陌上菅对藻类的化感效应,从氧化性角度探索其化感作用机制,为后续将陌上菅应用于其他恶性藻类治理时可能会对斜生栅藻等常见藻类的破坏提供一定的数据。
1 材料与方法(Materials and methods)
1.1 实验材料
陌上菅采自2019年6月安徽省升金湖国家自然保护区杨娥头保护点(30°20′56″ N,117°2′24″ E),取烘干至恒重的陌上菅全株于粉碎机中粉碎后过1 mm筛。在150 mL锥形瓶中加入1 g陌上菅粉末以及100 mL去离子水,使用超声波清洗机(KQ-250DE,昆山市超声仪器有限公司)浸提20 min,获得粗提液。浸提完成后将粗提液以9 000 r·min-1离心3 min,上清液用滤纸过滤至锥形瓶中,作为陌上菅浸提液原液(10 g·L-1)于4 ℃储存备用。斜生栅藻(编号FACHB-12)购自中国科学院水生生物研究所淡水藻水库,在25 ℃的BG11培养基中生长(光照度为2 000 lx),将受试生物培养至指数生长期以供使用(约6.6×106cells·mL-1)。
1.2 生物量测定
根据升金湖绿藻密度变化范围[22],设定体系中斜生栅藻的初始藻密度分别为5×105cells·mL-1和1×106cells·mL-1。在无菌条件下加入一定量先前培养的藻液,再分别取10、25和50 mL陌上菅浸提液原液,最后加入BG11培养基中使整个体系保持150 mL,陌上菅浸提液的浓度分别为0.67、1.67和3.33 g·L-1,每个处理设置3个重复,以不加任何陌上菅浸提液的藻液作为对照组,共24个处理。将锥形瓶置入培养箱中继续培养,设置光照度2 000 lx,温度为25 ℃,培养时间共持续15 d。于实验第0、5、10和15天取样测定有关参数。使用光密度法在紫外可见光分光度计(TU-1900,北京普析通用仪器有限责任公司)波长为680 nm下测定藻液的吸光度,采用细胞计数法建立生物量-吸光度的标准曲线,得光密度(y)和藻密度(x)线性方程为:y=905.98x+4.0993 (R2=0.9974),确定藻细胞密度[23]。
1.3 叶绿素测定
参照Zhang等[24]的方法,用丙酮(≥99.5%,国药集团化学试剂有限公司)提取Chla,通过紫外可见光分光度计在645 nm和663 nm处测定其吸光度,根据下列公式计算Chla含量:
Chla(mg·L-1)=13.96A663-6.88A645
1.4 抗氧化系统相关指标测定
吸取10 mL的藻液加入到离心管中,然后在4 000 r·min-1(4 ℃)条件下离心15 min,倾去上清液,然后向离心管中加入2 mL预冷的0.05 mol·L-1pH为7.8的磷酸缓冲液,使用液氮反复冻融3次,破碎液在10 000 r·min-1(4 ℃)条件下离心30 min,获得的上清液即为粗酶液,于-20 ℃储存以备进一步使用。超氧化物歧化酶(SOD)用氮蓝四唑(NBT)光化还原法测定[25],一个单位(U)的SOD被定义为50%抑制NBT光化学还原的酶量,按下列公式计算SOD活性:
SOD活性(U·cells-1) = [(A0-AS)×V]/(A0×0.5×VT×Va×C)
式中:A0为对照管吸光度;AS为样品管吸光度;V为提取液总体积(mL);VT为测定时提取液用量(mL);Va为离心的藻液体积(mL);C为藻细胞密度(cells·mL-1)。
过氧化氢酶(CAT)参照Rao等[26]的方法测定,一个单位的CAT被定义为在1 min内A240降低0.1为一个酶活性单位(U),按下列公式计算CAT活性:
CAT活性(U·cells-1) = (ΔA240×V)/(0.1×VT×1×Va×C)
ΔA240=AS0-(AS1+AS2)/2
式中:AS0为煮死酶液对照管吸光度;AS1、AS2为样品管吸光度;V为提取液总体积(mL);VT为测定时提取液用量(mL);Va为离心的藻液体积(mL);C为藻细胞密度(cells·mL-1);1为反应时间(min)。
丙二醛(MDA)含量参照Heath和Packer[27]的方法测定,根据MDA与硫代巴比妥酸(TBA)的定量反应来测定MDA的含量。在532、600和450 nm处测定吸光度,按下列公式计算MDA的含量:
MDA浓度(μmol·L-1) = 6.45×(A532-A600)-0.56×A450
然后再用μmol·(107cells)-1(藻细胞密度)表示MDA的含量。
1.5 细胞膜完整性与酯酶活性测定
斜生栅藻细胞培养15 d后,收集不同处理的藻液,参照Xiao等[28]的方法使用流式细胞仪(flow cytometry,FCM) (Cytoflex型,美国BeckmanCoulteer公司)测定了斜生栅藻藻细胞的细胞膜完整性和酯酶活性,使用66.8 mg·L-1碘化丙啶(PI) (>94%,上海易汇生物科技有限公司)溶液和10 mg·L-1荧光素二乙酸醋(FDA) (~97%,合肥巴斯夫生物科技有限公司)溶液染色15 min。氩离子激光器(激发波长480 nm)对藻细胞进行激发。采用FL2检测器(564~606 nm)检测PI染色细胞,用以评估细胞膜的完整性。数据以染色细胞百分比表示:
染色细胞(%)=(PI染色细胞的数量/FCM检测到的细胞总数量)×100
FDA的荧光用FL1检测器(515~545 nm)检测藻细胞内酯酶活性,依据荧光强度将藻细胞划分为:酯酶活性抑制群(R1)、酯酶活性正常群(R2)和酯酶活性激发群(R3),并分别统计其占总细胞的百分比。
1.6 数据处理
采用Excel 2016和SPSS 25.0 (SPSS Inc.,Chicago,IL,USA)软件对数据进行整理、统计分析,采用单因素(one-way ANOVA)和双因素(two-way ANOVA)方差分析确定不同浓度陌上菅浸提液对斜生栅藻生长及生理的影响,采用最小显著差异法(LSD)进行多重比较(α=0.05)。用Flowjo软件(Tree Star,San Carlos,CA,USA)分析计算FCM所检测到的信号值,使用Origin 2018(OriginLab Corp.,Wellesley Hills,USA)绘图。图表中数据表示为平均值±标准差。
2 结果(Results)
2.1 陌上菅浸提液对斜生栅藻生长的影响
初始藻密度和陌上菅浸提液浓度均能显著影响斜生栅藻藻细胞的密度,但它们之间的交互作用并没有显著影响(表1)。总体来看,陌上菅浸提液对斜生栅藻生长具有一定的抑制效果(图1)。在陌上菅浸提液添加的第5天,未见浸提液对斜生栅藻的密度有显著的抑制效果,甚至在初始藻密度为5×105cells·mL-1的条件下,陌上菅浸提液的添加轻微但不显著地促进了斜生栅藻的生长。然而,暴露于陌上菅浸提液10 d,与对照相比,添加了陌上菅浸提液的斜生栅藻藻密度显著降低(P<0.05),不同浓度陌上菅浸提液处理间藻密度无明显差异(P>0.05)。当实验进行到第15天,陌上菅浸提液显著抑制了斜生栅藻的生长(P<0.05)。相较对照陌上菅对斜生栅藻藻密度的最大抑制率可达59.6% (1.67 g·L-1)。在初始藻密度为1×106cells·mL-1时,与对照组相比实验前10 d陌上菅浸提液的添加虽然抑制了斜生栅藻的生长,但抑制效果并不显著(P>0.05) (图1(b))。当实验进行到第15天,陌上菅浸提液显著抑制了斜生栅藻的生长(P<0.05)。整体来看,陌上菅浓度较高时,抑制率随时间的增加而升高,浓度较低时随时间的增加先上升后降低。对照组藻密度随时间而增加,高浓度陌上菅浸提液处理下,藻密度呈单峰曲线。3.33 g·L-1陌上菅浸提液处理下,藻密度在第5天达到最大值,仅为2.51×106cells·mL-1。

图1 陌上菅浸提液对斜生栅藻藻密度的影响注:(a)初始藻浓度5×105 cells·mL-1;(b)初始藻浓度1×106 cells·mL-1;同一时间不同小写字母表示差异显著(P<0.05);下同。Fig.1 Effect of Carex thunbergii aqueous extract on the algal density of Scenedesmus obliquusNote:(a) Initial algal density at 5×105 cells·mL-1;(b) Initial algal density at 1×106 cells·mL-1;different letters indicated significant difference among different treatments in the same time at 0.05 level;the same below.
2.2 对斜生栅藻光合系统的影响
Chla可反映斜生栅藻潜在光合能力,一旦Chla的合成被抑制,细胞的生长也将受到抑制。斜生栅藻Chla的含量受初始藻密度和陌上菅浸提液浓度的影响显著,但是初始藻密度和陌上菅浸提液浓度交互作用对Chla含量没有显著的影响(表1)。由图2可知,Chla含量与藻密度的变化趋势基本保持一致。对照处理的斜生栅藻Chla含量随时间延长而增加。初始藻密度为5×105cells·mL-1时,在添加3.33 g·L-1陌上菅浸提液5 d后,Chla合成较对照显著升高(P<0.05)。然而,在暴露于陌上菅浸提液10 d后,添加了陌上菅浸提液的Chla含量均显著低于对照组(P<0.05),不同浓度陌上菅浸提液处理间藻密度无明显差异。当实验进行到第15天,3.33 g·L-1陌上菅浸提液处理下,Chla含量仅为对照组的28%。初始藻密度为1×106cells·mL-1时,在陌上菅浸提液添加的第5天,未见浸提液对斜生栅藻的Chla有显著的抑制效果。在暴露于陌上菅浸提液10 d后,与对照相比,添加了陌上菅浸提液的Chla含量显著降低。

图2 陌上菅浸提液对斜生栅藻叶绿素a含量的影响Fig. 2 Effect of Carex thunbergii aqueous extract on the chlorophyll a content of Scenedesmus obliquus

表1 不同初始藻密度和陌上菅浸提液浓度及其互作对斜生栅藻生物量和生理生化特性影响的双因素方差分析Table 1 Two-way ANOVA for the effect of different initial algal density and concentration of Carex thunbergii aqueous extract and their interaction on biomass and physiological characteristics of Scenedesmus obliquus
2.3 对斜生栅藻抗氧化酶活性的影响
陌上菅浸提液处理显著影响了斜生栅藻的抗氧化酶系统,而初始藻密度对抗氧化酶活性均不具显著作用。藻密度和陌上菅浸提液的交互作用显著影响了SOD活性但对CAT活性影响并不显著(表1)。对照处理的斜生栅藻SOD和CAT活性在整个实验期间始终保持在稳定的范围内。初始藻密度为5×105cells·mL-1时(图3(a)),在陌上菅浸提液添加的第5天,0.67 g·L-1和1.67 g·L-1浸提液显著刺激了斜生栅藻SOD活性。在暴露于陌上菅浸提液10 d,与对照组相比不同浓度浸提液处理下SOD活性显著增加,最大值可达4.6 U·(107cells)-1(3.33 g·L-1组),是对照组的4.1倍。然而,在实验第15天,不同浓度陌上菅浸提液处理下的SOD活性均有所下降,其中0.67 g·L-1陌上菅浸提液处理下SOD活性下降至与对照组同等水平。初始藻密度为1×106cells·mL-1时(图3(b)),当实验进行到第5天,1.67 g·L-1浸提液则显著刺激了斜生栅藻SOD活性。在暴露于陌上菅浸提液10 d,与对照相比,添加了陌上菅浸提液的斜生栅藻SOD活性显著增加(P<0.05)。然而,陌上菅浸提液添加第15天,SOD活性均有所下降,其中1.67 g·L-1和3.33 g·L-1浸提液处理下SOD活性下降至与对照组同等水平(P>0.05)。

图3 陌上菅浸提液对斜生栅藻超氧化物歧化酶(SOD)活性的影响Fig. 3 Effect of Carex thunbergii aqueous extract on the superoxide dismutase (SOD) activity of Scenedesmus obliquus
斜生栅藻在陌上菅浸提液的作用下CAT活性的变化如图4所示。初始藻密度为5×105cells·mL-1和初始藻密度为1×106cells·mL-1时,不同浓度陌上菅浸提液处理下斜生栅藻CAT活性变化趋势大体一致。添加0.67 g·L-1陌上菅浸提液的第5天,浸提液对斜生栅藻有明显刺激效果。然而,在暴露于陌上菅浸提液10 d,CAT活性下降至与对照组接近水平。在实验第5天,与对照组相比,添加1.67 g·L-1和3.33 g·L-1陌上菅浸提液处理的CAT活性与对照组无明显差异。第10天,1.67 g·L-1浸提液则显著刺激了斜生栅藻CAT活性,并在初始藻密度为5×105cells·mL-1时达到最大值0.27 U·(107cells)-1,是对照组的4倍。当实验进行到第15天,3.33 g·L-1陌上菅浸提液处理的CAT活性与对照组出现明显差异,显著刺激了斜生栅藻CAT活性(P<0.05)。

图4 陌上菅浸提液对斜生栅藻过氧化氢酶(CAT)活性的影响Fig. 4 Effect of Carex thunbergii aqueous extract on the catalase (CAT) activity of Scenedesmus obliquus
2.4 对斜生栅藻MDA含量的影响

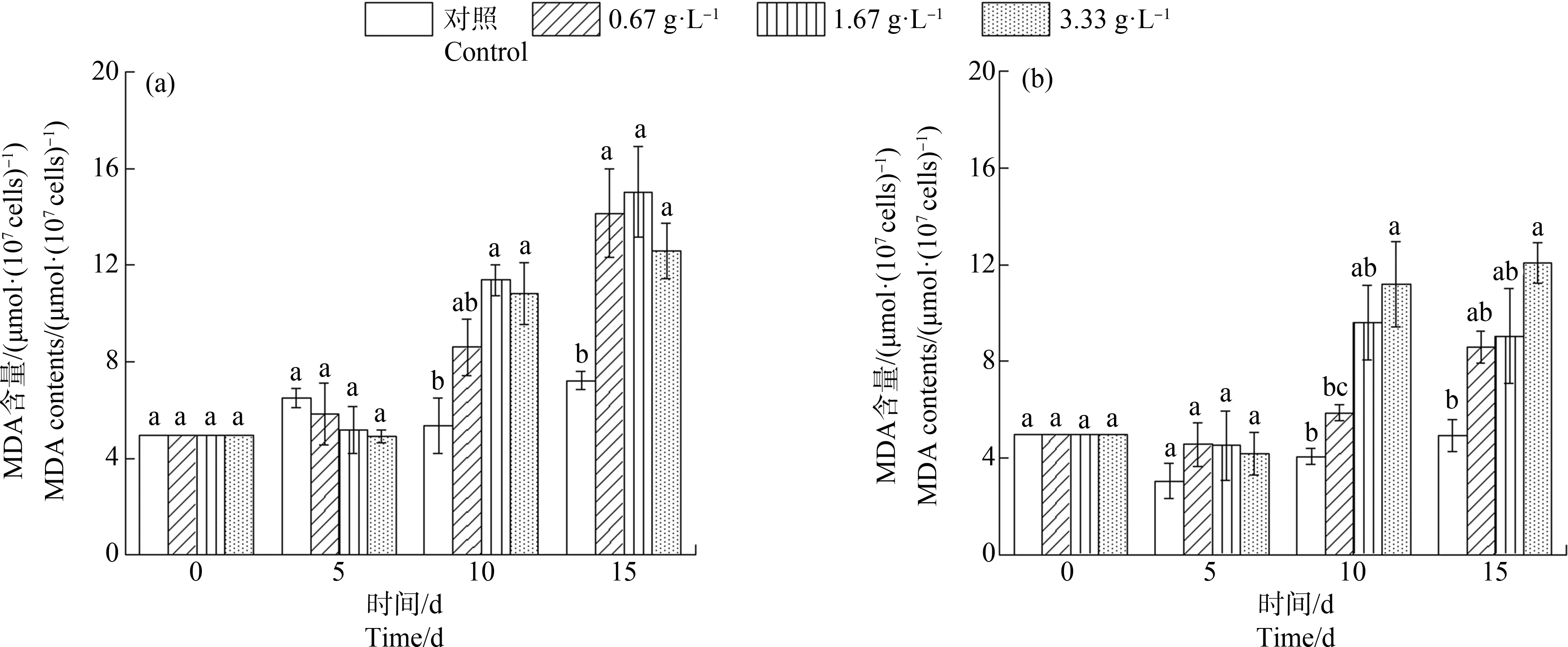
图5 陌上菅浸提液对斜生栅藻丙二醛(MDA)含量的影响Fig. 5 Effect of Carex thunbergii aqueous extract on the malondialdehyde (MDA) content of Scenedesmus obliquus
2.5 对细胞膜完整性和酯酶活性的影响
相较对照,陌上菅浸提液的添加显著增加了凋亡细胞的占比(图6)。在实验第15天,初始藻密度5×105cells·mL-1和1×106cells·mL-1时,0.67 g·L-1陌上菅浸提液处理下,凋亡细胞的占比从对照组的3%分别增加到9%和25%,1.67 g·L-1陌上菅浸提液处理下分别增加到14%和27%。陌上菅浸提液的浓度为3.33 g·L-1时,细胞的凋亡率下降至8%左右。
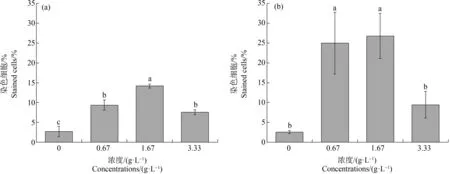
图6 陌上菅浸提液对斜生栅藻细胞膜完整性的影响Fig. 6 Effect of Carex thunbergii aqueous extract on the cell membrane integrity of Scenedesmus obliquus
根据FDA染色后的荧光强度将藻细胞分为酯酶活性抑制群(R1)、酯酶活性正常群(R2)和酯酶活性激发群(R3)。与对照组相比,陌上菅浸提液的添加导致R2群藻细胞占比显著下降。不添加陌上菅浸提液的对照处理15 d后,R2群藻细胞占比90%以上。而1.67 g·L-1陌上菅浸提液处理下,R2群占比降为77.6% (初始藻密度5×105cells·mL-1)和63.1% (1×106cells·mL-1) (图7)。陌上菅浸提液处理的R1和R3区细胞数量均有所增加。初始藻密度为5×105cells·mL-1,添加了陌上菅浸提液的R1群细胞占比显著高于对照,0.67 g·L-1陌上菅浸提液处理下,R1群细胞占比为7.2%,显著高于对照 (1.9%)。添加了陌上菅浸提液后R3群细胞占比也显著增高,皆高于10%。初始藻密度为1×106cells·mL-1时,不同处理下R1群细胞占比无显著差异,但陌上菅浸提液处理显著增加了高活性R3区细胞的比例。1.67 g·L-1陌上菅浸提液处理下R3区细胞占比最高(29.3%),显著高于对照的R3区细胞占比(4.7%)。

图7 陌上菅浸提液对斜生栅藻酯酶活性的影响注:依据荧光强度将藻细胞划分为酯酶活性抑制群(R1)、酯酶活性正常群(R2)和酯酶活性激发群(R3),图中数据为不同酯酶活性藻细胞占比。Fig.7 Effect of Carex thunbergii aqueous extract on the esterase activity of Scenedesmus obliquusNote:R1 represents a decrease in esterase activity;R2 represents esterase activity in the control cells;R3 represents an increase in esterase activity;data are expressed as the percentage of S. obliquus cells with various esterase activity.
3 讨论(Discussion)
近年来利用植物化感作用控制藻类生长被认为是极具前景的生态防治水华暴发的方法,其中湿生植物具有较强生物活性潜能,资源丰富,探讨湿生植物对藻类的化感作用及机制具有重要的现实意义[29-30]。本研究结果表明,湿生植物陌上菅的浸提液能够有效抑制斜生栅藻生长,降低其藻密度。陌上菅浸提液的浓度以及藻液的初始密度对斜生栅藻的藻密度均有显著性影响。在初始藻密度为5×105cells·mL-1时,陌上菅浸提液处理5 d对斜生栅藻有轻微的促进效应。与对照组相比,陌上菅浸提液的添加对藻密度整体呈先促后抑作用,可能是前期陌上菅浸提液的加入给藻细胞提供了营养物质刺激了藻细胞的生长,而后期陌上菅化感效应起主导作用抑制了藻细胞进一步繁殖生长。Hong等[31]也认为芦苇中重要的化感物质EMA对羊角月牙藻(Selenastrumcapricornutum)的化感作用具有多重效应,从而导致不同初始藻密度的羊角月牙藻生长和生理生化指标对EMA的响应不同。初始藻密度为1×106cells·mL-1时,不同浓度陌上菅浸提液对斜生栅藻的藻密度呈整体抑制。初始藻密度为5×105cells·mL-1时,1.67 g·L-1陌上菅浸提液处理下,抑制率在第15天达到最大值59.6%。这说明陌上菅具有有效控制藻类增长的可能性。同时,虽然与对照组相比经陌上菅浸提液处理15 d后斜生栅藻的生长受到明显抑制,但是与初始藻密度相比,处理15 d后的斜生栅藻藻密度仍然有生长的趋势,可以看出斜生栅藻对陌上菅浸提液有较强的耐受力。
Chla是蓝绿藻中的主要光合色素,是决定光合速率的重要因素。经不同浓度陌上菅浸提液处理后斜生栅藻的Chla含量显著低于对照组。与先前研究结果相似,菹草(Potamogetoncrispus)分别与普通小球藻(Chlorellavulgaris)和铜绿微囊藻共同培养6 d后,小球藻和铜绿微囊藻的Chla含量均显著降低[32]。本实验中Chla含量的降低说明由于陌上菅浸提液抑制了斜生栅藻的光合作用,进而导致其生理代谢的异常。
不同浓度陌上菅浸提液对藻细胞的损伤导致ROS增加,随之细胞脂质过氧化增加进一步加剧了细胞损伤程度。为了抵消或抵抗陌上菅浸提液带来的不良影响,藻细胞需提供能量以维持一些基因的表达以及酶和化合物的合成,进而导致藻细胞酯酶活性增加。这与以往的化感控藻实验中,如EMA的添加促使铜绿微囊藻酯酶活性增加的原理相似[38]。同时,抑制群和激发群细胞含量增加为陌上菅浸提液削弱斜生栅藻的酶促系统提供了额外的经验证据[39]。
在陌上菅浸提液添加第15天,不同浓度陌上菅浸提液对斜生栅藻的藻密度抑制均达到了40%以上,最高抑制率达到59.6%,而藻细胞凋亡率最高仅为27%。陌上菅浸提液处理后,斜生栅藻藻密度显著降低,但绝大数的藻细胞仍保持其细胞膜完整性。这说明陌上菅对斜生栅藻的抑藻效应表现为“algistatic (阻止藻种群生长)”。浸提液虽然在一定程度上能够导致少量个体藻细胞凋亡,但是主要的抑制作用是通过抑制藻细胞光合作用,改变细胞酯酶活性,诱导过氧化损伤等从而延迟了斜生栅藻种群的增长速度。同样在其他环境对蓝藻的胁迫下也得到了相似的结果,如:人面子(Dracontomelonduperreanum)落叶水浸出液、大麦秸秆腐解液和稻草提取液对铜绿微囊藻的化感作用相似,均是在一定剂量的暴露下延迟藻细胞的生长[40-42]。陌上菅浸提液化感物质控藻方式更多是减缓藻种群生长速度而非直接致死,因此导致斜生栅藻在较强外界压力下进一步进化及变异的可能性相对较小,生态安全性较好。尽管目前没有研究对陌上菅浸提液的化感物质进行分析,但是Li等[43]研究认为有机酸可能是灰化苔草中抑制铜绿微囊藻生长的主要化感物质,然而陌上菅具体的化感物质成分还需在未来的研究中进一步探讨。
本研究结果表明,陌上菅浸提液添加以及初始藻密度能够显著影响斜生栅藻生长和生理。初始藻密度影响了斜生栅藻对不同浓度浸提液的响应敏感性。随着培养时间延长,陌上菅浸提液对藻密度抑制效应提高。初始藻密度为5×105cells·mL-1时,经1.67 g·L-1陌上菅浸提液处理15 d斜生栅藻藻密度相较对照抑制率最高,可达59.6%。陌上菅浸提液可以破坏藻细胞膜完整性,直接导致细胞凋亡,初始藻密度为1×106cells·mL-1陌上菅浸提液浓度为1.67 g·L-1时细胞凋亡率最高达27%。但陌上菅对藻密度抑制效应主要是抑制藻细胞的生长和繁殖。陌上菅浸提液处理下,藻细胞叶绿素明显降低,抗氧化酶活性大幅度提升,MDA含量显著上升,酯酶活性正常的细胞占比降低。综上所述,陌上菅浸提液可通过削弱一系列生理活动从而抑制斜生栅藻种群增长,更深入的研究可为利用陌上菅进行化感抑藻提供参考依据,为陌上菅的资源化利用提供思路。

