血栓弹力图指导颅内动脉瘤患者介入围术期抗血小板治疗
王冠宇,郭腾云,王舒楠,陈立朝
(1.陆军特色医学中心神经外科,重庆 400042;2.陆军特色医学中心放射科,重庆 400042)
支架辅助弹簧圈栓塞术不仅可以使颅内动脉瘤的瘤腔闭塞,还可以降低动脉瘤的复发率,现已广泛应用于临床[1]。然而,血栓形成导致的脑缺血事件仍然是支架置入术后的首要并发症[2]。因此,如何在颅内动脉瘤支架辅助栓塞手术前后降低血栓相关脑缺血事件的发生率至关重要。目前,阿司匹林与氯吡格雷联合使用的双重抗血小板治疗是国内外广泛采用的治疗方法,其可通过抑制血小板活性来预防支架内血栓形成所导致的脑缺血事件[3]。但有研究显示,5%~12%的患者对氯吡格雷的抗血小板药物反应不理想,甚至无反应[4]。近年来,可逆结合P2Y12的抑制剂替格瑞洛成为一种可与阿司匹林联用的抗血小板药物,但替格瑞洛与氯吡格雷相比抗血小板治疗的效果如何,以及如何选择这两种药物为患者制定更合理的双重抗血小板治疗方案成为了当前支架辅助栓塞颅内动脉瘤患者围术期治疗的重要问题。
血栓弹力图是一种止血系统的即时检测测试,可通过评估凝块的形成和溶解,从而了解凝血、血小板功能、血小板—纤维蛋白原相互作用和纤维蛋白溶解情况[5]。目前血栓弹力图在心脑血管、创伤和普外科手术中被广泛应用,用于管理抗凝和抗血小板治疗[6]。本研究在支架辅助栓塞颅内动脉瘤患者的围术期使用血栓弹力图检测患者的血小板功能,指导患者双重抗血小板治疗方案,以探讨血栓弹力图对减少血栓相关脑缺血事件的应用效果。
1 资料与方法
1.1 临床资料
回顾性分析陆军特色医学中心神经外科于2018年1月至2021年12月收治的行支架辅助栓塞颅内动脉瘤的156例患者的临床资料。根据患者双重抗血小板用药情况分为氯吡格雷组(阿司匹林联用氯吡格雷)106例、替格瑞洛组(阿司匹林联用替格瑞洛)38例和药物调整组[阿司匹林联用氯吡格雷后二磷酸腺苷(adenosine diphosphate,ADP)检测不理想改为阿司匹林联用替格瑞洛]12例。纳入标准:①经DSA或CTA检查确诊为颅内动脉瘤;②入院后行颅内动脉瘤支架辅助栓塞术;③围术期予以双重抗血小板治疗并应用血栓弹力图监测血小板功能。排除标准:①未能按照要求接受双重抗血小板治疗;②未定期行血栓弹力图监测血小板功能。本研究经陆军特色医学中心伦理委员会审批[医研伦审(2018)第94号]。
1.2 方法
患者围术期口服双重抗血小板药物治疗,氯吡格雷组口服阿司匹林100 mg(每日1次)+氯吡格雷75 mg(每日1次),服用2~4 d后检测血栓弹力图;替格瑞洛组口服阿司匹林100 mg(每日1次)+替格瑞洛90 mg(每日2次),服用2~4 d后检测血栓弹力图;药物调整组为口服阿司匹林100 mg(每日1次)+氯吡格雷75 mg(每日1次),服用2~4 d后检测血栓弹力图时ADP指标不理想者改为口服阿司匹林100 mg(每日1次)+替格瑞洛90 mg(每日2次),继续服用2~4 d后再次检测血栓弹力图。
1.3 观察指标
收集3组患者血栓弹力图检测结果,包括花生四烯酸(arachidonic acid,AA)抑制率、ADP抑制率、ADP通道血凝块最大强度(MA-ADP)等,记录患者住院期间脑缺血事件发生情况。
1.4 统计学方法

2 结果
2.1 缺血事件及氯吡格雷无反应情况
156例患者中发生脑缺血事件4例,发生率为2.56%;在服用了氯吡格雷的患者(即氯吡格雷组和药物调整组)中,将血栓弹力图检测结果ADP抑制率为0的患者记为对氯吡格雷无反应,共有7例(5.93%)。
2.2 氯吡格雷组与替格瑞洛组服药情况比较
氯吡格雷组与替格瑞洛组AA抑制率比较差异无统计学意义(P>0.05);与氯吡格雷组比较,替格瑞洛组患者的ADP抑制率明显升高,MA-ADP显著降低,差异均有统计学意义(P<0.05),见表1。
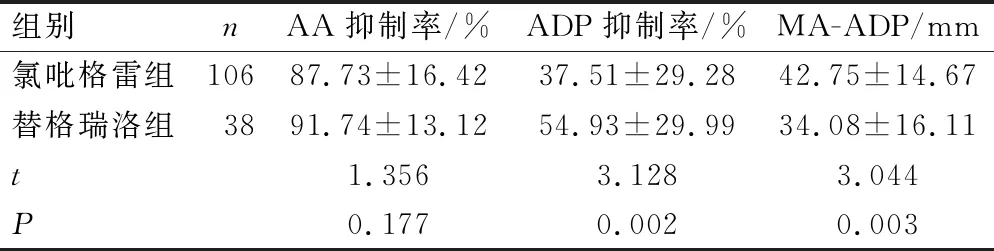
表1 氯吡格雷组与替格瑞洛组血栓弹力图检测结果比较
2.3 药物调整后患者改善情况
药物调整组患者改服替格瑞洛后的AA抑制率差异无统计学意义(P>0.05),ADP抑制率较服用氯吡格雷时显著升高,而MA-ADP显著降低,差异均有统计学意义(P<0.05),见表2。
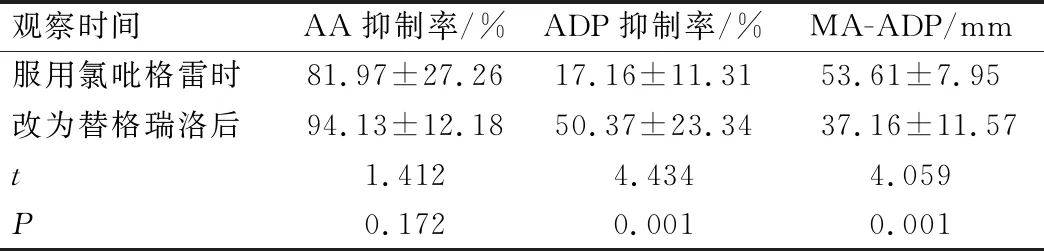
表2 药物调整组的改善情况(n=12)
3 讨论
颅内动脉瘤破裂是导致蛛网膜下腔出血的主要原因,由于其致死率及致残率高,临床上常常需要尽早采取手术治疗[7]。研究表明,随着神经介入材料的发展,以支架辅助栓塞术为主的血管内介入治疗正在成为颅内动脉瘤外科治疗的重要方式,然而,自1991年首个可拆卸支架诞生以来,预防与支架手术相关的血栓栓塞并发症一直是一项挑战[8-9]。阿司匹林联合氯吡格雷是目前双重抗血小板治疗预防血栓形成的最常见方案。氯吡格雷是P2Y12受体的不可逆抑制剂,有研究表明,有5%~12%的患者对氯吡格雷的抗血小板药物反应不理想[4];在Harahsheh等[10]的研究中,甚至有30%~44%的患者发生氯吡格雷耐药,可能与遗传易感性、并发症、合并用药、年龄、种族等影响因素有关[10]。本研究中有7例患者在服用氯吡格雷后测得ADP抑制率为0,占服用氯吡格雷总人数的5.93%,提示对氯吡格雷严重耐药的可能性。替格瑞洛是一类新型抗血小板药物,是一种非竞争性、直接作用的P2Y12受体拮抗剂,能够可逆地抑制受体信号传导和随后的血小板活化[11]。因此,对氯吡格雷耐药的患者,替格瑞洛能否替代其发挥更好的治疗效果是本研究关注的重点。
相较于凝血酶原时间、活化部分凝血活酶时间、血小板计数等传统实验室检测,血栓弹力图具有操作简单、结果生成迅速的优势,且单一测试可提供有关凝血、血小板功能、血小板—纤维蛋白原相互作用和纤维蛋白溶解的信息[12]。阿司匹林阻止AA在环氧酶的代谢以抑制血小板的聚集,AA抑制率通常可反映阿司匹林的药效;氯吡格雷与替格瑞洛则是通过抑制ADP与血小板受体P2Y12的结合来达到抗血小板聚集的目的,ADP抑制率则通常用于反映氯吡格雷或替格瑞洛等药物的效果[13]。本研究通过收集血栓弹力图检测的AA抑制率、ADP抑制率、MA-ADP等指标来评估患者接受双重抗血小板治疗后的效果。
低于30%的ADP抑制率提示ADP受体抑制剂效果不足。有研究显示,颅内动脉瘤患者支架治疗后的血栓栓塞并发症与ADP抑制率有关,对氯吡格雷的耐药性可能会增加血栓栓塞并发症的风险[14]。MA-ADP反映血小板活性对ADP诱导的血凝块强度,当MA-ADP大于49.95 mm时缺血事件发生的风险显著增大[15];Yuan等[16]报道,MA-ADP对缺血事件具有很强的预测作用;Corliss等[17]研究发现MA-ADP和ADP抑制率之间存在很强的相关性,表明MA-ADP和ADP抑制率都可以用于评估血小板抑制。本研究结果显示,对于单纯接受了阿司匹林联用氯吡格雷治疗的患者,其ADP抑制率要低于单纯接受阿司匹林联用替格瑞洛的患者,而MA-ADP高于后者。本研究还收集了12例因服用氯吡格雷后血栓弹力图检测显示ADP抑制率不理想而改服替格瑞洛患者的资料,结果显示,患者的ADP抑制率在改用替格瑞洛后显著提升,且MA-ADP明显降低。这可能是由于替格瑞洛能够更好地通过ADP途径抑制血小板的聚集,尤其在对氯吡格雷耐药的人群中,替格瑞洛效果显著,可通过达到更高的ADP抑制率与更低的MA-ADP来降低血栓形成的风险。在对急性冠状动脉综合征患者的研究中,替格瑞洛表现出了比氯吡格雷更有效的血小板聚集抑制作用,且起效更快,表明与氯吡格雷相比,替格瑞洛可能有助于降低血栓事件的发生率[18],本研究结果与之相符。本研究结果显示,对于氯吡格雷耐药的患者,替格瑞洛也可以发挥出良好的替代效果,且替格瑞洛抑制血小板聚集的效果在人群中优于氯吡格雷;当然,笔者并不认为这预示着替格瑞洛可以全面替代氯吡格雷的抗血小板治疗,这还需要更多的研究进行评估。然而,有研究报道,阿司匹林联用替格瑞洛的双重抗血小板治疗尽管可有效减少血栓并发症,但与出血事件的风险增加有关,因此,临床医生在考虑使用替格瑞洛时必须评估缺血事件和出血事件发生的风险[19]。据相关研究统计,支架辅助栓塞颅内动脉瘤术后的缺血事件发生率为7%~20%[20-21];本研究共收集了156例支架辅助栓塞颅内动脉瘤患者,发生缺血事件4例,发生率仅为2.56%,说明血栓弹力图可用于监测支架辅助栓塞颅内动脉瘤患者的血小板功能,并可在围术期对患者双重抗血小板治疗方案进行有效指导,不仅能及时发现对氯吡格雷耐药的患者,更换其治疗方案,还可将脑缺血事件的发生率控制在相对较低的水平,这对预防术后缺血事件的发生具有重要意义。
本研究也存在一些局限性,样本量较小,且为单中心回顾性研究,对行血栓弹力图检测时患者的服药时间无法精准控制,对患者缺血事件的统计缺乏长期随访,研究结果可能存在一定误差。因此,如何选用氯吡格雷或替格瑞洛为患者精准化制定双重抗血小板治疗方案,未来还需要更大的样本量以提高研究结果的准确性。

