仿古(高锡高铅)青铜材料在酸性土壤模拟溶液中的腐蚀行为
张黎明,王修园,周和荣,师静蕊
(武汉科技大学材料与冶金学院,武汉 430081)
青铜器是中国文物宝藏中一颗光彩夺目的明珠[1-3],现存大部分青铜器经过漫长时间的地下埋藏,受到不同程度的腐蚀,关于其腐蚀过程和机制已经有大量研究报道,且有多种腐蚀模型。ROBBIOLA等[4]将青铜腐蚀分为两类:一类是表面存在平整且致密的腐蚀产物层,其中包括一层薄的富Sn层和富Cu的矿化层;另一类是锈蚀产物结构存在较多缺陷,局部腐蚀严重,腐蚀扩散直至整个器物完全溃烂。BANNISTER等[5]提出晶间腐蚀理论,认为腐蚀会优先发生于有杂质或不纯的晶粒或晶界位置。王昌隧等[6]认为青铜腐蚀机理为晶界腐蚀,由于Cl-的参与形成了有害锈Cu2(OH)3Cl。张晓梅等[7]观察到出土青铜残片表面和内部存在晶间腐蚀。SCOTT等认为选择性腐蚀的发生取决于环境中的O2含量,缺O时δ相优先发生腐蚀[8];WALKER[9]研究了锡青铜在海水中的腐蚀行为,发现Cu含量越高的区域腐蚀发生越迅速,有学者认为小孔腐蚀是青铜的常见腐蚀形式[10-11]。另有大量文献[12-16]研究了含Cl-环境对青铜合金的腐蚀影响,其表面腐蚀产物主要为铜的氧化物和氯化物。大量文献利用现存青铜器分析推导了青铜的腐蚀过程,而直接利用青铜材料研究青铜器腐蚀行为的报道较少。考古发现的青铜器大多为铅锡青铜[17],本工作选用仿古工艺浇铸了高锡高铅青铜材料,对其在酸性土壤模拟溶液中的腐蚀行为进行了研究。
1 试验
1.1 试样及设备
试验用青铜材料采用仿古工艺浇铸而成,主要含金属铜、锡和铅,厚度为3 mm,化学成分(质量分数)为:Cu 66.35%,Sn 17.81%,Pb 15.84%,属于高锡高铅青铜。浸泡腐蚀试验和XRD分析用试样尺寸为20 mm×10 mm×3 mm,表面用砂纸(400~1 000号)逐渐打磨并除油后,在无水乙醇中进行超声波清洗,烘干称量后置于干燥器内保存备用。试验前,再次称量试样。用于显微组织观察和初期腐蚀萌生试样的尺寸为10 mm×10 mm×3 mm,选取一个10 mm×10 mm的面作为观察面,用砂纸(600~5 000号)逐级打磨后用1.5 μm抛光膏抛光后,采用10%(体积分数)三氯化铁盐酸酒精溶液侵蚀试样。电化学阻抗(EIS)试验用试样尺寸为10 mm×10 mm×3 mm,保留一个10 mm×10 mm工作面,背面焊接铜导线,使用环氧树脂将非工作面绝缘封闭。进行阻抗测试前将工作面用砂纸(600~1 000号)逐级打磨,随后用去离子水和酒精清洗吹干后备用。
1.2 试验方法
用Leica Metallographic Microscope DM2700M型金相显微镜观察试样的显微组织,利用SmartLab SE型X射线衍射仪(XRD)分析试样的腐蚀产物。采用场发射扫描电子显微镜及配套能谱仪(FE-SEM,Nova Nano 400;EDS)对试样腐蚀形貌及腐蚀产物成分进行观察及表征。
采用去离子水和分析纯试剂配制江西鹰潭地区酸性土壤模拟溶液[18],提高了试验溶液中的NaCl含量,以加速腐蚀。采用NaOH调节溶液pH为5.0,溶液组成见表1。初期腐蚀萌生试验过程如下:将试样置于溶液中分别腐蚀30 min和60 min后,观察试样表面的腐蚀情况。连续浸泡腐蚀试验过程如下:将试样悬挂浸泡于溶液中10,30,60,180 d后进行腐蚀质量损失测量[19]和腐蚀产物观察分析。其中,腐蚀速率按公式(1)计算。

表1 试验溶液中各组分的含量 Tab. 1The content of components of test solution g/L
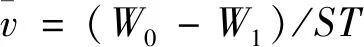
(1)
其中,W0为原始试样质量,W1为腐蚀后试样的质量,S为试样表面积,T为浸泡时间。
电化学阻抗测试在Corr Test CS310电化学工作站上进行,采用常规三电极体系,电解液为配制的江西鹰潭地区酸性土壤模拟溶液。工作电极为电化学试样,参比电极为饱和氯化钾甘汞电极(SCE),辅助电极为铂电极。待试样在试验溶液中的开路电位稳定后进行EIS测试,频率为0.1 Hz~100 kHz,电压为10 mV。所有测试均在室温下进行。用ZSimpWin软件对EIS谱进行拟合。
2 结果与讨论
2.1 基体的显微组织
由图1可见:试样由α相(白亮区域)、(α+δ)共析相(灰色区域)和游离态Pb相(黑色颗粒)组成[17]。α相整体较为平整均匀,(α+δ)共析相中共析α相细小无规则,被共析δ相包裹。游离态Pb由于本身性质的原因在抛光腐蚀过程中脱落或溶解,位于形貌图中空洞处。

图1 试样的显微组织Fig. 1 Microstructure of the sample
2.2 试样的腐蚀速率
由图2可见:在试验溶液中,材料腐蚀质量损失整体呈上升趋势,腐蚀速率随浸泡时间延长整体呈减小趋势,当浸泡时间为10 d时,试样的腐蚀速率最大(1.603 4 g/m2·d),当浸泡时间为10~30 d时,腐蚀速率迅速减小,浸泡时间为30~180d时,腐蚀速率趋于平缓。这可能是因为浸泡初期试样表面发生腐蚀后形成的腐蚀产物覆盖于试样表面阻碍了腐蚀介质接触基体,并且随浸泡时间延长溶液中的氧逐渐消耗,也在一定程度上对腐蚀速率产生影响。
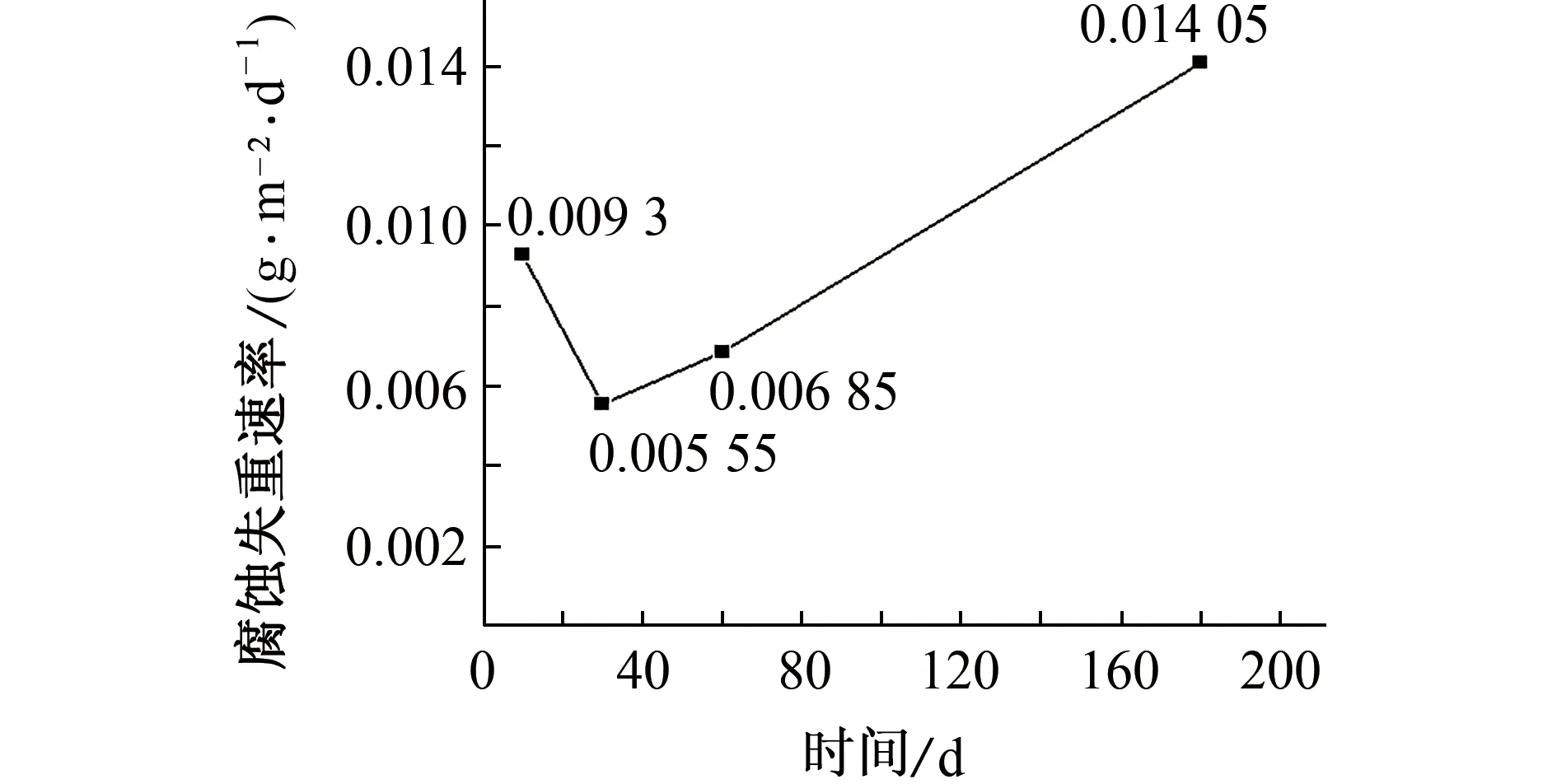
(a) 平均腐蚀失重曲线
2.3 电化学阻抗谱
由图3可见:在试验溶液中浸泡不同时间后,Nyquist图表现出相似的电容回路。这意味着不同腐蚀时间下的腐蚀机制相同,但腐蚀速率可能会有所不同[19-20]。另外,在Bode图中观察到一个相位角峰值,它对应于电荷转移和双电层电容的时间常数[21]。图3中插图为拟合EIS谱的等效电路,其中Rs表示欧姆溶液电阻,Rct对应于电荷转移电阻,Qdl表示试样与溶液之间存在的双电层电容,W表示韦伯(Warburg)阻抗。Qdl是一个恒相位元件(CPE),可以解释双电容层的非理想行为,它的阻抗(ZCPE)表达式见式(2):

(a) Nyquist图
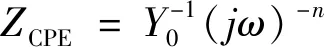
(2)
式中,Y0是与频率无关的导纳,j是-1的平方根,ω是角频率,n是CPE的指数。表2给出了EIS谱等效电路中各元件的拟合参数。chi-squared(χ2)值均在10-3这一量级,表明该等效电路可行,且质量较好。
由表2可见:导纳Qdl总体上随腐蚀时间延长而减小,表明试样与电解液界面面积增大[22-24],指数n同样随腐蚀时间延长总体呈减小趋势,这两个参数的变化与试样在腐蚀过程中表面粗糙度的增大相关。通常,Rct与腐蚀速率成反比,表中Rct在腐蚀0~10d过程中随腐蚀时间延长而减小,即腐蚀速率随腐蚀时间延长而增大,Rct在腐蚀10~180 d过程中随腐蚀时间延长而增大,表明腐蚀速率随腐蚀时间延长而减小。W值与材料耐蚀性相关,W越大材料耐蚀性越好,表中W值的变化趋势与Rct的类似。Rct与W结果表明试样在试验溶液中的腐蚀速率变化过程如下:试验0~10 d,腐蚀速率随试验时间延长而增加,试验10~180 d,腐蚀速率随试验时间延长而减少。EIS结果与浸泡试验结果吻合。
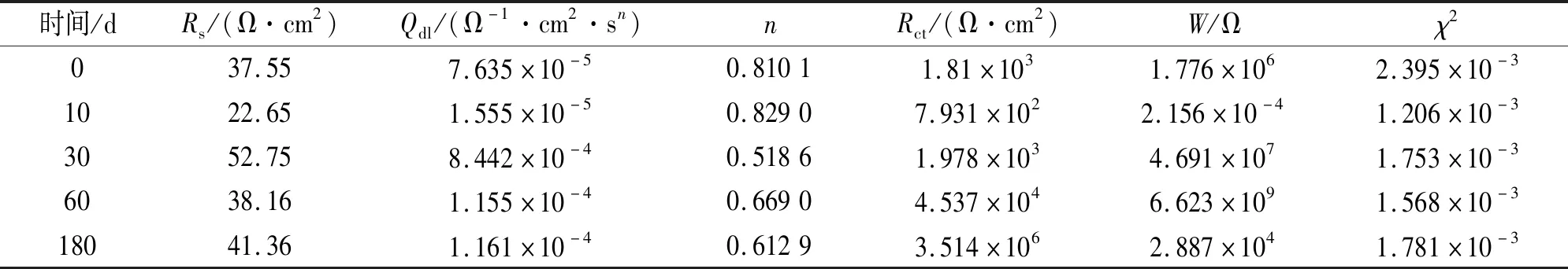
表2 EIS拟合结果Tab. 2 Fitting results of EIS
2.4 腐蚀形貌及腐蚀产物
由图4可见:经过30 min腐蚀后,试样表面部分区域发生腐蚀,腐蚀产物为颗粒状和针片状;图4(b)中Pb颗粒表面及周围出现絮状腐蚀产物;图4(c)中Pb颗粒处出现较深腐蚀坑,周围存在颗粒状和针片状产物。α相和(α+δ)相未发生明显的腐蚀溶解。对图中不同特征的腐蚀形貌进行EDS点扫描分析,结果表明腐蚀产物中含有Pb、O、Cu、Cl等元素,Pb含量最高,很明显Pb颗粒发生腐蚀溶解并且腐蚀产物呈扩散分布。
由图5可见:在试验溶液中腐蚀3 h后,试样表面分布了大量针状腐蚀产物和絮状腐蚀产物;针状腐蚀产物的EDS结果表明其中包含Pb、O、Cl三种元素,且Pb含量最高;絮状产物的主要元素组成有Pb、Cu、Sn、O,且Pb含量最高。
由图6可见:在酸性土壤模拟溶液中浸泡后,试样表面几乎被白色腐蚀产物全面覆盖,该腐蚀产物结构较为疏松。且白色腐蚀产物下方材料表面也发生颜色和形貌的改变, Pb颗粒的位置出现明显的腐蚀坑。腐蚀初期,试样表面变化最大,随着浸泡时间的延长,试样表面腐蚀产物无明显变化。
由图7和表3可见:经过不同时间浸泡后,试样表面的腐蚀产物均为层片状,无明显差异,腐蚀产物主要有Pb、Cu、O,其中Pb含量最高。图7(d)中片层状腐蚀产物下方存在颗粒细小紧密附着于基体上的腐蚀产物,该区域Cu的质量分数为71.27%,且存在少量Sn。证明表面最表层的白色产物主要是Pb的产物,白色产物下方附着于基体的密集颗粒状产物主要是Cu的产物,含有少量Sn的产物。微观形貌观察结果表明,试样中Pb颗粒发生严重腐蚀,产物分布于最外层,α和(α+δ)相腐蚀较轻且为均匀腐蚀,产物分布于Pb的腐蚀产物下方附着于基体。

表3 试样表面腐蚀产物的EDS分析结果Tab. 3 EDS analysis results of corrosion products on the sample surface %
由图8和表4 可见:腐蚀产物层含有Pb、Cu、Sn、O、Cl。点2、3和点7、8分别为腐蚀产物层中距离基体不同距离的点(点2和7为最表层产物,点3和8为最内层产物),不同位置Sn含量的不同表明Sn的产物分布于腐蚀产物层最内层靠近基体。点4、5、6是分别是基体内部同一深度的游离态Pb、α相和(α+δ)相,只有点4中存在O元素,证明试样发生腐蚀时游离态Pb相的腐蚀倾向性最大,最容易发生腐蚀,与初期腐蚀分析结果吻合。而α相和(α+δ)相呈均匀腐蚀。截面观察分析结果与表面分析结果吻合。
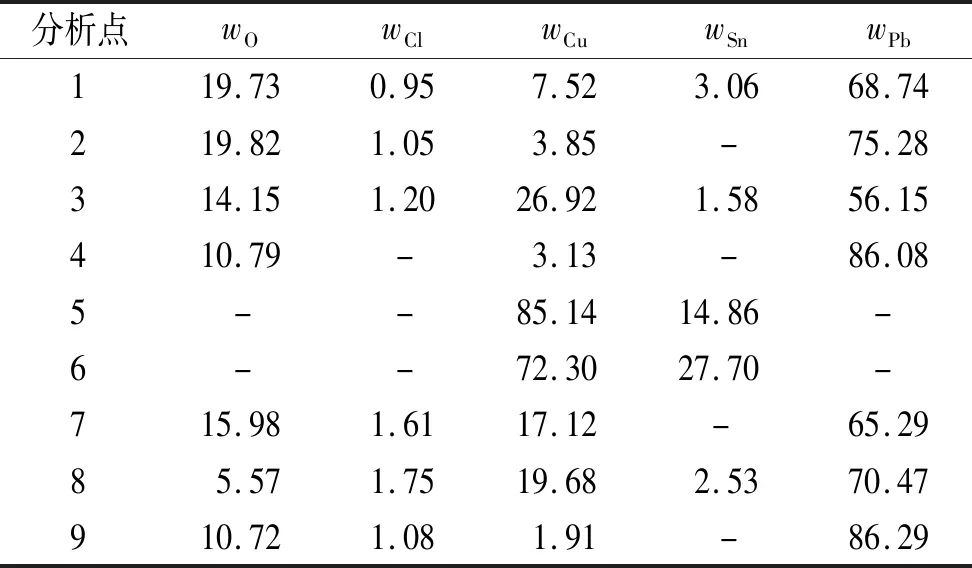
表4 试样截面腐蚀产物层的EDS分析结果Tab. 4 EDS analysis results of the corrosion product layer of the sample section %

(a) 整体表面形貌

(a) 整体腐蚀形貌

(a)0 d (b)10 d (c)30 d (d)60 d (e)180 d图6 在试验溶液中浸泡不同时间后,试样的表面宏观形貌Fig. 6 Macro surface morphology of samples after immersion in the test solution for different times
由图9可见:在试验溶液中浸泡不同时间后,试样表面腐蚀产物成分为Cu2O、SnO2和PbO。结合EDS分析结果可见, PbO是表面白色产物,Cu2O和SnO2则是位于白色产物下方的腐蚀产物。

图9 试样在试验溶液中浸泡不同时间后的表面腐蚀产物XRD图谱Fig. 9 XRD patterns of corrosion products on the surface of samples immersed in test solution for different times
2.5 讨论
青铜材料是模仿古代青铜器成分和工艺铸造的,结合图1可知试样中存在三种相即α相(α+δ)相以及游离态Pb。综合图4和图5可知:腐蚀30 min后试样表面腐蚀较轻,出现絮状、颗粒状以及少量针片状产物;腐蚀3 h后试样表面被针状和絮状腐蚀产物覆盖,几乎覆盖整个基体表面。从腐蚀初期的形貌观察结果可知,试样表面的Pb颗粒首先发生腐蚀,α和(α+δ)相无明显变化,该现象与图8所示截面观察结果吻合,表明试样中优先发生腐蚀的相为游离态Pb相。初期腐蚀产物主要是Pb的化合物以及少量Cu的产物。随着腐蚀时间延长,腐蚀产物逐渐增多,长期浸泡后试样表面覆盖了大面积白色腐蚀产物,且分布较为均匀,白色产物下方存在黄色细小颗粒状腐蚀产物(图6,图7),为Cu和Sn的氧化物。结合图8可见:Cu和Sn的腐蚀产物位于腐蚀产物最内层靠近基体,Pb的化合物处于腐蚀产物层表层。结合形貌观察结果和XRD分析结果可知,试样中Pb颗粒即游离态Pb相优先发生腐蚀,腐蚀产物为白色的PbO,根据文献分析其腐蚀反应见式(3)和(4)[25-26]:

(3)

(4)
试样中的α相和(α+δ)相呈均匀腐蚀,生成的腐蚀产物位于整个腐蚀产物层下方,是黄色细密分布的颗粒状产物,经XRD分析应为Cu2O和SnO2。腐蚀过程中Cu在氧气的作用下会氧化形成Cu+,从而生成Cu2O,氧化还原反应式为:

(a) 10 d (b) 10 d (c) 30 d (d) 30 d

(5)

(6)
Sn在电化学腐蚀反应过程中氧化形成Sn2+,Sn2+与Cl-结合形成SnCl2,继续被氧化形成SnO2[27-30]:

(7)

(8)

(9)
Pb发生腐蚀后,Pb元素从原本Pb颗粒的位置发生转移,形成腐蚀坑,这一过程会导致试样腐蚀加速,而游离态Pb在试样中占比最少,因此初期腐蚀过程中试样表面Pb颗粒消耗殆尽后,腐蚀速率逐渐下降。与此同时,Cu和Sn的腐蚀产物结构紧密,在一定程度上可以阻碍腐蚀介质与产物下方基体的接触,从而阻碍腐蚀发展,进一步降低腐蚀速率。结合浸泡试验和EIS分析结果可知,试样在连续浸泡腐蚀过程中,当试验时间为0~10d时,腐蚀速率是增大的,而试验时间为10~180 d时,腐蚀速率呈减小的趋势。结合许多关于古代青铜器文物的腐蚀研究结果可见[1,2,6,7,31-33],器物表面的腐蚀产物包含Cu2O、SnO2和PbO等产物,这与本工作研究结果较为吻合。不过本工作中生成的腐蚀产物不如出土青铜器复杂,这是由于本工作相对真实情况下的腐蚀时间更短,更接近青铜器在土壤埋藏过程中的初期腐蚀。
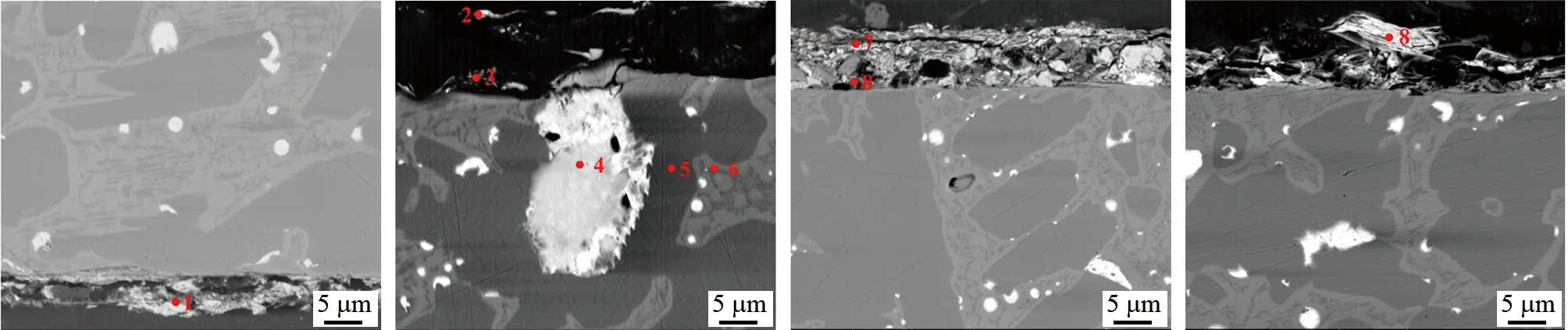
(a) 10 d (b) 30 d (c) 60 d (d) 180 d图8 试样在试验溶液中浸泡不同时间后的截面微观形貌Fig. 8 Cross-scetion micro morphology of the sample after immersion in the test solution for different times
3 结论
(1) 高锡高铅青铜材料基体组织中存在三种相,即α相,(α+δ)相,以及游离态Pb。α相平整均匀,(α+δ)相组织呈细小网状,游离态Pb相为颗粒状。
(2) 在江西鹰潭地区酸性土壤模拟溶液中连续腐蚀180 d的过程中,腐蚀初期,试样表面生成絮状、颗粒状、针状腐蚀产物。随着腐蚀时间延长,试样表面生成均匀分布的白色腐蚀产物,游离态Pb腐蚀后形成腐蚀坑。白色腐蚀产物微观形貌为细小层片状(PbO),白色产物下存在密集的颗粒状产物(Cu2O、SnO2)。模拟溶液中的浸泡腐蚀与土壤埋藏环境的真实腐蚀具有一定程度上的关联性。
(3) 青铜材料中游离态Pb相先发生腐蚀,腐蚀程度最大,α相和(α+δ)耐蚀性高于Pb相,呈均匀腐蚀。
(4) 浸泡试验和EIS分析结果证明,在酸性土壤模拟溶液中,青铜材料的腐蚀速率在试验时间为0~10 d时呈增大趋势,试验时间为10~180 d时逐渐减小。

