基于“证据推理与模型认知”探究乙烯
娄心媛 陈 未
(江苏省溧水高级中学 211200)
1 问题的提出
《普通高中化学课程标准(2017年版)》中对于“证据推理与模型认知”素养的描述是通过分析、推理等方法认识研究对象的本质特征、构成要素及其相互关系,建立认知模型,并能运用模型解释化学现象,揭示现象的本质规律.乙烯是最简单的不饱和烃,建立好正确的模型后为后面学习苯等奠定了基础.通过对乙烯进行深度学习,进一步强化了化学中物质“结构决定性质,性质决定用途”的观念,培养学生形成“宏-微-符”的思维方式,建立模型和证据推理的化学核心素养.
2 教学过程实录
教学环节一:创设情境,初识乙烯
引入:播放微视频-专家介绍乙烯的催熟作用以及身边的聚乙烯产品.
教师活动:了解了乙烯的生活用途后,带领学生观看“扬子石化”的宣传片—乙烯来源于石油,是一种重要的化工原料.随后,展示一瓶收集好的乙烯,让学生观察,并请学生代表进行操作验证.
学生活动:学生归纳总结乙烯的物理性质(颜色、气味,加水验证溶解性等).
设计意图:基于生活中乙烯的用途,激发学生的学习兴趣,学生感受到化学源于生活,又服务于生活.扬子石化就坐落在南京,是著名化工企业,而乙烯又代表了一个国家的石油化工水平,立足化工生产国情,唤起学生的爱国情和责任感.
教学环节二:建模乙烯,实验验证
教师活动:带领大家回顾前面学习的甲烷的化学性质.
学生活动:甲烷化学性质很稳定,不与强酸、强碱、强氧化剂如高锰酸钾反应,能燃烧,可初步推测乙烯能燃烧,不与高锰酸钾反应,结合资料卡片,猜测乙烯可与溴水发生了反应.
资料卡片1:①乙烯为易燃化学品,置于良好通风处保存,并远离火源.②水果采摘后会有大量乙烯产生,容易加快水果腐烂.果农用如下方法保鲜水果:在水果箱中放入经饱和高锰酸钾水溶液浸过的砖块或蛭石,密封保存,能延长水果的保质期.③二溴乙烷(CH2Br-CH2Br)用作脂肪、油、树脂等的溶剂,谷物和水果等杀菌剂、木材的杀虫剂等.由乙烯与溴等量反应制得.
学生活动:学生对比甲烷性质并阅读资料卡片,推测乙烯可能具有的化学性质:①燃烧产生淡蓝色火焰;②不与高锰酸钾反应;③使溴水褪色,并与乙烷作对比.
师生合作演示实验,通过投屏展示给全班学生,学生完成表1.对比发现实验1和2的实验现象与预测的并不符合,实验1乙烯燃烧有黑烟,是因为含碳量高,燃烧不充分;至于为什么能使高锰酸钾溶液和溴水褪色,可能与乙烯的结构有关.

表1
设计意图:学生结合已有的烷烃知识以及提取资料信息大胆的预测乙烯的化学性质,通过客观的实验现象,形成了认知冲突,激发了学生的求知欲,强化了有机物中结构决定性质的重要性,为下面探究乙烯的结构作铺垫.
教学环节三:分工合作,搭建乙烯
教师活动:利用碳价层电子4和氢价层电子1的理论事实,给出提示:价层电子对互斥理论,利用工具箱中的橡皮泥小球和棍子来搭建乙烷(C2H6)和乙烯(C2H4)的球棍模型,进行对比,并写出乙烷和乙烯的分子式、电子式、结构式、结构简式以及空间构型.
学生活动:小组分工合作,搭建模型,书写表2.

表2
通过构建实物模型(如图1所示),学生发现与乙烷不同的是:乙烯是平面型结构;存在着一个碳碳双键,碳碳双键的存在使得乙烯能够使酸性高锰酸钾溶液和溴水褪色.因此,可以利用酸性高锰酸钾溶液和溴水来鉴别乙烯和乙烷.

图1
设计意图:用实物模型将微观物质宏观化,囿于思维限制,学生很难一下子搭出乙烯的模型.教师引导学生从熟悉的乙烷去入手,每个碳失去两个氢原子后各有一个电子,又形成了一对共用电子对.整个探究过程中,学生兴致高昂,积极主动参与到模型搭建中来,在欢快的氛围中完成知识的建构.
教学环节四:证据推理,完善模型
教师活动:已知乙烯与酸性KMnO4溶液反应,生成CO2和H2O,标出反应前后碳元素的化合价,分析乙烯使酸性KMnO4溶液褪色的本质是发生了什么类型的反应?
学生活动:乙烯中碳-2价变为二氧化碳中的+4价,化合价升高,发生了还原反应,酸性KMnO4是强氧化剂,所以乙烯使酸性KMnO4溶液褪色的本质是发生了氧化还原反应.
教师活动:那么溴水为什么会褪色呢?请结合资料卡片分析,乙烯与溴反应的产物是什么?对比乙烯和产物的球棍模型,找出两者区别.
学生活动:由资料卡片1可得:乙烯与溴水反应生成了1,2-二溴乙烷.对比乙烯和1,2-二溴乙烷的球棍模型,得出乙烯中的碳碳双键变成碳碳单键,两个溴原子分别加在了两个碳上.
教师活动:乙烯中的碳碳双键为什么变成了碳碳单键呢?反应又是如何发生的,尝试着用球棍模型把这个反应演示出来,并写出对应的化学方程式.播放乙烯与溴加成的微观动画.
资料卡片2:见表3
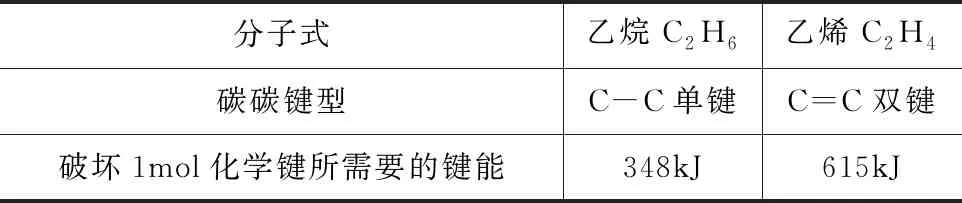
表3
学生活动:观看动画,得出乙烯使溴水褪色是因为乙烯的碳碳双键不稳定,双键中的一根键易断裂,溴分子中的溴溴单键断裂,两个溴原子分别加到断键的两个碳原子上形成了1,2-二溴乙烷.
1,2-二溴乙烷
教师活动:引出加成反应的定义.有机物分子中的不饱和键(双键或三键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应叫做加成反应.
设计意图:通过以往教学发现学生对乙烯使酸性高锰酸钾溶液和溴水褪色的原因易混淆.这里一开始引领学生运用旧知,分析乙烯使高锰酸钾褪色是因为氧化还原反应;再提示资料卡片中乙烯与溴反应是生成1,2-二溴乙烷,让学生利用手中工具探索形成过程,得出褪色是因为双键中的一根键断裂而发生的加成反应,更有利于学生参与到课堂中来,并利用多媒体辅助教学,使抽象枯燥的分子结构更加形象化,学生更易于理解接受,有效地突破本节课的重难点.
教学环节五:模型迁移,事实评价
教师活动:一定条件下,乙烯还能和H2、HCl、H2O 发生加成反应,写出有关反应的化学方程式.(提示:可借助模型完成.)
学生活动:搭建模型并完成化学方程式书写.


CH3CH2OH(乙醇)
这些生活实例,你会解释吗?南方产的水果,多数在未成熟时采摘下来,运到北方后,向库房中充入少量乙烯再销售;反之,为了延长果实和花朵的寿命,方便远距离运输,人们在装有果实或花朵的密闭容器中放置浸泡过高锰酸钾溶液的硅土,用来吸收花朵或水果中产生的乙烯.
这些生活现象进一步让学生对乙烯有了更深的了解.
设计意图:学会模型迁移,举一反三.
教师活动:介绍乙烯的用途并对乙烯知识点进行总结.

