沙利度胺抗肿瘤机制基础研究分析
庄伟霞 陈莉 王谋锋 江丽 余慧玲
沙利度胺波折的药物发展史源于药物本身独特的结构和仍在探索的药理效应。从臭名昭著的致畸剂到免疫调节剂、抗炎药物等的华丽转身,沙利度胺显示了强大而多效的药理效应。本文以CNKI 为数据库,搜索1995~2021 年所有有关“沙利度胺、抗肿瘤”词条的研究性文献,排除综述、会议文章、论著、共识、Meta 分析、同一项目组相似研究论文等,最终获取82 篇高质量基础研究性论文。根据获取的文章数据,在中国有关于沙利度胺抗肿瘤机制的研究在2008 年和2011 年达到高峰,分别为12 篇、11 篇。见图1。聚焦领域前五分别是血液系统肿瘤、肝癌、肺癌、妇科肿瘤、胃癌。见图2。本研究以沙利度胺在不同部位肿瘤的基础研究为线索,分析并探寻其抗肿瘤可能的各种路径和机制,以期为后续研究提供理论依据。
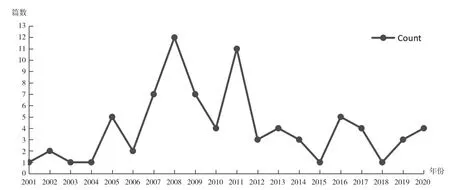
图1 沙利度胺在中国的抗肿瘤作用机制研究
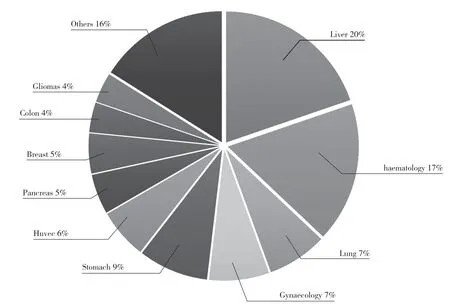
图2 不同部位机理研究的占比
1 血液系统肿瘤
骨髓增殖性肿瘤、多发性骨髓瘤、白血病、骨髓增生异常综合征等都是较为经常碰到的血液系统肿瘤。肿瘤细胞增殖与生长或许与Notch 信号传导途径参与有关联,杨啊晶[1]模拟骨髓微环境,通过实验发现左旋沙利度胺对骨髓瘤U266 细胞的生长具有抑制作用,也会使其凋亡,在这种情况下,Notch 基因表达处于上调状态。而人骨髓成纤维样基质细胞(human bone marrow fibroblastoid stromal cell line,HFCL)也抑制细胞生长,但对凋亡和Notch 不影响。说明Notch 信号传导在不同细胞类型表现是有差异的。在抑制U266细胞增殖过程,Notch 基因表达增加说明Notch 信号传导对凋亡有促进作用,进一步证实沙利度胺的抗肿瘤作用。为了研究沙利度胺的体内抗瘤作用及作用机制,卢洁[2]以三氧化二砷(arsenic trioxide,ATO)和沙利度胺单用及联用方式治疗人骨髓增生异常综合征(myelodysplastic syndrome,MDS)荷瘤小鼠。实验表明,沙利度胺在蛋白质和基因水平上在体内诱导细胞凋亡的机制可能是通过参与两条重要信号途径得以实现:一是通过线粒体介导的、Caspase 依赖的细胞内凋亡,线粒体是ATO 诱导细胞凋亡的重要作用靶点(涉及Caspaseg9,7,6,3,以及Smac/DIABLO,凋亡蛋白抑制因子cIAP 蛋白和Survivin;而不是Caspase8)。二是通过核因子NF-κB(涉及NF-κB 及其抑制因子IκB-ɑ 和转录调节因子AP1、SP1 的重要作用)。
JAK2V617F 的突变存在于骨髓增殖性肿瘤(MPN)中。吴小谢等[3]通过研究指出干扰素联合沙利度胺对红白血病细胞株(HEL)的增殖具有抑制作用,同时也会诱其凋亡,但是在影响JAK2V617F 突变基因的表达上作用并不明显。他们指出,抗肿瘤的作用并不是通过沙利度胺下调JAK2V617F 突变基因表达产生的。B7-1 分子在多发性骨髓瘤免疫逃逸机制有着显著的影响。杨云等[4]通过实验发现在骨髓瘤细胞或者患者骨髓细胞中缺乏B7-1 分子,或者B7-1 分子表达不显著。由此认为沙利度胺或许可以上调B7-1 分子表达,从而实现抗肿瘤免疫效果。李娟等[5]的研究丰富了沙利度胺作用机制。她们发现沙利度胺可以减少难治、复发多发性骨髓瘤(MM)患者骨髓微环境白细胞介素(IL)-1β mRNA、IL-6 mRNA、肿瘤坏死因子-α(TNF-α)mRNA 的表达。同时,还探索通过沙利度胺联合单克隆抗体利妥昔单抗来研究沙利度胺对骨髓瘤瘤细胞CD20抗原表达是否有促进作用。吴广银等[6]通过研究发现沙利度胺可以下调TNF-α 表达,从而对肿瘤血管起到抑制作用。另有许多医学研究团队多是从血管内皮生长因子(VEGF)为效应指标切入,证明沙利度胺单用或联合其他药物具有抑制作用。见表1。
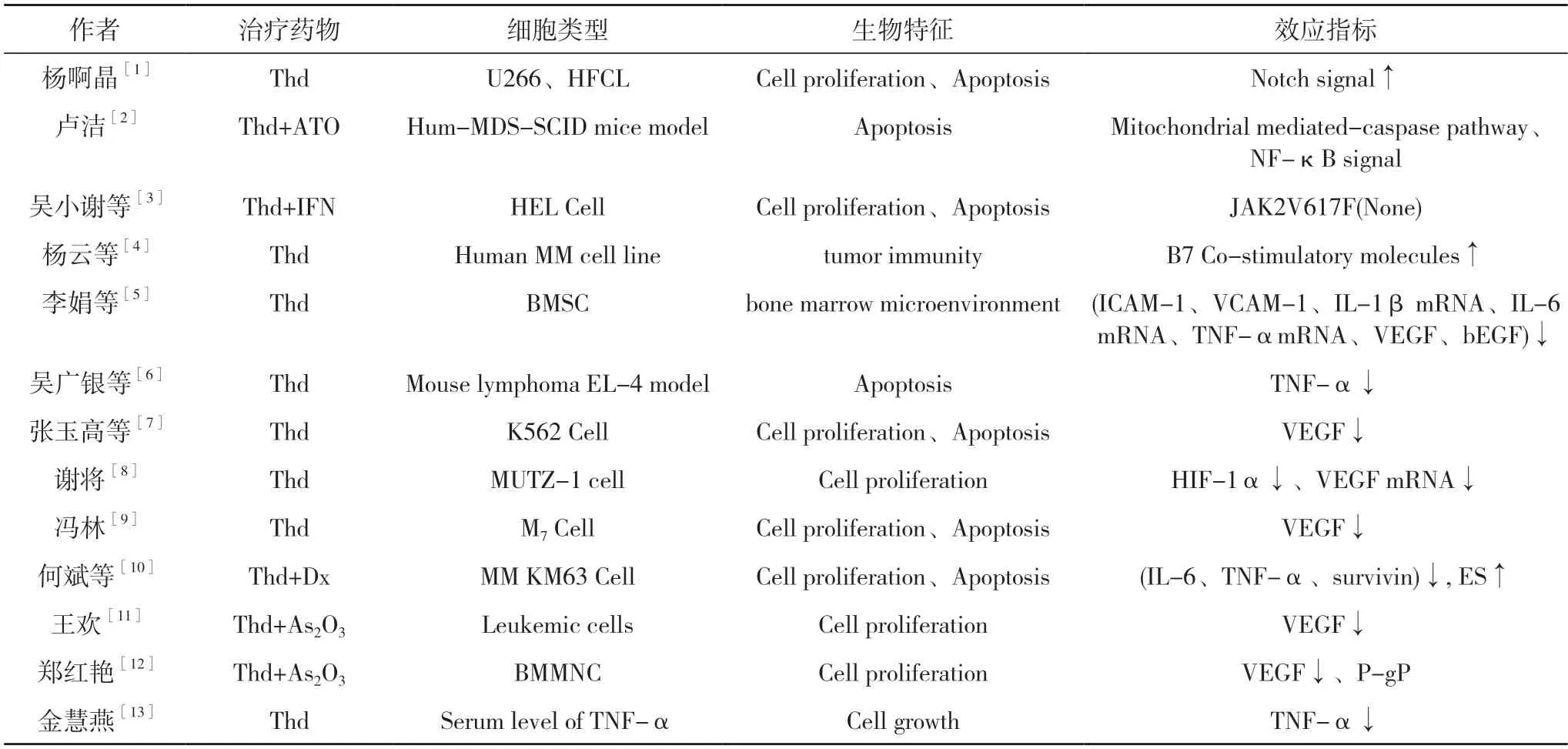
表1 沙利度胺对血液系统肿瘤作用机制的研究
2 肝癌
晚期肝癌的有效治疗路径仍在探索中。时下肝癌治疗路径多尝试合并用药和个体化精准用药,利用药物不同机制与作用差异互补,企图在新的组合中找到更为有效并能应用到临床的方案。国内学者研究抗肝癌机制多采用沙利度胺联合其他药物,比如沙利度胺与一线化疗药如平阳霉素、5-氟尿嘧啶(5-FU)、阿霉素、表阿霉素等协同抗肿瘤机制研究[14-22]。见表2。也有部分学者采取沙利度胺单药研究,从不同方面进行佐证[23]。钱洪[15]从体内外证实沙利度胺的抗肿瘤作用。刘业卿[14]则是利用影像学原理直接监测沙利度胺在肝癌方面的疗效。他们的研究表明沙利度胺可使生长迅速的肿瘤的血管密度显著降低,存活瘤细胞层的厚度显著降低。但与之相关的应用99mTc-HL91 乏氧显像剂的适用性及其最佳条件问题,仍有待进一步试验敲定。裴正浩[18]的相关研究显示沙利度胺可有效抑制骨桥蛋白基因的表达。王喜安等[20]的研究则有其他的结论。他们在移植性肝癌(HAC)小鼠腹腔注射环磷酰胺,发现抑瘤率虽高达 83.8%,但对肿瘤组织微血管密度(MVD)无丝毫影响。化疗药治疗过程常出现耐药,这可能与其仅杀伤肿瘤细胞,而无抗肿瘤血管生长作用以致肿瘤复发有关。另一对照组沙利度胺灌胃给药,不单抑瘤率具备差异统计学意义,而且小鼠MVD 降低。这一实验设计结果和相关研究结果相吻合,提示联合沙利度胺与细胞毒类药物起到较好的治疗效果。
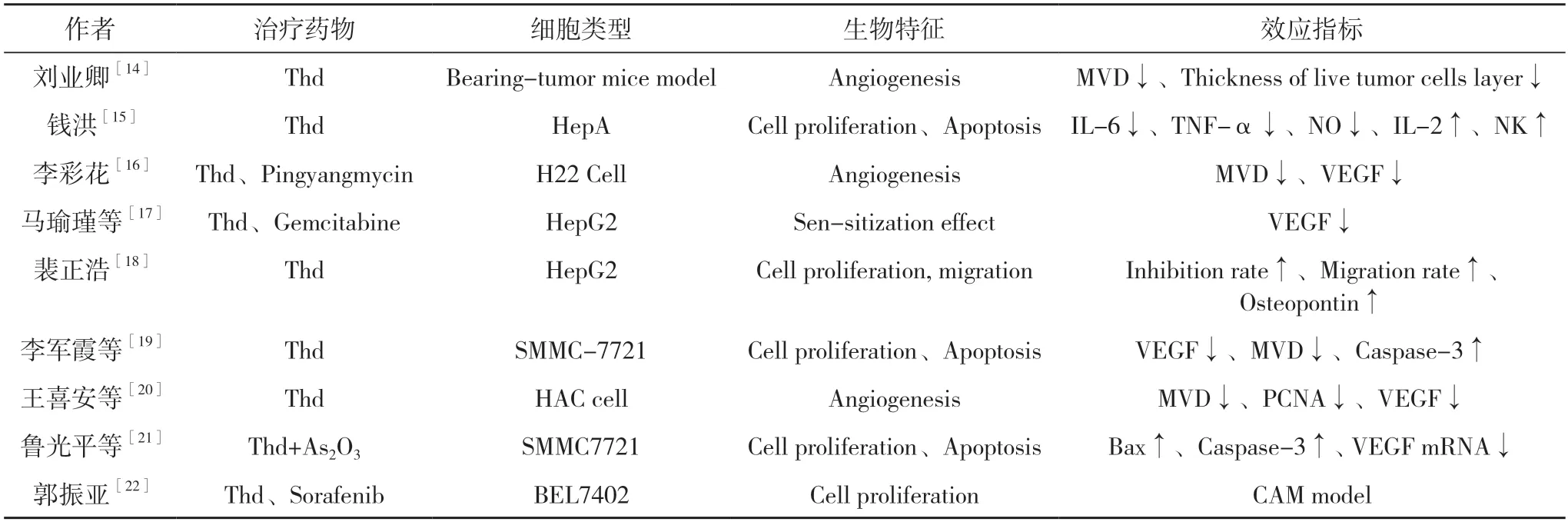
表2 沙利度胺对肝癌的作用机制研究
3 胃癌
李钧[24]在他的博士学位论文中对沙利度胺单药或联用5-FU 后MGC-803 细胞的增殖情况、影响及其凋亡因素等进行了研究。研究结果显示,两药联用能明显增强细胞的抑制和凋亡作用,同时出现过氧化物酶体增殖物激活受体-γ(PPAR-γ)表达增加与B 淋巴细胞瘤-2 基因(Bcl-2) 表达减少的现象。赵丹等[25]研究显示,低剂量替尼泊苷(VM-26)合并沙利度胺,一是抑制人胃癌BGC-823 裸鼠移植瘤变大;二是限制新生血管重塑,且没有致骨髓的造血功能异常等副作用。李慧[26]在裸鼠种植人胃癌模型中证实了沙利度胺可使PPAR-γ、caspase-8 表达逐渐增强,Bcl-2 表达减少。丛风云[27]发现沙利度胺高剂量时[30 mg/(kg·d)]抑制肿瘤周围淋巴血管生长和淋巴结进一步转移,但对肿瘤生长无影响。
4 肺癌
徐小峰等[28]准备5 组不同浓度的沙利度胺,并将其用于人肺腺癌细胞A549 细胞,经过实验发现VEGF、VEGF-C mRNA 和蛋白水平的表达均呈现降低趋势。汤小梅[29]通过把沙利度胺、顺铂(DDP)二者联合起来使用,发现联合使用对A549 细胞的增殖具有显著的抑制作用,并且当顺铂的浓度≥0.5 mg/L时,还会呈现叠加效果。许阳[30]发现沙利度胺与埃克替尼的联合使用,对肺癌细胞株 PC9 细胞表皮生长因子受体(EGFR)和 VEGF 通路信号转导均产生抑制作用。同时指出,这两者的联合使用还可遏制PC9 细胞的迁移能力。张依[31]通过实验发现沙利度胺阻滞细胞生长并诱导凋亡发生在G1 期,并且该作用与浓度-时间具有相关关系。结果显示VEGF 与 HIF-1α、和NF-κB 呈正相关,与VEGF 和 组织金属蛋白酶抑制因子-3(TIMP-3)、基质金属蛋白酶-1(MMP-1)呈负相关。该实验还联合依托泊苷证实了序贯用药的意义,先依托泊苷后沙利度胺的用药方案抑制效果明显优于先沙利度胺后依托泊苷方案。黄海宁等[32]通过 RNA 干扰及慢病毒感染法构建稳定敲低Cereblon 蛋白(CRBN)的 A549 细胞株(A549CRBN),实验表明当沙利度胺的浓度为100 μmol/L 时,显著抑制细胞迁移;CRBN 低表达时,不仅A549CRBN细胞迁移能力明显下降,而且其N-cadherin 和vimen-tin mRNA 表达水平也显著降低。这也许与沙利度胺通过CRBN 依赖方式(图3)来抑制N-cadherin 与vimentin 表达有关。
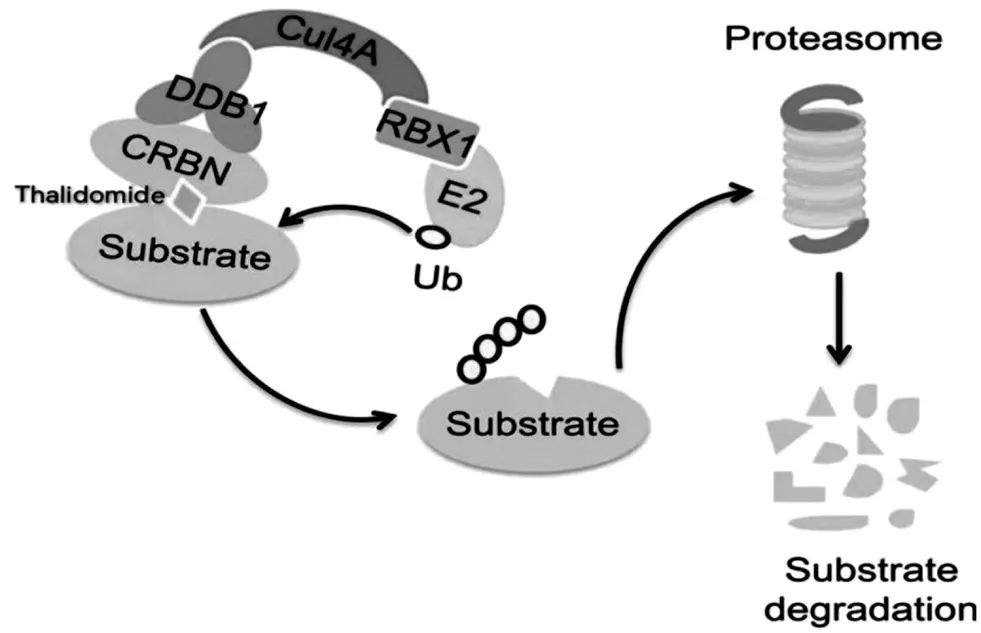
图3 沙利度胺通过CRBN 依赖方式抑制N-cadherin 与Vimentin 表达
5 讨论
综上所述,文中各项基础实验从各个角度、各种信号转导途径探索沙利度胺抗肿瘤作用。这些作用机制集中体现在:①通过上调或者下调诸如IFN-γ、TNF-α、T 淋巴细胞、IL-10 等免疫表达因子发挥作用,达到促凋亡的效应[33,34];②通过对VEGF、BEGF 等产生抑制作用[35]、对缺氧诱导因子转录和表达进行阻止或对环氧化酶-2(COX-2) 表达进行下调等方式来发挥抗肿瘤血管生成的作用[36];③与化疗药物或酪氨酸激酶抑制剂(TKI)或靶向免疫治疗药物一起使用,产生叠加效果,更有甚者会扭转耐药性;④体现在增强放射治疗疗效层面。涉及机制理论除了传统的血管生成抑制理论、促凋亡因子、免疫调控等[37-39],也拓展了部分领域研究比如基因代谢方面、耐药方面、联合用药顺序、合并中国传统草药、放射疗法等[35,40]。说明有关沙利度胺的抗肿瘤机制研究已经从经典的抗血管生成途径和促凋亡途径转向更细微、更多元化的领域。比如Xia 等[41]最新的研究显示对于非小细胞肺癌(NSCLC),沙利度胺可通过FGD5-AS1/miR-454-3p/ZEB1 轴介导的VEGFA 表达抑制和PD-1/PD-的调控L1检查点来抑制NSCLC 血管生成和免疫逃逸。这些既丰富了沙利度胺抗肿瘤药理机制理论,也为其临床用药提供新的思路。
其次不同的肿瘤部位,沙利度胺发挥的作用及途径不尽相同。沙利度胺在血液系统肿瘤中应用可能与肿瘤血管生成,与Notch 信号转导途径、线粒体介导的Caspase 依赖的细胞内凋亡途径有关,效应指标VEGF上调,TNF-α 下调。同时可能由于肿瘤类型自身的特点,沙利度胺亦在免疫逃逸和肿瘤微环境等方面发挥影响。在肝癌方面应用沙利度胺抗肿瘤机制研中常以HepG2 细胞作为研究,效应指标多以MVD 体现,且以联合化疗药物治疗为主。在抗胃癌机制研究中显示高剂量沙利度胺[30 mg/(kg·d)]虽无法抑制肿瘤生长,却可抑制肿瘤淋巴血管生长,阻碍淋巴结转移,提示高剂量沙利度胺可能在肿瘤间血管方面的抑制作用大于对实体瘤本身的作用。在抗肺癌的基础研究,发现沙利度胺作用点主要在细胞周期G1期,且与依托泊苷存在序贯用药的意义。CRBN 既是沙利度胺致畸的重要靶点,也是沙利度胺的结合蛋白。沙利度胺很可能通过CRBN 抑制肿瘤细胞的迁移。
本文通过对中国近二三十年有关沙利度胺在抗肿瘤效应方面的机制基础研究,总结分析了沙利度胺在常应用肿瘤部位领域机制研究情况,包括细胞类型、研究模型、研究方法、生物效应指标、可能涉及的机制理论,初步比较分析不同肿瘤部位基础研究的异同点,为沙利度胺在抗肿瘤方面的进一步应用提供理论基础[42]。当然受限于各方面因素,本研究依然存在诸多不足,如针对某一部位肿瘤沙利度胺协同抗肿瘤效应的具体通路和作用靶点等问题亟需各位同仁共同努力解决。

