紫杉醇(白蛋白结合型)联合顺铂治疗晚期复发子宫颈癌的临床效果及安全性分析
刘挺
子宫颈癌是临床常见的女性恶性肿瘤,其发病率和致死率在女性恶性肿瘤中分别居于第二位和第四位[1]。子宫颈癌原发于子宫颈,其早期症状不明显,晚期则会出现阴道反复出血等临床症状,因此子宫颈癌患者临床就诊时往往已处于晚期,此时手术效果不佳,术后容易复发[2]。对于子宫颈癌晚期复发的患者,化疗是最佳的治疗手段[3-4]。目前临床使用的一线化疗方案是顺铂联合紫杉醇进行化疗,但是化疗的副作用明显,部分患者无法坚持完成化疗疗程[5-6]。为了解决这一问题,近年来阳江市人民医院采用紫杉醇(白蛋白结合型)联合顺铂对晚期复发子宫颈癌患者进行治疗,观察临床效果,分析治疗安全性,现报道如下。
1 资料与方法
1.1 一般资料
选择2020年1月-2021年6月于阳江市人民医院进行晚期子宫颈癌治疗的患者64例。纳入标准:(1)均确诊为子宫颈癌晚期,且复发;(2)肝肾功能健全;(3)无化疗禁忌证;(4)预计生存期超过6个月;(5)Karnofsky评分>70分。排除标准:(1)无法耐受化疗;(2)中途自动退出。使用随机数字表法将患者分为观察组和对照组,每组32例。观察组,年龄37~66岁,平均(55.19±4.82)岁;病理分型:鳞癌21例,腺癌8例,混合癌3例。对照组,年龄35~61岁,平均(55.29±5.57)岁;病理分型:鳞癌24例,腺癌6例,混合癌2例。两组基线资料比较,差异无统计学意义(P>0.05)。本研究已经医院伦理委员会批准,患者及家属均知情同意并签署知情同意书。
1.2 方法
对照组给予多西他赛联合顺铂(DP)方案进行治疗。具体方案如下:化疗前1 d开始给予地塞米松片(生产厂家:广东南国药业有限公司,批准文号:国药准字H44024618,规格:0.75 mg×100片)10 mg,1次 /d,静脉滴注,连续 3 d;化疗前给予苯海拉明(生产厂家:盐酸苯海拉明注射液,批准文号:国药准字 H37020713,规格:1 ml∶20 mg)20 mg肌注1次。多西他赛注射液(生产厂家:四川美大康佳乐药业有限公司,批准文号:国药准字H20123222,规格:1 ml∶20 mg)75 mg/m2,0.9% 氯化钠注射液250 ml,第1天,静点;顺铂(生产厂家:江苏豪森药业集团有限公司,批准文号:国药准字 H20040813,规格:6 ml∶30 mg/瓶)75 mg/m2,0.9%氯化钠注射液500 ml,第2、3天,静点。21 d为1个疗程,共4个疗程。
观察组给予注射用紫杉醇(白蛋白结合型)联合顺铂方案进行治疗。注射用紫杉醇(白蛋白结合型)(生产厂家:石药集团欧意药业有限公司,批准文号:国药准字H20183044,规格:100 mg/瓶)270 mg/m2,0.9% 氯化钠注射液 500 ml,第 1 天,静点;顺铂 75 mg/m2,0.9% 氯化钠注射液 500 ml,第2、3天,静点。21 d为1个疗程,共4个疗程。
两组治疗过程中根据出现的不良反应给予止呕、保肝等相应治疗。
1.3 观察指标及评价标准
比较两组临床疗效、治疗前后肿瘤最大径的变化、肝肾功能变化及不良反应。(1)临床疗效评价。参考文献[7]RECIST相关评价标准,完全缓解(CR):全部靶病灶均消失,所有病理淋巴结的短直径减少至<10 mm;部分缓解(PR):所有靶病灶直径之和与治疗前相比减少≥30%;稳定(SD):介于PR和PD间;进展(PD):靶病灶直径之和增加≥20%,且增加的绝对值≥5 mm,或出现新病灶。总有效=CR+PR+SD。(2)肝肾功能指标。包括谷丙转氨酶(ALT)、谷草转氨酶(AST)、总胆红素(TBIL),肾功能指标包括胱抑素C(CysC)、尿素氮(BUN)、血肌酐(Cr),血液标本收集后2 h内使用 3 000 r/min 离心机离心 20 min,取上清液,进行测定。CysC使用免疫投射比浊法测定,BUN、Cr使用酶法检测,所有指标使用奥林巴斯AU2700型生化检测仪进行测定,试剂盒为北京利德曼公司提供。所有操作严格按照试剂盒说明进行。所有检验均由本院常规实验室进行,固定由一名资深检验员进行操作。(3)不良反应。根据世界卫生组织(WHO)抗癌药物急性及亚急性毒性反应分度标准评估两组不良反应,分别为0~Ⅳ度,级别越高不良反应越严重[8]。比较两组骨髓抑制、消化道反应、脱发、肝肾功能损害、外周神经毒性等不良反应发生情况。
1.4 统计学处理
采用SPSS 19.0软件对所得数据进行统计分析,计量资料用(±s)表示,组间比较采用独立样本t检验,组内比较采用配对t检验;计数资料以率(%)表示,比较采用χ2检验,等级资料采用Mann-WhitneyU检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组临床疗效比较
观察组治疗总有效率为87.50%,明显高于对照组的65.63%,差异有统计学意义(P<0.05),见表1。
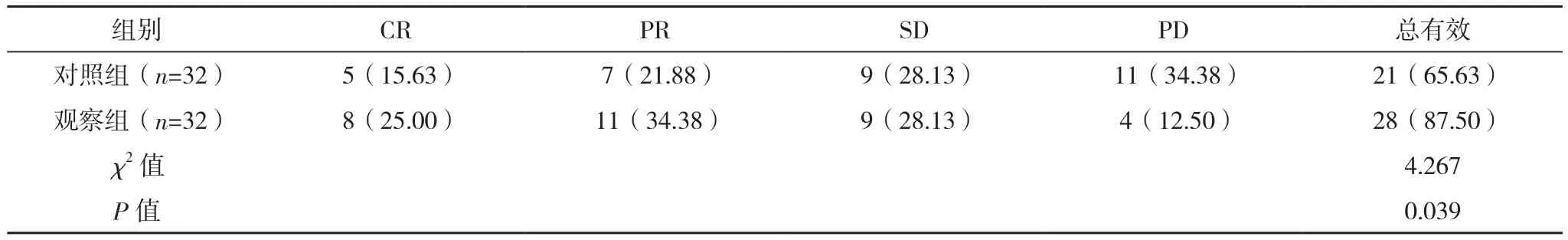
表1 两组临床疗效比较[例(%)]
2.2 两组治疗前后肿瘤最大径比较
治疗前,两组肿瘤最大径比较,差异无统计学意义(P>0.05);治疗后,两组肿瘤最大径较治疗前均缩小,且观察组小于对照组,差异均有统计学意义(P<0.05),见表 2。
表2 两组治疗前后肿瘤最大径比较[cm,(±s)]

表2 两组治疗前后肿瘤最大径比较[cm,(±s)]
组别 治疗前 治疗后 t值 P值对照组(n=32) 3.28±0.54 2.51±0.43 6.310 <0.001观察组(n=32) 3.19±0.66 2.02±0.41 8.518 <0.001 t值 0.597 4.665 P值 0.553 <0.001
2.3 两组治疗前后肝肾功能比较
治疗前,两组肝肾功能指标比较,差异均无统计学意义(P>0.05);治疗后,两组ALT、AST、TBIL、Cr、CysC、BUN均高于治疗前,但观察组上述指标均低于对照组,差异均有统计学意义(P<0.05),见表 3、表 4。
表3 两组治疗前后肝功能比较(±s)
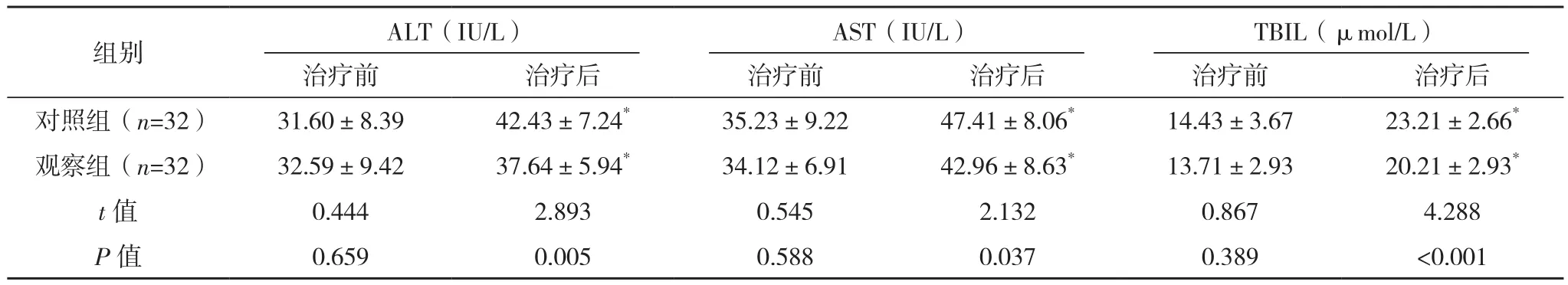
表3 两组治疗前后肝功能比较(±s)
*与本组治疗前比较,P<0.05。
治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组(n=32) 31.60±8.39 42.43±7.24* 35.23±9.22 47.41±8.06* 14.43±3.67 23.21±2.66*观察组(n=32) 32.59±9.42 37.64±5.94* 34.12±6.91 42.96±8.63* 13.71±2.93 20.21±2.93*t值 0.444 2.893 0.545 2.132 0.867 4.288 P值 0.659 0.005 0.588 0.037 0.389 <0.001组别 ALT(IU/L)AST(IU/L)TBIL(μmol/L)
表4 两组治疗前后肾功能比较(±s)

表4 两组治疗前后肾功能比较(±s)
*与本组治疗前比较,P<0.05。
治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组(n=32) 1.17±0.25 2.06±0.14* 121.58±18.06 219.55±46.17* 5.18±1.88 8.22±2.06*观察组(n=32) 1.14±0.13 1.51±0.10* 124.25±19.84 171.30±49.77* 5.12±2.04 7.11±2.11*t值 0.602 18.084 0.563 4.021 0.122 2.129 P值 0.549 <0.001 0.575 <0.001 0.903 0.037组别 CysC(mg/L)Cr(μmol/L)BUN(mmol/L)
2.4 两组化疗不良反应比较
两组骨髓抑制、消化道反应、脱发、肝肾功能损害、外周神经毒性发生程度比较,差异均有统计学意义(P<0.05),见表5。

表5 两组化疗不良反应比较(例)

表5(续)
3 讨论
子宫颈癌是发生于宫颈部位的恶性肿瘤,2018年世界卫生组织的统计表明其发病率为13/10万人,死亡率为7/10万人,仅2018年全球子宫颈癌发病56.9万例,死亡31.1万例[9]。我国40~50岁为子宫颈癌的发病高峰年龄段。人乳头状瘤病毒(HPV)已被确认为该病的最危险因素[10]。虽然子宫颈癌被认为是唯一一种可预防的恶性肿瘤,子宫颈癌疫苗近年来已经开始应用于临床,同时早期子宫颈筛查也提高了子宫颈癌早期发现的概率,降低了子宫颈癌的死亡率,但是,由于子宫颈癌早期没有明显症状,仍然有很多患者发现时已处于中晚期,无法根治,且容易复发[11]。因此,子宫颈癌仍然是威胁女性生命的主要恶性肿瘤之一。
紫杉醇联合顺铂一直作为子宫颈癌的一线化疗药物,但对晚期复发子宫颈癌而言,该治疗方案效果不如初发型子宫颈癌,而药物剂量也需要增加,这种情况下药物的毒副作用也会显著增加,患者往往由于不耐受药物而不得不中断治疗,或由于严重不良反应而降低生存质量[12]。
紫杉醇(白蛋白结合型)既往应用于治疗联合化疗失败的乳腺癌患者,或复发性乳腺癌患者,而不作为一线化疗用药,近年来开始尝试应用于晚期复发子宫颈癌患者。该药物不同于其他配方的紫杉醇制剂,是紫杉醇与白蛋白结合的药物。其中紫杉醇作为药物活性成分起到主要的抑制肿瘤的作用,而人血白蛋白作为辅料存在,起到分散、稳定微粒及运载紫杉醇的作用。紫杉醇通过对微管蛋白的作用而起到抑制肿瘤有丝分裂的作用,因此从理论上说,该作用机制可以适用于几乎所有的实体肿瘤,具有广谱、高效的特点[13]。但是紫杉醇具有一个非常明显的缺陷,紫杉醇的溶媒中含有聚氧乙基代蓖麻油,聚氧乙基代蓖麻油会刺激机体释放组胺,进而导致过敏。因此常规化疗中使用的紫杉醇用药前必须给予皮质激素和抗组胺药物的预处理,避免出现药物严重不良反应[14]。因此,2005年美国批准了首个紫杉醇(白蛋白结合型)药物,该药物通过纳米技术将药物和人血白蛋白结合成直径为130 nm的颗粒,显著降低了人体的过敏反应,同时也降低了紫杉醇化疗所导致的血液毒性、消化道毒性、神经毒性,也简化了给药方案[15]。
本研究结果显示,观察组治疗总有效率为87.50%,明显高于对照组65.63%,差异有统计学意义(P<0.05);治疗后,两组肿瘤最大径较治疗前均缩小,且观察组小于对照组,差异均有统计学意义(P<0.05)。说明对于晚期复发子宫颈癌而言,紫杉醇(白蛋白结合型)联合顺铂对肿瘤的抑制和杀伤效果优于多西他赛联合顺铂的治疗方案。这与白蛋白作为载体后,紫杉醇能够更好地被人体吸收有关,紫杉醇在人体的吸收率增加,就会在同等剂量的化疗药物用量下增加药物的治疗作用。治疗后,两组ALT、AST、TBIL、Cr、CysC、BUN均高于治疗前,但观察组上述指标均低于对照组,差异均有统计学意义(P<0.05)。两组骨髓抑制、消化道反应、脱发、肝肾功能损害、外周神经毒性发生程度比较,差异均有统计学意义(P<0.05)。说明虽然两组治疗方案均对患者的肝肾功能造成一定损伤,但是紫杉醇(白蛋白结合型)对肝肾功能的损伤较小,其他不良反应也较少。
综上所述,紫杉醇(白蛋白结合型)联合顺铂对晚期复发子宫颈癌有较好的临床效果,能够更好地抑制肿瘤,且安全性较高,对肝肾功能损伤小,副作用更低,更减少了预处理的过程,因此具有较好的临床应用前景。

