高效液相色谱法测定药物涂层球囊中紫杉醇含量的不确定度评定
孙钰朋,杜福映,郭利娟,张丽莹,孟晓依
(山东省医疗器械和药品包装检验研究院,国家药品监督管理局生物材料器械安全性评价重点实验室,山东省医疗器械生物学评价重点实验室,济南 250101)
支架内再狭窄是一种常见的经皮冠状动脉介入治疗的并发症,是由血管中膜炎性反应引起的平滑肌增殖和细胞外间质生成而造成的[1-3]。为了解决阻碍冠状动脉介入治疗发展的难题,人们设计了药物涂层支架并广泛应用[4-8]。但药物涂层支架同样会引发支架内再狭窄的问题[9],于是人们将药物涂层技术应用到球囊上,开发药物涂层球囊,以期攻克支架内再狭窄的难关[10-11]。
20 世纪60 年代,人们从太平洋紫衫中获得了具有抗肿瘤作用的提取物[12]。1971 年,Wani 等明确了提取物中关键成分的结构组成,并将这种成分命名为紫杉醇[13]。紫杉醇是第一种在临床应用的紫杉烷类化合物,对多种癌症都有良好的治疗作用[12]。此外,人们还发现紫杉醇具有抑制平滑肌细胞增殖的作用[14-15]。同时,紫杉醇的化学结构决定了其拥有较强的疏水性,使其在体内释放后能够在释放位置有效的保留[16]。紫杉醇的这些特性,使其成为了药物涂层球囊的首选药物[17]。
测量结果的质量应有定量的说明,以便评价其可靠程度。评定和表示测量结果的不确定度是一种表征测量结果质量的公认方法[18]。测量不确定度是表征合理地赋予被测量值的分散性,与其测量结果相联系的参数[19]。笔者用高效液相色谱法测定了药物涂层球囊中的紫杉醇含量[20],参照CNAS-G 006 《化学分析中不确定度的评估指南》[21],对测定过程中影响最终结果的不确定度来源进行了分析,并进行了不确定度评定,为测量结果的准确性和可靠性提供了有效的保证,为类似实验方法的监督评价提供了有力的数据支撑。
1 实验部分
1.1 主要仪器与试剂
高效液相色谱仪:Waters ACQUITY UPLC H-CLASS 型,美国沃特世公司。
电子天平:Mettler Toledo XP205型,感量为0.01 mg,瑞士梅特勒托利多公司。
涡旋混合器:VORTEX-5 型,海门市其林贝尔仪器制造有限公司。
超声清洗器:KQ3200DE 型,昆山市超声仪器有限公司。
紫杉醇对照品:质量分数为99.8%,批号为100382-201904,中国食品药品检定研究院。
乙腈、甲醇:均为色谱纯,德国默克公司。
实验用水:超纯水,由Millipore 纯水机制备。
1.2 实验步骤
1.2.1 标准溶液的配制
紫杉醇标准储备液:1 070.85 mg/L,精密称定紫杉醇标准品10.73 mg,置于10 mL 容量瓶中,用乙腈溶解,定容,摇匀。
紫杉醇标准工作溶液:用移液管分别精密量取0.10、0.20、0.50、0.80、1.00 mL 紫杉醇标准储备液,分别置于10 mL 容量瓶中,用乙腈定容,摇匀,得到质量浓度分别为10.71、21.42、53.54、85.67、107.1 mg/L 的紫杉醇系列标准工作溶液。
1.2.2 样品处理
取药物涂层球囊,置于具塞试管中,用移液管精密量取25.00 mL 乙腈置于试管中,摇匀,超声10 min,得到样品溶液。用移液管精密量取1.00 mL 样品溶液,置于10 mL 容量瓶中,用乙腈定容、摇匀,用0.22 μm 滤膜过滤,得到样品溶液。
1.2.3 色谱条件
色 谱 柱:Agilent XDB C-18 柱(150 mm×4.6 mm,5 μm,美国安捷伦科技有限公司);流动相:甲醇-水-乙腈(体积比为23∶41∶36,下同),流量为1.0 mL/min;柱温:35 ℃;检测波长:227 nm;进样体积:10 μL。
2 数学模型
药物球囊扩张导管中的紫杉醇含量按照式(1)计算:

3 测量不确定度来源
根据实验步骤及数学模型可知,影响样品中紫杉醇含量测定结果不确定度的因素有标准溶液配制、样品处理、标准曲线拟合、测量重复性等。实验过程中有关的不确定度来源如图1 所示。

图1 测量不确定度来源
4 测量不确定度评定
4.1 紫杉醇标准溶液配制过程引入的不确定度
紫杉醇标准溶液配制过程中产生的不确定度包括标准储备液和标准工作溶液引入的不确定度。
4.1.1 紫杉醇标准储备液质量浓度引入的不确定度

电子天平称量引入的相对标准不确定度:

(2)容量瓶引入的不确定度:所用10 mL(Vs)容量瓶经过计量校准,其校准证书显示扩展不确定度U(Vs)=0.007 mL(k=2)。由此可知,10 mL 容量瓶引入标准不确定度:
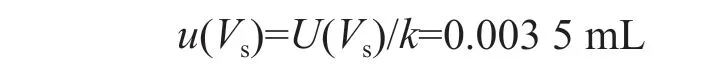
10 mL 容量瓶引入相对标准不确定度:

(3)温度变化引入的不确定度:实验室的温度为(20±5)℃,温度波动引起的体积变化呈均匀分布,k= 3,溶剂乙腈的体积膨胀系数为1.37×10-3℃-1,则10 mL 容量瓶因温度变化引入的相对标准不确定度:

(2)溶液稀释定容引入的不确定度:由4.1.1(2)可知,所用10 mL 容量瓶引入的相对标准不确定度urel(V10)=0.000 35。

4.2 样品处理过程引入的不确定度
药物涂层球囊前处理过程中产生的不确定度包括样品溶液制备和稀释引入的不确定度。
4.2.1 样品溶液移取引入的不确定度
实验室所用25 mL 移液管经过计量校准,其校准证书显示扩展不确定度U(V25)=0.007 mL(k=2)。由此可知,标准不确定度u(V25)=U(V25)/k=0.003 5 mL,相对标准不确定度urel(V25)=u(V25)/25=0.000 14。则样品溶液移取引入的相对标准不确定度:
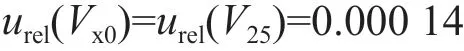
4.2.2 样品溶液稀释引入的不确定度
(1) 1 mL 移液管引入的不确定度。由4.1.2(1)可知,1 mL 移液管引入的相对标准不确定度urel(V1)=0.002。
(2) 10 mL 容量瓶引入的不确定度。由4.1.2(2)可知,所用10 mL 容量瓶引入的相对标准不确定度urel(V10)=0.000 35。
将以上两个分量合成,得样品溶液稀释引入的相对标准不确定度:

4.3 测量重复性产生的不确定度
笔者对7 份药物涂层球囊进行了测定,每份样品重复测定3 次,结果见表1。
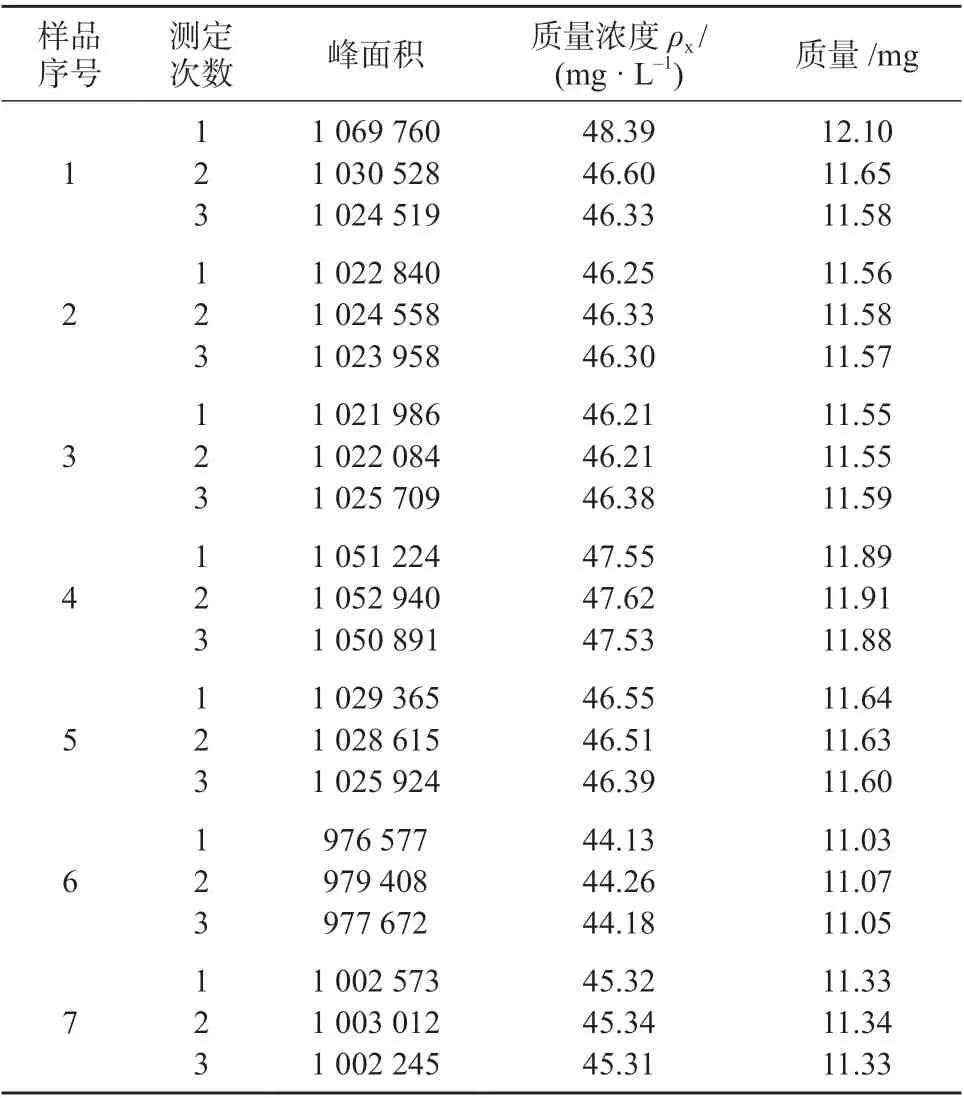
表1 紫杉醇含量测定结果
根据上述测定结果计算得知,药物涂层球囊中紫杉醇含量平均值mav=11.54 mg,测定次数为21次,计算得单个测定值的标准偏差s=0.281 0 mg,本次实验由测量重复性引入的标准不确定度:

由测量重复性引入相对标准不确定度:
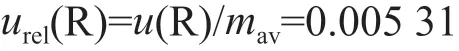
4.4 标准曲线拟合引入的不确定度
对每个浓度的紫杉醇标准工作溶液重复测定3 次,得到的色谱峰面积列于表2。根据最小二乘法,拟合得到标准曲线方程y=21 883ρ+10 784,r2=0.999 8。
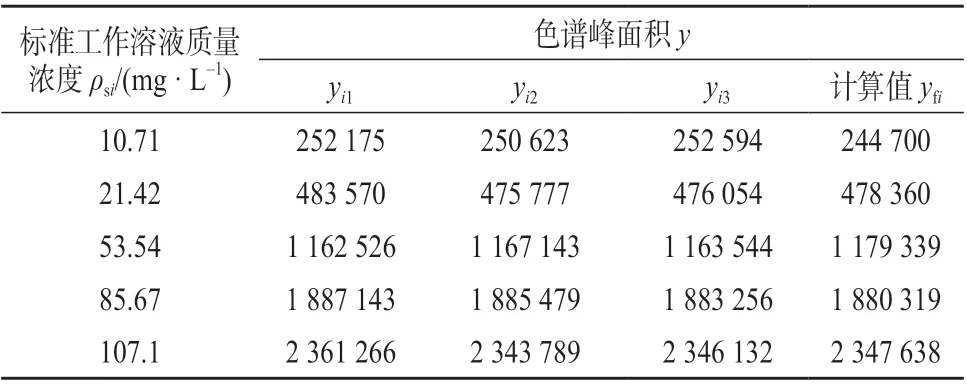
表2 紫杉醇标准工作溶液浓度、色谱峰面积对应关系

将表2 数据代入式(2)计算可得s(y)=10 367.32。

4.5 合成标准不确定度
根据上述相对标准不确定度的分析与计算,高效液相色谱法测定药物涂层球囊中紫杉醇含量的合成相对标准不确定度:
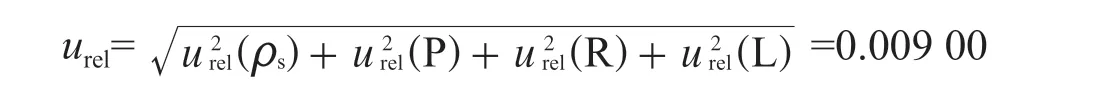
药物球囊扩张导管中紫杉醇含量m=11.54 mg,则合成标准不确定度u=m×urel=0.104 mg。
测定过程中各个不确定度分量对最终的不确定度贡献大小见表3。

表3 不确定度分量统计表
根据表3 可知,高效液相色谱法测定药物涂层球囊中紫杉醇含量的测量不确定度主要来自测量重复性和标准工作溶液的配制两个方面。样品溶液的制备与稀释过程,对最终结果的不确定度影响较小。
4.6 扩展不确定度和结果报告
根据GB/T 27418—2017 《测量不确定度评定和表示》的规定,测量不确定度最多为两位有效数字[18]。按正态分布,取包含因子k=2,即包含概率为95%,则扩展不确定度U=u×k=0.21 mg。高效液相色谱法测定药物涂层球囊中紫杉醇含量的结果可表示为(11.54±0.21) mg(k=2)。
5 结语
通过建立高效液相色谱法测定药物涂层球囊中紫杉醇含量不确定度评价模型,保证了对药物涂层球囊中紫杉醇含量测试结果的有效性和合理性,为高效液相色谱法测定药物涂层球囊中紫杉醇含量的质量控制提供了有效而可靠的测量体系。高效液相色谱法测定药物涂层球囊中紫杉醇含量的测量不确定度来源主要是测量重复性和标准工作溶液的配制。因此,在测定过程中,实验人员可以增加样品重复测量次数,以减少测量重复性对测量结果的影响。同时,实验人员应注意测试操作的规范性,确保测量结果的准确可靠。

