经导管主动脉瓣置换术中对合缘对齐和冠状动脉对齐的研究进展
奚思宇 张海山 高远 梁长彬 孙英贤 郭亮
既往认为外科主动脉瓣置换术(surgical aortic valve replacement,SAVR)是主动脉瓣狭窄(aortic stenosis,AS)患者的标准治疗方案,而经导管主动脉瓣置换术(transcatheter aortic valve replacement,TAVR)仅适用于高龄、合并症多或心肺功能差的外科手术风险高危或禁忌的AS患者[1]。但是近年来,随着TAVR技术的成熟,TAVR逐渐被应用于外科手术中低风险或年轻的患者[2]。因此,如何避免TAVR术中急性冠状动脉闭塞,保证术后有可行的冠状动脉路径以及提高瓣膜的耐久性等问题的研究日益得到重视[3-7],并提出了对合缘对齐和冠状动脉对齐技术。
1 定义
对合缘指的是原生或人工瓣膜相邻瓣叶的结合部位。对合缘对齐是指在主动脉瓣置换术中将人工瓣膜对合缘与原生瓣膜对合缘对齐。
对合缘对齐的评价方法:因瓣膜置换术后,原生瓣膜对合缘难以识别,故通常根据冠状动脉与对合缘的相对关系来评价对合缘的对齐程度。通过比较术前和术后的CT以确定对合缘对齐的程度:先在垂直于主动脉轴的横截面上确定右冠状动脉的位置,通过右冠状动脉和主动脉中心点画一条直线,分别测量该线与右冠状动脉窦(right coronary cusp,RCC)/左冠状动脉窦(left coronary cusp,LCC)对合缘、LCC/无冠状动脉窦(noncoronary cusp,NCC)对合缘、NCC/RCC对合缘的成角,计算其在术前、术后计算机断层显像(computed tomography,CT)上的差值,最后计算平均角度偏差,分为精准对齐(≤15°偏差)或轻度(>15°且≤30°偏差)、中度(>30°且≤45°偏差)或重度(>45°且≤60°偏差)对合缘未对齐(commissural misalignment,CMA)[8]。如图1所示,测量术前、术后CT中各对合缘与右冠状动脉之间成角并计算出平均差值为36.3°,即中度CMA。

图1 计算术前、术后计算机断层显像上各对合缘与右冠状动脉之间成角的差值,最终得出平均差值为36.3°,即中度对合缘未对齐
冠状动脉对齐是指在主动脉瓣置换术中将人工瓣膜对合缘置入于左、右冠状动脉开口的正中位置,也就是说将人工瓣膜对合缘与左、右冠状动脉开口的角平分线对齐。
冠状动脉对齐的评价方法:重度冠状动脉重叠,是指瓣膜置换术后人工瓣膜对合缘与冠状动脉开口之间的成角为≤20°;中度冠状动脉重叠,成角为>20°且≤35°;无冠状动脉重叠风险,成角为>35°[9]。如图2所示,术后CT提示左、右冠状动脉开口的角平分线与人工瓣膜对合缘的成角为10°(图2A),左冠状动脉开口与最近的人工瓣膜对合缘的成角为46°(图2B),右冠状动脉开口与最近的人工瓣膜对合缘的成角为38°(图2C),即双侧冠状动脉均无重叠风险。

图2 术后断层显像提示左、右冠状动脉开口的角平分线(橙色虚线)与人工瓣膜对合缘(白色虚线)的成角为10°(A);左冠状动脉开口与最近的人工瓣膜对合缘的成角为46°(B);右冠状动脉开口与最近的人工瓣膜对合缘的成角为38°(C),即左、右冠状动脉均无重叠风险
2 对合缘对齐和冠状动脉对齐的比较
对于大多数患者来说,左、右冠状动脉分别位于左、右冠状动脉窦的中心位置,即对合缘之间的中心位置,因此对合缘对齐和冠状动脉对齐应该是相同的。
Wang等[10]连续性纳入400例接受TAVR治疗的患者[200例三叶式主动脉瓣(tricuspid aortic valve,TAV),200例type 1二叶式主动脉瓣(bicuspid aortic valve,BAV)],比较其左冠状动脉窦-右冠状动脉窦中心线及左、右冠状动脉中心线的差异并将其分为四组:无差异(≤10°),轻度差异(>10°且≤20°),中度差异(>20°且≤30°)和重度差异(>30°)。最终得出结论:在97%的三叶瓣患者和93%的二叶瓣患者中,左冠状动脉窦-右冠状动脉窦中心线及左、右冠状动脉中心线无差异或仅有轻度差异,并且三叶瓣和二叶瓣患者中该差异的分布相似。也就是说,在大多数患者中,TAVR术中使用左右冠状动脉窦重叠法以获得对合缘对齐的同时也能有效地将这一人工瓣膜对合缘置入左、右冠状动脉开口的中心附近,即获得冠状动脉对齐。
3 保证对合缘对齐的优势
3. 1 避免冠状动脉术中闭塞
冠状动脉闭塞(coronary obstruction,CO)是TAVR的一种少见但十分凶险的并发症,发生率小于1%,而死亡率却接近50%,其中左主干最常受累,分为急性CO和延迟性CO[11]。TAVR术中出现急性CO时,患者常表现为严重低血压,超过50%的患者心电图会出现ST段抬高,且其中1/3以上的患者会出现心律失常,以室性心律失常为主[12]。CO的常见原因有冠状动脉开口高度过低、主动脉窦相对较小、原生瓣膜的瓣叶冗长或肥厚、瓣尖团状钙化附着、窦管结合部较低且内径较小等。除此之外,重度对合缘未对齐或重度冠状动脉重叠导致人工瓣膜对合柱遮挡冠状动脉也是TAVR术中CO的重要原因。
另外,对于计划行二次TAVR即瓣中瓣的患者来说,CO的风险约是首次行TAVR的6倍。在这种情况下,可能会需要使用主动脉瓣叶切割预防医源性冠状动脉阻塞(BASILICA)技术以增加冠状动脉的灌注,降低CO的发生率。当冠状动脉开口在主动脉窦中心时,BASILICA技术可以发挥最大的治疗效果。虽然该技术的安全性和有效性还未得到确切证实,但可以肯定的是,该技术不适用于中重度CMA患者。因此,首次TAVR时保证对合缘对齐也同样重要[13-15]。
3. 2 保证TAVR术后有可行的冠状动脉路径
研究表明重度AS患者中有50%合并严重的冠状动脉疾病,这可能是由于二者具有相同的危险因素如年龄、性别、高血压病、吸烟、高脂血症等。因此随着行TAVR术患者的年轻化,对于TAVR术后冠状动脉介入治疗通路的研究也变得越来越重要[16-17]。
2020年Ochiai等[18]通过分析66例置入Evolut R/Evolut PRO瓣膜和345例置入SAPIEN 3瓣膜患者的术后CT,将冠状动脉开口位于裙边下方或裙边上方人工瓣膜联合柱前定义为术后冠状动脉通路不良。结果发现Evolut R/Evolut PRO组左冠状动脉34.8%(23例)、右冠状动脉25.8%(17例),SAPIEN 3组左冠状动脉15.7%(54例)、右冠状动脉8.1%(28例)存在TAVR术后冠状动脉通路不良,并且在16例接受Evolut R/Evolut PRO瓣膜以及64例接受SAPIEN 3瓣膜置入后行冠状动脉介入治疗的患者中,冠状动脉通路不良的患者择期行冠状动脉介入治疗的成功率较通路良好的患者显著降低,其中Evolut R/Evolut PRO组(0比77.8%,P=0.003)和SAPIEN 3组(33.3%比91.4%,P=0.003)的差异均有统计学意义。因此,术后冠状动脉通路不良严重影响了患者术后冠状动脉的诊断治疗,通过优化冠状动脉对齐可以很大程度上解决这一问题。
3. 3 减轻TAVR术后主动脉瓣中心反流的发生率,增加人工瓣膜的耐久性
由于AS患者瓣环及瓣叶钙化不均匀,原生瓣叶的对合缘和瓣叶对人工瓣架挤压程度存在不均一性,这就决定了对合缘的对齐情况不同可能对人工瓣架产生不均一的挤压,从而影响了人工瓣膜的功能和耐久性。
2018年Fuchs等[8]对28例接受SAVR治疗的患者和212例接受TAVR治疗的患者,术前、术后CT进行分析以确定对合缘对齐的程度,通过出院前和3个月随访时的经胸超声心动图检查结果,评估左心室射血分数、主动脉跨瓣压的平均值和峰值、主动脉瓣口面积、主动脉瓣中心和瓣周反流以及二尖瓣反流,并采用计算流体动力学模拟的方法研究对合缘对齐对冠状动脉充盈的影响。发现28例接受SAVR治疗的患者中有27例(96%)精准对齐,1例为轻度CMA。212例接受TAVR治疗的患者中22%为精准对齐,25%为轻度CMA,22%为中度CMA,31%为重度CMA。出院前经胸超声心动图提示,中重度CMA的患者(7/112,6.3%)轻度主动脉瓣中心反流的发生率显著高于轻度CMA或精准对齐的患者(1/100,1.0%)(P=0.046)。分析3个月后的经胸超声心动图也得到了相同的结论(7.8%比1.1%,P=0.030)。另外,对合缘对齐可能会减少人工瓣膜瓣叶的压力,尤其是针对椭圆形的原生瓣膜而言,从而延长其寿命,即瓣膜的耐久性[19]。因此,保证对合缘对齐可以降低TAVR术后主动脉瓣中心反流的发生率,增加人工瓣膜的耐久性。
4 局限性
4. 1 冠状动脉口的偏心性
冠状动脉口的偏心性通常用冠状动脉偏心角度来表示:在术前CT上分别将左、右冠状动脉开口以及相应的主动脉窦(左冠状动脉窦/右冠状动脉窦)中心与主动脉瓣中心点连线,测量两线间夹角即冠状动脉偏心角度。
虽然在大多数情况下获得对合缘对齐的同时也能获得冠状动脉对齐,但是由于冠状动脉口的偏心性,少数病例即使在人工瓣膜与原生瓣膜对合缘精准对齐的情况下,也会出现严重的冠状动脉重叠。2022年Redondo等[9]通过分析100例接受TAVR治疗的患者,将其基于潜在的BASILICA疗效(最佳的是冠状动脉开口在主动脉窦中心)分为3组:无冠状动脉重叠发生风险(从对合缘到冠状动脉开口>35°),中度风险(>20°且≤35°),重度风险(≤20°),得出100例中有32例尽管是理想的对合缘对齐,但仍存在中重度冠状动脉重叠(≤35°)的风险。该研究还指出右冠状动脉相对于左冠状动脉呈较高的偏心性,瓣膜按对合缘对齐置入后存在中重度冠状动脉重叠发生风险的解剖截断点为右冠状动脉偏心角度>24.5°,左冠状动脉偏心角度>19°,或冠状动脉间夹角>147.5°或<103°。此时通过优化冠状动脉对齐可以有效防止重度冠状动脉重叠,减少中度冠状动脉重叠的发生率,同时提高后期冠状动脉路径的可行性。
4. 2 主动脉窦的对称性
通常在术前CT上先分别测量三个主动脉窦两侧对合缘间的夹角,然后根据最大的主动脉窦夹角定义主动脉窦对称性:对称(≥120°且≤125°),轻度不对称(>125°且≤130°),中度不对称(>130°且≤135°)及重度不对称(>135°)。
有研究得出TAV与BAV主动脉窦对称性的差异无统计学意义(P<0.001)[10]。50%的TAV主动脉窦严格对称,只有2.5%的TAV主动脉窦为重度不对称,而52.5%的BAV主动脉窦为重度不对称。因此,对合缘对齐技术对于BAV的应用有其局限性。与TAV相比, BAV患者因其瓣膜结构特殊,出现AS症状较早,瓣膜钙化程度也相对较重[20],我国目前行TAVR患者的平均年龄低于欧美国家,出现BAV的概率也相应增加,所以优化冠状动脉对齐可能更适合于我国的TAVR。
5 对合缘对齐和冠状动脉对齐的实现方法
既往认为SAVR置入的人工瓣膜与原生瓣膜的对合缘是精准对齐的,而TAVR置入的瓣膜是随机放置的,因此与原生瓣膜之间的关系也是随机的[8]。但是近年来,随着TAVR技术的提高,术者逐渐可以控制TAVR术中瓣膜的置入方向。
5. 1 ACURATE系列瓣膜
ACURATE系列瓣膜是波科公司研发的一种自膨胀式瓣膜系统,其释放方式不同于其他自膨胀瓣膜自下而上地释放。ACURATE系列瓣膜自上而下地释放,即先释放远心端,露出锚定装置,自动定位后,再释放近心端。由于远心端较大的支架网格孔径,瓣膜置入后对未来行冠状动脉介入治疗的影响较小[21]。ACURATE瓣膜的对合缘上方设计有X线下清晰可辨的对合柱,在不同的X线透视角度下显示出不同的形态,并且可以自由旋转调整对合缘方向。如图3A所示,在左右冠状动脉窦重叠角度上,旋转瓣膜使其中一个对合柱呈90°,另两个对合柱呈30°,释放后如图3C所示,总体上呈II-I的形态,右侧对合柱刚好位于原生瓣膜LCC/RCC对合缘处。在三窦共面角度上,如图3B所示,旋转瓣膜使其中一个对合柱呈0°,另两个对合柱呈60°,释放后如图3D所示,总体上呈I-I-I的形态。但是在三窦共面角度上,很难辨别中间的对合柱在透视图的前方还是后方,可能为精准对齐,也可能是重度CMA,因此需通过旋转观察对合柱运动方向或其他体位进一步确定对合柱位置。这种方法目前仅有小部分中心进行尝试,尚未广泛应用[22]。
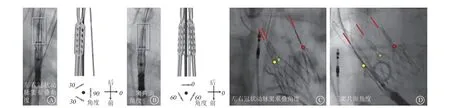
图3 在左右冠状动脉窦重叠角度上,旋转瓣膜使其中一个对合柱呈90°,另两个对合柱呈30°(A),释放后总体上呈II-I 的形态(C);在三窦共面角度上,旋转瓣膜使其中一个对合柱呈0°,另两个对合柱呈60°(B),释放后总体上呈I-I-I 的形态(D)
2021年Kitamura等[22]比较了10例采用左右冠状动脉窦重叠位进行对合缘对齐法置入ACURATE neo瓣膜的患者和16例随机置入的患者。采用左右冠状动脉窦重叠位进行对合缘对齐时旋转人工瓣膜使其中一个对合柱位于透视图的最右侧,即与原生瓣膜LCC/RCC对合缘对齐。术后CT分析发现采用该方法置入与随机置入瓣膜的患者实现对合缘精准对齐的比例(90%比31%,P=0.005)。同年Bieliauskas等[23]也对采用上述方法行ACURATE neo2瓣膜置入的20例患者进行研究,发现TAVR术中旋转输送系统使冲洗孔朝向6点钟方向更容易实现对合缘对齐,并且根据术后CT统计得出其中15例精准对齐,5例轻度CMA,成功避免了中重度CMA。因此,左右冠状动脉窦重叠位进行对合缘对齐法是安全可行的。
但是,上述研究中提出的人工瓣膜的置入方法是针对对合缘对齐的,并不适用于冠状动脉口严重偏心或者主动脉窦重度不对称的患者。2021年De Marco等[24]通过对45例置入ACURATE neo瓣膜行TAVR治疗的患者进行研究分析,提出了针对冠状动脉对齐的个体化的CT分析方法。根据术前CT确定左、右冠状动脉的角平分线处,取其向右冠状动脉偏移30°方向为投射点进行瓣膜置入,相当于左冠状动脉切线位(图4A),然后如图4B所示,旋转输送系统使冲洗孔朝向6点钟方向,置入过程中如图4C所示,旋转人工瓣膜使其中1个对合柱位于屏幕最左侧,另外两个对合柱位于右侧,此时理论上可以如图4D所示完全避免冠状动脉的重叠,术后CT发现45例患者均未出现重度冠状动脉重叠。该研究还对人工瓣膜和原生瓣膜对合缘对齐的情况进行评估:45例患者中有34例精准对齐、9例轻度CMA、2例中度CMA,没有重度CMA。因此,基于此个体化CT分析算法进行冠状动脉对齐的方法是安全有效的,可以有效避免人工瓣膜对合缘和冠状动脉的重叠,同时提高对合缘对齐的程度。

图4 根据术前CT 确定左、右冠状动脉的角平分线处(黄色虚线),取其向右冠状动脉偏移30°方向为投射点(蓝色虚线)行瓣膜置入(A),旋转输送系统使冲洗孔朝向6 点钟方向(B),置入过程中旋转人工瓣膜使其中1 个对合柱位于屏幕最左侧,另外两个对合柱位于右侧(C),此时理论上可以完全避免冠状动脉的重叠(D)
5. 2 Evolut系列瓣膜
Evolut系列瓣膜是美敦力公司的一种自膨胀式瓣膜系统,瓣架的远心端有一个C-tab标识,对应人工瓣膜的一个对合缘,其输送系统胶囊部位也有“帽子”标识(hat marker),并且在TAVR术中的透视图下两者呈90°夹角关系,该标记有助于实现对合缘对齐。
2018年Tang等[25]首先对17例接受CoreValve/Evolut R瓣膜行TAVR治疗的患者进行回顾性研究,发现52.9%的患者中人工瓣膜的对合缘与一支或双侧冠状动脉重度重叠,并且发现瓣膜初始的置入方向可能会影响最终对合缘对齐程度。2019年Tang等[26]又对来自2个中心的118例接受EvolutR/Pro瓣膜的患者进行研究,将位于输送系统胶囊部位的“帽子”标识在术中透视图(三窦共面角度)上的位置分为中心后侧(center back,CB)、小弯侧(inner curve,IC)、大弯侧(outer curve,OC)和中心前侧(center front,CF),并且将置入后瓣膜上的C-tab标识所在位置也按上述方法进行描述。结果显示,33.1%的患者术后左冠状动脉重度重叠,20.3%右冠状动脉重度重叠,14.4%双侧冠状动脉重度重叠,39.0%一支或双侧冠状动脉重度重叠。而对于“帽子”标识在初始插入时处于OC或者CF位置的患者来说,术后仅19.5%左冠状动脉重度重叠,6.1%右冠状动脉重度重叠,2.4%双侧冠状动脉重度重叠,23.2%一支或双侧冠状动脉重度重叠(P<0.001)。2020年Tang等[5]对来自多个中心的245例接受Evolut瓣膜的患者采用上述方法进行研究也得出相同结论。25.3%的患者术后左冠状动脉重度重叠,15.5%右冠状动脉重度重叠,9.8%双侧冠状动脉重度重叠,31.0%一支或双侧冠状动脉重度重叠。与“帽子”标识初始放置位于IC和CB上相比,在OC和CF方向上冠状动脉重度重叠的发生率明显降低(P<0.001):左冠状动脉15.7%比66.0%,右冠状动脉7.1%比51.1%,双侧冠状动脉重度重叠2.5%比40.4%,一支或双侧冠状动脉重度重叠20.2%比76.6%。此外,该研究对其中连续的107例患者采用以下方法进行操作:旋转输送系统使冲洗孔朝向3点钟方向进入体内,输送系统胶囊上的“帽子”标识在降主动脉和瓣环平面时处于OC位置(图5A~B),瓣膜释放后C-tab指向IC方向,最终获得良好的冠状动脉对齐(图5C)。与既往传统操作,即冲洗孔朝向12点钟方向相比,冲洗孔朝向3点钟方向更容易使“帽子”标识在初始置入时处于OC或CF的位置,从70.2%提高到91.6%(P=0.002)。冠状动脉重度重叠发生率也大大降低,左冠状动脉重度重叠从31.4%降至18.7%(P=0.033),右冠状动脉重度重叠从20.7%降至11.2%(P=0.071),双侧冠状动脉重度重叠从14.0%降至5.6%(P=0.047),一支或双侧冠状动脉重度重叠从38.0%降至24.3%(P=0.032)。2021年Tang等[27]再次比较240例采用上述改良方法和154例采用传统技术置入Evolut瓣膜的患者,发现采用改良的TAVR置入技术可以使冠状动脉重度重叠的发生率明显降低(P<0.01),其中左冠状动脉重度重叠14.2%比27.9%,右冠状动脉重度重叠11.7%比27.3%,双侧冠状动脉重度重叠5.0%比13.6%,一支或双侧冠状动脉重度重叠20.8%比41.6%。综上,针对Evolut瓣膜,输送系统进入体内时冲洗孔朝向3点钟方向更有利于“帽子”标识在初始置入时处于OC或者CF位置,进而提高最终置入时的冠状动脉对齐程度。
虽然上述方法简单并且安全有效,但是并未针对患者主动脉根部的具体解剖结构进行个体化分析。2021年Kitamura等[28]也针对Evolut瓣膜进行了一次研究并且提出了新的置入方法:由于Evolut瓣膜上的C-tab和“帽子”标识呈90°夹角关系,故如图5D所示,采用左右冠状动脉窦重叠位行瓣膜置入时保证C-tab位于透视图的最右侧即与原生瓣膜LCC/RCC对合缘对齐,同时可以保证“帽子”标识位于透视图的中心前侧,若此时释放瓣膜,理论上可实现对合缘精准对齐。该方法应用于13例行SAVR术后人工瓣膜衰败需行TAVR术的患者中,其中12例患者术中“帽子”标识成功位于透视图的中心前侧,术后CT中仅发现1例(7.7%)右冠状动脉重度重叠,均未发生左冠状动脉重度重叠。因此,该方法可以有效地降低重度冠状动脉重叠的发生率,但是该方法在原生瓣膜中(即首次TAVR)的可行性还有待进一步研究。
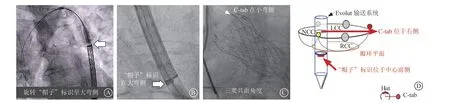
图5 在三窦共面角度上,旋转Evolut 输送系统使“帽子”标识在降主动脉(A)和瓣环平面(B)时处于大弯侧,瓣膜释放后C-tab 指向小弯侧(C);模式图(D)在左右冠状动脉窦重叠位上,使Evolut 瓣膜的C-tab 位于右侧与右冠状动脉窦/左冠状动脉窦对合缘对齐,“帽子”标识位于中心前侧,即可保证对合缘对齐
5. 3 其他
5. 3. 1 SAPIEN 3系列瓣膜 SAPIEN 3系列瓣膜是爱德华公司的球扩式主动脉瓣膜系统,因其独特的短支架结构,使得置入该瓣膜后再行冠状动脉介入治疗时导丝或导管可以直接跨过人工瓣膜到达冠状动脉开口处,但是保证对合缘对齐对于提高瓣膜的耐久性、二次TAVR以及BASILICA技术的应用仍有一定的意义。2020年Tang等[5]的一项多中心研究中,对483例接受SAPIEN 3瓣膜患者的术前CT及术中透视图(三窦共面角度)进行了分析,瓣膜的一个对合缘初始装载方向如下:3点钟方向104例(21.5%),6点钟方向126例(26.1%),9点钟方向136例(28.2%),12点钟方向117例(24.2%)。结果显示,总体上左冠状动脉重度重叠的发生率为36.9%,右冠状动脉重度重叠为38.7%,双侧冠状动脉重度重叠为23.6%,一支或双侧冠状动脉重度重叠为51.3%。其中左冠状动脉重度重叠(P=0.71)、双侧冠状动脉重度重叠(P=0.19)、一支或双侧冠状动脉重度重叠(P=0.10)的发生率与瓣膜的初始装载方向无关,但是右冠状动脉重度重叠更容易发生在初始装载方向为6点钟方向(6点钟方向51.6%,3点钟方向28.8%,9点钟方向36.8%,12点钟方向35.9%,P=0.003)。因此,SAPIEN 3瓣膜的初始装载方向对冠状动脉对齐程度几乎没有影响,具体如何实现对合缘对齐有待进一步研究。
5. 3. 2 国产自膨胀瓣膜 目前尚无国产瓣膜对合缘对齐或冠状动脉对齐的相关研究报道。
6 总结与展望
随着Venus A plus、Vita-Flow Ⅱ、Taurus-elite等瓣膜的出现,中国开始进入TAVR瓣膜的可回收时代。瓣膜置入难度略有下降,其置入深度、瓣膜大小的选择和瓣周漏等问题得到了有效解决,更多医师开始关注输送系统的轴向调整问题,即对合缘对齐技术。与此同时,我国TAVR逐渐应用于外科手术中低风险或年轻的患者,预期寿命逐渐延长,对于人工瓣膜使用寿命的要求也就越来越高,未来术后需要行冠状动脉造影或介入治疗的患者数量也将逐渐增多。因此,研究如何提高TAVR术中对合缘对齐和冠状动脉对齐技术尤为重要。然而,现有的数据大多是针对进口瓣膜的,缺少对国产瓣膜的研究,因此,针对国产瓣膜的对合缘对齐和冠状动脉对齐的技术有待进一步探索。
利益冲突所有作者均声明不存在利益冲突

