ACEF评分联合炎性因子评估小儿川崎病冠状动脉损害的临床价值
彭 珍,闫孝永
川崎病是一种以全身中型、小型血管特异性炎症为主的自身免疫性疾病,也称为皮肤黏膜淋巴结综合征,多见于0~5岁的儿童[1]。川崎病在世界范围内均有发生,亚裔人群中发病率最高,我国川崎病发病率逐年增加[2]。川崎病为全身性血管炎症,易发生在冠状动脉,因此,川崎病患儿多伴有冠状动脉损害,严重者出现心肌梗死甚至死亡[3]。川崎病发病机制尚未明确,急性期炎性因子水平升高[4]。炎性因子种类众多,发挥主要作用的包括肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(interleukin-1β,IL-1β)、白细胞介素-6(IL-6)、白细胞介素-10(IL-10)等。年龄、肌酐和射血分数(age,creatinine and ejection fraction,ACEF)评分对心血管疾病的危险分层有重要的参考意义[5]。本研究观察ACEF评分联合炎性因子构建预测模型评估小儿川崎病并发冠状动脉损害的风险。
1 资料与方法
1.1 研究对象 选取2017年3月—2019年2月在我院住院的川崎病患儿113例。参与本研究的患儿家长均已知晓本研究内容,并签署知情同意书。
1.2 纳入与排除标准
1.2.1 纳入标准 川崎病诊断标准:初次发作,发病年龄<6岁;持续5d以上发热,且不明原因,经抗生素治疗无效;具有以下5项临床症状中的4项及以上,①双眼结膜充血,且无脓性分泌物;②口腔及咽部黏膜充血,口唇发干、皲裂,舌乳头出现凸起;③皮疹,无结痂和水疱;④手足硬性水肿,掌趾红斑;⑤颈部淋巴结非脓性肿大;若患儿经心脏超声诊断出现冠状动脉损害,无需出现上述5种症状中的4种。冠状动脉损害诊断标准:患儿<5岁,冠状动脉内径>3 mm;患儿≥5岁,冠状动脉内径>4 mm;冠状动脉局部内径较邻近节段扩大1.5倍以上;内径z值≥2.0;冠状动脉内膜回声增强或动脉管腔出现明显不规则回声。
1.2.2 排除标准 入院后使用丙种球蛋白或糖皮质激素的患儿;葡萄球菌、肺炎衣原体感染等炎症疾病患儿;药物过敏、黏膜皮肤眼综合征、重症多发性红斑等非特异性炎症患儿;血培养阳性的败血症患儿;患有遗传代谢病、原发性心、脑、肾功能障碍疾病、肿瘤等;资料不全或患儿家长不同意行心脏超声检查。
1.3 研究方法 收集患儿临床资料,包括性别、年龄、川崎病类型、发热时间等。入院后次日清晨抽取患儿空腹静脉血5 mL,离心取上层血清,采用全自动细胞计数仪检测外周白细胞计数(white blood cell,WBC),采用血细胞分析仪检测血红蛋白(hemoglobin,Hb)、红细胞分布宽度(red cell volume distribution width,RDW),采用自动红细胞沉降速率分析仪检测红细胞沉降率(erythrocyte sedimentation rate,ESR),采用透光率比浊法检测血小板计数(blood platelet,PLT),采用血脂生化检测试剂盒检测三酰甘油(triglyceride,TG)、高密度脂蛋白胆固醇(high density lipoproten-cholesterol,HDL-C)、低密度脂蛋白胆固醇(low density lipoproten-cholesterol,LDL-C),采用酶联免疫吸附法检测C反应蛋白(C-reactive protein,CRP)、IL-1β、IL-6、IL-10、TNF-α。入院5~7 d 后行心脏超声检查,若患儿符合冠状动脉损害诊断标准,作为冠状动脉损害组,其他患儿纳入非冠状动脉损害组。ACEF=年龄/左室射血分数+1(若肌酐>176 μmol/L)。

2 结 果
2.1 冠状动脉损害组和非冠状动脉损害组临床资料比较 113例患儿中,发生冠状动脉损害46例。冠状动脉损害组和非冠状动脉损害组ESR、IL-1β、IL-6、IL-10、TNF-α和ACEF评分比较,差异有统计学意义(P<0.05)。详见表1。
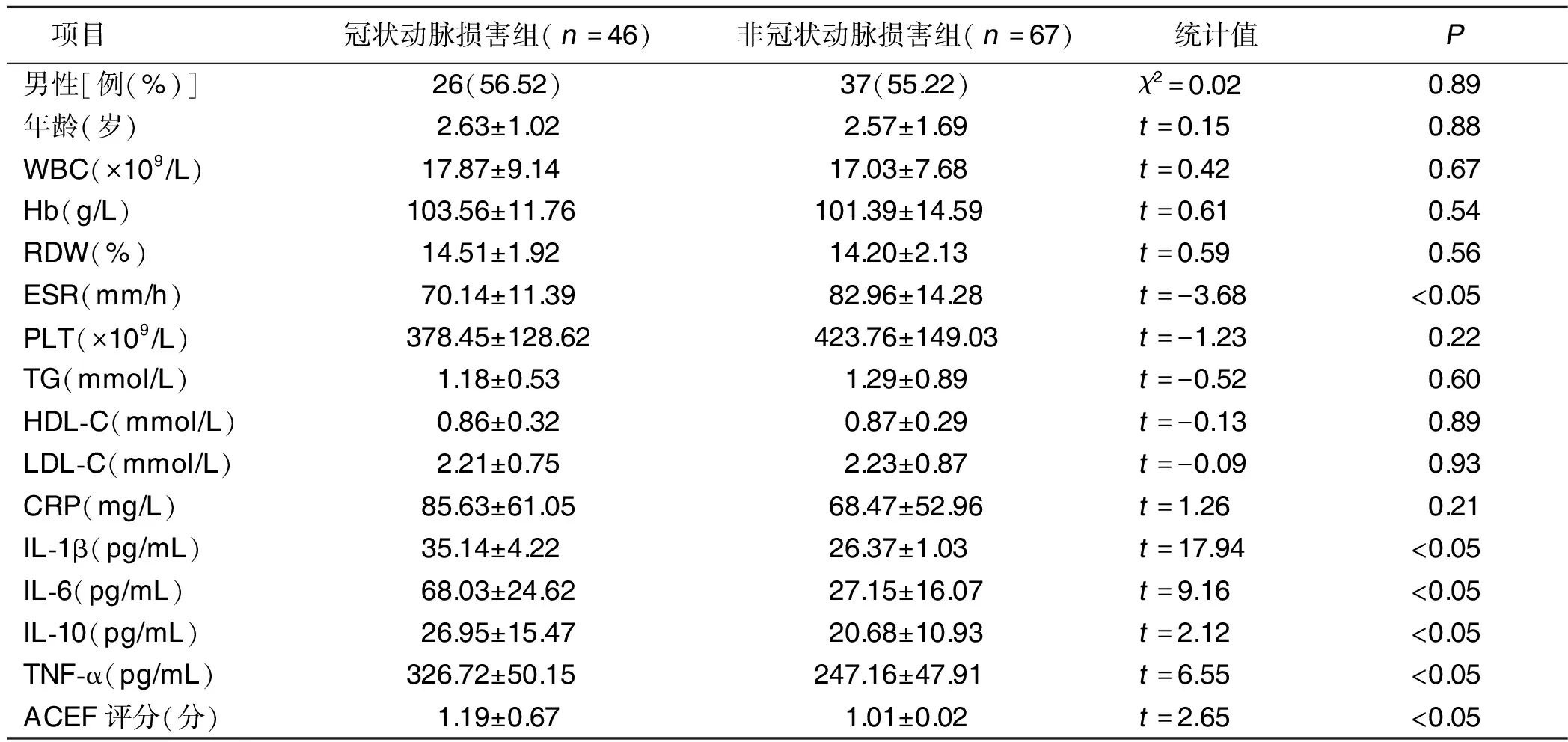
表1 冠状动脉损害组和非冠状动脉损害组临床资料比较
2.2 影响川崎病患儿并发冠状动脉损害的多因素分析 自变量赋值:ESR<75 mm/h=1,≥75 mm/h=0;IL-1β>28 pg/mL=1,≤28 pg/mL=0;IL-6>40 pg/mL=1,≤40 pg/mL=0;IL-10>22 pg/mL=1,≤22 pg/mL=0;TNF-α>270 pg/mL=1,≤270 pg/mL=0;ACEF评分>1.0分=1,≤1.0分=0。多因素Logistic回归分析结果显示:川崎病患儿IL-1β>28 pg/mL、IL-6>40 pg/mL、IL-10>22 pg/mL、TNF-α>270 pg/mL和ACEF评分>1.0分是川崎病患发生冠状动脉损害的独立危险因素。详见表2。

表2 川崎病患儿并发冠状动脉损害的多因素分析
2.3 构建中高危川崎病患儿并发冠状动脉损害的预测模型 基于多因素分析结果,将IL-1β、IL-6、IL-10、TNF-α和ACEF评分纳入构建川崎病患儿并发冠状动脉损伤风险的Nomogram预测模型。详见图1。

图1 基于ACEF评分联合炎性因子构建的Nomogram川崎病患儿并发冠状动脉损害风险的预测模型图
2.4 Nomogram预测模型和各独立风险因素对中高危川崎病患儿并发冠状动脉损害预测效能比较 通过ROC曲线比较Nomogram预测模型和各独立危险因素单独预测川崎病患儿并发冠状动脉损害的效能,结果显示:ACEF评分联合炎性因子的Nomogram预测模型ROC曲线下面积(AUC)为0.863,大于各危险因素单独预测ROC曲线的AUC,IL-1β为0.688,IL-6为0.730,IL-10为0.737,TNF-α为0.674,ACEF评分为0.627。详见表3、图2。

表3 Nomogram预测模型和各独立风险因素预测效能比较

图2 川崎病患儿并发冠状动脉损伤风险的Nomogram预测模型效能的ROC曲线图
2.5 Nomogram模型评价 通过对ACEF评分联合炎性因子的Nomogram预测模型得到的预测值和川崎病患儿并发冠状动脉损害的实际测定值绘制校正曲线,进行一致性检验,表明该模型预测值和实际测定值的相关性较好。详见图3。

图3 川崎病患儿并发冠状动脉损伤的Nomogram预测模型预测无并发风险校正曲线
3 讨 论
川崎病是一种非化脓性非特异性自限性血管炎症,发病年龄以学龄前期为主,主要集中在婴儿和幼年[6]。近15年,全球川崎病发病率呈逐年升高趋势,是儿童后天获得性心脏病的重要病因[7],威胁儿童的生命健康及生活质量。因此,寻找可靠的诊断指标,对川崎病患儿进行早期干预,实现对冠状动脉损害的早期预防是近年来的研究热点。
ACEF评分是基于简约法则,本研究采用ACEF评分预测择期冠状动脉旁路移植术(CABG)患儿术后30 d死亡率[8-9]。该评分仅包含3个简单变量,但表现出的预测能力与欧洲心脏手术风险评估系统 (EuroScore)相当[10]。有研究报道,ACEF评分较SYNTAX评分能较好地预测心源性死亡和心肌梗死的风险模型[11],患儿年龄、左室射血分数和肌酐对川崎病并发冠状动脉损害的预测均有影响,因此本研究将ACEF评分纳入预测指标的评估中。
关于川崎病的发病机制主要有血管内皮功能紊乱、免疫细胞异常活化与分泌、感染和超抗原学说等[12]。川崎病的病因和发病机制尚未明确,与免疫激活密切相关已得到众多研究支持,免疫系统激活后产生多种细胞因子和炎性介质,包括肿瘤坏死因子、干扰素、IL-1、IL-6、IL-8、IL-10等,这些炎性因子可诱导产生内皮损伤,也是导致急性发热的病理基础[13]。有研究显示,川崎病急性期患儿外周血IL-1β呈高表达,内皮细胞激活与之相关[14]。川崎病动物模型研究发现,IL-1受体拮抗剂可抑制小鼠大动脉异常扩张和冠状动脉瘤形成[15],提示IL-1信号通路激活在川崎病发病机制中发挥着重要作用。张新艳等[16]研究显示,川崎病急性期炎症小体活性增强,促进IL-1β分泌,跨膜转运到细胞与免疫细胞表面的IL-1受体结合,激活IL-1信号通路,加重炎症反应。相关研究表明,TNF-α、IL-1β、IL-6、干扰素-γ等均参与川崎病血管炎症反应[17]。TNF-α是由T细胞、活化的巨噬细胞和单核细胞产生,可增加内皮细胞通透性并诱导内皮细胞黏附因子表达,促使白细胞和血小板黏附于血管内皮表面,从而引起血管内凝血,造成血管壁损伤[18]。TNF-α具有多种生物学作用,可改变血管内皮细胞结构,抑制内皮细胞生长,减缓修复损伤[19]。黄宏琳等[20]研究显示,川崎病患儿血清TNF-α含量高于健康儿童,并发冠状动脉损害患儿血清TNF-α高于非冠状动脉损害患儿,提示川崎病患儿冠状动脉损害与血清TNF-α含量关系密切。IL-6是由活化的Th2细胞、单核吞噬细胞等产生,可诱导B细胞分化、产生抗体,诱导T细胞活化增殖和分化,参与机体免疫应答,具有显著的促炎特性,同时IL-6升高引起淋巴细胞凋亡延迟,免疫应答加剧,从而损害血管内皮细胞[21]。有研究显示,川崎病患儿血清IL-6水平较健康儿童升高,且冠状动脉损害患儿血清IL-6高于非冠状动脉损害患儿,表明IL-6可能参与川崎病的疾病过程,并引起冠状动脉炎性损伤[20]。IL-10可抑制多种细胞因子和生长因子合成,降低动脉粥样硬化风险[22]。有研究显示,动脉粥样硬化斑块中观察到IL-10 mRNA表达,正常的血管壁未观察到IL-10染色情况,提示发生炎症反应的细胞和组织中大量炎性因子生成同时抗炎因子表达,是机体一种代偿性保护机制[23]。
本研究比较冠状动脉损害组与非冠状动脉损害组临床生化指标,结果显示,炎性因子和ACEF评分>1.0分可作为川崎病并发冠状动脉损伤的高危因素。本研究通过Nomogram预测模型将ACEF评分和炎性因子结合,预测模型的列线图中根据各项指标数值对应列线图上方的分值,累计分值相加得到总分,对应列线图下方风险数值可评估川崎病患儿合并冠状动脉损害风险。Nomogram模型可整合不同变量,并将统计预测模型简化为单项指标的风险分值,通过列线图形式进行多变量评分统计,方便医护人员使用。本研究构建的Nomogram预测模型的AUC为86.3%,多指标联合预测效能高于各指标单一预测效能,同时在预测模型准确度方面,预测模型校正曲线显示预测值和实际测定值一致性较高,可见本研究构建的模型准确度较好。川崎病患儿并发冠状动脉损害是多因素作用的结果,不同环境、种族、地域可能产生影响,由于缺少定量、定性标准,不便于形成评价指标,因此未纳入研究范围。今后研究可考虑对上述因素形成定量、定性评价标准,以较好地预测川崎病患儿并发症。
综上所述,川崎病患儿并发冠状动脉损害与IL-1β、IL-6、IL-10、TNF-α和ACEF评分有关,通过构建基于IL-1β、IL-6、IL-10、TNF-α和ACEF评分的Nomogram预测模型可有效预测川崎病患儿并发冠状动脉损害的风险,从而进行早期干预治疗。

