CO2咸水层封存关键参数及其实验表征技术研究进展
叶航,郝宁,刘琦
(温室气体封存与石油开采利用北京市重点实验室(中国石油大学(北京)非常规油气科学技术研究院), 北京市 昌平区102249)
0 引言
2020年9月,我国提出“二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现碳中和”,为我国应对气候变化和绿色低碳发展明确了目标与方向。碳捕集利用与封存(carbon capture,utilization and storage,CCUS)技术是指将CO2从工业过程、能源利用或大气中分离出来,直接加以利用或注入地层以实现CO2永久减排的过程[1]。“双碳”愿景下,大力发展CCUS技术不仅是我国减少碳排放、保障能源安全的战略选择,而且是构建生态文明和实现可持续发展的重要手段。CCUS 技术作为我国实现双碳目标技术组合的重要组成部分,是目前实现大规模化石能源零排放利用的唯一选择,是保持电力灵活性的主要手段,是钢铁水泥等难减排行业的必要方案,CCUS 与新能源耦合的负排放技术还是实现碳中和目标的托底技术保障[2]。
1 CO2咸水层封存概述
在众多CCUS技术中,CO2地质封存是我国能源工业领域实现碳中和目标的“压舱石”和“兜底”技术,根据科技部、中国工程院等权威机构预测,预计2060年减排贡献超过5~10亿t/a。CO2地质封存过程中一般选择枯竭油气藏、不可开采的煤层和咸水层3 种地质构造作为封存场所,从而实现CO2的长期有效封存[3-4]。其中,相较于油气藏和煤层封存,咸水层封存具有封存潜力大(我国咸水层CO2封存容量约为24200亿t)和地理分布广的优点,因而在CO2地质封存方面发挥主导作用[5]。目前,国内外CO2咸水层封存技术均已趋于成熟,已有多个项目进入工业示范或商业应用阶段,表1 给出了国内外主要CO2咸水层封存示范项目[6]。

表1 国内外CO2咸水层封存案例Tab.1 Cases of CO2 sequestration in saline aquifers at home and abroad
准确评估CO2在不同地质条件下的封存潜力是CCUS技术大规模实施的重要基础[7],美国能源部(US-DOE)和碳封存领导人论坛(CSLF)等机构均提出过CO2地质封存潜力的评估方法,并已在全球范围内得到应用[8-9]。然而,尚未有统一且广泛可用的方法用以评估CO2封存潜力,现有研究使用了不同的边界条件、算法和现场数据,导致评估结果存在较大差异[10]。相较于油气藏和煤层,CO2咸水层封存的潜力评估更为困难,这是因为咸水层具有连续性,各种CO2封存机理往往同时以不同的速率和时间尺度发挥作用,从而增加了封存潜力评估的复杂性[11-13]。因此,为保证评估的准确性,应同时考虑CO2在咸水层中不同的封存机理。
尽管目前对于CO2咸水层封存机理的研究较多,但往往单一研究某种机理,鲜有同时考虑所有机理的研究。本文在分析CO2咸水层封存机理的基础上,总结了各机理研究实验中常用的表征技术,讨论了近年来不同表征方法和参数对咸水层封存潜力评估的影响,以期形成一套相对完善的咸水层封存机理研究方案,为准确评估CO2咸水层封存潜力提供理论基础。
2 CO2咸水层封存机理
2.1 CO2封存机理
CO2在咸水层中的封存是一个漫长而复杂的地球化学过程,在此期间CO2一般存在3 种形态,即分子状态、溶解状态和化合物状态,因此根据CO2进入咸水层后的状态和变化可将咸水层封存机理分为构造封存、残余气封存、溶解封存和矿化封存[14-15]。构造封存和残余气封存为物理过程,封存量较大,但是被封存的CO2不稳定,易受到断层、裂隙等构造运动的影响而发生泄漏,属于CO2注入初期的过程;溶解封存和矿化封存为化学过程,需要的反应时间较长,其封存量比物理封存机制少,但是更加稳定和安全,溶解封存在CO2注入初期至中期占10%~20%,而矿化封存属于CO2注入中期至后期阶段的封存过程。咸水层中CO2封存机理演化过程[16-17]如图1所示。

图1 CO2咸水层封存机理演化示意图Fig.1 Diagram of the evolution of CO2 sequestration mechanism in saline aquifers
可见,不同的CO2封存机理具有不同的作用时间尺度,且对CO2封存的贡献度和安全性也具有一定差异。因此,在咸水层封存中,往往不是某种单一的封存机制在发挥作用,而是各种封存机理的作用贯穿整个封存过程,但在不同时间段内的封存贡献程度不同。
2.2 构造封存机理
构造封存是指将CO2以超临界或气态形式注入低渗透或不渗透盖层下方的地层空间,从而将CO2封存于构造圈闭和地层圈闭中(类似于油藏中油气的储存方式)[18]。超临界CO2(0.6~0.7 g/cm3)和咸水(1~1.05 g/cm3)之间的密度差会产生浮力,使得注入的CO2在浮力作用下向地层上部运移。然而,不渗透的盖层会阻挡横向或侧向的运移,从而使其在盖层底部聚集,盖层的阻挡作用受黏性力、毛细管力和重力之间平衡关系的影响[17]。构造圈闭是封存CO2的关键机制,如果没有构造圈闭,注入的CO2最终可能会从注入地点运移到其他不希望储存的地下位点,甚至可能运移到可以逃逸到大气中的地方[14]。该机理得以发生的地质构造包括背斜、断层、地层超覆或岩性尖灭等[12,15]。
在进行构造封存潜力评估时,往往需要确定咸水层体积、孔隙度和残余水饱和度等参数,计算方法[8]如下:

式中:V'CO2t为CO2在咸水层中的地层构造封存体积,m3;V'trap为圈闭咸水层体积,m3;A为圈闭咸水层面积,m2;H为咸水层的平均厚度,m;Sw为残余水饱和度;φ为咸水层岩石的有效孔隙度。
在咸水层封闭性良好的前提下,地层岩石的孔隙度是影响CO2封存潜力的最直接因素,二者呈正相关。此外,残余水饱和度是决定CO2封存潜力的重要参数,受地层水成分、CO2排驱方式、温度、压力、岩石类型、岩石性质(孔隙度越大,残余水饱和度越大;渗透率越低,残余水饱和度越大)、润湿性和表面张力等因素的影响[19]。
2.3 残余气封存机理
残余气封存是指CO2在地层中进行运移时,随着CO2饱和度减小,连续的CO2逐渐分离,形成羽流。当CO2羽流穿过多孔介质岩石时,由于孔喉结构差异会产生贾敏效应,导致部分CO2会以残留气体的形式保留在孔隙中,最终以残余气的形式进行封存[15,20-21]。但该机理不仅需要CO2通过多孔介质,还需地层水回流,占据之前由CO2气体所占据的岩石孔隙,这样才能使CO2得以封存。残余气封存的效果与岩石孔隙连通性、咸水层岩性和孔隙内流体性质等因素密切相关。一般情况下,适合CO2封存的储层孔隙通常小于1 mm,且连通性好,孔隙度为10%~30%。尽管CO2羽流主体部分的浮力足以克服孔隙中的毛细管力,但在运移的过程中羽流的边缘和尾部会有少量CO2“脱落”,从而永久地保留在孔隙中。残余气封存的作用在CO2停止注入后变得更为突出。而且,残余气封存增大了CO2与地层水和岩石的接触时间,对溶解封存和矿化封存均有促进作用[22-23]。
评估残余气封存潜力的计算方法[8]如下:
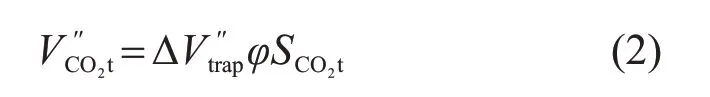
该封存机理与时间相关,封存潜力随着CO2的扩散迁移和时间的推移而增大。因此,必须在某一确定时间点对残余气封存潜力进行评估,该时间点即封存潜力的边界值。由于ΔVtrap只能通过数值模拟来确定,因此只能通过局部和现场规模的评估来获得残存气体封存的潜力,也正因如此,残存气封存的理论封存潜力无法计算,只有有效封存潜力、实际封存潜力和匹配封存潜力可以根据计算中的限制边界进行计算[24-25]。
2.4 溶解封存机理
溶解封存是指注入的CO2与咸水层中的地层水接触后通过扩散、对流等作用发生溶解反应,从而以溶解状态封存于咸水层,是一个连续的、依赖于时间的过程[25]。CO2在水中的溶解包含物理溶解和化学溶解2个过程。物理溶解即CO2以分子形式溶于水中,其分子结构不发生变化,溶解度在一定温压条件下服从亨利定律;化学溶解即CO2与水反应生成碳酸(H2CO3),并电离产生HCO3
-和H+。与物理溶解相比,化学溶解量相对较小[15]。溶解封存的速率取决于CO2与地层水的接触率和地层水中CO2的饱和度。随着时间的推移,当CO2饱和水比原始地层水的密度高1%左右时,其就会因重力作用向下运移,使得CO2不受浮力的影响,从而确保CO2能够安全、有效地封存[26]。然而,若CO2被固定在构造和地层圈闭中,由于其只能在圈闭底部与地层水接触,使得溶解过程变得缓慢,且溶解封存潜力也会降低。这是因为溶解过程取决于CO2的浓度梯度,溶解度随着CO2浓度的增加而降低。
可依据CO2在地层咸水中的溶解度评估溶解封存潜力[21],计算方式如下:

式中:MCO2t为CO2在咸水层中的溶解封存量,Mt;ρw为CO2饱和时的咸水密度,kg/m3;XCO2s为在咸水层中的质量溶解度,是温度、压力和矿化度的函数。
可见,CO2溶解量取决于咸水层的温度、压力、地层水矿化度、储层物性等因素。一般情况下,CO2的溶解度随着压力的增大而增大,但随着温度、矿化度和pH 值的增大而减小[27]。此外,盖层斜率或倾角也会影响溶解封存的效率[28]。
2.5 矿化封存机理
矿化封存是指CO2溶于地层水后,形成弱碳酸,碳酸进一步与周围的岩石矿物或有机物质发生地球化学反应,生成固体碳酸盐矿物质的过程,是CO2咸水层封存中最永久、最安全的封存机理。该过程中涉及的地球化学反应如下:
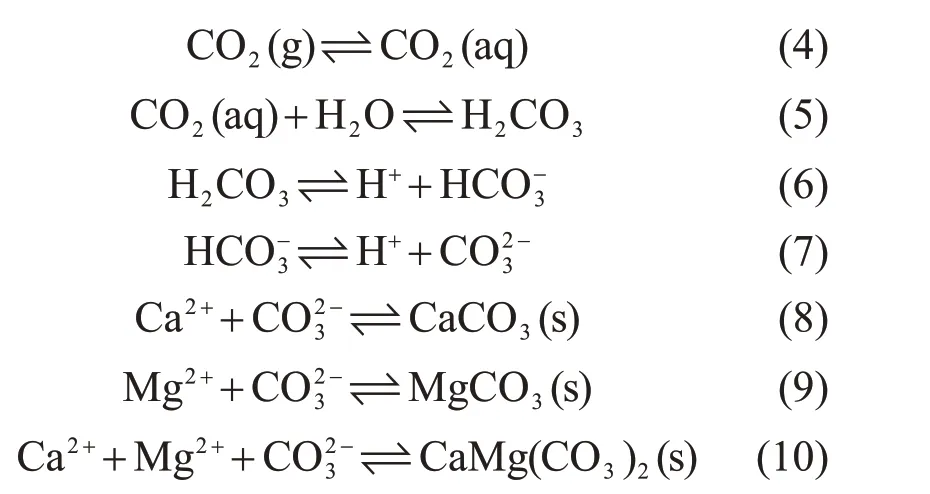
CO2在咸水层中的地球化学反应机理存在一个碳酸盐溶解和沉淀的反应过程,碳酸分解出的碳酸根离子(CO32-)与地层水中存在的多种不同的二价金属阳离子(如Ca2+、Mg2+等)反应,从而形成方 解 石(CaCO3)、 菱 镁 矿(MgCO3) 和 白 云 岩(CaMg(CO3)2)等碳酸盐矿物[29]。相较于其他封存机制,该过程较慢,作用时间尺度为100~10000 a。
矿化封存的反应速率取决于地层水和岩石基质的化学成分、温度、压力、矿物颗粒与含CO2地层水之间的接触面积以及流体在岩石界面上的流速。界面的大小取决于矿物颗粒大小,流速取决于岩石渗透率、水力梯度和水的黏度,而水的黏度则取决于水温、矿化度和压力。CO2矿化封存作用因岩石类型和矿物成分的不同而有很大差异,若储层为碳酸盐类(主要由方解石和白云岩组成),则地化反应速率很快;若储层为砂岩且岩性以稳定的石英颗粒为主,则一般不发生反应或反应时间很长[25]。碳酸盐矿物沉淀的形成主要取决于咸水的pH值,pH值在9.0以上时有利于矿化封存过程。然而,一旦向咸水中注入CO2,pH 值就会下降。因此,咸水层封存过程中有必要提高咸水的pH值并保持其稳定[30-31]。
3 CO2咸水层封存实验表征技术
3.1 常用表征技术
明晰CO2在储层中的CO2−咸水−岩石相互作用,以及由此引起的物理与化学变化,是保证CO2安全封存的先决条件[32]。为更好地确定CO2注入后的空间分布、运移过程、多孔介质中多相流的相对渗透率以及CO2羽流的相态等内容,并依据不同的封存机理准确评估咸水层的CO2封存效率,常需使用不同的表征技术确定相关参数,从而保证CO2在咸水层中的长期、有效封存。不同封存机理研究中常用的表征方法见表2。
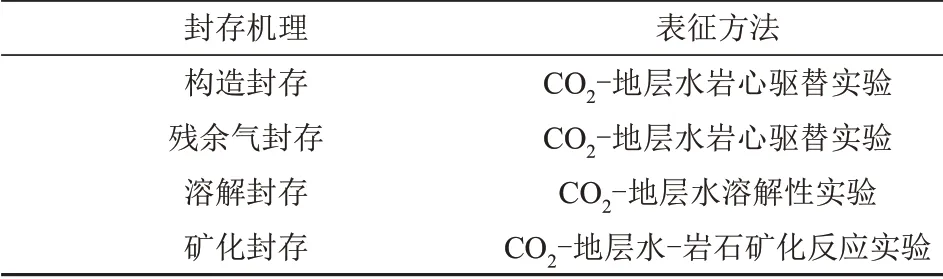
表2 不同封存机理常用表征方法Tab.2 Common characterization methods for different storage mechanisms
3.2 储层岩石表征技术
储层岩石为CO2的流通和安全封存提供了保障,岩石矿物表面与CO2的相互作用对于理解矿物沉淀在CO2封存过程中的作用机制具有重要意义,因此对岩石进行多技术、多尺度表征十分必要。
岩石特征应包括整体、表面和孔隙特征,以及表面和界面上的岩石−流体相互作用,通常使用X 射线衍射、热重分析、岩石演化热解、气体吸附、电子显微镜和X 射线光电子能谱(X-ray photoelectron spectroscopy,XPS)等手段对岩石进行评估,以确定岩石样品表面的矿物成分、元素组成、孔隙体积和吸附物种等有效信息。
氯霉素标准样品,甲醇(HPLC级色谱纯),乙腈、蒸馏水、乙酸乙酯、NaCl、MgSO4、NaOH、醋酸铵、磷酸氢二铵均为国产分析纯,蜂蜜(5种不同品牌)购自超市。
XPS 通常被用来确定岩石表面的化学成分,并将其与岩石的润湿性相关联。近常压光电子能谱(ambient-pressure XPS,AP-XPS)能够在高温、环境压力条件下确定岩石样品表面存在的气体和水分,从而量化矿物−流体间的相互作用。岩石表面的流体通常包括CO2、水和碳氢化合物气体等,通过单独或同时研究这些储层中的原位流体,可以深入了解注入CO2后对岩石表面和界面成分的影响,并明晰CO2封存机制[33]。
此外,CT扫描技术具有重构岩样三维孔隙结构的优点,是表征储层岩石孔隙度、渗透率及流体饱和度等参数的有效手段。利用CT扫描技术能够有效描述储层条件下岩石样品的化学反应过程,并可通过孔隙结构分析CO2及咸水的流动过程,从而为CO2咸水层封存的风险评估提供技术支持[34]。
3.3 CO2-地层水岩心驱替实验
研究CO2−咸水多相运移过程对于评估CO2咸水层封存的潜力及封存安全性至关重要。目前,对CO2咸水层封存的大多数研究都采用岩心驱替实验,实验过程一般模拟实际储层的温度(10~70 ℃)和压力(3~150 MPa)条件。考虑多相流特征的岩心驱替实验研究是厘清CO2注入过程中/注入后CO2−咸水−岩石相互作用机理、确定CO2注入速度、明晰CO2在储层中的扩散和评估CO2长期有效封存的最有效方法[35]。
岩心直径、岩心长度、压力和温度是岩心驱替实验过程中最重要的参数,这些参数能够决定整个实验的成败[36]。因此,结合取样岩心的实际地质状况,应该更加注意所使用的参数是否合适。一般情况下,实验室所用岩心的直径为20~60 mm,岩心长度为50~150 mm;实验压力和温度一般取决于实际储层条件,但目前研究所用的温度、压力范围大多集中在40~60 ℃和10~30 MPa[37-40]。
为了更准确地研究咸水层中CO2的运移情况,应与特定的表征仪器结合使用,以便进行更为全面的分析。例如,可将示波器探头与高温高压岩心夹持器或三轴装置中的试件耦合用于岩心驱替实验;此外,光致发光体积成像、磁共振成像和X 射线CT 等3D 成像技术能够测量多孔介质中稳定或非稳定的多相流,其与驱替装置的耦合使用能够进一步明确CO2在岩心内的分布情况[41-42]。
3.4 CO2−地层水溶解性实验
CO2在咸水中的溶解受分子扩散、多孔介质中流体速度变化引起的弥散和自然对流的控制,在此过程中CO2溶解度、扩散系数及因溶解而引起的体系密度、体积变化等参数是评估溶解封存潜力的重要理论基础,往往需要不同的技术表征[43]。
3.4.1 溶解度
溶解度测定方法包括静态法、平衡液取样分析法、压力降落法、气体PVT测定法和可变体积PVT 法等。不同的测定方法各有其优劣,如压力降落法耗费时间较久,平衡液取样分析法易在取样过程中破坏体系平衡,气体PVT测定法计算较为繁杂,因此应根据实际情况选用合适的测定方法。CO2溶解度通常受到温度和压力的影响,随压力的增加而增加、温度的增加而降低,在低压区压力对CO2的溶解度影响较小[44]。
扩散系数在很大程度上取决于溶质(CO2)和溶剂(咸水)的性质,以及多孔介质和体系的热力学性质,其测定方法可分为直接法和间接法。直接法中,气体扩散系数是通过在进行扩散实验时收集的流体混合物的成分测量的;间接法所需的时间较少,可通过测量CO2−咸水体系的性质,间接估算分子扩散系数。这是因为扩散过程会改变CO2-咸水体系的各种性质,如界面张力、气体压力、气体体积等。此外,可以使用X射线CT扫描技术来监测气体扩散过程,以确定液体中的气体分布[45]。
3.5 CO2−地层水−岩石矿化反应实验
CO2−地层水−岩石矿化反应实验有2 种类型:长周期高温高压矿化实验(间歇浸式反应器/高压釜)和连续流动实验(岩心驱替)。矿化反应实验中通常将小块岩石(或粉末样品)放置于地层咸水中,在咸水层实际温压条件下与CO2反应一段时间。在整个实验过程中,以特定的时间间隔将地层咸水样本从间歇反应器中取出,通过分析地层咸水的pH 和离子浓度变化等参数确定CO2的溶解情况。实验结束后,使用高分辨率成像技术(如扫描电子显微镜、透射式电子显微镜、X 射线衍射仪)观测岩石样品,以确定其表面矿物成分的变化。连续流动实验中,通常向岩心注入超临界CO2,然后注入地层咸水或模拟咸水,并对出口水样的化学成分和岩石样品的矿物组成进行分析[5]。
CO2−咸水−岩石的相互作用取决于各种因素,包括咸水层的CO2饱和度和离子浓度等。研究表明,CO2浓度(咸水层pH 值)对矿化封存有显著影响,且离子的存在是发生CO2−咸水−岩石相互作用的必需条件[46]。目前,已报道的大多数研究都是在较高的温度和压力条件下(高于实际储层条件)进行,以加速CO2−咸水−岩石反应。然而,矿化封存是一个长期的过程,短期规模的实验对于预测实际储层条件下的封存过程不甚准确,因此有必要进行低温-长周期时间尺度的实验。
4 咸水层封存潜力评估关键参数
4.1 残余水饱和度对咸水层封存的影响
CO2咸水层封存排水过程中形成的残余水会影响构造封存的潜力,且其引起的压力积聚会降低CO2咸水层封存效率[47]。因此,为提高CO2在含水层中的流动能力,封存过程中应尽可能降低残余水饱和度。
影响残余水形成的因素很多,包括咸水与CO2之 间 的 界 面 张 力(interfacial tension,IFT)、CO2−咸水−岩石体系中的接触角、储层岩石物理性质、CO2性质等[48]。Iglauer 和Saraji 等[49-50]研究表明咸水与CO2间的IFT直接影响咸水层对CO2的捕获能力,并决定了残余气封存效率以及最终咸水和CO2在地层中的流动性能。Li 等[51]指出CO2−咸水−岩石接触角的减小使得CO2的毛管压力增加,从而降低了储层中流体的流动能力,导致残余水饱和度增大。Reynolds 等[52]认为岩石的非均质性能够显著降低CO2的相对渗透率,从而导致残余水饱和度增大,故均质岩层更适用于CO2咸水层封存。Bachu等[53]研究表明,高渗透条件下岩石中的残余水饱和度更高,说明在渗透率较高的咸水层中更易形成残余水。Szulczewski 等[54]指出CO2封存和残余水的形成具有时间依赖性,较长的CO2注入周期有助于减小残余水饱和度,进而提高CO2封存能力。索瑞厅等[47]研究发现,残余水饱和度受压力影响较大,且较小的黏度比和较大的密度差能够增大残余水饱和度。
4.2 残余气饱和度对咸水层封存的影响
残余气饱和度是评估残余气封存潜力的重要参数,受初始含气饱和度、岩石润湿性、孔隙度、渗透率及岩样类型等多个因素的影响[22,55]。
Zapata 等[56]模拟结果表明,在CO2注入期内,储层中约60%的CO2以可流动的游离相的形式存在,其中20%的CO2通过残余气封存的,且受岩相的相对渗透率和毛管压力的影响。Ali等[57]研究发现,有机酸能够改变CO2−咸水−岩石体系的润湿性,且随着润湿性由水湿转为油湿,残余CO2饱和度逐渐降低。Zhao 等[58]研究表明,矿化度会引起咸水黏度和CO2与咸水间IFT的变化,且残余CO2饱和度随着矿化度的增大先增大后减小,封存机制发生转变。Rasmusson等[59-60]指出,残余气封存是CO2在咸水层有效封存的关键,但其本质上是一个孔隙尺度的过程,并基于孔隙网络模型估算了初始CO2饱和度和残余CO2饱和度之间的关系,结果发现,其对前进接触角的敏感性较低,有利于残余气封存过程。Xu等[61]研究了温度和压力对咸水层中CO2分布的影响,结果表明:随着压力的增加,CO2前缘运移速度减小,残余CO2饱和度增大;随着温度的升高,CO2前缘运移速度增大,残余CO2饱和度减小。Kamal等[62]认为表面活性剂−交替气体(surfactant alternating gas,SAG)注入可作为CO2封存的流度控制方法,且随着表面活性剂浓度的增加,残余气饱和度增大。
4.3 溶解度对咸水层封存的影响
CO2在咸水中的溶解度基本上取决于温度、压力、矿化度和地层岩石的类型及组成等因素,一般情况下,CO2在咸水中的溶解度随着压力的升高和温度的降低而增加,随着孔隙流体矿化度的升高而降低[5]。
Bakhshian[63]模拟结果表明,注入速率和表面润湿性能够影响CO2溶解封存时界面的传质过程,随着注入速率的提高,介质对咸水的润湿性增强,CO2的溶解度增大。Wan等[64]研究了不同类型离子对CO2溶解度的影响,发现溶解度大小关系为MgCl2 在注入过程中,地层水会不断蒸发,从而引起盐析现象,进而导致地层孔隙度和渗透率发生变化,从而影响CO2封存效率。盐析现象是一个复杂的过程,取决于热力学条件(压力、温度、矿化度)、注入方案(注入速度、注入周期)、岩石和流体性质(孔隙度、渗透率)以及完井方案等参数[71]。 Grude 等[72]研究表明,在高矿化度(25%)和中等渗透率(∼100 mD)的储层中,盐析是CO2注入过程中压力上升的主要原因。André 等[73]研究发现,较高的注入速率将导致更高的压力梯度,从而抑制毛细管流量向蒸发表面的回流,最终降低盐析的可能性。Edem等[74]研究了离子类型和矿化度对盐析现象的影响,结果表明,与NaCl 和KCl 相比,MgCl2和CaCl2对盐析效应的影响更大,且盐析程度随矿化度的增大而增大,最终导致岩心样品的孔隙度和渗透率降低。Yusof 等[75]研究表明,在高矿化度条件下,CO2注入能力降低幅度最大,因为盐析程度越严重,孔隙空间越小,堵塞比越大。高志豪等[76]模拟发现,地层水矿化度对盐析及其反馈作用的影响最大,CO2注入速度的影响次之,地层渗透率的影响最小。 CO2咸水层封存过程中,各种封存机理往往同时以不同的速率和时间尺度发挥作用,从而增加了封存潜力评估的复杂性。针对特定封存机理进行实验表征,对于准确评估封存潜力具有重要意义。在分析CO2咸水层封存机理的基础上,总结了当前常用的封存机理表征技术,讨论了其关键参数对咸水层封存的影响,以期为现场工作提供思路。 1)根据封存机理的不同,CO2咸水层封存的表征技术主要包括储层岩石表征、CO2-地层水岩心驱替实验、CO2-地层水溶解性实验、CO2-地层水-岩石矿化反应实验等,但各表征技术都有其限制性,应根据实际需要选择合适的方法进行实验探究。此外,CO2咸水层封存潜力受残余水饱和度、残余气饱和度、溶解度和盐析程度等多个参数的影响,实验过程中应着重分析以上参数在封存过程中的作用,以确保潜力评估的准确性。 2)当前我国CO2咸水层封存技术尚处于工业示范阶段,距离大规模现场应用还有一定距离,为进一步深入了解咸水层封存机制,未来工作应从以下方面开展:开展全过程封存机理(构造封存、残余气封存、溶解封存、矿化封存)分析,目前咸水层封存机理研究大多针对单一机理,对理解CO2咸水层封存过程相对片面,全过程分析有利于揭示不同机理及其耦合相互作用关系,从而建立咸水层全过程封存机理系统评价体系;开展海上咸水层封存项目研究,我国东部沿海地区源汇匹配情况较好,适宜进行海上咸水层封存,但我国缺乏海上咸水层封存项目经验,因此针对海上咸水层封存项目开展封存机理研究、盖层安全性及封存潜力评价,有助于我国咸水层封存技术的进一步发展。 3)此外,为确保CO2的安全有效封存,有关CO2咸水层封存技术的环境风险与地质安全性评价工作有待进一步研究和实践,并需对封存场地的安全和环境管理与监测工作加以重视,从而构建CO2咸水层封存科学选址、安全监测预警以及规范应急全流程理论与技术方法体系,为我国CO2咸水层封存技术规模化、商业化奠定理论与技术基础。4.4 盐析现象对咸水层封存的影响
5 结论

