富马酸替诺福韦二吡呋酯对乙型肝炎母婴传播阻断的效果
杨秀珍,陈兴,姜先杏
广东省阳江市公共卫生医院,广东 阳江 529500
0 引言
乙型肝炎病毒(hePatitis B virus,HBV)就是引起乙型肝炎的病原体,该病毒包含有正嗜肝DNA病毒属和禽嗜肝DNA病毒属两个属,而引发人体感染的正是正嗜肝DNA病毒属[1]。而HBV的传播与感染也正是全球性的重点公共卫生问题,我国是人口大国,人口众多,也因此成为HBV高流行区,主要传播途径有:血液传播、医源性传播、母婴传播以及性传播等,其中,母婴传播相较于其他几类途径而言,传播风险更大,且感染概率更高,这也正是我国成为HBV感染高发的主要原因之一[2]。但因妊娠期属于一种特殊的生理过程,药物安全性不仅影响胎儿正常生长发育干预,甚至危及母婴生命安全,故选择安全且有效的乙型肝炎母婴传播阻断药物是临床研究的重点,近年来,随着基因工程疫苗的生产和投入,乙肝疫苗的普及率逐年上升,感染率呈下降趋势[3]。核苷酸类似物作为临床常用药物,可有效降低HBV-DNA母体载量,有效阻断乙型肝炎在母婴间的传播,而富马酸替诺福韦二吡呋酯为新型核苷酸类逆转录酶抑制剂,可有效抑制HBV的复制作用,从而达到稳定病情的目的,且该药物可强效对抗其他核苷类药物造成的HBV变异株,且不会对患者妊娠造成不良影响,具备较高的安全性[4]。鉴于此,本次研究就富马酸替诺福韦二吡呋酯对乙肝病毒的母婴传播阻断进行进一步探究分析,现有详情如下。
1 资料与方法
1.1 一般资料
本次研究共有研究对象120例(2021年3月-2022年5月),按照患者意愿(对照组患者拒绝在孕期内进行抗病毒治疗,研究组则接受孕期内抗病毒治疗)将入选患者分为研究组和对照组,每组患者各60例。
研究组:年龄20~35岁,平均(26.78±3.37)岁;产程1~3次,平均(1.35±0.53)次;谷丙转氨酶(ALT)为(23.16±2.78)U/L;HBV DNA为(6.37±0.42)U/mL;文化水平:高中及其以下12例,大专11例,本科及其以上7例。对照组:年龄21~34岁,平均(26.82±3.41)岁;产程1~3次,平均(1.41±0.42)次;ALT为(23.21±2.73)U/L;HBV DNA为(6.35±0.38)U/mL;文化水平:高中及其以下11例,大专10例,本科及其以上7例。两组患者在各项一般资料相较无差,对研究所得结论公正性无影响(P>0.05),具有对比价值。
纳入标准:①均在妊娠期且孕妇HBsAg和乙型肝炎e抗原均为阳性(患者HBV感染史在半年以上),且HBV DNA≥2×105U/mL;②妊娠周数<24周;③年龄等一般资料完善。
排除标准:①合并有其他病毒感染或免疫缺陷病毒感染等疾病;②合并有严重脏器不全等疾病,或存在认知、意识、表达、神经及精神障碍等;③妊娠期间服用其他抗病毒药物或使用过类固醇、细胞毒及免疫调节药物者;④确诊肝衰竭孕妇;⑤三维超声检查可见胎儿异常者;⑥孕早期服用可能导致胎儿畸形类药物者;⑦合并严重恶性肿瘤、癌细胞扩散者;⑧离床资料缺损或丢失者。
1.2 方法
对照组患者定期安排产检、孕期内进行常规保肝治疗,并在新生儿出生后对其进行疫苗接种及免疫球蛋白治疗。
研究组患者则在孕周24周时,开始使用富马酸替诺福韦二吡呋酯片及常规保肝治疗,详细如下:富马酸替诺福韦二吡呋酯片(药品名称:韦瑞德;生产厂家:AsPenPortElizabeth(Pty)Ltd;批准文号:进口药品注册证号:H20 130589;药品规格:300mg×30片×盒),用法用量:1粒(300mg)/次,1次/d,自第24孕周起,依照用法用量坚持用药,直至分娩当天停药。
在两组新生儿出生后12h内注射重组酵母乙型肝炎疫苗10μg和乙型肝炎免疫球蛋白100U(第1针疫苗),并在后续新生儿满月(出生1个月)、新生儿6个月分别进行第2针、第3针疫苗,每次接种10μg。对于早产儿、低出生体重儿,若生命体征稳定则在出生12h内尽早注射重组酵母乙型肝炎疫苗10μg和乙型肝炎免疫球蛋白100U(第1针疫苗),再按0、1、6个月程序接种3针疫苗;若生命体征不稳定,应在生命体征平稳后尽早接种第1针疫苗。
1.3 观察指标
①分别在两组患者孕24周和分娩时,对HBsAg和HBeAg阳性率进行统计并对比。②分别在治疗第6周和分娩前对两组患者的空腹外周静脉血进行采集,静脉血每次采集5mL,按3000r/min离心15min,取上层清液(血清)采用酶联免疫吸附测定检测ALT水平,(ALT水平与log10HBV DNA检验)[5-6]。③两组新生儿接种疫苗疗程结束后1个月HBsAg阳性率和HBeAg阳性率。④记录两组新生儿阻断成功率及孕妇不良反应发生率。
1.4 统计学分析
本次研究数据通过SPSS 21.0统计软件进行分析处理,所得概率、比例等计数资料采用χ2检验,所得计量数据则采用t检验。
2 结果
2.1 两组患者孕周24周和分娩时HBsAg和HBeAg阳性率状况
两组患者孕周24周时,两组患者的HBsAg和HBeAg阳性率对比无差异(P>0.05),但分娩时再次进行HBsAg和HBeAg阳性率进行检测并对比,经对比发现,两组患者分娩时的HBeAg阳性率及HBsAg阳性率对比无较大差异(P>0.05),两组患者分娩时数据对比虽无统计学意义(P>0.05),但研究组相较仍更具优势。具体数据见表1。
2.2 两组患者孕24 周和分娩时ALT 和log10HBV DNA水平
不同时期两组患者的ALT水平对比无差异,但两组患者不同时期log10HBV DNA水平相比,第24孕周对比无差异,但分娩时两组患者的log10HBV DNA水平存在显著差异(P<0.05),具体见表2。
表2 两组患者孕24 周和分娩时ALT 和log10HBV DNA 水平对比(±s)
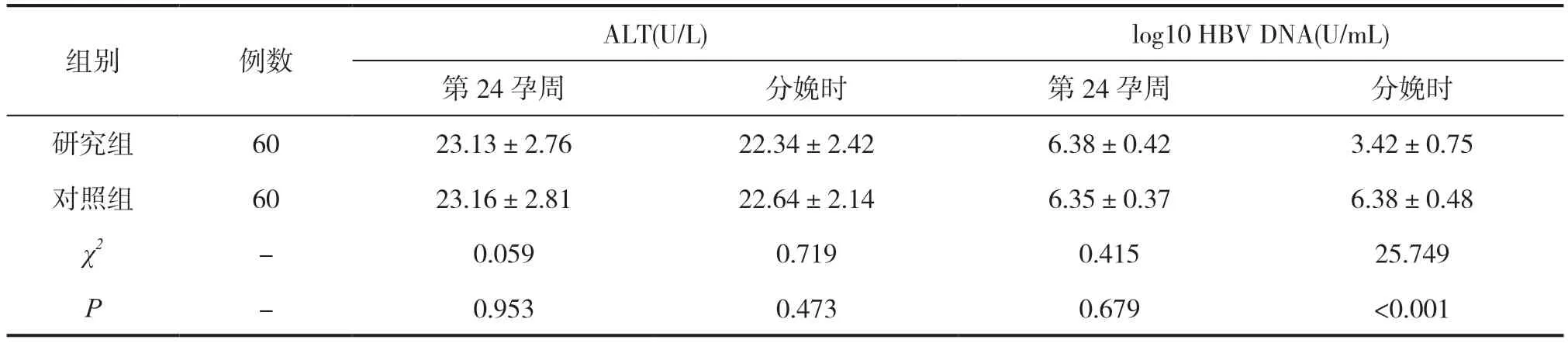
表2 两组患者孕24 周和分娩时ALT 和log10HBV DNA 水平对比(±s)
2.3 两组新生儿出生7个月HBsAg和HBeAg阳性率状况
经过对两组新生儿同时期检测数据对比发现:两组新生儿出生7个月后的HBsAg和HBeAg阳性率对比均存在有显著差异(P<0.05),详见表3。
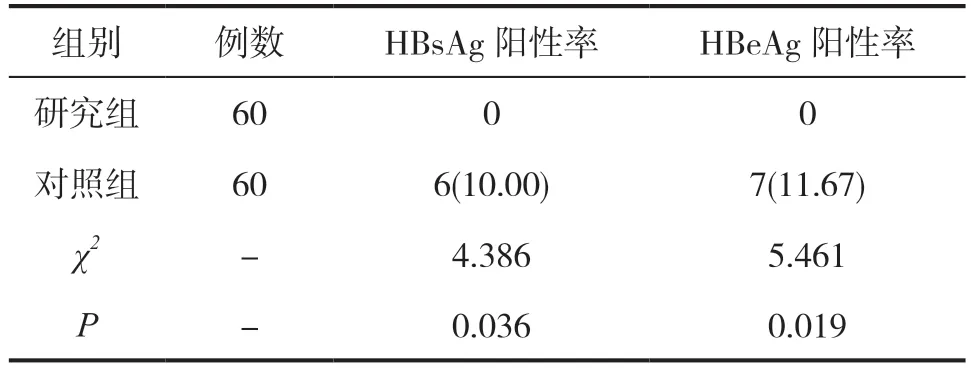
表3 两组新生儿出生7 个月HBsAg 和HBeAg 阳性率状况对比[n(%)]
2.4 两组新生儿阻断成功率及孕妇不良反应发生率比较
研究组阻断成功率高于对照组(P<0.05),其不良反应发生率低于对照组,但比较无差异意义(P>0.05),详见表4。
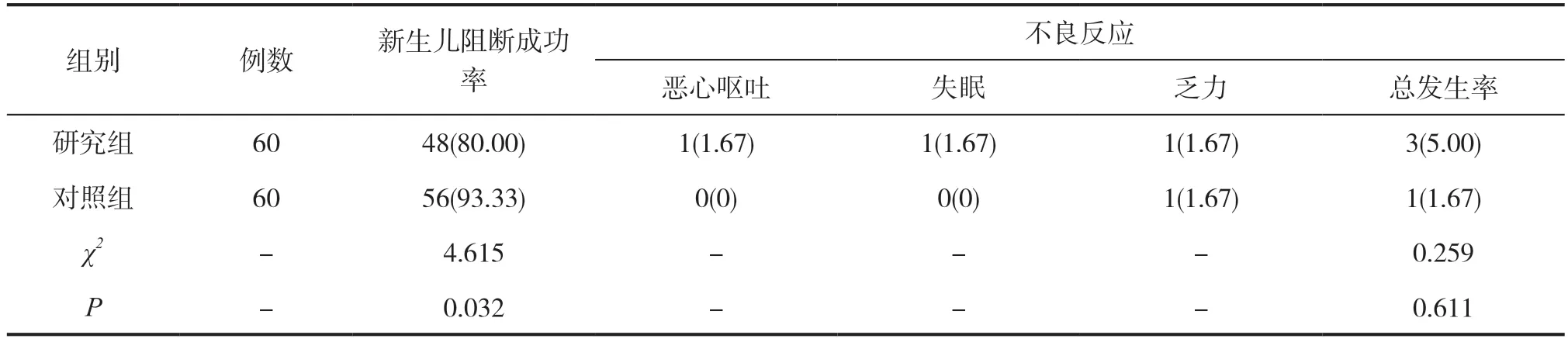
表4 两组新生儿阻断成功率及孕妇不良反应发生率比较[n(%)]
3 讨论
乙型肝炎是我国常见的传染病,具有较高的发病率,可通过母婴、体液及血液等方式传播,严重威胁患者身体健康,而母婴传播是目前HBV病毒传播的主要途径,若新生儿感染乙肝病毒,极有可能进展为肝细胞癌,严重威胁婴儿生命安全[7]。丙氨酸氨基转移酶是肝细胞中含量较高成分,若肝细胞死亡,会在血液中大量释放,故丙氨酸氨基转移酶可作为检测肝炎的重要指标,乙肝病毒基因可准确显示病原体传染性的水平,若孕妇乙肝病毒基因较高,胎儿感染乙肝病毒的概率显著增加。乙肝病毒在孕妇妊娠期间可造成其肝脏负担增加,继而影响肝脏代谢、合成及解毒等功能,严重威胁母婴安全,因此采取有效措施,积极阻断乙肝病毒的母婴传播尤为重要,是确保胎儿健康成长的关键[8]。目前针对乙型肝炎疾病治疗多以抗病毒为主,保肝药物中的细胞膜组成成分可有效恢复受损肝细胞,但无法抑制病毒复制,故治疗效果不佳。而富马酸替诺福韦二吡呋酯片属于一种专科抗病毒药物,为核苷酸类似物,在医嘱下合理应用该药物,可发挥显著的抗病毒作用,且对胎儿的影响较小,安全性较高[9]。孕妇通过口服后,该药物可在体内转化为替诺福韦,与脱氧核糖底物有效结合,从而达到病毒聚合酶抑制作用,有效阻断病毒复制,从而阻断母婴传播,同时,富马酸替诺福韦二吡呋酯片经服用后不会被胃肠道吸收,可进行酯化、成盐,具有显著的水溶性,安全性较高;药物在2h后药物中的有效成分替诺福韦可达到血药峰值,对阻断母婴传播有重要意义[10]。但需注意,食物会对该药物的生物利用度产生一定的影响,而进食期间药物的生物利用度会增加,故嘱咐孕妇保持空腹用药,从而最大限度的发挥药效[11]。
本次研究中,对两组患者孕周24周和分娩前HBsAg和HBeAg阳性率状况进行检测,经过数据对比发现,两组患者孕周24周时,两组患者的HBsAg和HBeAg阳性率对比无差异(P>0.05),分娩时虽有一定变化,但变化轻微依旧无统计学差异;对不同时期两组患者的ALT水平对比无差异,但两组患者不同时期log10HBV DNA水平相比,第24孕周对比无差异,但分娩时两组患者的log10HBV DNA水平存在显著差异(P<0.05);两组新生儿出生7个月后的HBsAg和HBeAg阳性率、阻断成功率对比均存在有显著差异(P<0.05)。表明富马酸替诺福韦二吡呋酯的母婴阻断效果显著,可有效避免胎儿感染乙肝病毒。分析其原因,富马酸替诺福韦二吡呋酯是一种一磷酸腺苷的开环核苷膦化二酯结构类似物,需要经二酯的水解转化为替诺福韦,然后通过细胞酶的磷酸化形成二磷酸替诺福韦(链末端终止剂),从而抑制HIV-1反转录酶和HBV反转录酶的活性。二磷酸替诺福韦对DNA聚合酶a、b和线粒体DNA聚合酶是弱抑制剂[12]。富马酸替诺福韦二吡呋酯适用于治疗慢性乙肝成人和≥12岁的儿童患者,需要注意的是,在治疗中富马酸替诺福韦二吡呋酯不应与TRUVADA或ATRIPLA合用。在陈益香等[13]研究中,以100例妊娠孕妇为例,给予替诺福韦治疗至分娩,对照组仅接受保肝治疗,新生儿均采取阻断治疗。对比结果显示,观察组新生儿阻断成功率较高,观察组不良反应发生率较低,表明替诺福韦阻断HBV母婴传播的效果显著,且安全性较高,与本文研究结果一致。
综上所述,富马酸替诺福韦二吡呋酯在母婴间对乙型肝炎的传播中具有良好的阻断效果,有效降低了乙肝病毒母婴传播发生率。建议推广应用。

