从化学学科核心素养的角度解析和认识高考实验题
——以“江苏省2021年普通高中学业水平选择性考试”实验题为例
江苏 董拥军
高考评价体系主要由“一核”“四层”“四翼”三部分内容组成。其中,“一核”为核心功能,即“立德树人、服务选才、引导教学”,是对素质教育中高考核心功能的概括,回答“为什么考”的问题;“四层”为考查内容,即“核心价值、学科素养、关键能力、必备知识”,是素质教育目标在高考中的提炼,回答“考什么”的问题;“四翼”为考查要求,即“基础性、综合性、应用性、创新性”,是素质教育的评价维度在高考中的体现,回答“怎么考”的问题。同时,高考评价体系还规定了考查载体——情境,以此承载考查内容,实现考查要求。
笔者通过对2020年及2021年江苏省高考试卷的结构对比,归纳如下表所示。
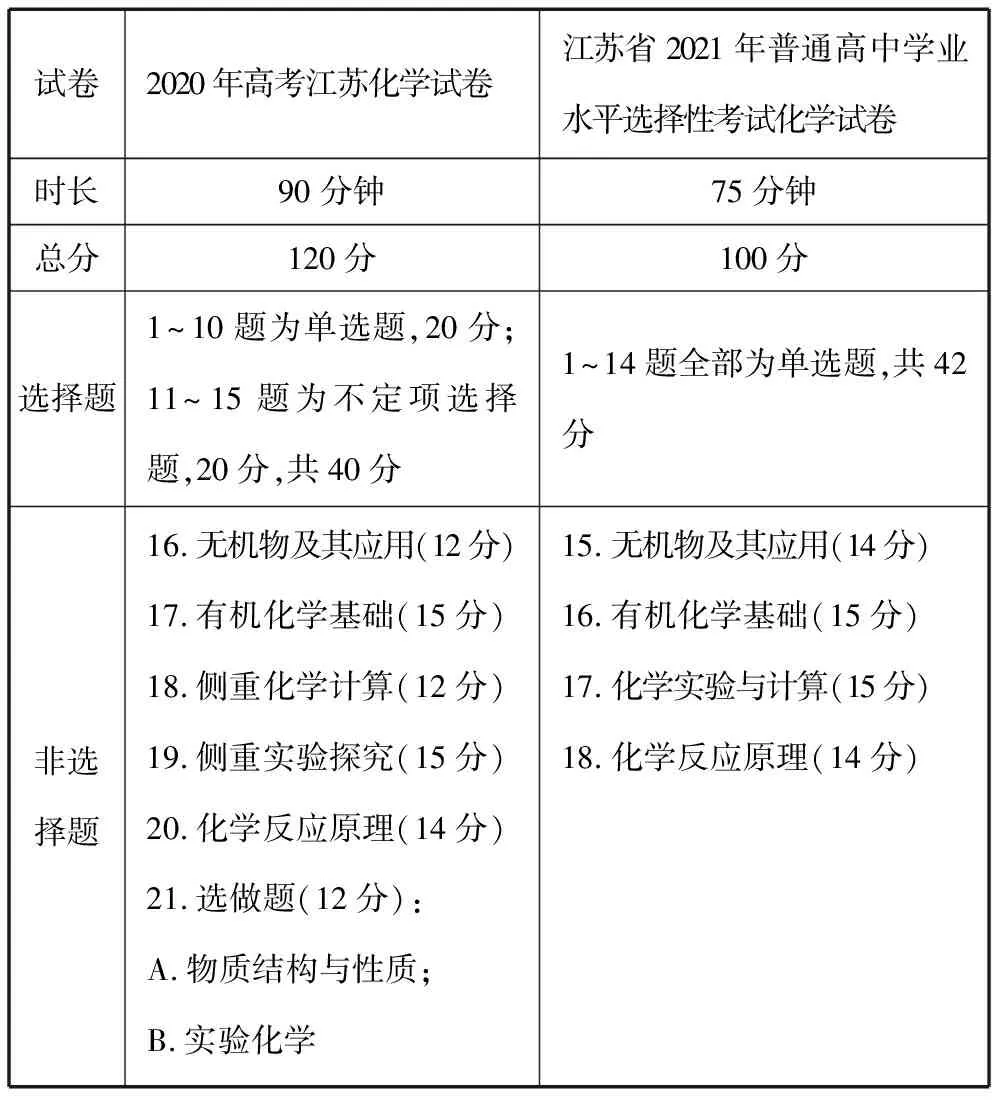
新旧试卷结构比较
从表中可以发现江苏省2021年高考试卷中关于化学实验的考查发生了重大变化,由原本的“侧重化学计算、侧重实验探究”变为2021年高考化学试卷的“化学实验与计算”。2021年高考试卷中化学实验部分除了考查学生化学实验基础知识和基本技能、评价不同类型化学实验及探究活动的核心思路与基本方法外,还重点考查了学生的科学探究与创新意识的化学学科核心素养,尤其是将化学实验与计算结合起来进行考查。化学实验不是单纯的物质变化和现象特征的变化,更伴随着物理量的变化。反应有关的多种物理量必然伴随着化学变化而产生不易察觉的变化,只有秉承严谨的科学态度和创新精神,才能发现这些变化的物理量之间的内在联系。而化学计算也不同于数学计算,它是建立在化学实验的基础之上的,不是纯粹的数学计算,还包含化学反应原理相关知识。
学科核心素养是学科育人价值的集中体现,是学生通过学科学习而逐步形成的正确价值观念、必备品格和关键能力。化学学科核心素养包括“宏观辨识与微观探析”“变化观念与平衡思想”“证据推理与模型认知”“科学探究与创新意识”“科学态度与社会责任”等5个方面。
化学实验是研究和学习物质及其变化的基本方法,是科学探究的一种重要途径。科学探究是进行科学解释和发现、创造和应用的科学实践活动。科学探究过程包括发现问题和提出假设、设计方案、实施实验、获取证据、分析解释或建构模型、形成结论及评价等核心要素。理解从问题或假设出发确定研究目的、依据研究目的设计方案、基于证据进行分析和推理等对于科学探究的重要性。学会物质检验、分离、提纯和溶液配制等化学实验基础知识和基本技能。研究物质性质,探究反应规律,进行物质分离、检验和制备等不同类型化学实验及探究活动的核心思路与基本方法。体会实验条件控制对完成科学实验及探究活动的作用。发展学生对化学实验探究活动的好奇心和兴趣,养成注重实证、严谨求实的科学态度,增强合作探究意识,养成独立思考、敢于质疑和勇于创新的精神。笔者以江苏省2021年普通高中学业水平选择性考试中的有关实验的试题为例,进行深入的分析,以期给广大教师提供参考。
一、评价学生对化学实验基础知识和基本技能的掌握
化学知识是解决实际问题、完成测试任务不可或缺的工具。高考考查要求学生能设计常见物质制备、分离、提纯、检验等简单任务的方案,能从物质类别和元素价态变化的视角说明物质转化的路径;要求学生运用已有的化学实验基础知识和基本技能及从试题中领悟到的相关知识来解决所提出的问题。如例1所示:
【例1】(2021·江苏省普通高中学业水平选择性考试·3)下列由废铜屑制取CuSO4·5H2O的实验原理与装置不能达到实验目的的是
( )

甲

乙

丙

丁
A.用装置甲除去废铜屑表面的油污
B.用装置乙溶解废铜屑
C.用装置丙过滤得到CuSO4溶液
D.用装置丁蒸干溶液获得CuSO4·5H2O
【参考答案】D
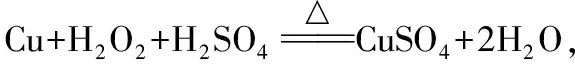
二、评价学生面对化学实验及探究活动时的核心思路与基本方法
“实践探究”是指学习者在面对生活实践或学习探索问题情境时,组织整合相应的知识与能力、运用不同的技术方法进行各种操作活动以解决问题的综合品质,是个体改造世界的核心品质,是完成认知学习和实践的关键环节。认识化学科学研究需要实证与推理,注重宏观与微观的联系,能依据现象和数据,进行分析和推理,得出合理的结论,并对实验结果进行反思,说明证据和结论之间的关系。
【例2】(2021·江苏省普通高中学业水平选择性考试·11)室温下,通过下列实验探究NaHCO3、Na2CO3溶液的性质。
实验1:用pH试纸测量0.1 mol·L-1NaHCO3溶液的pH,测得pH约为8
实验2:将0.1 mol·L-1NaHCO3溶液与0.1 mol·L-1CaCl2溶液等体积混合,产生白色沉淀
实验3:向0.1 mol·L-1Na2CO3溶液中通入CO2,溶液pH从12下降到约为9
实验4:向0.1 mol·L-1Na2CO3溶液中滴加新制饱和氯水,氯水颜色褪去
下列说法正确的是
( )
【参考答案】C
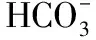

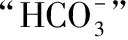
室温下:Ka1(H2CO3)=4.3×10-7、Ka2(H2CO3)=5.6×10-11、Ksp(CaCO3)=2.8×10-9
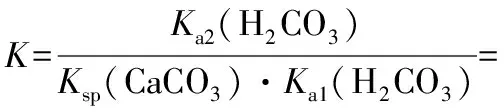
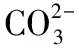

本题通过对电离平衡、水解平衡、沉淀溶液平衡等移动的分析,考查学生的微粒观、平衡观和守恒观;结合实验现象、数据等证据素材,引导学生形成认识水溶液中离子反应与平衡的基本思路,能解释证据与结论之间的关系,确定形成科学结论所需要的证据和寻找证据的途径;能认识化学现象与模型之间的联系,能运用多种认识模型来描述和解释物质的结构、性质和变化,预测物质及其变化的可能结果;能依据物质及其变化的信息建构模型,建立解决复杂化学问题的思维框架。发展学生“宏观辨识与微观探析”“变化观念与平衡思想”和“证据推理与模型认知”等化学学科核心素养,培养学生的系统思维能力。
三、评价学生的科学态度和创新精神
试题需能评价学生是否具有严谨求实的科学态度,能尊重事实和证据,具有探索未知、崇尚真理的意识,考查学生能否从问题和假设出发,依据探究目的,设计并优化探究方案,运用化学实验等方法进行实验探究,能对观察记录的信息进行加工并获得结论,能运用已有知识和方法综合分析化学反应过程的各种影响,权衡利弊,敢于质疑,勇于创新。
【例3】(2021·江苏省普通高中学业水平选择性考试·17)以软锰矿粉(含MnO2及少量Fe、Al、Si、Ca、Mg等的氧化物)为原料制备电池级MnO2。
(1)浸取。将一定量软锰矿粉与Na2SO3、H2SO4溶液中的一种配成悬浊液,加入到三颈瓶中(如图1),70℃下通过滴液漏斗缓慢滴加另一种溶液,充分反应,过滤。滴液漏斗中的溶液是________;MnO2转化为Mn2+的离子方程式为
。
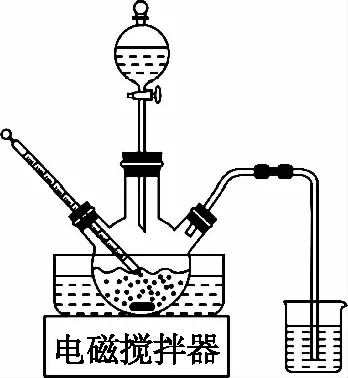
图1

(3)制备MnCO3。在搅拌下向100 mL 1 mol·L-1MnSO4溶液中缓慢滴加1 mol·L-1NH4HCO3溶液,过滤、洗涤、干燥,得到MnCO3固体。需加入NH4HCO3溶液的体积约为________。

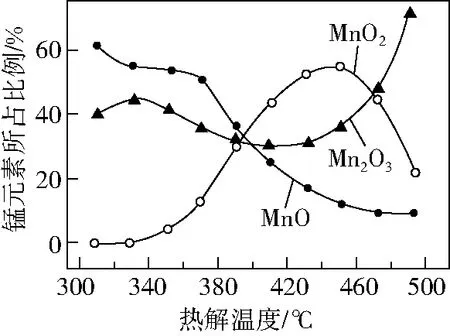
图2
为获得较高产率的MnO2,请补充实验方案:取一定量MnCO3置于热解装置中,通空气气流,
,
固体干燥,得到MnO2。(可选用的试剂:1 mol·L-1H2SO4溶液、2 mol·L-1HCl溶液、BaCl2溶液、AgNO3溶液)。

(2)100
(3)200 mL
(4)加热到450℃分解一段时间,将冷却后的固体边搅拌边加入至一定量1 mol·L-1稀H2SO4中,加热,充分反应后过滤,洗涤,取最后一次洗涤滤液加盐酸酸化的BaCl2溶液,若溶液不出现浑浊,过滤

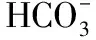
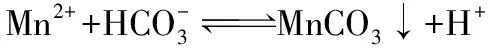
室温下Ka2(H2CO3)=5.6×10-11、Ksp(MnCO3)=9×10-11
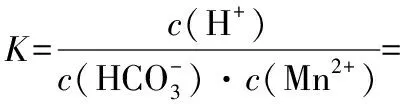
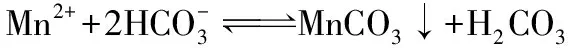
室温下Ka1(H2CO3)=4.3×10-7、Ka2(H2CO3)=5.6×10-11、Ksp(MnCO3)=9×10-11
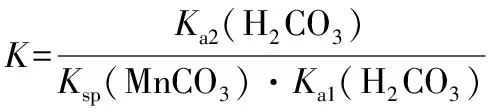
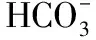

①画从MnCO3制备MnO2的大体流程:
②控制实验条件以完成实验及探究活动:热解对温度的选择——通过对图像的分析得出应选择450℃;酸化时要求所用酸的选择——Mn2O3氧化性强于Cl2,所以应选择1 mol·L-1H2SO4溶液;


