老年营养风险指数联合血尿酸对老年急性呼吸窘迫综合征患者预后的预测价值
向英,谢芳,刘婷婷,常彬宾,王璋
(中国人民解放军西部战区总医院干部科,成都 610083)
急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)是一种常见的危重病,以低氧血症和严重呼吸窘迫为特征,可导致多器官功能障碍综合征甚至死亡[1]。随着医疗技术的发展,ARDS诊治取得了一定成效,但病死率仍高达30%~40%,严重危害患者生命健康[2]。目前,临床上应用急性生理学和慢性健康状况评分Ⅱ(acute physiology and chronic health evaluation Ⅱ,APACHE Ⅱ)和序贯性器官衰竭评估(sequential organ failure assessment,SOFA)评分等指标预测ARDS患者发病风险和预后,但这些指标预测价值较低,计算复杂耗时,在临床应用中受到限制[3]。老年营养风险指数(geriatric nutritional risk index,GNRI)是一种可用于评估老年患者营养水平,计算简单且经济客观的指标,仅根据身高、体质量和血清白蛋白水平便可计算,常用于评价高危老年住院患者和脓毒症患者预后[4]。血尿酸(serum uric acid,SUA)是嘌呤代谢的最终产物,具有促氧化和抗氧化特性,与新型冠状病毒肺炎等疾病预后相关[5]。ARDS患者多伴有营养不良及SUA水平升高,但两者与ARDS患者预后是否相关,目前国内外研究报道较少。本研究探讨GNRI和SUA对老年ARDS患者预后的预测价值,以期为临床诊治提供理论依据。
1 对象与方法
1.1 研究对象
回顾性分析2018年1月至2021年9月中国人民解放军西部战区总医院收治的159例老年ARDS患者的临床资料。根据氧合指数分为轻度组[(200 mmHg<氧合指数≤300 mmHg(1 mmHg=0.133 kPa),35例]、中度组(100 mmHg<氧合指数≤200 mmHg,70例)和重度组(氧合指数≤100 mmHg,54例)。根据28 d预后情况分为生存组116例和死亡组43例。纳入标准:ARDS患者符合2012年“柏林定义”关于ARDS的诊断标准[6];发病时间≤24 h;年龄≥80岁。排除标准:诊断为ARDS后≤24 h死亡;患有血液性疾病、肿瘤、免疫系统疾病;严重肝肾功能衰竭;心力衰竭或容量过负荷引起的呼吸衰竭;患有肺癌、急性肺栓塞、肺结核及慢性阻塞性肺疾病等肺部疾病;入院前使用促尿酸排泄药物及其他原因引起的继发性SUA升高;中途转院或放弃治疗。
1.2 方法
收集患者基线资料,包括年龄、性别、体质量指数(body mass index,BMI)、既往病史、APACHE-Ⅱ、SOFA评分、氧合指数及ARDS致病原因等。所有患者入院时均采集空腹静脉血3 ml,以3 500转/min速度离心10 min分离血清,放置于-20℃冰箱保存备用,采用尿酸酶法检测SUA水平。计算GNRI,GNRI=1.489×血清白蛋白(g/L)+41.7×实际BMI/(22 kg/m2)[7]。
1.3 统计学处理
2 结 果
2.1 生存组和死亡组患者基线资料比较
本研究老年ARDS患者病死率为27.04%(43/159)。生存组和死亡组患者APACHE Ⅱ评分、SOFA评分、氧合指数和病情严重程度比较,差异均有统计学意义(P<0.05;表1)。

表1 生存组和死亡组患者基线资料比较
2.2 生存组和死亡组患者GNRI和SUA水平比较
与生存组相比,死亡组患者GNRI水平显著降低,SUA水平显著升高,差异均有统计学意义(均P<0.05;表2)。
表2 生存组和死亡组患者GNRI和SUA水平比较
2.3 不同病情患者GNRI和SUA水平比较
ARDS重度组患者GNRI水平显著低于轻度组和中度组,SUA水平显著高于轻度组和中度组,差异均有统计学意义(P<0.05;表3)。
表3 不同病情患者GNRI和SUA水平比较
2.4 GNRI和SUA水平与氧合指数的相关性分析
Pearson相关性分析显示:氧合指数与GNRI呈正相关(r=0.412),与SUA呈负相关(r=-0.403),差异均有统计学意义(P<0.01)。
2.5 GNRI和SUA水平对老年ARDS患者预后的预测价值
ROC曲线分析显示:GNRI和SUA预测老年ARDS患者预后的曲线下面积(area under curve,AUC)分别为0.811(95%CI0.744~0.878)和0.830(95%CI0.762~0.898),最佳截断点分别为83.07分和493.13 μmol/L,灵敏度分别为81.38%和81.40%,特异度分别为70.69%和71.55%。二者联合预测的AUC为0.892(95%CI0.841~0.943),灵敏度和特异度分别为83.72%和81.90%(图1)。Kaplan-Merier曲线分析显示,与GNRI≥83.07分患者相比,GNRI<83.07分患者28 d死亡率显著增加;与SUA≤493.13 μmol/L患者相比,SUA>493.13 μmol/L患者28 d死亡率显著增加,差异均有统计学意义(P<0.05;图2~3)。

图1 GNRI和SUA预测老年ARDS患者预后的ROC曲线

图2 不同水平GNRI患者28 d死亡情况Kaplan-Merier曲线
3 讨 论
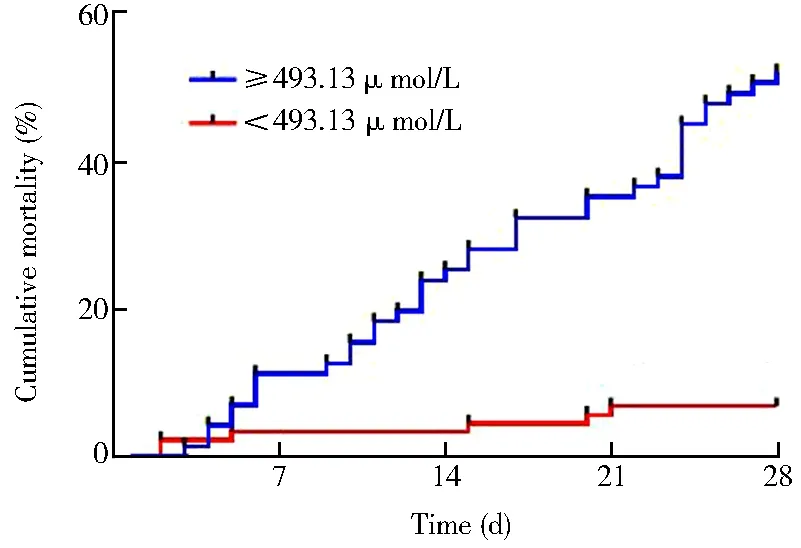
图3 不同水平SUA患者28 d死亡情况Kaplan-Merier曲线
ARDS具有死亡率高,预后差的特点,其发病率和病死率随年龄增加呈增长趋势[8],为重症监护室常见疾病。研究表明[9],营养素摄入减少会导致营养状况不佳,增加老年患者感染的风险。营养不良还会损害呼吸功能,增加肺炎风险。GNRI用于评估老年患者营养状况,是预测长期护理的老年患者死亡率的评价指标[10]。杨琴等[11]研究发现,老年重症肺炎患者GNRI水平明显降低,且与病情严重程度和预后密切相关。Yoo等[12]回顾性分析224例ARDS患者30 d预后情况,发现生存组GNRI水平高于死亡组,且GNRI水平越低,ARDS患者死亡的风险越高,与本研究结果一致。本研究发现,死亡组老年ARDS患者GNRI水平较生存组低,且GNRI水平与氧合指数呈正相关。氧合指数作为肺部氧合状态的综合指标,能够反应患者肺部氧气交换功能,可评估ARDS患者的病情严重程度,其水平越低表明患者肺功能受损越严重。GNRI水平越低代表体内蛋白质损耗越严重,而机体白蛋白水平降低会使血浆胶体渗透压降低,大量液体从肺血管渗入肺泡及肺间质,加剧肺间质水肿、加重肺损伤,从而加速ARDS患者病情恶化,影响患者预后[13]。且营养不良会降低宿主防御过程中对内源性营养物质的利用,致使患者免疫功能下降,感染风险增加,预后较差[14]。
SUA作为代谢指标,除药物和高嘌呤饮食外,受其他因素影响较小,对调节肺和气道上皮细胞氧化应激具有重要意义[15]。Pehlivanlar-Kucuk等[16]纳入128例重症患者的多中心前瞻性队列研究发现,死亡组患者SUA水平高于非死亡组,且当SUA水平高于4.5 mg/dl时,死亡风险增加2.638倍。本研究发现死亡组SUA水平较生存组高,且SUA水平与氧合指数呈正相关,提示SUA水平越高,肺损伤越严重,患者预后越差。许郭华等[17]研究发现,ARDS患者SUA水平高于健康人群,且死亡组患者SUA水平高于生存组。Lee等[18]研究发现,低SUA组ARDS患者预后优于高SUA组,且低SUA水平与较高的生存率显著相关,与本研究结果相似。可能原因为ARDS患者缺氧状态下会影响能量代谢,引起次黄嘌呤积累和尿酸大量生成。此外,ARDS患者常伴有氧化应激,通过影响细胞膜通透性及信号传导,使能量代谢受到影响,也会造成SUA水平升高[19]。而高水平SUA能够激活内源性淋巴细胞、中性粒细胞和单核细胞,促使白细胞介素-1β(interleukin-1β,IL-1β)产生。IL-β通过与Toll样受体信号结合,激活促炎转录因子,促进炎性因子的释放,从而使患者病情加重、预后变差[20]。
ROC曲线分析结果显示:GNRI联合SUA对老年ARDS患者预后具有较高的预测价值,优于单独应用。Kaplan-Merier曲线分析结果显示,不同水平GNRI与SUA患者28 d病死率比较差异有统计学意义(P<0.05),进一步提示GNRI和SUA与老年ARDS患者预后相关。
综上所述, GNRI和SUA水平与老年ARDS患者病情严重程度相关,二者联合应用对老年ARDS患者预后有较高的预测价值。但本研究为单中心回顾性研究,且未监测老年ARDS患者不同时期的GNRI和SUA水平,结果可能存在一定偏倚。今后还需开展多中心前瞻性研究,动态监测GNRI和SUA水平变化,进一步验证上述结果。

