超声引导下乳腺微创旋切术在筛查触诊阴性早期乳腺癌中的应用
张 勤 常万利 王遵义
(河北省沧州市中心医院甲乳外三科,沧州 061000)
乳腺癌是威胁全世界女性健康的常见恶性肿瘤之一,目前已跃居我国女性恶性肿瘤发病率的首位[1]。近年来,随着政府对乳腺癌筛查工作的推动以及人们体检意识的增强,很多女性在体检过程中发现乳腺小结节。因结节体积小(<10 mm),临床触诊难以发现。即使乳腺超声BI-RADS 3~4a 类,依然有乳腺癌风险,且有些患者往往有很大的心理压力。如何在临床触诊阴性的乳腺结节患者中筛查出早期乳腺癌是乳腺外科医师面临的问题。为避免早期乳腺癌的漏诊,必要时需对可疑病灶进行活检,目前活检方式有空芯针粗针吸穿刺活检(core needle biopsy,CNB)、微创旋切活检系统以及开放性手术活检。对于乳腺小结节,采用传统的开放性手术切除活检具有一定的难度,空芯针粗针吸穿刺活检获取的组织量有限,存在病理低估。随着超声及乳腺微创技术的发展,超声实时引导下应用微创旋切术切除乳腺肿瘤的手术方式越来越受到临床重视以及患者的认可。超声引导下微创旋切术对乳腺小结节能够准确定位与完整切除,并可能作为发现早期乳腺癌的重要手段[2]。2016年6月~2019年6月我科对临床触诊阴性的乳腺小结节(≤10 mm)在超声引导下行微创旋切术,旨在探讨超声引导下乳腺肿物微创旋切术作为一种活检方式在筛查早期乳腺癌中的应用价值,报道如下。
1 临床资料与方法
1.1 一般资料
本组568例(1071个病灶),均为女性。年龄18~65岁,中位年龄35.8岁。438例健康体检超声检出乳腺结节,130例既往超声提示乳腺结节复查,均无乳头溢液,无皮肤红肿及破溃,伴或不伴有乳腺疼痛,临床查体均为阴性。结节直径0.4~1.0 cm,(0.62±0.34)cm。单发323例,2个227例,3个18例。左侧235例,右侧226例,双侧107例。BI-RADS分类:3类426例,共803个结节;4a类142例,共268个结节。
病例选择标准:超声检出乳腺小结节(≤10 mm),BI-RADS 4a类或3类(有乳腺癌家族史、患者思想负担较重、乳腺结节定期超声复查后较前增大),临床查体阴性,均能耐受弹力绷带加压包扎,无凝血功能障碍、无妊娠及严重心、肺、肾功能不全等。
1.2 方法
术前告知患者手术的优缺点及相关并发症,患者均签署知情同意书。
采用安珂(EnCor)乳腺真空辅助微创旋切系统(Encor CM3000,美国巴德医疗科技有限公司)和彩色多普勒超声诊断仪。术前超声检查确定结节大小及位置,并在体表标记。切口尽量选择乳房的腋前线或乳晕周围。常规碘伏消毒,铺无菌单、超声探头及手柄套无菌套。20 ml利多卡因+20 ml含有肾上腺素的NaCl(1 mg肾上腺素+250 ml 0.9% NaCl)配好局麻液体进行局部浸润麻醉。以11号尖刀片做 0.5 cm切口。超声引导下将 EnCor旋切刀长轴平行于探头长轴穿入乳腺组织内,将刀槽放置在病灶正下方或侧方,显示出旋切刀长轴和肿瘤位置。然后“十字交叉”旋转超声探头,横切面显示出旋切刀短轴和肿瘤位置。根据刀槽与肿物的位置关系及时多次、多方向调整旋切刀凹槽方位,使其始终保持对准乳腺结节进行旋切,直至乳腺结节消失。观察切除的组织标本与正常组织的界限是否能够完整拼凑瘤体组织,同时将切除的病灶组织与超声测量的结节体积相比较,确认结节完整切除,再次超声检查是否有残留病灶。检查完毕,手术残腔弹力绷带加压包扎48~72 h,以减少术后血肿的发生。
2 结果
每个结节旋切时间(3.1±1.3)min。555例 (97.7%)共1058个结节为良性病变,其中腺纤维瘤672个,乳腺腺病伴腺瘤形成趋势(含乳腺腺病) 371个,导管内乳头状瘤6个,其他良性病变(乳腺炎、上皮增生活跃伴或不伴不典型增生等) 9个。重度不典型增生2例(0.4%),再次进行局部扩大切除术。恶性病变11例 (1.9%),其中浸润性导管癌8例,导管原位癌3例,见图1、2。BI-RADS 3类426例中4例乳腺癌,恶性率0.9%(4/426);4a类142例中7例乳腺癌,恶性率4.9%(7/142)。11例乳腺癌的超声特征及其他乳腺癌高危因素见表1,BI-RADS 4a类或3类均无明显恶性典型征象,往往合并其他考量因素进行手术,如乳腺癌家族史、焦虑等。
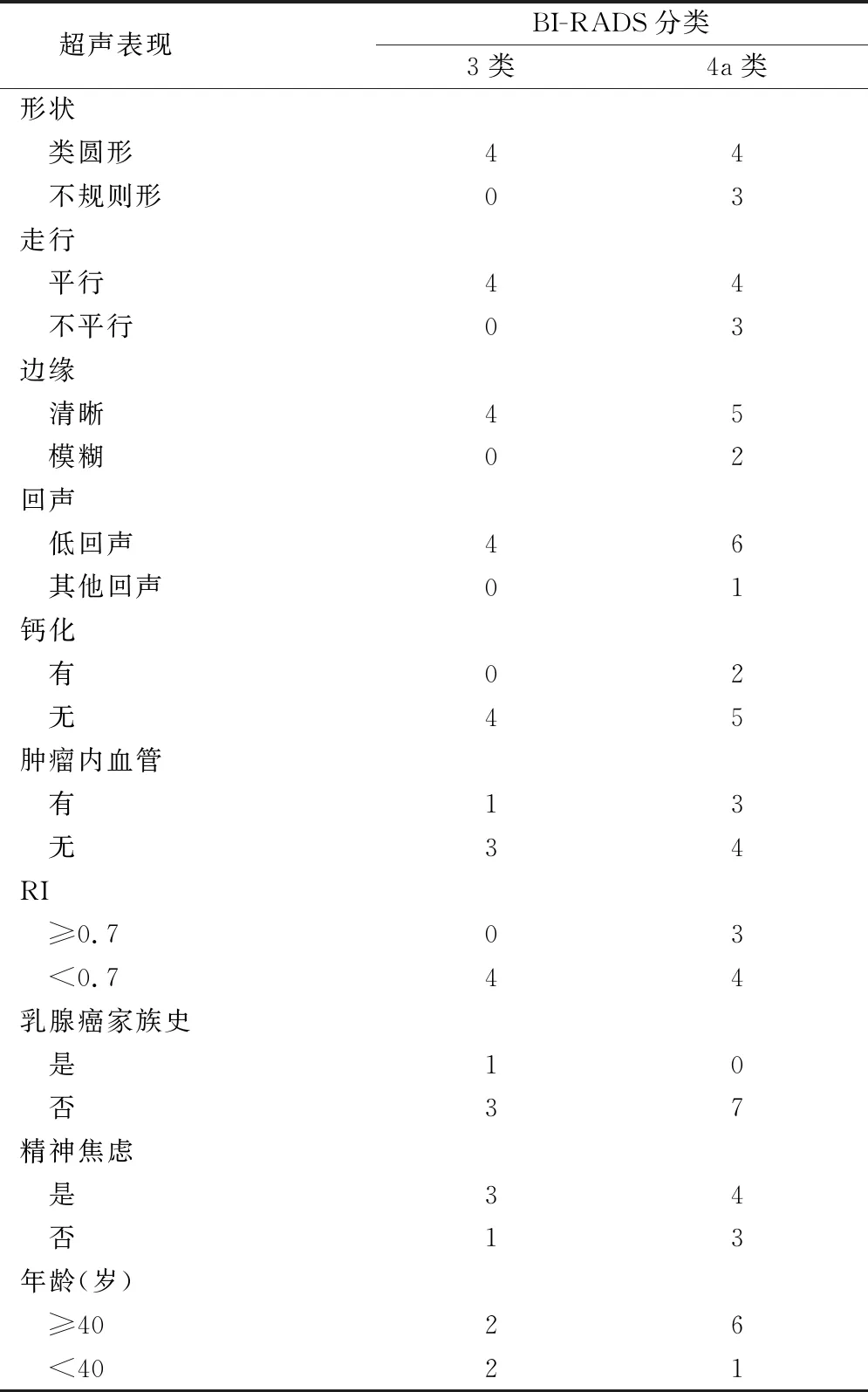
表1 11例乳腺癌超声特征及乳腺癌高危因素
术后第3天进行第1次换药,78例(13.7%,78/568)去除弹力绷带后术区出现皮下淤血,未行特殊处理,继续弹力绷带加压至术后1周,定期回院复查,2~4周自行吸收。术后1周电话随访,148例诉术区肿块,于当地医院或我院行超声检查考虑术后积液,告知无需特殊处理。1例良性肿瘤术后15 d参加拔河比赛后出现术侧乳房胀痛,回院复查,查体见乳房术区一5.0 cm×4.0 cm包块,边界不清,内可触及波动感,20 ml注射器给予抽吸,抽出不凝血8 ml,抽吸完毕后于残腔处继续给予纱布及弹力绷带加压包扎,2周后拆除绷带,4周后恢复正常。在开展手术初期,1例出现肺损伤,在进行局麻进针过程中,针尖未完全显示清楚的情况下,进针过深,误入胸腔,术中患者突发咳嗽,痰中带血,立即停止操作,给予吸氧等对症处理,10 min后患者好转后继续完成手术。
555例良性病变术后6个月开始门诊复查,其后依据具体情况,每6~12个月进行复查,共489例(88.1%)进行规律复查,随访时间26~68个月,中位随访时间47.9月,超声检查未见肿瘤残留。11例乳腺癌辅助治疗结束后每3~6个月进行规律随访,无一例发生复发或转移。
3 讨论
近年来,乳腺肿瘤在各年龄段人群中的检出率逐渐增多,新发早期乳腺癌的比例在不断提高。一般情况下,正常体检者在接受检查时,大约有3%的可能性发现微小乳腺结节。Mariotti等[3]报道15%~30%临床触诊阴性的病灶为恶性。因为结节体积小,临床触诊难以发现,传统开放性手术切除有一定难度。超声引导下乳腺微创旋切术能准确快捷对临床触诊阴性乳腺小结节进行切除活检,具有诊断与治疗双重作用的新技术,有助于早期乳腺癌的检出,目前在我院临床工作中得到了很好地应用。
3.1 BI-RADS分类与活检手术适应证
临床工作中,对于超声BI-RADS 4a类和3类的乳腺小结节患者,按照 BI-RADS 临床管理原则,进行半年或1年定期超声或者钼靶随访即可,但是部分患者由于心里紧张、焦虑或者不能保证规律性定期复查,选择穿刺活检或手术切除,有些患者因有乳腺癌家族史选择尽早手术切除。表1可以看出,BI-RADS 3类及4a类乳腺小结节,超声下恶性特征并不典型,但因潜在的风险性,可能会给患者带来很大的困扰和焦虑,甚至有的患者每隔2~3个月频繁进行复查,所以对这样的患者进行活检是必要的。霍彦平等[2]报道1718例BI-RADS 3类中发现21例乳腺癌(恶性率1.22%),本组BI-RADS 3类乳腺小结节恶性率0.9%(4/426),与其报道相似。BI-RADS 3类但病理为恶性的4例中,2例年龄<35岁,其中1例有乳腺癌家族史(妈妈与姐姐均为乳腺癌),即便告知BI-RADS 3类(图1)恶性风险极小,但患者恐癌压力极大,心情焦虑,因此行微创旋切手术,病理结果为导管内癌。刘晨晨等[4]报道152例BI-RADS 4a类接受微创旋切术,其中8例浸润性导管癌,恶性率5.2%(8/152),本组BI-RADS 4a类恶性率为4.9%(7/142),与其报告结果相似。7例恶性中1例6个月前外院行传统乳腺肿物切除术,复查超声提示原瘤床位置一小结节,无法判断是术后瘢痕形成亦或是因结节较小上次手术漏切,本次微创旋切手术后病理为浸润性癌(图2)。本组BI-RADS 4a类患者中腺纤维瘤伴重度不典型增生2例(0.3%)。Page等[5]报道在长达25年的随访中,不典型增生患者乳腺癌的累积发生率接近30%。故直接切除比不切除(继续观察)降低恶变的风险。因BI-RADS 3、4a 类患者存在小风险恶性肿瘤可能性,因此,进行定期规律随访尤为必要。如果合并其他因素,如恐癌、精神焦虑、不能配合进行定期复查、有乳腺癌发病高危因素(如乳腺癌家族史、BRCA1/2基因突变、过量服用雌激素、乳腺增生等),建议临床重视度升级,有必要积极进行活检。
3.2 超声引导下微创旋切术对于乳腺小结节切除活检的精准性及可操作性
对于临床触诊阴性的患者,采用开放性手术具有盲目性,不能确定是否彻底清除结节,即便实现结节切除,也无法保证切除的结节是超声检查发现的结节。往往为确保结节能够完整切除,需要切除多量结节周围的腺体组织,造成不必要的创伤[6]。切口较大,易留下瘢痕,影响乳房外观。超声引导下微创旋切是在超声实时引导下进行操作,术前由超声科医生进行定位,术中进行反复比对,能够快速精准的找到小结节,并能够确保切除的结节为超声所发现的结节。对于<1 cm小结节,一般2~3刀即可切除干净,对于多发结节,可通过1个切口实现多个象限结节的切除,且可达到准确定位与完整切除,充分体现微创、手术时间短、并发症少、美观等优势。本组555例良性病变中,489例(88.1%)随访26~68个月,中位随访时间47.9月,超声检查未见肿瘤残留,可能因为肿瘤较小,易于切除干净。因此,微创旋切活检术对于临床触诊阴性的小结节的切除具有独特的优势,既能实现对肿瘤进行切除活检,又能对实现对恶性肿瘤早诊早治,提高治愈率。
3.3 超声引导下微创旋切术在早期乳腺癌活检中的优势
对于为直径10 mm左右的乳腺小结节,常规影像学检查往往无法较准确判断其良恶性,应穿刺活检或者切除活检明确其良恶性,再完成相关后续治疗[7]。CNB可以提供可靠的病理组织学诊断,但穿刺针需要反复进出乳房进行取材,且对于小结节存在定位不准,尤其对伴有微钙化的结节,取材有限,存在病理低估等,10%~25%的病例不能提供精确的诊断,因此,CNB对于小结节的诊断具有局限性。微创旋切术在超声引导下进行,对较小的结节可达到定位精准,将结节完整切除,获取样本量大,病理检查无遗漏,诊断准确率高,不会出现低估风险,被认为是临床触诊阴性的乳腺癌筛查的理想方法[8]。
3.4 超声引导下微创旋切术后乳腺癌手术的注意事项
微创旋切术后乳腺结节确诊恶性后,可根据术前影像学评估进行适宜的术式,如保乳术、单纯乳房切除术、重建修复整形术、前哨淋巴结活检术及腋窝淋巴结清扫术等。Uematsu等[9]对穿刺针冲洗液进行检测,真空辅助穿刺针的针道种植率约33%。如果乳腺微创术中冰冻病理为恶性,应在随后的手术中完整切除针道。因此,术前应把每例患者当成恶性来进行切口设计,需考虑到针道完整切除后乳房切口的可选择性及可行性等。本组1例术后病理发现肿瘤残留(导管内癌成分),早期乳腺癌保乳手术中,真空辅助旋切术并不能替代传统的保乳手术[10]。超声引导下微创旋切术有助于筛查早期乳腺癌,提高保乳率,为保留乳腺外形美观及腋窝功能保护起到了积极的推动作用。
3.5 超声引导下微创旋切活检手术并发症
微创旋切手术并发症主要有术中出血、术后血肿、肺损伤、感染、肿物残留、手术失败中转开放性手术等。出血是最常见的并发症。本组术后远期活动性出血1例,发生率0.2%(1/568),皮下瘀斑78例,发生率13.7%(78/568)。发生原因多为术后处理不佳,包括按压时间不够、包扎松脱或移位等[10]。本例远期出血原因:①肿瘤位置较深,贴近乳房后间隙,血管丰富,术中出血较多;②患者乳房体积较大、下垂,术后加压包扎纱布位置点易变动,加压效果欠佳,术后72 h去除加压包扎未行有效固定;③患者术后剧烈活动。为降低出血风险,局部麻醉时,在麻醉药物中加入适当比例的肾上腺素。另外,一定要严格把握手术适应证,对于有出血倾向、凝血机制障碍、加压包扎困难的患者不予进行手术治疗[11]。本组肺损伤1例,发生率0.2%(1/568),总结发生原因是未严格遵循“不见刀尖不进针”的原则,麻醉针头较细,肺损伤较小,未出现血气胸,如果是旋切刀头误入胸腔后果将不堪设想。此种风险对于乳房较小的患者尤其注意防范,可在乳房后间隙注射含有肾上腺素的局麻药物进行充分隔离。尤其注意穿刺针角度与力度,避免刺入胸腔导致气胸发生[12,13]。本组患者未发生气胸、感染、肿物残留等。
综上所述,超声引导下乳腺微创旋切术定位精准、创伤性小、安全可靠,作为活检手段,在触诊阴性的乳腺小结节(≤10 mm)中筛查早期乳腺癌具有独特的优势,为早期乳腺癌的诊断、手术治疗方案选择提供准确诊断依据,尤其适合乳腺BI-RADS 3及4a类结节合并乳腺癌发病高危因素(恐癌、精神焦虑,或者有乳腺癌发病高危因素的患者,如乳腺癌家族史、BRCA1/2基因突变、过量服用雌激素、乳腺增生等),不能积极配合进行定期复查者,乳腺结节微创旋切术进行活检显得尤为必要。

