磷酸盐对土壤吸附一硫代砷的影响
张进贤,单慧媚*,廖丹雪,彭三曦,杜海玲,刘允全,石 谦
磷酸盐对土壤吸附一硫代砷的影响
张进贤1,单慧媚1*,廖丹雪2,彭三曦3,杜海玲1,刘允全1,石 谦1
(1.桂林理工大学,广西环境污染控制理论与技术重点实验室,岩溶地区水污染控制与用水安全保障协同创新中心,广西 桂林541004;2.广西生态工程职业技术学院生态环境保护学院,广西 柳州 545003;3.桂林理工大学地球科学学院,广西 桂林 541004)
通过设计批实验和表征分析,探究不同浓度的磷酸盐影响下,一硫代砷酸盐(MTA)在土壤上的吸附特征和机理.结果发现,Elovich 动力学模型和Langmuir等温吸附模型可较好地拟合MTA在土壤中的吸附过程,相关系数2分别为0.983和0.994,表明土壤吸附MTA发生在局部位置,吸附过程主要以非均相扩散为主,拟合所得最大单层吸附量为254.214mg/kg.MTA与磷酸盐共存时,随着溶液中磷酸盐初始浓度的增大,土壤对MTA的平衡吸附量逐渐下降,对磷酸盐的吸附量逐渐增大;SEM-EDS结果表明无论是否添加磷酸盐,反应后的土壤表面都能检测到少量As,但添加磷酸盐条件下土壤表面的As含量则相对较低,证实磷酸盐的存在降低了土壤对MTA的吸附;XRD结果表明MTA能与土壤中的铁铝矿物发生络合反应生成内球络合物-[2Al(H2AsO4)3]、≡Al2O2AsO(SH)和-[2Fe(H2AsO4)3],而磷酸盐会与土壤表面的羟基形成内球络合物,导致土壤对MTA的吸附能力减弱.
一硫代砷;土壤;吸附;磷酸盐
全世界许多国家都有高砷地下水分布,而印度、孟加拉国和中国一些地区中的地下水受砷污染最严重[1-5].砷有多种存在形式,其中亚砷酸盐毒性最大,其次,砷酸盐,硫代砷,有机砷毒性相对较小[6].水环境中砷的存在形式影响其迁移与转化,而砷的化学形态又取决于水介质氧化还原条件和水中硫化物浓度[7].在地下水中,砷酸盐在氧化条件下占优势,亚砷酸盐在好氧环境向缺氧环境转变时占优势[8].随着氧化还原电位的进一步降低,在含溶解性硫化物水体中或由微生物介导下硫酸盐还原产生的硫化物中,硫原子会逐渐将砷酸盐和亚砷酸盐中的氧原子取代,形成硫代砷(亚)酸盐,根据硫原子取代氧原子的个数,可形成一至四硫代砷(亚)酸盐[9].砷和磷属于同一主族元素,两者具有相似的化学特征,它们在水溶液中通常都以含氧阴离子的形式存在,并且砷酸盐和磷酸盐两者的离子半径和解离常数很相近[10].砷酸根与磷酸根在针铁矿表面会发生竞争吸附,两者会在针铁矿表面形成内圈层络合物,都会吸附在铁氢氧化物表面的内圈层上. 磷酸根对砷酸根和亚砷酸根的吸附都具有抑制作用,而且磷酸根对亚砷酸根的抑制作用更明显[11-14].上述所有的研究都是以不同的吸附材料(铁氢氧化物、改性膨润土、针铁矿和沉积物)为基础,探究磷酸盐对砷酸盐和亚砷酸盐的竞争吸附影响,鲜有学者研究磷酸盐与硫代砷之间是否存在竞争吸附的影响.
硫代砷作为近些年最新发现的砷形态,在富硫、富铁的还原性环境中一硫代砷酸盐(MTA)是主要的且稳定存在的砷形态[15-17].硫代砷酸盐在自然环境中有一定的赋存条件,浅层地下水中一、二硫代砷酸盐只存在于pH=5.5~6.1之间,且它们的含量占总砷的17%[17];地热水中pH值在2.1~9.3之间才存在硫代砷酸盐,且在碱性条件下的样品里,硫代砷酸盐的含量较高[18];三硫代砷酸盐不太稳定,在保存5~12d后,基本所有的三硫代砷酸盐都会转化为砷酸盐[19].除了上述在地热水和浅层地下水中出现硫代砷酸盐,近年在天然泥炭地和水稻根部也发现了硫代砷砷酸盐的存在,且主要存在于中性至碱性土壤中[15,20].
在发现新形态硫代砷后,许多学者对硫代砷展开了研究. 在水铁矿,针铁矿,硫铁矿和黄铁矿分别对MTA、四硫代砷酸盐、砷酸盐和亚砷酸盐的吸附研究中发现水铁矿对4种形态的砷都具有强烈的吸附作用,黄铁矿几乎瞬间吸附完MTA.故所有条件相同,当存在铁氧化物时,硫代砷酸盐比砷酸盐和亚砷酸盐具有更强的迁移性[21].当有共存离子影响时,磷酸盐和胡敏酸(HA)会抑制MTA的吸附,而硝酸盐会促进MTA的吸附[22].这些学者都是单独考虑MTA,探究其在不同介质上或添加不同竞争离子的吸附特征,鲜有学者研究地下水溶液中磷酸盐对原位土壤中硫代砷吸附与迁移的影响.
基于上述问题,本文选取MTA作为研究对象,在实验室条件下模拟自然环境中土壤和MTA之间的相互反应,重点探究不同浓度磷酸盐的影响下,MTA在土壤上的吸附特征和作用机理,以期为我国高砷地下水的治理与控制提供一定的理论参考.
1 材料与方法
1.1 试剂与材料
江汉平原仙桃市是我国典型的饮水型砷中毒病区[23].故本文从江汉平原仙桃市通顺河附近采集土壤,通过自然晾晒干燥后研磨处理,过滤筛得到粒径0.15~0.18mm的土样.土样的主要成分如表1所示.
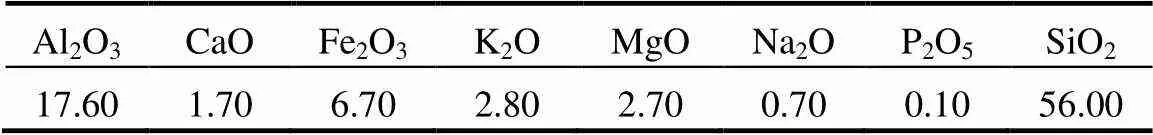
表1 土壤主要成分(%)
本文所用MTA为实验自制,具体制备流程参见文献[24-25]方法.将6. 50g NaAsO2和4. 00g NaOH 溶于20mL去离子水,加入1. 44g单质硫,在智能石墨电热板(DB-1EFS,上海力辰邦西仪器科技有限公司,控温范围0~400℃)上加热至溶液温度>95℃,保持沸腾2h.过滤溶液中多余的单质硫,滤液在4℃下冷却,真空干燥.将晶体溶解于去离子水中,加乙醇使其重结晶,倒出多余水溶液只剩晶体,干燥后得到一硫代砷酸钠,晶体化学结构式:Na3AsO3S·7H2O,溶液中存在形式HAsSO3-3(的取值为0~3).本文制备所得MTA纯度>98.5%.MTA在地下水模拟液中的含量及形态随时间的变化如图1所示.

图1 溶液中MTA形态变化
右侧阴影表示溶液中MTA含量及形态发生了变化
本文所用MTA地下水模拟液是根据土样采集区内的地下水化学特征配置而成,其水化学组成如表2所示.测样时用到亚砷酸根和砷酸根的标准溶液购自中国计量科学院,物质的量浓度分别为(1.011±0.016)和(0.233±0.005)µmol/g.实验添加的磷酸盐为无水磷酸二氢钠NaH2PO4,纯度为AR,麦克林有限公司.
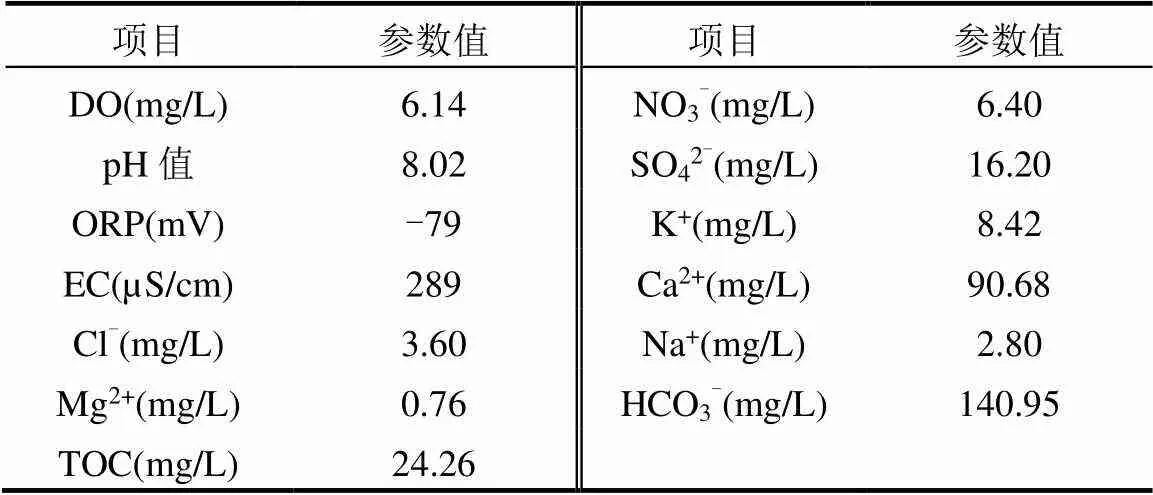
表2 地下水溶液的水化学特征
1.2 实验设计
1.2.1 动力学吸附实验 实验设计0.15,1和49 mg/L,3个不同浓度的MTA地下水模拟溶液.称取0.5g土壤于50mL离心管,分别加入50mL MTA初始浓度为0.15,1和49mg/L的地下水模拟溶液,实验反应到10min,20min,30min,40min,50min,1h,2h,4h,7h,9h和12h分别取样,用0.45µm的滤膜过滤后放入冰箱待测.溶液反应前pH值调为7,实验在150r/min水浴振荡中进行,实验温度控制在(25±1)℃.整个实验设计2个平行组.
1.2.2 等温吸附实验 实验设计1,2,3,4,5,10,20,30,40和50mg/L,10个不同浓度的MTA地下水模拟溶液.称取0.5g土壤于50mL离心管,分别加入50mL MTA初始浓度为1,2,3,4,5,10,20,30,40和50mg/L的地下水模拟溶液,反应到24h分别取样,用0.45µm的滤膜过滤后放入冰箱待测.溶液反应前pH值调为7,实验在150r/min水浴振荡中进行,实验温度控制在(25±1)℃.整个实验设计2个平行组.
1.2.3 磷酸盐对土壤吸附MTA的影响 实验设计5,25,50,100和150mg/L,5个不同浓度磷酸盐溶液.称取0.5g土壤于50mL离心管,分别加入50mL MTA初始浓度为1mg/L,磷酸盐浓度分别为5,25,50,100和150mg/L的混合溶液,实验反应到24h分别取样,用0.45µm的滤膜过滤后放入冰箱待测.溶液反应前pH 值调为7,实验在150r/min 水浴振荡中进行,实验温度控制在(25±1)℃.整个实验设计2个平行组.
1.3 仪器与测试
溶液中MTA、砷酸盐和亚砷酸盐的测试采用液相色谱-原子荧光联用仪(LC-HG-AFS,北京吉天SA-20A型),液相色谱选择阴离子交换柱PRP- X100分离提取砷酸盐、亚砷酸盐和一硫代砷酸盐,各种形态的出峰时间依次为2~3,8~10和18~ 22min[24,26].溶液中磷酸盐的质量浓度测定采用钼酸铵分光光度法,该方法测定磷酸盐(以P计)的检出限为0.01mg/L,测定范围0.04~1.00mg/L,波长为880nm[27].
反应前后土壤的表面形貌特征及元素分析采用场发射扫描电镜及元素分析(SEM-EDS,型号JSM-7900F);物相组成利用X射线衍射仪(XRD,X'Pert3 Powder型多功能X-射线衍射仪(荷兰帕纳科公司,Cu靶,=1.54056°Å)分析,测试扫描步长为0.02626°,扫描速度为0.6565°/s,扫描范围为5°~90°.
1.4 吸附模型
1.4.1 平衡吸附量 MAT在土壤上的平衡吸附量计算公式如下[28]:
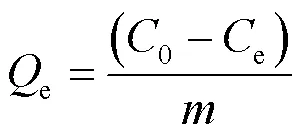
式中:e为MTA在达到吸附平衡后的吸附量,mg/kg;0为溶液中MTA初始时的质量浓度,mg/L;e为反应达吸附平衡时溶液中MTA的质量浓度,mg/L;为反应溶液的体积,L;为反应吸附介质的质量,kg.
1.4.2 等温吸附模型 在吸附实验中,污染物在固相介质上的吸附量与其在液相浓度之间的关系曲线即为吸附等温线.本文采用了Langmuir热力学吸附模型和Freundlich热力学吸附模型对MTA在土壤上吸附过程进行拟合分析[29].
1.4.3 动力学吸附模型 采用准一级动力学模型、准二级动力学模型和叶洛维奇(Elovich)动力学方程[30-34]进行拟合分析.
2 结果与分析
2.1 动力学吸附特征
如图2所示,从整体上看,虽然溶液中MTA浓度不同,但吸附过程中平衡吸附量与时间的关系曲线基本相似,都呈现出3个阶段:前期快速吸附阶段,中期缓慢吸附,到7h最后达到吸附平衡.这种趋势与前人在研究砷酸盐、亚砷酸盐和硫代砷在河砂,矿物和土壤上吸附的结果一致[24,28].吸附到达平衡时,土壤对3种不同浓度MTA的吸附量分别为9.076,45.44和219mg/kg.
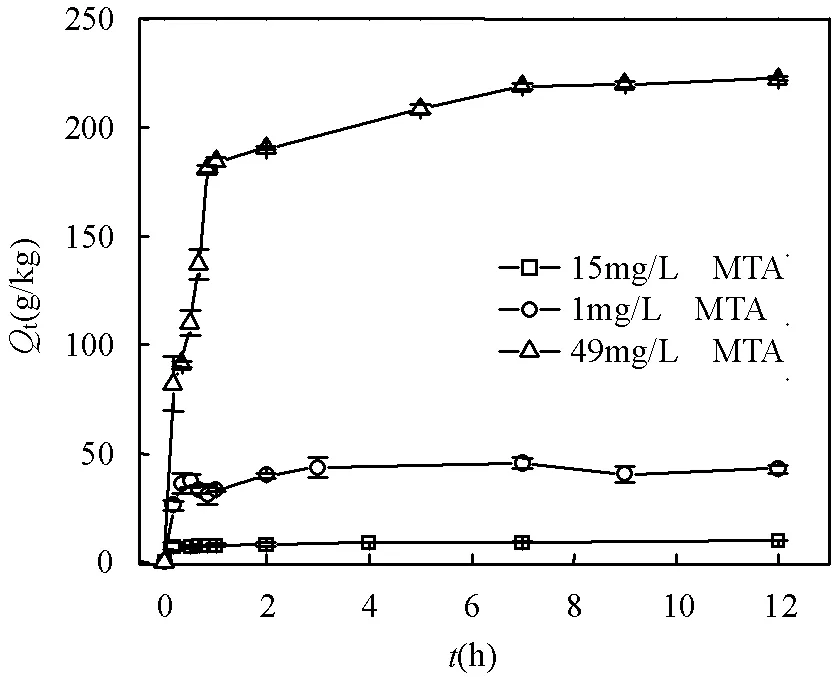
图2 不同浓度MTA溶液在土壤上的吸附动力学曲线
不同浓度MTA在土壤上的吸附动力学模型拟合关系如图3所示,拟合参数如表3所示.MTA浓度为0.15mg/L时,前期快速吸附阶段准二级动力学模型拟合较好,中期缓慢吸附阶段和平衡吸附阶段,Elovich 动力学模型与实验结果拟合较好,相关系数2均大于0.98.MTA浓度为1mg/L时,准二级动力学模型很好地拟合前期快速吸附阶段,相关系数2为0.914;Elovich 动力学模型与中后期吸附阶段拟合效果好,相关系数2为0.923.MTA浓度为49mg/L时,前期快速吸附阶段与准二级动力学模型拟合程度高,相关系数2为0.963;中后期吸附阶段与Elovich动力学模型拟合较好,相关系数2为0.925.
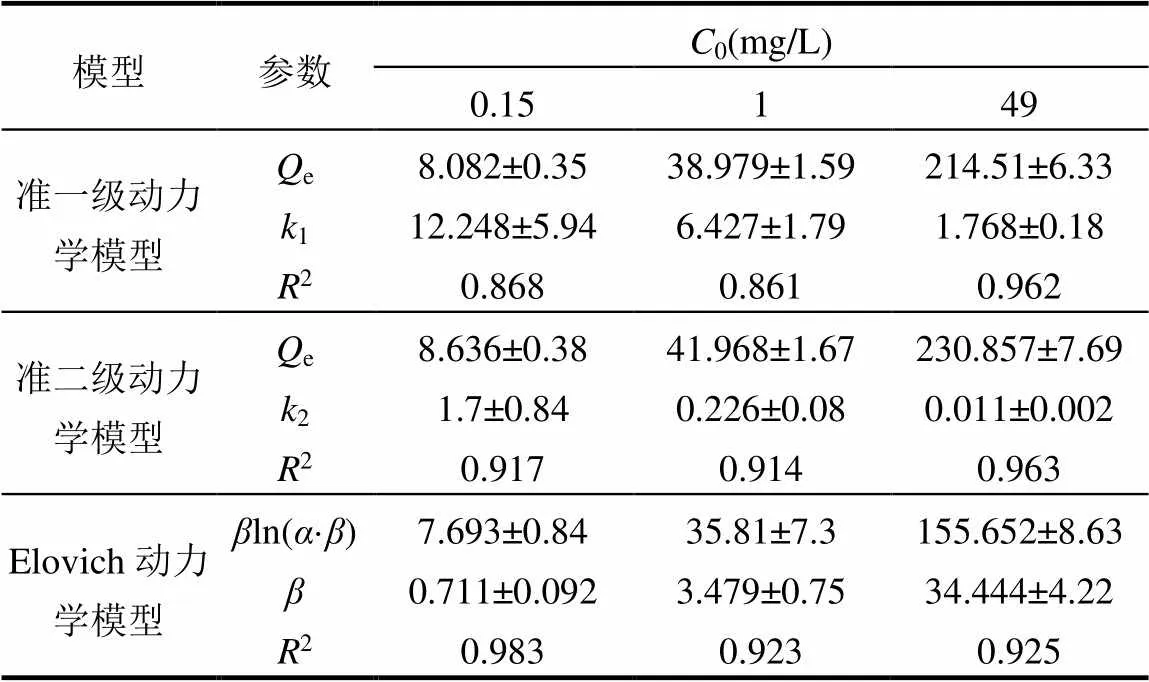
表3 不同浓度MTA在土壤上的吸附动力学模型参数
注:e为平衡态时的吸附量,mg/kg;1为吸附速率常数,min-1;2为吸附速率常数,min-1;、为Elovich 常数,分别表示初始吸附速率[g/(mg×min)]及解吸常数(g/mg).
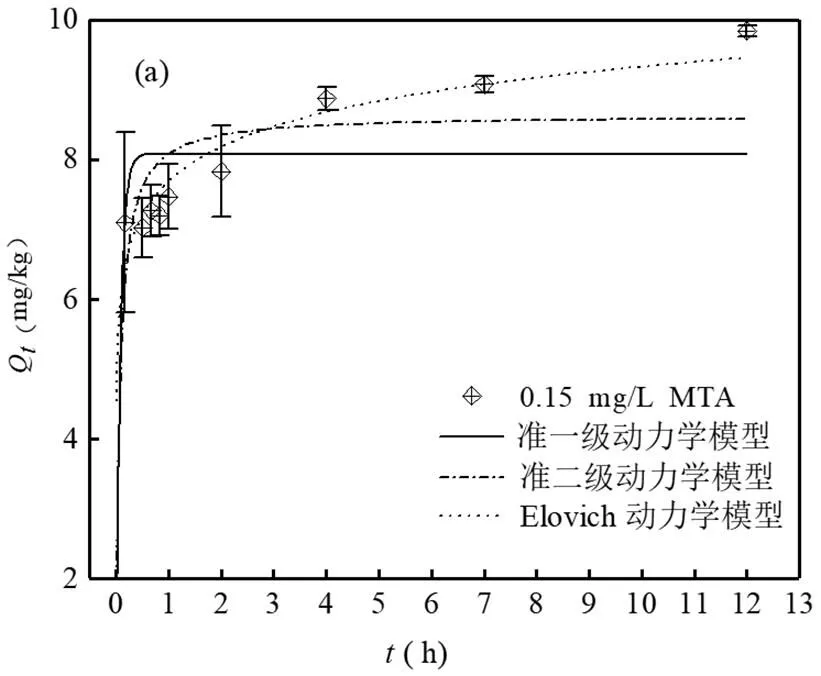
Q表示时刻的吸附量,mg/kg
准二级动力学模型和Elovich 动力学模型都假设吸附发生在局部位置,前者吸附过程以化学吸附为主,后者是对非均相扩散过程的描述,并且吸附剂与吸附质之间发生相互作用[30,34].在前期快速吸附阶段,准二级动力学模型都可以很好拟合各个浓度MTA在土壤上的吸附,表明前期土壤对MTA的吸附发生在局部位置,且吸附过程存在化学反应,可能有配位、络合作用发生.在中后期吸附阶段,Elovich 动力学模型较好的拟合各个浓度MTA在土壤上的吸附,表明土壤和MTA在这段时间两者之间存在相互作用,并且吸附发生在局部位置,吸附过程主要以非均相扩散为主.
2.2 等温吸附特征
如图4所示,MTA的平衡吸附量随溶液初始浓度增大而增大,直至最后MTA初始浓度为50mg/L时趋于稳定.主要由于吸附介质对溶液中溶质的吸附在很大程度上受扩散作用的控制,扩散作用的影响范围受溶液中溶质的浓度影响,与溶质的质量浓度成正比[35],因此在0~50mg/L的质量浓度范围内,随地下水溶液中MTA初始浓度的增大,MTA的平衡吸附量也会随着变大.当超过50mg/L时,由于溶液中吸附介质表面吸附位点有限,此时溶液中的吸附过程会趋于平衡,吸附趋于饱和状态.
Freundlich和Langmuir等温吸附模型对土壤吸附不同浓度MTA的拟合参数如表4所示,可发现Langmuir等温吸附模型对土壤吸附MTA的拟合度较高,相关系数2为0.994.由于Langmuir等温吸附模型是基于吸附剂表面结构均匀同质,并且是单分子层吸附,故MTA在土壤上拟合所得最大单层吸附量为254.214mg/kg.

图4 MTA在土壤上的等温吸附曲线
Q为MTA在达到吸附平衡后的吸附量,mg/kg

表4 MTA在土壤上的等温吸附模型参数
注:m为单层吸附条件下的吸附容量,mg/kg;f为吸附作用强度,(mg/kg)/(L/mg);1/为衡量等温线线性与否的参数.
2.3 磷酸根的影响
如图5所示,随着溶液中磷酸盐的初始浓度增大,土壤对MTA的平衡吸附量逐渐下降,对磷酸盐的吸附量逐渐增大.当溶液中磷酸盐的初始浓度增大到150mg/L时,MTA在土壤上的平衡吸附量减小到最低值,添加150mg/L磷酸盐时MTA在土壤上的平衡吸附量比不添加磷酸盐时下降了47.22%.反应前后溶液中磷酸盐浓度的变化如图6所示,从中可发现,反应后的磷酸盐浓度都有明显的减少,并且初始浓度越大的溶液,反应后磷酸盐浓度的减小程度越大.

图5 不同初始浓度的磷酸盐对土壤吸附MTA的影响
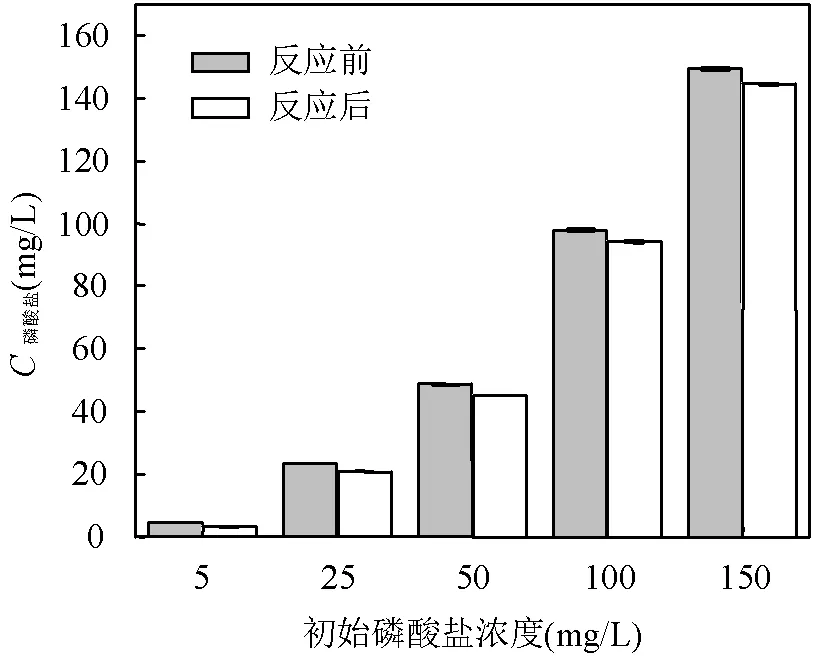
图6 反应前后溶液中磷酸盐浓度的变化
图5中MTA平衡吸附量随着磷酸盐初始浓度增大而减小的趋势,表明磷酸盐对土壤吸附MTA存在抑制作用,可能因为P和As是同族元素,P与As具有相似的物理化学性质和解离常数,两者共存溶液时会发生竞争吸附[22].溶液中的磷酸盐通常以含氧阴离子的形式存在,与砷在溶液中的存在形式一样,其在水溶液中的吸附行为与砷相似,会和砷竞争吸附位点从而抑制砷的吸附[36].再者,磷酸根离子拥有较强的置换能力,可将已存在于双电层的扩散层中的砷酸根和在水合氧化物表面或内层的砷酸根置换出来,从而增强了砷在地下水中的迁移能力,抑制了砷的吸附[37].
所以,土壤表面吸附位点数目一定的情况下,当MTA和磷酸盐在竞争土壤表面吸附点时,随着溶液中磷酸盐浓度越来越大,磷酸盐会占据土壤表面的吸附位点,并且已吸附在土壤表面的MTA也会被磷酸盐置换出来,使得磷酸盐在土壤上的吸附量增加,从而导致MTA在土壤上的吸附量降低.
2.4 土壤表征分析
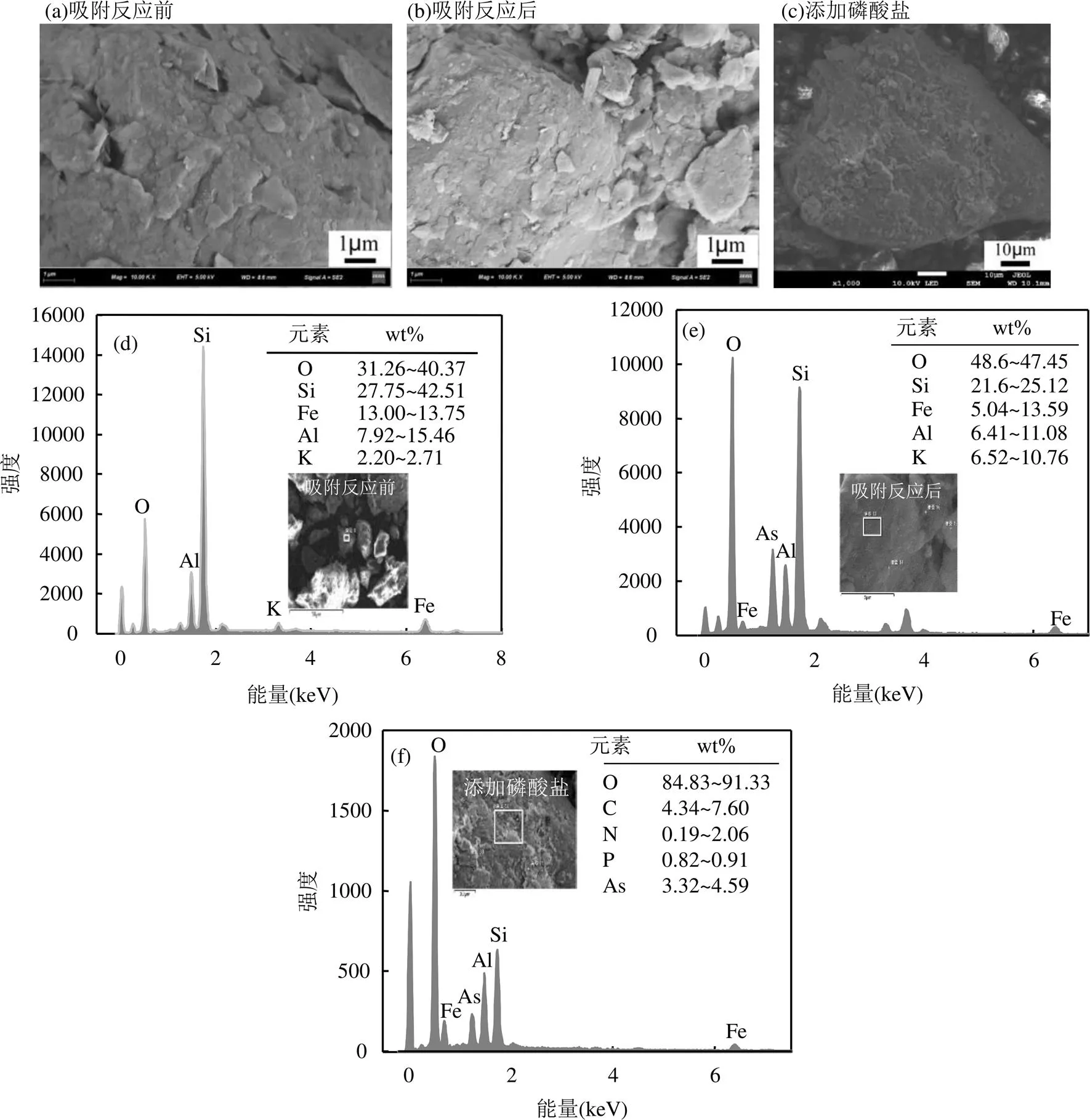
图7 土壤吸附MTA反应前后和添加磷酸盐的SEM-EDS图
2.4.1 土壤表面形貌特征 如图7所示,反应前,可看出土壤的表面由较完整的片状板结在一起;反应后,土壤的表面有一些变化,表面分布有很多细碎的小片,完整程度有所下降,分布较为破碎;添加磷酸盐后,土壤表面细碎的小片都变为破碎的颗粒,表面完整度下降很明显,表面分布极为破碎.
EDS元素半定量分析结果显示无论是否添加磷酸盐,反应后的土壤表面都检测到砷,且添加磷酸盐条件下土壤表面As的质量分数相对较小,证实了磷酸盐的存在降低了沉积物对MTA的吸附,而且磷酸盐添加后的土壤表面检测到P元素,说明磷酸盐可能附着在土壤表面或与土壤发生了反应.
2.4.2 土壤物相变化 土壤吸附MTA反应前、反应后和添加磷酸盐(5mg/L)的XRD谱图如图8所示,XRD图谱中,特征峰都出现在相同的位置,最明显的尖锐峰出现在2=26.62°处,分析得到其主要成分是石英和白云母,在主峰右侧的小峰分析其主要成分是钠长石.将吸附反应前谱图与吸附反应后和添加磷酸盐的谱图分别做对比,发现在土壤吸附MTA反应后和添加磷酸盐后的谱图上都出现Na3Al2(AsO4)3(PDF#51-0346)和Fe8As10O23(PDF#35 -0462)这两种含砷络合物,说明了MTA会和土壤中含铁铝的黏土矿物发生反应,生成的这些络合物会附着在土壤表面或填充土壤上的孔隙[23,38].

表5是空白组与实验组反应前后地下水溶液的参数,从表中可发现空白组中SO42-的浓度在反应前后基本没变化,而实验组中SO42反应后-的浓度较反应前的浓度增大了20.4%,说明MTA与土壤之间可能发生了反应,最终有SO42-生成.反应前后的地下水溶液用国标硫化物的测定-亚甲基蓝分光光度法进行了测试,发现反应前后的地下水溶液中无硫化物的存在.

表5 反应前后地下水溶液参数
注:空白组是土壤在地下水溶液中反应24h,实验组是土壤在MTA地下水模拟液中反应24h.
MTA是硫原子取代了砷酸盐中一个氧原子的产物,其在溶液中存在形式为HAsSO3-3.余倩等[11]提到As(Ⅲ)的去除机理是As(Ⅲ)会和沉积物中的铁锰矿物通过范德华力和化学键的作用占据沉积物表面的活性位点,Tiwari等[39]研究新型杂化材料修复被As(Ⅲ)和As(Ⅴ)污染的地下水的结果表明,As(Ⅴ)的去除机理是As(Ⅴ)会与γ-Al2O3发生络合反应,生成内球络合物,其反应过程如下描述:
Sericite-Al(OH)3+3H2AsO4-→Sericite-[Al(H2AsO4)3
+3OH-(7)
或
Sericite-[2Al(OH)3]+3HAsO42-→Sericite-
[Al2(HAsO4)3]+6OH-(8)
Xiao等[7]对硫代砷在水-矿物界面吸附研究的结论证明了硫代砷酸盐在氢氧化铝表面会形成双齿双核络合物,硫代砷酸盐与铁氧化矿物发生反应,表面会有雌黄沉淀或可能形成毒砂类物质.硫代砷酸盐在氢氧化铝表面的反应过程如下描述:
Al2(OH)2+H2AsO3S-→≡Al2O2AsO(OH)
+ SH-+H2(9)
≡Al2(OH)2+H2AsO3S-→≡Al2O2AsO(SH)
+OH-+H2(10)
因为反应后的溶液中SO42-的浓度只增大了20.4%,所以MTA在土壤上的吸附过程除了脱硫反应还可能存在另一种反应过程.结合前人有关砷酸盐和硫代砷的吸附机理研究,推测MTA会和土壤中的含铝矿物之间可能有两种反应过程:
第一种是主要反应,MTA和土壤中的含铝矿物发生反应,MTA在反应过程中脱硫成砷酸盐,接着砷酸盐和Al结合形成内球络合物,脱出的硫形成HS-易氧化成SO42-.反应过程如下描述:
-2Al(OH)3+9O2+6OH-+6H2AsO3S-→
-[2Al(H2AsO4)3]+6SO42-(11)
第二种可能会发生的反应就是Xiao等[7]提出的结论,MTA与土壤中的含铝矿物反应不脱硫直接生成铝砷络合物.反应过程如下描述:
≡Al2(OH)2+H2AsO3S-→≡Al2O2AsO(SH)
+OH-+H2(12)
物相表征中检测到的AlAs化合物应该是上述反应过程生成物中的含铝砷的络合物,而检测到的Fe8As10O23依据上述反应,推测应该是土壤中的含铁矿物与MTA发生反应的产物,可能会有如下的反应过程:
-2Fe(OH)3+9O2+6OH-+6H2AsO3S-→
-[2Fe(H2AsO4)3]+6SO42-(13)
所以,MTA在土壤上的吸附机理就是MTA与土壤中的铁铝矿物发生反应生成对应的铁砷、铝砷络合物吸附在土壤表面的活性位点上.
土壤吸附MTA反应后的XRD谱图与添加磷酸盐后的XRD谱图做对比,发现除了都有Na3Al2(AsO4)3和Fe8As10O23这两种含砷络合物,添加磷酸盐后的XRD谱图上还出现磷酸盐络合物C4H16N8O4Ca(H2PO4)2(PDF#48-1221).Hua[12]在改性膨润土去除砷的研究中提到磷酸盐会与吸附剂表面的羟基形成内球络合物和砷竞争吸附位点; Lindegren等[14]也提出磷酸盐会在针铁矿表面形成络合物从而与砷发生竞争吸附.
因为磷酸盐也是一种内球形络合离子,可以吸附在矿物表面,它会和土壤表面的羟基形成内球络合物[12],占据土壤表面的吸附位点,使得土壤上MTA可利用的活性位点减少.所以,当两种离子共存在时,磷酸盐会影响土壤吸附MTA,导致MTA在土壤上的吸附量减少.
3 结论
3.1 土壤吸附MTA的过程呈现出3个阶段:前期快速吸附和中期缓慢吸附,在7h最后达到吸附平衡.3个浓度MTA动力学拟合后所得平衡吸附量从小到大依次为8.636,41.968和230.857mg/kg.动力学模型拟合结果表明土壤对MTA的吸附发生在局部位置,两者之间存在相互作用,吸附过程主要受颗粒内扩散作用影响.Langmuir等温吸附模型对土壤吸附MTA这一过程拟合度更高,MTA在土壤上拟合所得最大单层吸附量为254.214mg/kg.
3.2 MTA与磷酸盐共存时,随着溶液中磷酸盐初始浓度的增大,土壤对MTA的平衡吸附量逐渐下降,对磷酸盐的吸附量逐渐增大.
3.3 土壤表面电镜图表明添加磷酸盐反应后的土壤,表面完整度会下降并且表面也会变的极为破碎; EDS元素半定量分析进一步证实磷酸盐的存在降低了沉积物对MTA的吸附.
3.4 XRD结果表明MTA能与土壤中的铁铝矿物发生络合反应生成紧密层络合物-[2Al(H2AsO4)3],≡Al2O2AsO(SH)和-[2Fe(H2AsO4)3],磷酸盐的存在会抑制土壤吸附MTA.
[1] 段艳华,甘义群,郭欣欣,等.江汉平原高砷地下水监测场水化学特征及砷富集影响因素分析 [J]. 地质科技情报,2014,33(2):140-147.
Duan Y,Gan Y,Guo X,et al. Hydrogeochemistry and arsenic contamination of groundwater in the monitoring field,Jianghan Plain [J]. Bulletin of Geological Science and Technology,2014,33(2):140-147.
[2] 郭华明,郭 琦,贾永锋,等.中国不同区域高砷地下水化学特征及形成过程 [J]. 地球科学与环境学报,2013,35(3):83-96.
Guo H,Guo Q,Jiq Y,et al. Chemical characteristics and geochemical process of high arsenic groundwater in different regions of China [J]. Journal of Earth Sciences and Environment,2013,35(3):83-96.
[3] 何 薪,马 腾,王焰新,等.内蒙古河套平原高砷地下水赋存环境特征 [J]. 中国地质,2010,37(3):781-788.
He X,Ma T,Wang Y,et al. Geochemical characteristics of the As-bearing aquifer in the Hetao Plain,Inner Mongolia [J]. Geology in China,2010,37(3):781-788.
[4] 张昌延,何江涛,张小文,等.珠江三角洲高砷地下水赋存环境特征及成因分析 [J]. 环境科学,2018,39(8):3631-3639.
Zhang C,He J,Zhang X,et al. Geochemical characteristics and genesis analyses of high-arsenic groundwater in the Pearl River Delta [J]. Environmental Sience,2018,39(8):3631-3639.
[5] 刘秋龙,杨 昱,夏 甫,等.地下水中阴离子对球磨零价铁除砷影响 [J]. 中国环境科学,2019,39(5):2028-2033.
Liu Q,Yang Y,Xia F,et al. Impact of groundwater anions on the arsenic remove by milling zero valent iron [J]. China Environmental Science,2019,39(5):2028-2033.
[6] Sun S,Xie X,Li J,et al. Distribution and formation of thioarsenate in high arsenic groundwater from the Datong Basin,northern China [J]. Journal of Hydrology,2020,590(2):125-268.
[7] Xiao F,Wang S,Xu L,et al. Adsorption of monothioarsenate on amorphous aluminum hydroxide under anaerobic conditions [J]. Chemical Geology,2015,407:46-53.
[8] Wang Y,Lin J,Wang S,et al. Adsorption and transformation of thioarsenite at hematite/water interface under anaerobic condition in the presence of sulfide [J]. Chemosphere,2019,222:422-430.
[9] 严克涛,郭清海.地下水环境中的硫代砷研究进展 [J]. 水文地质工程地质,2019,46(6):132-141.
Yan K,Quo Q. Advances in thioarsenic in groundwater systems [J]. Hydrogeology & Engineering Geology,2019,46(6):132-141.
[10] O'reilly S,Strawn D,Sparks D. Residence time effects on arsenate adsorption/desorption mechanisms on goethite [J]. Soil Science Society of America Journal,2001,65(1):67-77.
[11] 余 倩,张 宇,邬建勋,等.江汉平原沉积物中磷酸盐与砷的竞争吸附机制 [J]. 中南民族大学学报(自然科学版),2020,39(4):337-342.
Yu Q,Zhang Y,Wu J,et al. Competitive adsorption mechanism of phosphate and arsenic in sediments from Jianghan Plain [J]. Journal of South-Sentral Minzu University (Natural Science Editon),2020,39(4):337-342.
[12] Hua J. Adsorption of low-concentration arsenic from water by co-modified bentonite with manganese oxides and poly (dimethyldiallylammonium chloride) [J]. Journal of Environmental Chemical Engineering,2018,6(1):156-168.
[13] Kubicki J,Kabengi N,Chrysochoou M,et al. Density functional theory modeling of chromate adsorption onto ferrihydrite nanoparticles [J]. Geochemical Transactions,2018,19:12.
[14] Lindegren M,Persson P. Competitive adsorption involving phosphate and benzenecarboxylic acids on goethite-Effects of molecular structures [J]. Journal of Colloid and Interface Science,2010,343(1):263-270.
[15] Besold J,Biswas A,Suess E,et al. Monothioarsenate transformation kinetics determining arsenic sequestration by sulfhydryl groups of peat [J]. Environmental Science & Technology,2018,52(13):7317- 7326.
[16] Planer-Friedrich B,Schaller J,Wismeth F,et al. Monothioarsenate occurrence in bangladesh groundwater and its removal by ferrous and zero-valent iron technologies [J]. Environmental Science & Technology,2018,52(10):5931-5939.
[17] Suess E,Wallschlaeger D,Planer-Friedrich B. Stabilization of thioarsenates in iron-rich waters [J]. Chemosphere,2011,83(11):1524-1531.
[18] Planer-Friedrich B,London J,Mccleskey R,et al. Thioarsenates in geothermal waters of yellowstone national park: Determination,preservation,and geochemical importance [J]. Environmental Science & Technology,2007,41(15):5245-5251.
[19] Stauder S,Raue B,Sacher F. Thioarsenates in sulfidic waters [J]. Environmental Science & Technology,2005,39(16):5933-5939.
[20] Wang J,Halder D,Wegner L,et al. Redox dependence of thioarsenate occurrence in paddy soils and the rice rhizosphere [J]. Environmental Science & Technology,2020,54(7):3940-3950.
[21] Couture R,Rose J,Kumar N,et al. Sorption of arsenite,arsenate,and thioarsenates to iron oxides and iron sulfides: A kinetic and spectroscopic investigation [J]. Environmental Science & Technology,2013,47(11):5652-5659.
[22] 廖丹雪,单慧媚,张进贤,等.一硫代砷在针铁矿上的吸附及影响因素 [J]. 环境科学,2020,41(7):3337-3344.
Liao D,Shan H,Zhang J,et al. Characteristics and influencing factors of monothioarsenate adsorption on goethite [J]. Environmental Sience,环境科学,2020,41(7):3337-3344.
[23] 李红梅,邓娅敏,罗莉威,等.江汉平原高砷含水层沉积物地球化学特征 [J]. 地质科技情报,2015,34(3):178-184.
Li H,Deng Y,Luo L,et al. Geochemistry of high arsenic shallow aquifers sediment of the Jianghan Plain [J]. Bulletin of Geological Science and Technology,2015,34(3):178-184.
[24] 廖丹雪,单慧媚,彭三曦,等.一硫代砷酸盐在介质上的吸附特征及机制 [J]. 环境科学,2020,41(1):284-292.
Liao D,Shan H,Peng S,et al. Characteristics and mechanism of monothioarsenate adsorption on sand,sediment and goethite [J]. Environmental Sience,2020,41(1):284-292.
[25] 王敏黛,郭清海,郭 伟,等.硫代砷化物的合成、鉴定和定量分析方法研究 [J]. 分析化学,2016,44(11):1715-1720.
Wang M,Guo Q,Guo W,et al. Synthesis identification and quantitative analysis of aqueous thioarsenates [J]. Chinese Journal of Analytical Chemistry,2016,44(11):1715-1720.
[26] Shan H,Liao,D,Zhan,H,et al. Development of LC-HGAFS method for direct measurement of monothioarsenate and application for its adsorption characteristics [J]. Applied Geochemistry,2020,122.
[27] 廖丹雪.一硫代砷酸盐的吸附特征及其影响因素的实验研究 [D]. 桂林理工大学,2020.
Liao D. Experimental Study on Adsorption Characteristics and Influencing Factors of Arsenate Monothioarsenate. [D]. Guilin Unvironmental of Technology,2020.
[28] 陈 辉,单慧媚,彭三曦,等.不同水化学因素对砷在河砂上的吸附影响研究 [J]. 环境科学学报,2021,41(7):2727-2739.
Chen H,Shan H,Peng S,et al. Hydrochemical Influences on Arsenic Adsorption by River Sand [J]. Acta Scientiae Circumstantiae,2021,41(7):2727-2739.
[29] Dalal R. Desorption of soil phosphate by anion〆xchange resin [J]. Communications in Soil Science & Plant Analysis,1974,5(6):531-538.
[30] Hannon J,Kerry J,Cruz-Romero M,et al. Kinetic desorption models for the release of nanosilver from an experimental nanosilver coating on polystyrene food packaging [J]. Innovative Food Science & Emerging Technologies,2017,44:149-158.
[31] Low M.. Kinetics of Chemisorption of Gases on Solids [J]. Chemical Reviews,1960,60(3):267-312.
[32] Mckay Y. Pseudo-second order model for sorption processes [J]. Process Biochemistry,1999,34(5):451-465.
[33] Weber W,Morris J. Kinetics of adsorption on carbon from solution [J]. Asce Sanitary Engineering Division Journal,1963,1(2):1-2.
[34] Shan H,Zhang J,Peng S,et al. Sorption of Monothioarsenate to the Natural Sediments and Its Competition with Arsenite and Arsenate [J]. International Journal of Environmental Research and Public Health,2021,18(23):128-139.
[35] 吴昆明,郭华明,魏朝俊.改性磁铁矿对水体中砷的吸附特性研究 [J]. 岩矿测试,2017,36(6):624-632.
Wu K,Guo H,Wei C. et al. Adsorption Characteristics of Arsenic in Water by Modified Magnetite [J]. Rock and Mineral Analysis,2017,36(6):624-632.
[36] Jain A,Loeppert R. Effect of competing anions on the adsorption of arsenate and arsenite by ferrihydrite [J]. Journal of Environmental Quality,2000,29(5):1422-1430.
[37] 邹 强,刘 芳,杨剑虹.紫色土中砷、磷的吸附-解吸和竞争吸附 [J]. 应用生态学报,2009,20(6):1383-1389.
Zou Q,Liu F,Yang J. Adsorption-desorption and Competitive of Arsenic and Phosphorus in Purple Soil [J]. Chinese Journal of Applied Ecology,2009,20(6):1383-1389.
[38] 黄爽兵,Even E,王焰新.高砷含水层沉积物矿物学特征及砷的活化 [J]. 矿物岩石,2012,32(4):7-11.
Huang S,Even E,Wang Y. Mineralogical Characteristics of Senmimenta and Arsenic Mobilization in the Aquifer,Jianghan Plain [J]. Mineralogy and Petrology,2012,32(4):7-11.
[39] Tiwari D,Lee,S M. Novel hybrid materials in the remediation of ground waters contaminated with As(III) and As(V) [J]. Chemical Engineering Journal,2012,204:23-31.
致谢:本文英文摘要和图表英文标题得到美国得克萨斯农工大学詹红兵教授的指导和帮助,在此表示衷心的感谢!
Effect of phosphate on monothiosarsenate adsorption to soil.
ZHANG Jin-xian1,SHAN Hui-mei1*,LIAO Dan-xue2,PENG San-xi3,DU Hai-ling1,LIU Yun-quan1,SHI Qian1
(1.Guangxi Key Laboratory of Environmental Pollution Control Theory and Technology,Collaborative Innovation Center for Water Pollution Control and Water Security in Karst Areas,Guilin University of Technology,Guilin 541004,China;2.College of Ecological and Environmental Protection,Guangxi Ecological Engineering Vocational and Technical College,Liuzhou 545003,China;3.College of Earth Sciences,Guilin University of Technology,Guilin 541004,China).,2022,42(8):3849~3857
In this study,batch experiments and characterization analysis were conducted to explore the characteristics and mechanism of MTA adsorption on soil by adding different concentrations of phosphate. Results showed that: the Elovich kinetic model and Langmuir isothermal adsorption model can better fit the adsorption process of MTA on soil,indicating that the adsorption process of MTA was mainly affected by the diffusion of pore size. The maximum adsorption capacity of MTA on soil was 254.214mg/kg. With the increase of the initial concentrations of adding phosphate in the solution,the equilibrium adsorption capacity of MTA on soil gradually decreases,and that of phosphate gradually increases. SEM-EDS results showed that a small amount of As was detected on the surface of soil whether adding phosphate or not. In the system with phosphate addition,the soil showed a relatively low content of As,confirming that the presence of phosphate can reduce the adsorption of MTA on soil. In addition,XRD results showed that MTA can form endosphere complexes of -[2Al(H2AsO4)3],≡Al2O2AsO(SH) and -[2Fe(H2AsO4)3] with Fe-Al minerals in soil samples,and phosphate can form endosphere complexes with hydroxyl groups on the surface of soil,weakening the adsorption of MTA.
monothiosarsenate;soil;adsorption;phosphate
X53
A
1000-6923(2022)08-3849-09
2021-12-23
国家自然科学基金资助项目(41877194,42062015,42167026),广西自然科学基金资助项目(桂科AD19110024,桂科AD19110062)
* 责任作者,副教授,shanhuimei@glut.edu.cn
张进贤(1997-),男,甘肃白银人,桂林理工大学硕士研究生,研究方向为地下水污染.发表论文4篇.

