Hofmeister效应对表面活性剂聚集行为影响研究进展
陈泽玉 孙立杰 刘畅瑶* 王 策 徐宝财
北京工商大学轻工科学技术学院,北京,100048

Hofmeister效应是一种无法被经典电解质理论所解释的特殊规律,于1888年由德国科学家Franz Hofmeister在蛋白质体系内发现,广泛存在于生物、化学系统,主要被用来研究盐对蛋白质的沉淀效率,人们据此提出了最经典的Hofmeister序列:N(CH3)4+>NH4+>Cs+>Rb+>Na+>Li+>Ca2+>Mg2+>Zn2+>Ba2+(阳离子);(阴离子)。Hofmeister效应的研究就围绕这个序列展开。Hofmeister序列存在随表面活性剂体系环境变化而发生改变的可能性,例如,个别离子出现顺序变换、哑铃型序列,甚至是顺序反转的现象等,具体序列取决于离子在体系中参与的相互作用类型,如溶菌酶溶液处于低pH值条件下时,由于阴离子与蛋白质表面带有正电荷的弱水化氨基之间的静电作用占主导地位,弱水化的结构破坏型离子(Chaotrope)与之相互作用强,导致盐化效应;强水化结构构造型离子(Kosmotrope)与之相互作用较弱,导致经典的Hofmeister序列发生反转[1-2]。最初,Hofmeister序列被提出用来预测盐对蛋白质的影响,但后来,它被外推到胶体体系,如含有表面活性剂的体系[3]。
表面活性剂是一种重要的工业助剂,在水中能自发地形成各种聚集体,添加盐可以简单、高效地改变其聚集形态,临界胶束浓度(CMC)和泡沫性能是表面活性剂的重要参数。在水溶液中,表面活性剂浓度达到CMC时形成球形胶束聚集体,在更高浓度下实现球形胶束到棒状胶束的转变。据报道[4],体系中添加盐能够诱导表面活性剂从胶束到囊泡的转变,主要与体系中的反离子类型、反离子的浓度、链长和头基结构有关。在表面活性剂和界面科学中,涉及盐的许多现象都表现出明显的Hofmeister效应,根据Nan Jiang等的研究成果,反离子对各种表面活性剂的胶束化和聚集都有显著的影响,通过向表面活性剂水溶液中加入无机盐,可以降低带电头基之间的静电排斥[5]。这有利于胶束聚集,从而导致CMC减小、胶束尺寸增大及从球形到蠕虫状胶束的转变。这个转变在一定盐浓度范围内有利于增加表面活性剂的黏弹性强度,明显改善压裂液的黏弹力性能,还能高效地减少原油/水界面表面张力,进一步提高采收率[6-7]。不同的反离子头基同样会对表面活性剂稳定的泡沫系统性能产生影响。泡沫由于受plateau排液的影响,属于不稳定热力学系统,加入表面活性剂能降低表面张力,增加泡沫膜间电荷斥力,使plateau排液效果减小,增加泡沫系统的稳定性。
因此,研究反离子头基与表面活性剂的聚集体的相行为及其泡沫性质之间的关系,即Hofmeister效应,对发展表面活性剂在应用领域的作用有重要影响。从现有的文献看,尽管这种效应已经被广泛研究,但背后的机制仍然存在疑问。本文通过综述不同种类的无机盐与有机盐对不同表面活性剂体系的聚集性能和泡沫性能的影响,以期能对研究表面活性剂的离子特异性效应有帮助。
1 阳离子表面活性剂体系
表面活性剂具有独特的“双亲”结构,在溶液中能够形成各种各样的聚集体,如胶束、囊泡、乳液、液晶相等[8]。根据表面活性剂的极性基团在水中能否电离,可以分为离子型表面活性剂和非离子表面活性剂,离子表面活性剂包括阴离子表面活性剂、阳离子表面活性剂和两性表面活性剂[9]。离子表面活性剂体系的Hofmeister效应主要体现在带有与表面活性剂亲水头基相反电荷的反离子对其各种性质的影响作用。
在水溶液中浓度较低时,表面活性剂以单分子形式存在,随着浓度增加,受极性基团静电斥力和非极性基团疏水作用的影响,表面活性剂将亲水端伸向溶液,疏水端伸向空气,溶液体系能量降低,逐渐形成胶束聚集体。电解质无机盐的加入通过提供反离子,使带电头基的静电斥力降低,改变体系中分子间相互作用力,促进胶束聚集,从而减少每个表面活性剂头基的有效面积,使表面活性剂CMC降低或胶束聚集数增加,并诱导球形胶束向非球形胶束转变,这一点与许多研究的实验结果相符[10-11]。除了无机盐,表面活性剂与有机盐之间的关系也被许多学者探索。Hui Ding等[12]研究了GCCl、GC-N和GC-S(式1)三种具有不同反离子的Gemini季铵盐,测得各自不同浓度的表面张力曲线(图1)。在低浓度时,溶液表面张力成线性下降,浓度逐渐增大,表面张力曲线出现“拐点”,后续溶液的表面张力几乎不改变,这个“拐点”所对应的浓度就是表面活性剂的CMC。
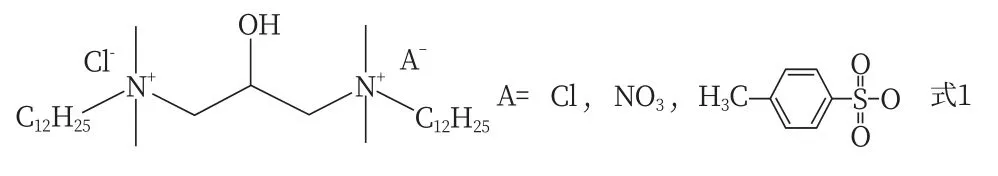
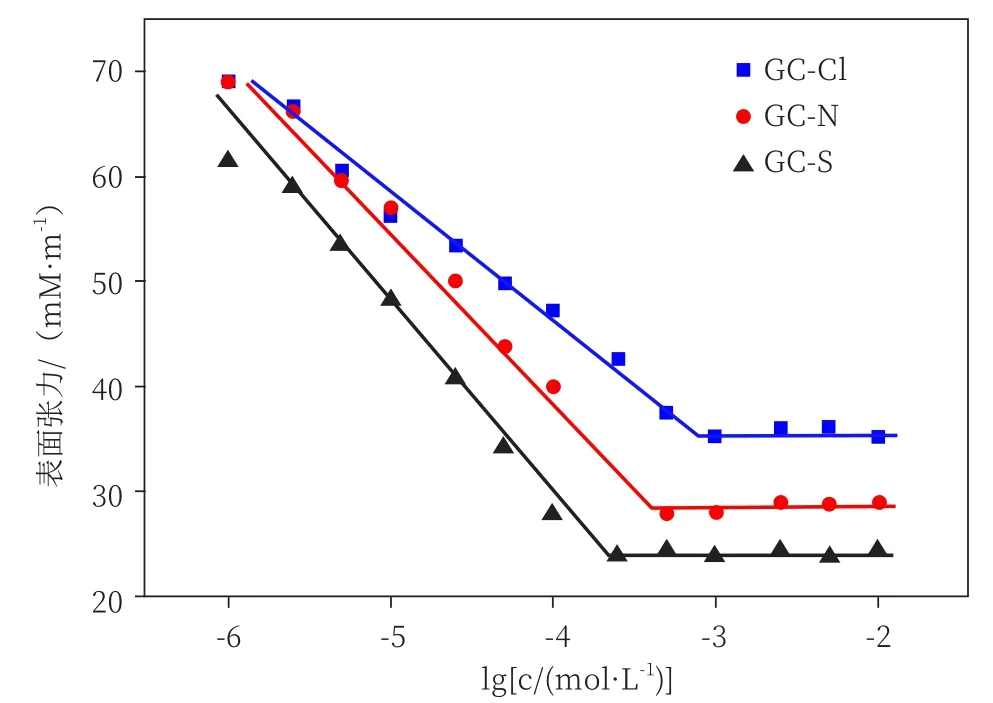
图1 在323 K下,GC—Cl、GC—N和GC—S的表面张力与表面活性剂浓度的对数图[12]
显然,形成胶束的难度:无机盐>有机盐,有机盐反离子对此类Gemini季铵盐表面活性剂胶束聚集的影响较大,促进作用最明显,用透射电镜(TEM)观察在三种表面活性剂CMC附近的结构转变(图2),可以发现GC-Cl和GC-N聚集形成球形胶束,其中GC-N形成的胶束半径较小,而GC-S聚集形成蠕虫状胶束。可能的原因是GC-S的反离子是有机反离子,结构中含有苯环,疏水作用强,导致胶束容易从球状转变为蠕虫状、棒状等非球状。这与Defeng Yu等[13]研究结论相似,他们通过测定C6H5COONa、p-C6H4(COONa)2、Na2SO4、NaCl四种盐分别对12-4-12 [四亚甲基-1,4-双(十二烷基二甲基溴化铵)]和12-4(OH)2-12[四亚甲基-2,3-二羟基-1,4-双(十二烷基二甲基溴化铵)]两种Gemini表面活性剂聚集行为的影响,发现四种盐都能降低表面活性剂的临界胶束浓度,但只有C6H5COONa可以同时降低其CMC和表面张力,并将12-4(OH)2-12从囊泡-胶束共存状态转化为囊泡,因此认为有机盐更能促进胶束聚集。此外,Mohd Akram等[14]的研究也发现,有机盐对表面活性剂聚集性能的影响比无机盐要大,通过实验,他们发现盐影响临界胶束浓度的效果为:NaAn>NaTos>Na3PO4>Na2SO4>NaCl。利用稳态荧光技术估计胶束中的单体聚集数(Nagg)及其盐组合,发现添加盐后胶束聚集数增加且有机盐反离子表面活性剂的聚集率也比无机盐的要高,影响聚集数的效果与影响CMC的效果顺序相同。

图2 CMC附近表面活性剂的透射电镜图[12]A.GC—Cl; B.GC—N; C.GC—S。
Mohd Akram等[14]还发现,盐的浓度同样会影响表面活性剂的聚集行为。由图3可知,Gemini表面活性剂12-E2-12(式2)聚集数(Nagg)随着盐浓度增加而增加。盐的加入会促进胶束的形成和生长,随着盐浓度的增加,表面活性剂CMC降低[15]。这个结论与Sabreena Yousuf等[16]得到的一样(图4),从图中不难看出,不管是有机盐还是无机盐,阳离子表面活性剂的CMC大都随着盐浓度的增加而降低,但降低趋势有所不同。
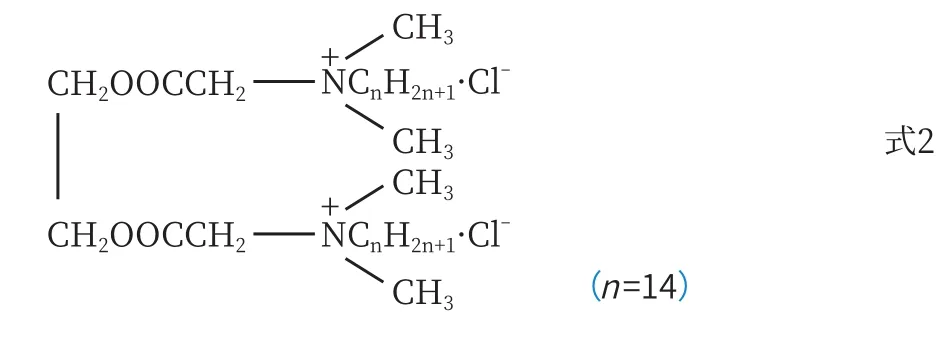

图3 Gemini表面活性剂12—E2—12(0.1 mM)聚集数(Nagg)的变化[14]
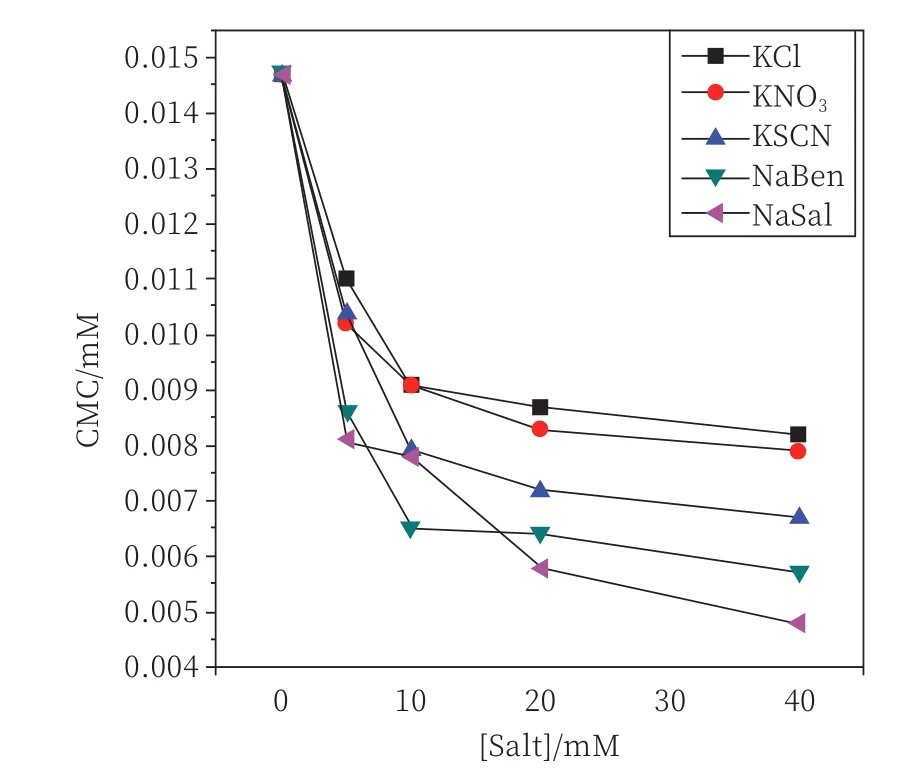
图4 Gemini表面活性剂14—E2—14的CMC随不同盐浓度的变化[16]
有机盐对CMC影响较大的原因可能是反离子中带有非极性结构,同时发挥了静电屏蔽作用和疏水作用,而无机盐只对表面活性剂头基产生静电屏蔽作用,反离子的疏水碳链越长,表面活性剂越容易聚集形成胶团,并实现球形胶束-非球形胶束-囊泡的转变[7,17]。这一点被Kajari Maiti等[18]的研究所证实。他们研究了大量盐对季铵盐阳离子胶束聚集的影响,结果表明,TTAB(十四烷基三甲基溴化铵)能够在有机盐的影响下形成长线状或虫状胶束。然而,表面活性剂的胶束化并不完全依赖于反离子的某一性质,反离子的疏水性是其中一个重要因素,但不能单独解释对胶束变化的影响。Sabine Manet等[19]研究了各种不同类型的阴离子对阳离子Gemini表面活性剂胶束聚集的影响,发现当胶束是球形的时候,胶束聚集数就与离子的性质无关。他们认为反离子没有单一的性质与CMC有关,但这些性质的参数共同决定了表面活性剂头基与反离子的形成离子对倾向,特别是反离子的水化作用,从而引起CMC的变化。
2 阴离子表面活性剂体系
在Hofmeister阳离子序列中,以Na+为分界线,左侧的阴离子水合能力强,被称为结构构造型离子,倾向于稳定蛋白质的天然折叠结构,导致盐析行为;右侧的离子水合程度差,被称为结构破坏型离子,破坏蛋白质结构,导致其变性或展开,表现出盐溶行为;Na+是两种不同离子之间的边界,对蛋白质的稳定性没有明显影响。
目前,研究Hofmeister效应的理论模型主要有水化匹配模型、极化模型等,这些理论模型各有优劣,但都未对Hofmeister效应的机制做出全面解释。水化匹配模型是Collins在2004年提出的一个简单而普遍的模型,假设离子为球形,电荷是点电荷且存在于离子中心,那么离子半径越大的离子,表面电荷密度越小,水合能力越弱,反之,则水化能力越强[4]。在水化匹配模型中,Collins认为,拥有相近水合能力的阴离子和阳离子的结合能力越强,即拥有较强水合能力的“硬”离子与带电相反的“硬”离子结合,它们之间的相互作用能力较强,若“硬”离子与水合能力较弱的“软”离子结合,则相互作用力弱。阴离子和阳离子结合成离子对时,两者需要同时发生部分去水化,这对于亲水能力相同的离子来说更容易实现。Nina Vlachy等[20]通过研究盐对阴离子型表面活性剂胶束到囊泡转变的影响,由水化匹配模型认为阴离子表面活性剂的CMC与表面活性剂头基与反离子形成稳定离子对的能力有关。
大量研究结果表明,离子水合半径越小,越能降低带电头基团之间的静电排斥,使离子与表面活性剂带电头基的作用力更强[22],形成的离子对越稳定。Li-Sheng Hao等[21]用表面张力法等方法测定了十二烷基磺酸盐分别在K+、Na+、Rb+条件下的临界胶束浓度,几种盐影响胶束聚集的效果从大到小:铷盐>钾盐>钠盐,与Hofmeister序列一致(图5),与Anna Jakubowsk[23]的研究结果一样。因此可以认为无机盐对表面活性剂聚集行为的影响与反离子水合半径有关:反离子半径越小,带电头基之间静电斥力越小,有利于表面活性剂形成聚集体。Collins水化匹配模型可以很好地解释这种现象:“软”的十二烷基磺酸根头基应该与“软”的铷离子头基结合,两者间作用力才更强,促进表面活性剂的胶束化[24]。
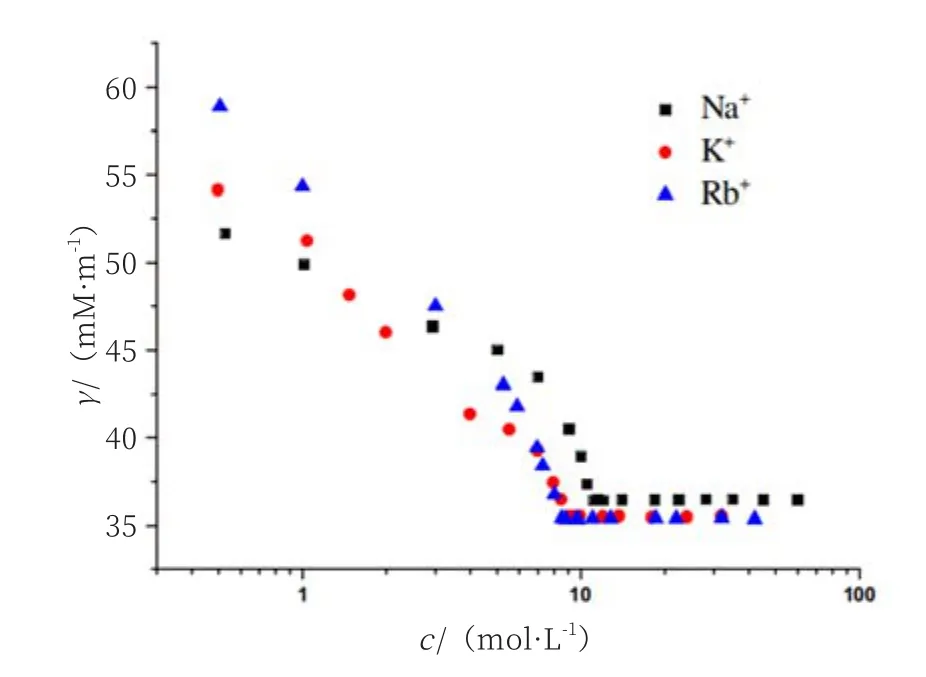
图5 Y+As-表面张力与浓度在318.15K的关系[21]
然而,水化匹配模型忽视了分子中的其他作用力,当分子间的相互作用影响更大时,可能出现与水化匹配模型相反的结果[1]。Hofmeister效应的经典理论—水化理论认为,根据离子与水分子之间的作用,无机盐按黏度系数,可以分成Kosmotrope和Chaotrope。最初Kosmotrope和Chaotrope被认为与离子半径和水合能力有关,水合能力强的离子即Kosmotrope型离子可以增强水的氢键作用,但后来光谱学的一些实验证明离子只能影响其第一层水化层内的氢键结构和动力学特征[4]。近来通过太赫兹(THz)等光谱技术证实,离子不但只会影响第一层水化层内的氢键结构,还会影响水的整体的氢键结构[25-26]。
研究表面活性剂的聚集行为并非易事,电导法分析和前文提到的荧光稳态分析是目前常用的方法,除此之外还有化学捕集法(CT)。化学捕集法是基于假设有序结构的表面区域和参比溶液中的脱重氮基反应的选择性相同时,利用一长一短两个探针16-ArN2+和1-ArN2+测定有序结构的界面区域和反应与头基模型对于水的选择性,从而计算出弱碱性阴离子和中性亲核试剂(包括水)与胶体的界面浓度信息,得到胶束表面反离子与头基的相互作用规律,从分子水平解释了体系中的离子特异性效应[27]。Changyao Liu等[28]通过化学捕集法提出了一个特异性离子对/水合模型,认为离子特异性效应胶束到囊泡的转变需要进行界面脱水,形成的离子对比单独的离子和头基团更小,水合度更少,从而影响填充参数和水结构。此外研究还发现,盐诱导的胶束到囊泡的转变对阳离子表现出明显的离子特异性,但对阴离子不敏感,与Mohmad Shafifi Sheikh等[10]得到的结论一样。因此一些金属阳离子,如银离子、铜离子等,对促进表面活性剂从胶束到囊泡的变化有显著影响也就不难理解了[29]。
溶液体系中的盐除了能改变离子表面活性剂的聚集状态,促进聚集,还对表面活性剂的泡沫性能有影响。孙立杰等[30]用泡沫扫描分析仪测定了具有不同反离子的两种表面活性剂的泡沫性能,并对比了在无机盐、有机盐条件下引发的Hofmeister效应对表面活性剂泡沫性能的影响(图6)。四种有机盐分别为四甲基溴化铵(TMAB)、四乙基溴化铵(TEAB)、四丙基溴化铵(TPAB)和四丁基溴化铵(TBAB)。结果表明,同一种反离子对不同表面活性剂起泡性影响不同,可能是因为两种表面活性剂在水化匹配模型中的“软”“硬”程度的差别;该文章同时也指出了这几种盐对于稳泡性的影响极小,可能是因为表面活性剂在泡沫膜表面吸附足够快,表面平衡较快,形成胶束迅速,能够快速阻碍气体扩散,增加泡沫排液的难度,从而提高稳泡性,与Hofmeister序列有关;添加盐对表面活性剂稳泡性有双重影响,可以用Collins理论解释。Soumyadip Sett等[31]认为反离子既可以稳定泡沫膜,也可以使其不稳定,两者间有一个临界浓度,超过这个临界浓度,反离子对泡沫有消除作用。反离子使表面活性剂泡沫不稳定的顺序与Hofmeister序列相同,稳定的顺序则相反。
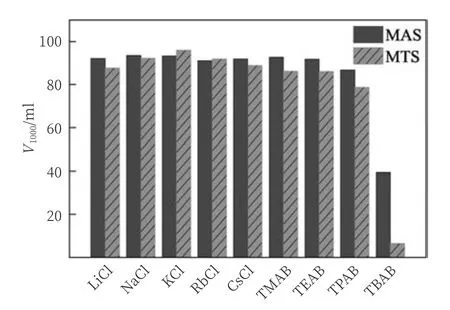
图6 MAS(肉豆蔻酰基 β—丙氨酸钠)、MTS(肉豆蔻酰基牛磺酸钠)加盐体系泡沫稳定性对比图[30]
3 非离子表面活性剂体系和混合体系
从现有文献看,关于非离子表面活性剂Hofmeister效应的研究不多,表面活性剂Hofmeister效应研究主要还是集中于离子表面活性剂。Irene Russo Krauss等[32]报道,Hofmeister效应几乎不影响非离子表面活性剂体系的聚集状态,任何盐存在时CMC都略低于水中的CMC,Hofmeister效应对于形成小胶束和高水合胶束的短链表面活性剂会增强。这可能是因为对于非离子表面活性剂而言,盐的添加主要是改变了溶剂的性质,使溶剂对疏水基团产生盐析或盐溶作用,从而改变非离子表面活性剂的CMC和浊点,进而改变其聚集状态,而不是作用于表面活性剂亲水基头部[33]。不同盐对非离子表面活性剂泡沫稳定性的影响不同,有些盐促进泡沫稳定而有些盐作用不明显,还有一些盐,主要是阴离子,则表现为明显的消泡效果,确切的规律仍未被掌握。这是因为非离子表面活性剂不带电,盐对非离子表面活性剂的影响不像对离子表面活性剂的影响那样简单。
具有盐析作用的盐即Kosmotrope离子,能够降低非离子表面活性剂的CMC和浊点,盐溶效应的盐即Chaotrope离子则作用相反,且离子水合半径越大,影响越强。因为半径大的离子很容易松散水化并结合胶束聚集物,相反,半径小的离子一般不表现出与胶束的特异性结合效应,并将其水化作用保持到胶束界面[34-35]。
虽然离子特异性效应在非离子表面活性剂表现不明显,但Irene Russo Krauss等发现,在非离子表面活性剂与阳离子表面活性剂混合体系中,盐对混合体系的聚集状态存在一定影响,如图7,他们通过对比不添加盐DATB-C8E5(十二烷基三甲基溴化铵-五乙基乙二醇单辛基醚)混合体系CMC值随DTAB摩尔分数αDTAB的变化关系和添加恒定0.4 mol·kg-1浓度不同盐CMC值随DTAB摩尔分数αDTAB的变化关系,可以观察到纯水中体系CMC值的增加与DTAB的摩尔分数有关,盐的加入使得反离子作用于DTAB的带电头基,降低表面活性剂电荷排斥作用,促进聚集。DATB-C8E5体系在添加盐后,CMC值随着αDTAB升高而降低,几种盐对这种趋势的影响程度:NaSCN>NaBr>NaCl,与Hofmeister序列有关。同时,通过动态光散射(DLS)观察DTAB-C8E5聚集体的水力半径(图8),发现在添加NaSCN时,水力半径随αDTAB增大而增大,且胶束的形态从球形变为棒状。这可能是因为SCN-具有较大极化率,增强了反离子在胶束表面的结合,通过胶束大小的增加和从球形到棒状的转变,有效地屏蔽了表面活性剂头基团之间的静电斥力。
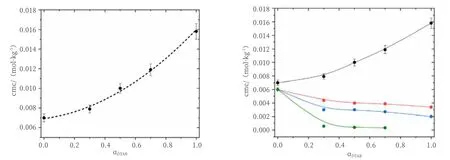
图7 水中DTAB—C8E5混合物的CMC值与DTAB摩尔分数αDTAB的关系(左);DTAB—C8E5混合物中在水(黑色)和NaCl(红色)、NaBr(蓝色)和NaSCN(绿色)条件下CMC值与DTAB摩尔分数αDTAB的关系(右)[32]

图8 由DLS确定的DTAB—C8E5聚集体的水力半径,在水中(黑色)和在NaCl(红色)、NaBr(蓝色)和NaSCN(绿色)的存在下与DTAB摩尔分数αDTAB的关系[32]
在表面活性剂实际应用过程中,其往往不以单一种类存在,而常与其他类型表面活性剂复配使用,并体现出较强的协同性。有研究认为,由于阴离子表面活性剂和阳离子表面活性剂头基之间电荷吸引作用,两者等摩尔比例混合物具有较大的协同效应,能够诱导复配体系胶束-囊泡的转变[36-37],并且受盐浓度的影响[38]。
4 总结和展望
表面活性剂的许多性质的研究离不开盐,Hofmeister效应对研究表面活性剂体系的聚集行为和泡沫性能有影响。从现有文献看,表面活性剂的Hofmeister效应研究主要以季铵盐阳离子表面活性剂、Gemini表面活性剂、表面活性剂复配体系为研究对象。对于离子表面活性剂体系而言,无机盐的加入主要是降低表面活性剂带电头基之间的电荷斥力,从而促进聚集,促进的效果与Hofmeister序列有关;有机盐的加入则是同时降低表面活性剂的静电斥力和疏水作用,使CMC值降低,有机盐的疏水链越长,对CMC降低的程度则越大。非离子表面活性剂的聚集行为几乎不受盐的影响,而表面活性剂复配体系同离子表面活性剂体系一样,易受到反离子的影响,且影响程度与Hofmeister序列有关,有研究认为,混合体系在盐的作用下能够自发地进行胶束到囊泡的聚集体转变。Hofmeister效应同样对泡沫的稳定性有影响,在离子表面活性剂体系中,反离子是作用在泡沫膜上,通过电荷相互作用,延长泡沫寿命或促进消泡;而非离子体系和混合体系中,盐对泡沫的影响规律仍未被发现,这对往后表面活性剂Hofmeister效应的研究将是一个挑战。
今后对表面活性剂Hofmeister效应的研究,首先是围绕一些经典理论和模型不能解决的问题,对理论进行补充,建立一个反离子性质参数集合与表面活性剂聚集性能关系的模型。其次,实际中表面活性剂总是复配使用,因此复配体系的Hofmeister效应研究也值得进一步研究,这对实现表面活性剂的应用功能具有重要意义。除此之外,在非离子表面活性剂方面,盐对其聚集行为和泡沫性能的影响都还存在研究空白,特别是关于泡沫性能的研究。总之,如何有效地通过Hofmeister效应实现表面活性剂聚集行为和泡沫性能的改变将是今后一段时间的重点问题。

