两类表面活性剂中间体的合成及表征
蔡永晨 许虎君
1.滁州学院科技处,安徽滁州,239000;2.江南大学化学与材料工程学院,江苏无锡,214122

表面活性剂是一类具有亲水头基和疏水尾链的特殊两亲体,它活跃于表(界)面,在较低浓度时,便具有显著降低表(界)面张力的能力,从而改变表(界)面状态。表面活性剂特殊的表(界)面化学性能使其在日化产品的合成[1-2]、新材料的制备[3]、三次采油[4]等领域具有广阔的应用前景。
两性表面活性剂作为表面活性剂中不可或缺的一类,虽然其研究开发时间较晚,但因其特殊的结构,使其兼具阴、阳离子表面活性剂的性能。例如,杀菌性、分散性、泡沫性、生物降解性等,近年来受到越来越多的关注[5]。N-烷基-β-氨基丙酸钠是两性表面活性剂中的一个品种,因其良好的亲肤性、低刺激性而成为日化产品的重要原料之一。N-烷基-β-氨基丙酸甲酯是合成N-烷基-β-氨基丙酸钠必不可少的原料,其制备过程通常是由烷基胺(十二胺、十四胺、十六胺)与丙烯酸甲酯按1∶1加成后得到的产物,在实验中发现N-烷基-β-氨基丙酸甲酯的合成偶尔会伴有双加成的副产物N-烷基亚氨基二丙酸二甲酯(D-12、D-14、D-16)存在[5],这样会对产品的性能产生影响。本文在此基础上通过控制反应物间的投料比例合成了十二胺与丙烯酸甲酯的单、双加成产物并表征了其结构。
1 实验部分
1.1 实验原料及仪器
十二胺、十四胺、十六胺,江苏博美达生命科学有限公司,丙烯酸甲酯、甲醇,国药集团有限公司。
集热式磁力搅拌器,DF-1、恒温搅拌油浴锅,HH-SJ2,常州市美特仪器制造有限公司,核磁共振谱仪,AVANCE Ⅲ HD 400 MHz,瑞士Bruker公司。
1.2 N-烷基-β-氨基丙酸甲酯的合成
单加成反应采用余学军等[6]报道的方法。过程如下:分别称取0.1 mol烷基胺溶于40 g无水甲醇中,按烷基胺与丙烯酸甲酯摩尔比为1∶1.2的量逐滴加入丙烯酸甲酯,保持25 ℃恒温搅拌24 h后,蒸出过量的丙烯酸甲酯及甲醇,得白色蜡状固体产物N-烷基-β-氨基丙酸甲酯(N-12、N-14、N-16)。反应方程式如图1所示。
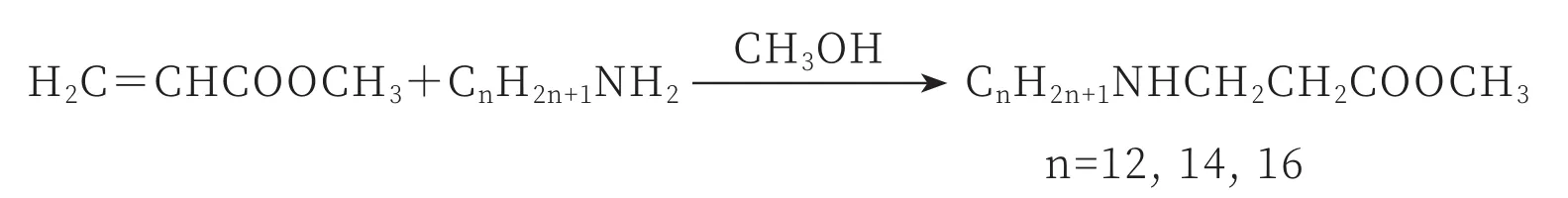
图1 N—烷基—β—氨基丙酸甲酯的合成路线
1.3 N-烷基亚氨基二丙酸二甲酯的合成
双加成可参考单加成反应。过程如下:分别称取0.1 mol烷基胺溶于40 g无水甲醇中,按烷基胺与丙烯酸甲酯摩尔比为1∶2.5的量逐滴加入丙烯酸甲酯,保持25 ℃恒温搅拌24 h后,蒸出过量的丙烯酸甲酯及甲醇,得到黄色液体产物N-烷基亚氨基二丙酸二甲酯(D-12、D-14、D-16)。反应方程式如图2所示。

图2 N—烷基亚氨基二丙酸二甲酯的合成路线
2 结果与讨论
2.1 N-烷基-β-氨基丙酸甲酯的结构表征
将待测物(N-12、N-14、N-16)用氘代氯仿溶解后移至核磁管中,在25 ℃下对样品进行1H NMR分析(以N-12为例),结果如图3所示,其中峰1为氘代氯仿的溶剂峰。其余氢的化学位移及归属见表1。
如图3、表1所示,在化学位移为3.742~3.611,为a位上的氢(3H),化学位移为2.975~2.715,为b位上的氢(2H),化学位移为2.687~2.323为c位、g位上的氢(4H),化学位移为2.171~1.863为d位上的氢(1H),化学位移为1.562~1.147为e位上的氢(20H),化学位移为0.987~0.715为f位上的氢(3H),总氢数为32.76,与理论值33相近,表明目标产物N-12的合成。
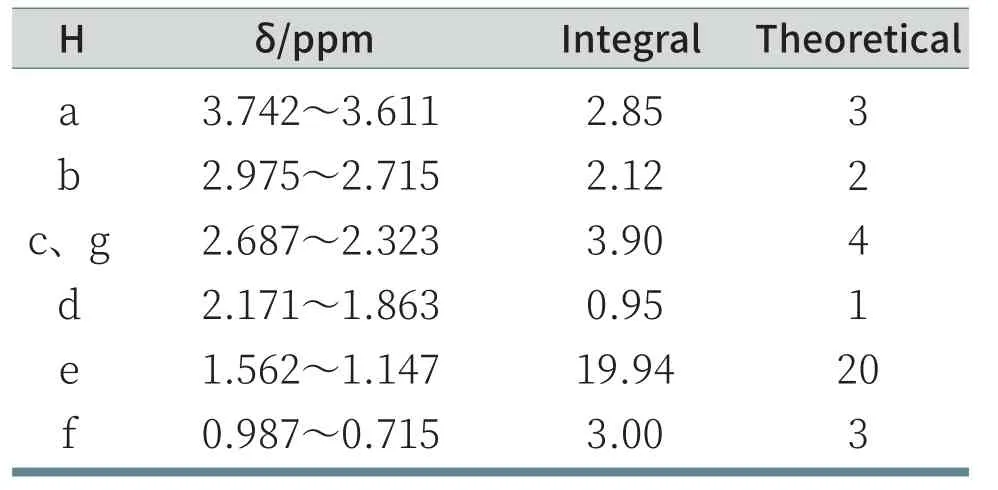
表1 N-12中氢的化学位移及归属

图3 N—12、N—14、N—16的核磁共振氢谱图
2.2 N-烷基亚基氨基二丙酸二甲酯的结构表征
将待测物(D-12、D-14、D-16)用0.6 ml的氘代甲醇溶解后移至核磁管中,在25 ℃下对样品进行1H NMR分析(以D-12为例),结果如图4所示,其中峰1为氘代甲醇的溶剂峰。其余氢的化学位移及归属见表2。
如图4、表2所示,在化学位移为3.714~3.602为a位上的氢(6H),化学位移为2.848~2.660,为c位上的氢(4H),化学位移为2.513~2.304为b位上的氢(6H),化学位移为1.489~1.142为d位上的氢(20H),化学位移为0.959~0.796为e位上的氢(3H),总氢数为38.6,与理论值39相近,表明目标产物D-12的合成。

图4 D—12、D—14、D—16的核磁共振氢谱图
2.3 产物的外观
将合成的单双加成产物N-n、D-n取出置于台面并静止一段时间,观看其外观,实验结果见表3。

表3 产物的外观
正如表3所示,N-n系列单酯基类表面活性剂中间体在室温下为白色蜡状固体,稍稍加热后变为溶液,而在室温下D-n双酯基类表面活性剂中间体则为黄色溶液,两类表面活性剂中间体呈现不同的状态。
3 结论
以烷基胺、丙烯酸甲酯为原料通过控制反应物间的投料比,合成了含有不同酯基的表面活性剂中间体,通过核磁验证产物的结构,在室温下两者也呈现出不同的状态,但有关这两类产物的化学性质还有待后续的实验去探究。

