替诺福韦和替比夫定对不同HBV DNA 载量孕妇母婴阻断效果观察
范岳琴 方群英 胡小娟 王苏梅 王 琛 程晓仙 赵 春
乙型肝炎病毒(hepatitis B virus,HBV)在临床上具有显著的发病率和死亡率[1],HBV 从受感染的母亲传染给婴儿被认为是一个关键因素。因此,预防母婴传播HBV 是降低HBV 感染发病率和死亡率的有效策略[2]。在孕妇妊娠30~32 周使用抗病毒药物替诺福韦(TDF)被发现对母婴传播具有较好的阻断作用[3]。此外,替比夫定(LdT)也被发现能够用于阻断HBV 母婴传播[4]。因此,通过抗病毒治疗对于阻断HBV 的母婴传播具有重要的作用。针对TDF 或LdT在HBV 母婴传播阻断的研究上,国内外的研究基本上聚焦于抗病毒药物对高HBV DNA 孕妇的母婴阻断效果或不分HBV DNA 含量孕妇的母婴阻断效果[5-6]。而不同水平的HBV DNA 孕妇使用阻断剂后的阻断效果及不良反应并没有被关注。因此,本研究旨在探讨TDF 或LdT 对不同HBV DNA 载量的乙肝阳性孕妇母婴阻断的效果。
1 资料与方法
1.1 一般资料 收集2018 年1 月至2019 年12 月在浙江省桐庐县妇幼保健医院治疗的HBV 感染孕妇97 例。根据不同治疗药物分为TDF 阻断组47 例,LdT 阻断组50 例。本研究经医院医学伦理委员会审核通过,审批号【2017】医伦审第(01)号。所有孕妇及家属均了解本研究并签署知情同意书。
1.2 纳入标准(1)在妊娠28 周后检测HBsAg 为阳性;(2)配偶不是乙肝患者或HBV 携带者;(3)入组后在本院成功分娩。
1.3 排除标准(1)有严重全身疾病,如心血管、肾脏、呼吸系统、神经系统等并发症,肝功能异常≥2×ULN、失代偿性肝硬化、肝癌、低磷血症,同时服用肾毒性药物、免疫调节剂、细胞毒性药物等;(2)孕早期有先兆流产史、三维B 超提示胎儿畸形、既往有死胎死产史;(3)配偶为HBsAg 阳性,合并其他传染病如:甲、丁、丙、戊肝、艾滋病、梅毒等;(4)入组前已接受了核苷类似物或抗病毒治疗。
1.4 治疗方法 TDF 组:不同HBV DNA 载量孕妇在孕23~28 周时给予TDF(正大天晴药业集团股份有限公司,批号191115101,每日300 mg)治疗。LdT组:不同HBV DNA 载量孕妇在孕23~28 周时给与LdT(北京诺华制药有限公司,批号190427101,每日600 mg)治疗。婴儿生出后、出生后1、6 个月使用艾美汉信疫苗(大连)有限公司公司的10 μg 乙肝疫苗(批号201805043)和出生后使用山东泰邦生物制品有限公司的100~200 IU 的乙型肝炎免疫球蛋白(批号20180703)。
1.5 观察指标(1)记录入组孕妇年龄、体质指数(BMI)、孕妇分娩方式(剖宫产或顺产)、HBV DNA量、血清和乳汁中TDF 含量。(2)记录新生儿评分(Apgar 评分)、乙肝抗体阳性情况、胎儿体质量、尿液中TDF 含量、血红蛋白量、丙氨酸氨基转移酶(ALT)。
1.6 检测方法(1)HBV DNA 的检测使用入组孕妇3 mL 的外周血,离心后分离血清,采用罗氏Cobas HBV Amplicor Monitor assay 试剂盒(巴塞尔,瑞士,批号11820559)检测。检测限为大于30 copies/mL 判定为阳性。(2)孕妇HBsAg 抗原和胎儿乙肝抗体的检测,取孕妇或胎儿的外周血3 mL,在离心分离血清后采用酶联免疫吸附法检测,试剂盒由厦门创新生物科技公司提供。(3)ALT 采用罗氏cobas800 c701分析仪(巴塞尔,瑞士)检测。(4)血红蛋白采用希森美康System XN-9000 多功能全自动血细胞分析仪(神户市,日本)检测。
1.7 统计学方法 应用SPSS 19.0 统计软件。符合正态分布的计量资料以均数±标准差()表示,采用t 检验,多组间比较应用单因素方差分析ANOVA。计数资料以例表示,采用χ2检验或F 检验。P<0.05 认为差异有统计学意义。
2 结果
2.1 不同HBV DNA 载量孕妇一般资料比较 根据HBV DNA 载量是否大于106copies/mL,将不同阻断剂组中孕妇分为高载量组(>106copies/mL)和低载量组(<106copies/mL)。两组孕妇在年龄、BMI 异常占比、血红蛋白异常占比、分娩方式上,差异无统计学意义(P>0.05),见表1。

表1 TDF 和LdT 组不同HBV DNA 载量孕妇一般资料比较
2.2 不同HBV DNA 载量孕妇所生胎儿乙肝抗体阳性情况及其他指标比较 在TDF 组中,不同HBV DNA 载量组胎儿乙肝抗体阳性占比并无明显差异(P>0.05);LdT 组中,低HBV DNA 载量组胎儿乙肝抗体阳性占比明显高于高HBV DNA 载量组(P<0.05);在其他指标比较上,不管是TDF 还是LdT 组,不同HBV DNA 载量组孕妇的胎儿体质量上均没有显著差异(P>0.05);在Apgar 评分这个指标上,不同HBV DNA 载量组孕妇评分上没有显著差异。但是在数值上高HBV DNA 载量组评分<10 的例数多一些,见表2。
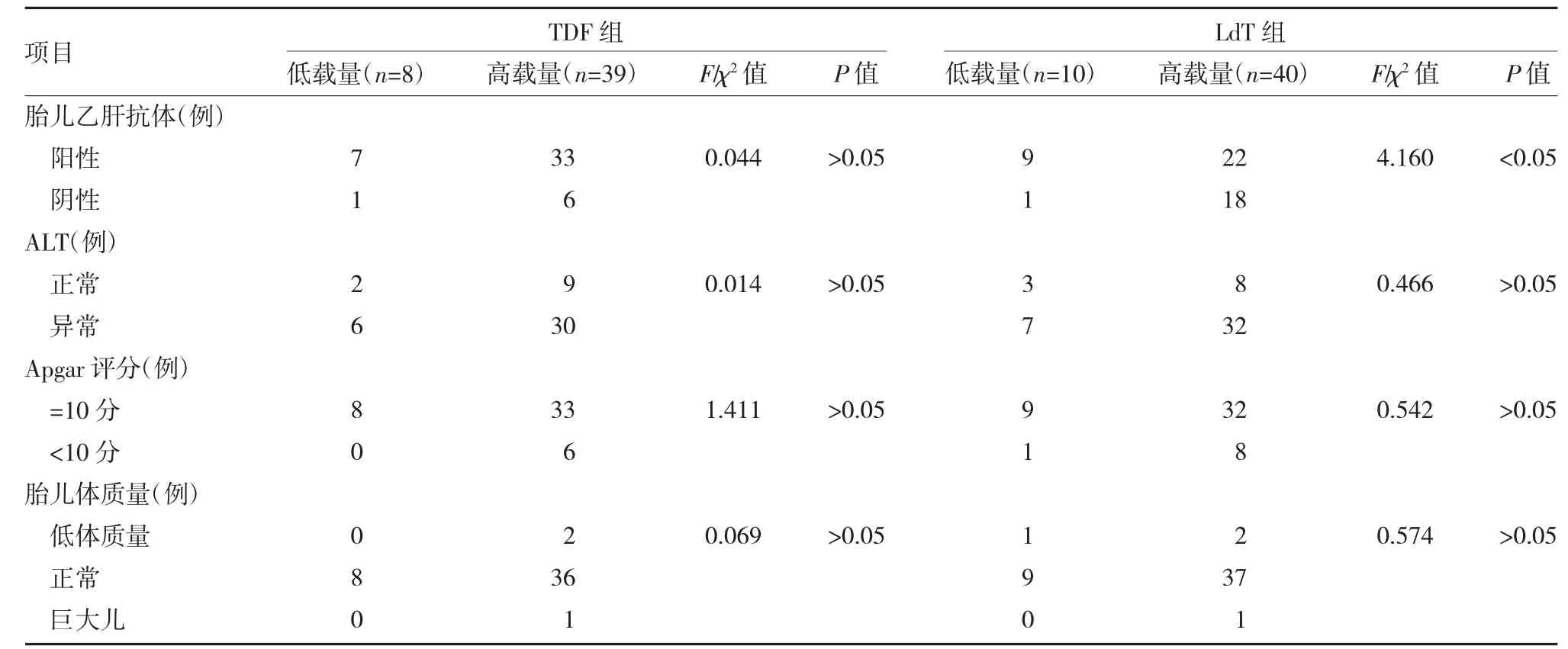
表2 TDF 和LdT 组孕妇所生胎儿指标比较
2.3 不同HBV DNA 载量孕妇血清、乳汁及胎儿尿液TDF 或LdT 残留量比较 不同HBV DNA 载量组中,孕妇血清和乳汁TDF 或LdT 残留量均无显著差异(P>0.05);对于胎儿尿液,TDF 的残留量在高载量组中显著高于低载量组(P<0.05),而LdT 的残留量在两组间无显著差异(P>0.05),见表3。
表3 TDF 和LdT 组孕妇血清、乳汁及胎儿尿液中药物残留量比较(ng/mL,)
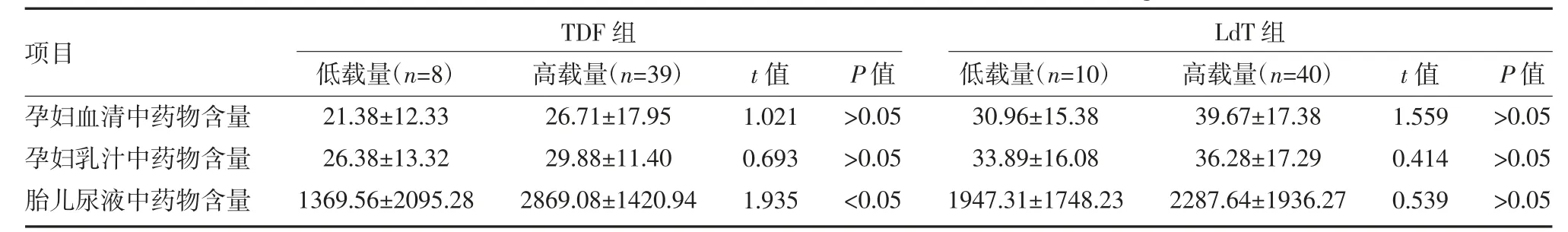
表3 TDF 和LdT 组孕妇血清、乳汁及胎儿尿液中药物残留量比较(ng/mL,)
注:低载量为HBV DNA 载量<106 copies/mL;高载量为HBV DNA 载量>106 copies/mL;TDF 为替诺福韦;LdT 为替夫比定;HBV 为乙型肝炎病毒
2.4 不同HBV DNA 载量孕妇使用TDF 或LdT 后的毒副作用 低载量组孕妇使用TDF 或LdT 过程中均无明显毒副作用,但是高载量组孕妇中,有4 例使用TDF 进行阻断的孕妇在过程中发生了明显的恶心或呕吐,而LdT 阻断的孕妇均无明显的毒副作用。
3 讨论
HBV 感染是全球性的公共卫生问题,患者长期发病会导致严重的肝病。而在HBV 慢性感染的传播途径中,母婴传播是主要的传播方式之一[7-8]。在目前已批准的抗HBV 治疗药物中,TDF 和LdT 是人们普遍认可的妊娠期孕妇预防母婴传播的药物。在过往的临床治疗中,对于LdT 及TDF 这两种药物的评价多集中于HBV 高载量孕妇。有研究者发现,LdT 和TDF 均能够有效阻断高HBV DNA 载量孕妇的母婴传播[9]。而随着研究者对于HBV 母婴传播的深入研究,人们也发现了不同的HBV DNA 载量对于乙肝孕妇母婴传播的效果也有明显的影响[10]。然而,现有的报道中关于TDF 或LdT 对不同水平HBV DNA载量孕妇阻断效果的比较的报道较少。因此,深入评价TDF 及LdT 药物对高低HBV DNA 载量孕妇的治疗效果及药物使用后的安全性有重要的临床意义。
本研究针对于不同水平HBV DNA 孕妇使用TDF 进行阻断的效果进行评价,发现在使用药物阻断后不同HBV DNA 载量组胎儿乙肝抗体阳性占比无明显差异。而在LdT 阻断的患者中,低HBV DNA载量组乙肝抗体阳性占比显著高于高HBV DNA 载量组胎儿乙肝抗体阳性占比。关于高载量孕妇的TDF 或LdT 阻断效果,有研究发现,孕中晚期口服TDF 或LdT 均可有效阻断母婴传播并具有良好的安全性[11]。而周培和渠淑云[5]在研究TDF 阻断高HBV DNA 载量孕妇母婴传播的观察中也发现,TDF 对于高载量HBV DNA 孕妇母婴传播效果是积极的。Sheng 等[12]也在评估核苷酸类似物预防高载量HBV DNA 孕妇母婴传播的有效性和安全性研究中证实,对于高载量HBV DNA 孕妇,LdT 治疗可有效降低HBV 母婴传播。而本研究的结果说明TDF 对于高载量和低载量HBV DNA 孕妇的母婴传播均具有较好的阻断效果。另一方面,LdT 对于提高低载量HBV DNA 孕妇所生胎儿的乙肝抗体阳性占比相比于高载量胎儿更有效。但是在母婴阻断效果上,LdT 对于高载量和低载量HBV DNA 孕妇的母婴传播均具有较好的阻断效果。
在妊娠期使用阻断剂进行母婴阻断的研究中,药物的安全性及对孕妇的不良反应也是临床医生用药时所考虑的因素。目前的研究对于HBV DNA 高载量孕妇使用TDF 或LdT 上均认为药物具有较高的安全性[5,11]。而本研究首次将使用TDF 或LdT 进行阻断的孕妇分为不同水平HBV DNA 载量后,全面比较了孕妇和胎儿的多种指标。结果发现,低载量组孕妇使用TDF 或LdT 过程中均无明显毒副作用。但是高载量组孕妇中,有4 例使用TDF 进行阻断的孕妇在过程中发生了明显的恶心或呕吐,我们通过检测孕妇血清、乳汁及胎儿尿液中TDF 或LdT 残留量发现,不同HBV DNA 载量组中孕妇血清和乳汁中TDF 或LdT 残留量均无显著差异。对于胎儿尿液,研究结果显示,TDF 的残留量在高载量组中显著高于低载量组,而LdT 的残留量在两组间无显著差异。上述结果提示,TDF 在高HBV DNA 载量孕妇及胎儿残留量高可能会对胎儿的身体造成不良的影响。这一结果也可能是样本量较少产生的。
综上,本研究结果表明,在HBV 母婴阻断效果上,两种药物均具有较好的阻断效果。但是在考虑药物安全性及不良反应的条件下,对于高HBV DNA载量乙肝阳性孕妇,可考虑优先使用LdT 提高母婴阻断效果。而针对于低HBV DNA 载量的孕妇,使用两种药物均可达到较好的阻断效果及安全性。而本研究的结论也需要临床上更多的样本进行深入论证。

