小檗碱联合阿奇霉素对小鼠腹腔金黄色葡萄球菌早期生物被膜感染的体内影响
林 健,周煜清,李智欢,吴志红
(1.莆田学院药学与医学技术学院,福建 莆田 351100;2.莆田学院医学微生态福建省高校重点实验室;3.福建东瑞制药有限公司)
金黄色葡萄球菌(Staphylococcus aureus,SA)是一种较为常见能够引发人类感染的病原菌,可侵入宿主并引起住院获得性感染,如肺炎、心包炎、骨髓炎以及脓毒症等系统性疾病[1]。SA入侵宿主细胞和不可逆附着在组织细胞和植入性医疗材料的表面[2],在细胞壁锚定蛋白(cell wall anchoring protein,CWA)介导下,分泌聚集因子和纤连蛋白结合蛋白等。SA菌株有两种状态:浮游状态和生物被膜状态。浮游金黄色葡萄球菌在物理或生物表面附着一定密度后,产生细胞外聚合物(exopolysaccharide,EPS),并进一步形成具有三维立体结构的生物膜层。由于处于生物膜状态的金黄色葡萄球菌比浮游状态对抗生素更具耐药性,通常不能被免疫系统清除[3],而导致植入性的细菌感染[4]。SA表面形成致密的细胞层通过多糖胞间黏附素(polysaccharide intercellular adhesion,PIA)黏附在一起,细菌一旦形成生物被膜,通过天然的三维立体结构渗透屏障、微环境的变化、细菌表型的改变以及细菌密度感应系统(quoru sensing,QS)调节等产生耐药性。生物被膜造成的耐药是感染难以控制的一个主要因素[5]。
盐酸小檗碱(berberine,Ber)是一种异喹啉生物碱,是治疗肠道感染的常用的药物之一[6]。除了其广谱的抑菌作用外,据报道小檗碱具有抗炎、抗氧化、抗肿瘤、降低血糖和抗心律失常的作用[7]。研究还报道了小檗碱对大肠杆菌和枯草芽胞杆菌具有抑菌作用[8]。本课题前期研究盐酸小檗碱能显著抑制金黄色葡萄球菌生物被膜的形成[9]。然而小檗碱对体内金黄色葡萄球菌生物被膜感染影响的研究鲜少。为了进一步探讨小檗碱联合阿奇霉素(Azithromycin,AZM)对体内金黄色葡萄球菌生物被膜感染的作用和盐酸小檗碱联合阿奇霉素用药是否能够缓解金黄色葡萄球菌感染后机体的炎症反应和抑制体内生物被膜的生长,本实验选用金黄色葡萄球菌(ATCC25923)作为实验菌株,利用输液管制备体外生物被膜,建立小鼠在体腹腔感染模型,再分别给予盐酸小檗碱、阿奇霉素单独用药和上述两种药物联合用药;给药24 h后取出载体,观察小鼠给药后感染组织的炎症反应,感染组织病理变化;扫描电镜(SEM)对比体内生物被膜的变化,验证盐酸小檗碱、阿奇霉素联合用药对SA早期BF体内感染的治疗效果,为中药单体联合抗生素治疗SA生物被膜相关感染提供理论依据。
1 材料与方法
1.1实验动物与试剂 SPF级BALB/c雌性小鼠(6-8W)28只,体质量(20±2)g,由上海斯莱克实验动物有限责任公司提供[许可证号:SCXK(沪)2019-0007];(2 mL∶0.25 g)注射用阿奇霉素(湖南科伦制药有限公司,生产批号:20190207);盐酸小檗碱(含量大于98 %,成都龙泉高科天然药业有限公司,生产批号:20190117));TSB胰蛋白胨大豆肉汤(北京奥博星生物技术有限责任公司),肉汤培养基(南通凯恒生物科技发展有限公司)以及营养琼脂培养基(南通凯恒生物科技发展有限公司)。
1.2菌株 金黄色葡萄球菌(ATCC25923),由莆田学院微生物实验室提供。
1.3载体 医用输液管(山东医得医疗用品有限公司),医用手术剪剪成长度约为1 mm、外径约6 mm、内径约4 mm,将其作为BF载体,共计40个。高压灭菌锅在121 ℃条件下灭菌20 min备用。
1.4方法
1.4.1菌悬液的配制 将实验菌株(ATCC25923)接种于TSB培养基中,于37 ℃摇床培养20 h,将菌液置于离心机3 000 r/min离心20 min,弃去上清液,菌体生理盐水清洗2次后,菌体用生理盐水重悬,使得菌悬液在波长600 nm时OD= 0.5,菌悬液置于4 ℃备用。
1.4.2准备BF载体 50 mL锥形瓶中加10 mL上述步骤中菌悬液,用手术镊子夹取制备的输液管载体10个放入菌悬液中。37 ℃,110r/min条件下,培养20 h,使细菌大量扩增黏附于制备的载体。准备移植载体入小鼠腹腔时,黏附在载体上的细菌数应为(6~7)×105CFU/mL。
1.4.3实验动物的准备 在进行实验之前,实验所用小鼠至少喂养1 W(鼠粮吴氏实验动物提供)。
1.4.4实验动物分组及建立腹腔感染模型 雌性实验用小白鼠28只,分为4组:空白对照组、AZM组(30 mg/kg)、Ber(30 mg/kg)、联合用药AZM(15 mg/kg)和Ber(15 mg/kg)组,随机分配每组7只。小鼠0.3 %水合氯醛麻醉后,于右下腹用医用手术剪,剪开约1 cm的切口,逐层分离肌肉组织,打开腹腔,迅速用无菌医用小镊子,从培养20 h的菌液中取出载体,用无菌的生理盐水洗去载体表面游离的SA,漂洗3 sec后,立即放入小鼠右下腹腔,用手术医用缝合线逐层缝合手术切口,在手术部位再次用医用酒精消毒处理。载体植入完毕后,AZM组在小鼠左下腹腔内注射阿奇霉素注射液(30 mg/kg),Ber组通过灌胃给药给予小鼠小檗碱(30 mg/kg)、联合给药组则灌胃的方法盐酸小檗碱(15 mg/kg)后,继续在小鼠左下腹腔内注射阿奇霉素(15 mg/kg),空白对照组在小鼠腹腔注射等量生理盐水。
待上述药物在小鼠体内作用24 h后,水合氯醛麻醉小鼠。拆除医用缝合线,逐层打开右下腹原手术切口,取出BF载体,放入先前准备的无菌生理盐水快速漂洗3 sec,再将载体放入装有1 mL无菌生理盐水的EP管内;同时剪取载体所在感染部分组织,放入组织盒,浸泡在配制的10 %的多聚甲醛溶液中,作常规HE染色,显微镜下观察切片进行病理学分析。
1.4.5载体表面菌落计数 装有载体的EP管,用旋涡震荡仪震荡10 min,然后取200 μL EP管中的菌液,用生理盐水按1∶10倍比稀释法,稀释到菌液为10个左右CFU/mL,每个平板各取1 000 μL的菌液到平板和20 mL 50 ℃营养琼脂混合均匀,凝固后于37 ℃ CO2培养箱培养24 h后,计算每个平板的菌落数。
1.4.6扫描电镜观察载体BF 首先用2.5 %戊二醛溶液固定载体,然后用PBS(pH 7.4),在4 ℃下漂洗3次,每次10 min,之后按顺序用50 %、70 %、80 %、90 %乙醇脱水1次,每次10 min,再用100 %乙醇脱水3次,每次均为10 min,最后在真空条件下镀金粉,扫描显微电镜下观察。
2 结果
2.1载体表面菌落计数 给药待药物作用24 h以后,取出载体,连续倍比稀释后进行表面菌落计数,其结果显示:单独给药组及联合给药组菌落数均少于空白对照组(P<0.01);AZM 组较Ber组少(P<0.01);Ber+AZM组菌落数较Ber、AZM单独给药组显著变少(P<0.01)。见表1。

表1 经不同药物作用24 h后载体生物被膜上的活菌计数
2.2扫描电子显微镜(SEM)观察载体BF 给药组等药物发挥作用24 h后,取出载体,利用SEM进行分析,结果显示:空白对照组SEM观察BF生长形态均比给药组形成的BF稠密且繁多,且有大量的细菌黏附;AZM组较Ber组稀疏;Ber+AZM组较Ber组和AZM组生物被膜稀薄平整,只见少量SA细菌黏附。见图1。
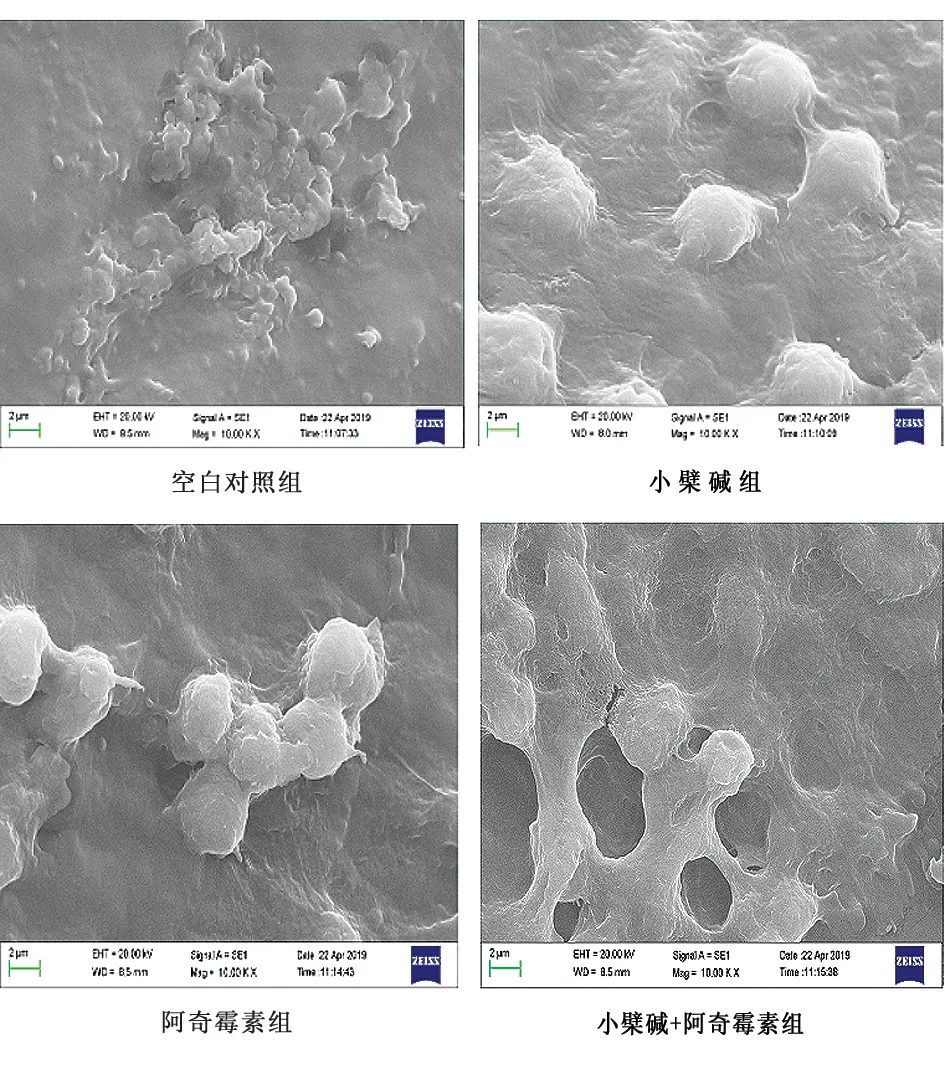
图1 载体生物被膜扫描电镜图(×10 000)
2.3腹腔感染组织病理变化 空白对照组载体周围组织有大量炎症细胞浸润,经药物治疗后炎症明显减轻,Ber+AZM组周围组织炎症减轻最为明显。见图2。

图2 腹腔感染组织HE染色图(×400)
3 讨论
根据美国国立卫生研究院的报告,超过80 %的感染与耐药细菌的生物膜感染有关,预计这种情况将对人类健康造成全球负担,每年有超过1 000万人死亡[10]。尽管投入了大量的人力和财力,但在1962~2000年期间,并没有研究出新的初级抗生素类别[11]。因此,寻找高效、毒性较低的抗生素替代品来控制金黄色葡萄球菌生物膜感染是一项紧迫的任务。近年来,临床多重耐药细菌的多重耐药性均与其生物被膜的产生密切相关[4]。相关领域的科研工作者在积极探索研究抗生物被膜的药物,单一抗生素得不到有效的治疗效果,因此需要天然化合物与抗生素联合治疗的手段来应对生物被膜所引起的感染。很多中药中提取单体在防止细菌形成生物膜或分散现有生物膜方面表现出优异的活性,如根皮素[12]、大黄素[13]、贯叶金丝桃素[14]、槲皮素[15]和鞣花酸[16]。目前抗生物被膜的研究主要局限于单独使用抗生素或者多种抗生素联合使用,中药单体与抗生素联用抗生物被膜的研究目前还主要集中在体外的实验研究,在体研究较少见。本实验通过在体实验观察中药单体联合抗生素治疗生物被膜感染有一定的创新性。
小檗碱(Ber)是一种存在于各种植物中的异喹啉生物碱,具有优良的抗菌性能。有报道小檗碱会破坏细菌细胞膜上的脂肪酸成分,并上调能够水解细胞壁的基因,从而破坏细菌细胞膜的完整性[17]。高浓度的小檗碱破坏了细菌细胞壁的结构,导致细菌细胞壁变薄甚至裂解,使阿米卡星更容易穿透细胞壁,从而影响到细菌中DNA的合成,进一步抑制了细菌蛋白的合成,导致细菌死亡[18]。另外前期研究发现小檗碱能显著抑制金黄色葡萄球菌生物被膜的形成[8]。
阿奇霉素是一种广谱的大环内酯类抗生素,对革兰氏阳性菌、革兰氏阴性菌和非典型细菌均有抑制作用,还有抗炎作用,能够减少密度感应系统(quorum sensing,QS)相关毒力因子的产生和生物被膜的形成[19]。阿奇霉素对金黄色葡萄球菌悬浮菌和生物被膜内的细菌具有较好的抗菌活性,通过影响金黄色葡萄球菌溶血素和肠毒素A的分泌而抑制生物被膜的形成[20]。
本实验建立小鼠在体感染SA模型,给药后,取出载体,通过连续倍比稀释以及SEM观察,计数结果:单独给药组及联合给药组菌落数都少于空白对照组(P<0.01);AZM组较Ber组少(P<0.01);Ber+AZM组菌落数较Ber、AZM单独给药组显著变少(P<0.01);扫描电子显微镜结果:空白对照组SEM观察BF生长形态均比Ber组、AZM组、Ber+AZM组形成的BF稠密且繁多;AZM组较Ber组稀疏;Ber+AZM组BF基本被药物清除,只见少量SA细菌黏附。
小檗碱、阿奇霉素在单独用药时可以破坏SA感染后早期形成的生物被膜;小檗碱对小鼠腹腔SA感染早期生物被膜的形成具有干扰作用,其与阿奇霉素联合用药显著增强对小鼠腹腔金黄色葡萄球菌感染的治疗作用,两药联合使用作用机制可能是小檗碱破坏金黄色葡萄球菌细胞壁,使得细菌细胞壁变薄或者裂解,使得更多的阿奇霉素穿透细胞壁抑制和影响α-溶血素和肠毒素A而抗生物被膜的作用。中药单体与抗生素抗感染机制不同,可以作用于感染的多个环节,与抗生素发挥协同作用,甚至能够逆转抗菌药物的耐药性,治疗生物被膜的相关感染。本课题通过小鼠在体实验利用小檗碱中药单体联合阿奇霉素抗生素治疗生物被膜感染,将为治疗细菌生物被膜感染提供新思路,有一定的临床意义。

