住院患者静注人免疫球蛋白超说明书用药的循证评价
曹晔,骆从艳,孙哲,冯新奥,王海滢,庞宁,刘芳*
1 北京大学第三医院药剂科,北京 100191;2新疆维吾尔自治区克拉玛依市第二人民医院药剂科,克拉玛依 834009
静注人免疫球蛋白(intravenous immunoglobulin,IVIg)是从大量健康人群混合血浆中纯化而来的血液制品,具有免疫调节和免疫替代的双重治疗作用,经静脉注射后,能迅速提高患者血液中的免疫球蛋白G(immunoglobulin G,IgG)水平,增强机体的抗感染能力和免疫调节水平[1]。作为血液制品,由于血浆来源短缺,以及预防经血液途径传播疾病的管理要求,应严格管控IVIg。近年来,IVIg在临床的应用范围不断扩大[2],而目前国内尚无IVIg相关的循证用药指南。超说明书用药可能会引发药品安全性、有效性以及医疗责任等问题,本研究对本院住院患者应用IVIg的超说明书用药情况进行调查,收集和整理循证医学证据,评价用药的合理性,为临床合理应用IVIg提供参考依据。
1 资料与方法
1.1 病例资料收集
通过电子病历系统,回顾性检索本院2018年1月~2020年12月应用IVIg的住院患者病历。采用Microsoft Excel软件收集并记录患者的基本信息(姓名、年龄、体重)、临床诊断、用药原因、用药方案(用法、剂量、溶媒、疗程等),并计算其构成比。
1.2 超说明书用药筛选
以国家药品监督管理局批准的静注人免疫球蛋白(pH4)(成都蓉生药业有限责任公司)药品说明书(修改日期2020年12月30日)为参考依据。筛选符合说明书明确列出的适应症的病历:原发性免疫球蛋白G缺陷症、重症感染、新生儿败血症、婴幼儿毛细支气管炎、原发性血小板减少性紫癜、川崎病,判定为符合药品说明书适应症;否则,判定为超说明书用药。再从用法用量、疗程、溶媒等方面进行病历筛选,判断其是否符合药品说明书;若不符合,也判定为超说明书用药。
1.3 超说明书用药的循证评价
1.3.1 国外说明书查询
查询FDA、EMA药品说明书,核对病历是否符合FDA、EMA说明书适应症。如不符合,则进一步对超说明书应用IVIg病例的用药方案进行证据检索,评价其是否有循证医学证据支持。
1.3.2 循证医学证据查询
按照《超说明书用药循证评价规范》推荐的方法[3],查阅Micromedex数据库进行Thomson分级。若系统已收录IVIg的某种超说明书用药,则直接引用;若未收录,则通过查阅PubMed、Embase、中国知网(CNKI)、万方数据库、维普数据库、中国生物医学文摘数据库,按照证据级别由高到低,依次获得超说明书用药目录[4]、国际及国家级权威学协会或组织发布的诊疗规范、临床诊疗指南、系统评价/Meta分析、随机对照研究、队列研究和病例对照研究(获得高等级的研究证据后,则不再继续检索低等级证据),然后再进行Thomson分级评价。搜索的关键词是人免疫球蛋白、丙种球蛋白、丙球、intravenous immunoglobulin、gammaglobulin和相应疾病诊断的中英文。
1.3.3 证据分级
对于Micromedex数据库中可检索到的IVIg应用,按照Thomson证据等级,证据强度由强到弱分别为高证据等级(A类)、中证据等级(B类)、低证据等级(C类)和无证据(见表1)。把符合FDA、EMA说明书、超说明书用药目录或相关疾病指南最高等级推荐等情况也作为A类证据。

表1 证据等级分类
2 结果
2.1 基本情况
2018年1月~2020年12月本院住院患者应用IVIg的病例共204例,超说明书用药共160例(78.43%)。其中超适应症用药125例(78.13%),超剂量用药17例(10.62%),超疗程用药18例(11.25%),无溶媒选择不合理情况。患者的基本情况见表2。

表2 超说明书用药病例的基本情况
2.2 超说明书用药分类
160例超说明书用药中,有125例为超适应症用药(见表3)。符合FDA说明书适应症的有40例(32.0%),其中预防血液恶性肿瘤的细菌感染38例(30.4%)。符合EMA说明书适应症的有2例(1.6%),为格林-巴利综合征。
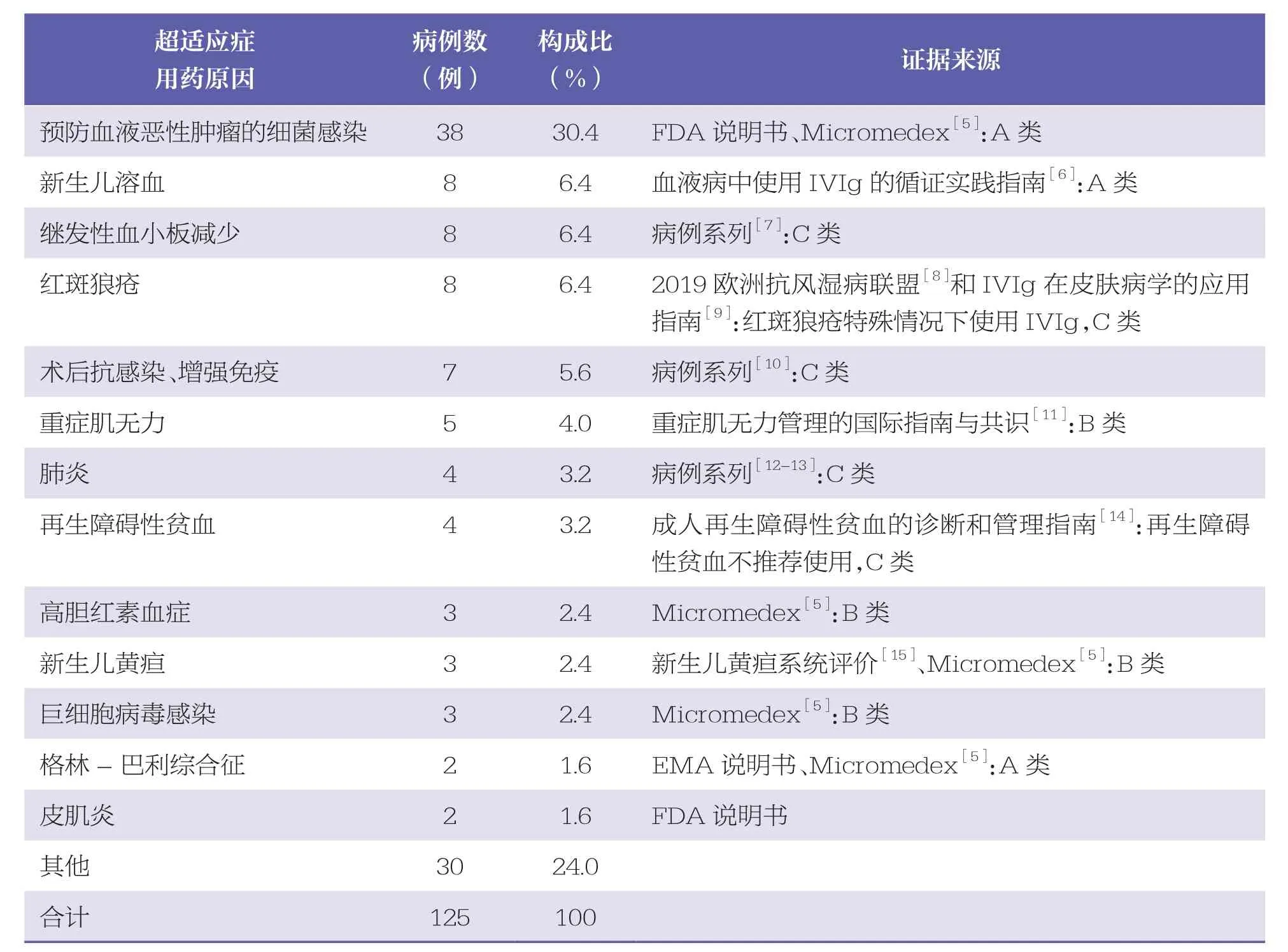
表3 超适应症用药情况
有17例超剂量用药,18例超疗程用药,二者中占比较高的均为重症感染,分别为12例(70.59%)和17例(94.44%),见表4。我国的药品说明书规定给予IVIg,重症感染者按每日200~300mg/kg体重剂量给予IVIg,连续使用2~3天。而12例超剂量用药中,6例为剂量不足,6例为剂量偏高;17例超疗程用药中,1例使用4天,12例使用5天,4例使用6天。

表4 超剂量和超疗程用药情况
2.3 超说明书用药的循证评价
对160例超说明书应用IVIg的用药原因进行分析,并对检索到的相关证据进行分级,见表5。56例(35.0%)为低证据等级(见表6);35例(21.9%)适应症符合说明书,但用法用量或疗程超说明书,通过各数据库文献检索,其中有33例(20.7%)未检索到上述超用法用量及疗程的相关研究证据,故判定为无证据。160例超说明书用药循证评价流程图,见图1。
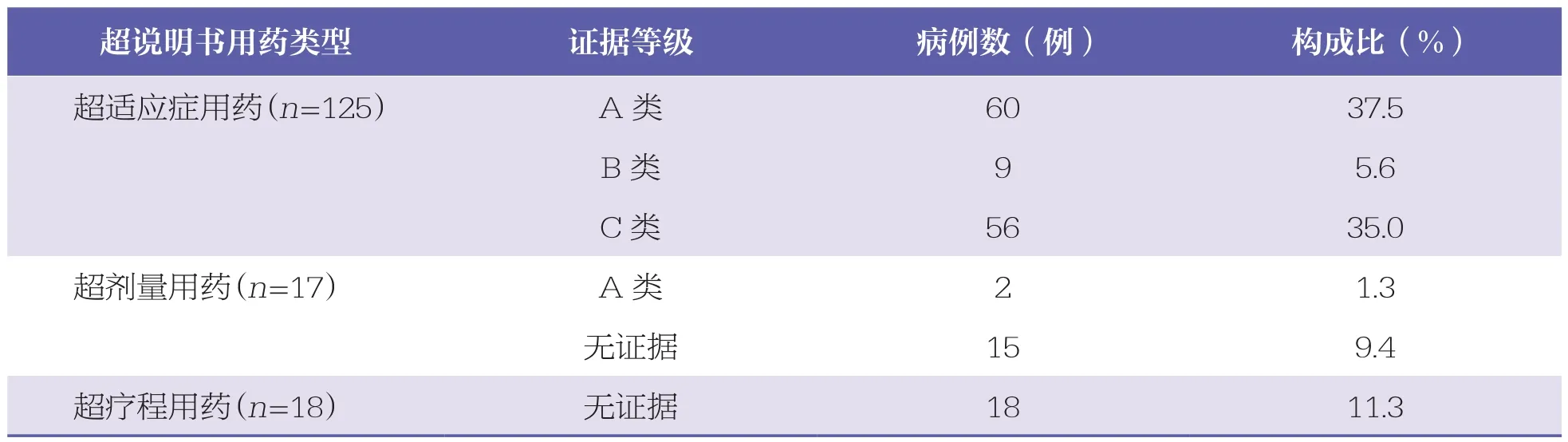
表5 超说明书用药的循证等级分布情况
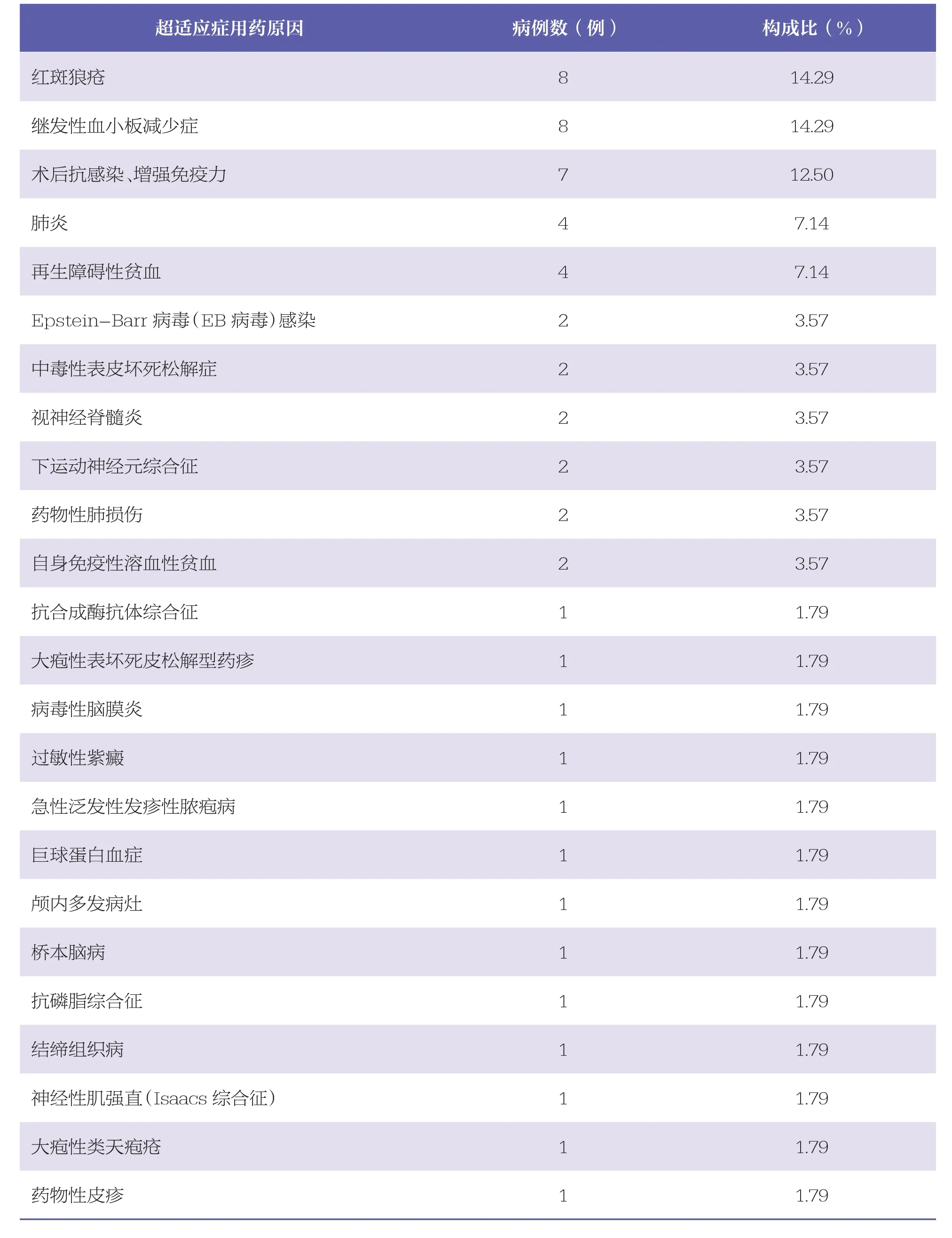
表6 低证据等级(C类)IVIg的应用 n=56
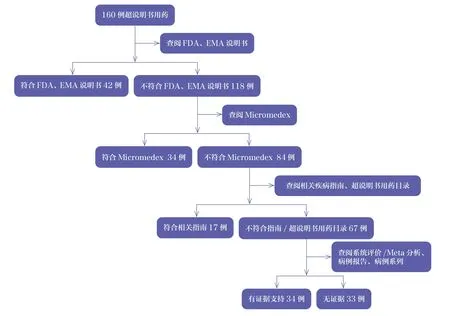
图1 超说明书用药循证评价流程图
3 讨论
3.1 超说明书用药比例较高的原因分析
我国IVIg适应症包括:①原发性免疫球蛋白缺乏症,如X联锁低免疫球蛋白血症,常见变异性免疫缺陷病,免疫球蛋白G亚型缺陷病等。②继发性免疫球蛋白缺陷病,如重症感染,新生儿败血症等。③自身免疫性疾病,如原发性血小板减少性紫癜,川崎病。FDA批准的适应症包括[5]:① 预防低丙种球蛋白血症和/或B细胞慢性淋巴细胞白血病相关的复发性细菌感染。② 皮肌炎。③ 甲型肝炎,预防用药。④ 慢性炎症性脱髓鞘性多发性神经病。⑤ 川崎病。⑥ 麻疹。⑦ 多传导阻滞运动神经病变。⑧ 暴露后预防妊娠风疹。⑨ 原发性免疫缺陷病。⑩ 特发性血小板减少性紫癜。水痘,水痘-带状疱疹免疫球蛋白不可获得时作为替代等。EMA批准的适应症包括[16]:① 原发性免疫缺陷病。② 继发性免疫缺陷病。③ 原发性免疫性血小板减少症。④ 格林-巴利综合征。⑤ 川崎病。⑥ 慢性炎性脱髓鞘性多发神经根神经病。⑦ 多灶性运动神经病。
本研究发现,本院IVIg超说明书用药比例较高(78.43%),涉及的科室也比较广泛。预防血液恶性肿瘤的细菌感染占比最高(23.75%),此适应症在FDA说明书适应症中。此外,2007年加拿大发布的《关于静脉注射免疫球蛋白治疗血液病的使用指南》[6]建议静脉注射免疫球蛋白0.4g/kg每3周1次,每4~6个月重新评估,作为预防成人血液恶性肿瘤患者细菌感染的合理选择;张宏亮等[17]对IVIg临床指南进行了系统评价,也推荐了此适应症。在Micromedex数据库中,用于预防血液恶性肿瘤的细菌感染的证据强度为A级。与之相比,我国2020版IVIg药品说明书适应症有“继发性免疫球蛋白缺陷病,如重症感染”,但没有明确界定“预防血液恶性肿瘤的细菌感染”这一适应症,导致此超说明书用药比例较高。此外,在本研究中发现的超说明书用药中,符合FDA说明书适应症有40例,符合EMA说明书适应症有2例。这也提示了我国药品说明书的适应症描述不够清晰,是导致超说明书用药较多的原因之一。
3.2 低证据和无证据等级的超说明书用药相关问题
药品说明书是具有法律效力的医疗文书,超说明书用药给医务人员带来一定职业风险,并且患者也承担着使用风险[18]。IVIg超说明书使用中,低证据等级用药56例(35.0%),无证据等级用药33例(20.7%)。其中用于术后抗感染与增强免疫是基于IVIg的药理作用,但临床实践中,这2种情况应用IVIg不仅不能增加抗感染效果,还可能加重患者病情。因为频繁使用IVIg可能抑制抗体产生[19],同时还增加了潜在的安全风险。药物的疗效与药物的正确使用密切相关,剂量不足导致治疗效果差;剂量过高、疗程过长,同样可能抑制抗体的产生并增加不良反应的发生率[19]。此外,国内外药品说明书中,都有对于IVIg的黑框警告。我国说明书中提示:因原料来自人血,虽然对原料血浆进行了相关病原体的筛查,并在生产工艺中加入了去除和灭活病毒的措施,但理论上仍存在传播某些已知和未知病原体的潜在风险[20];FDA黑框警告中也提示使用免疫球蛋白产品可能会导致血栓、肾功能不全、急性肾功能衰竭、渗透性肾病和死亡[21]。在经济性方面,IVIg属于资源短缺的血液制品,价格昂贵,且未纳入《国家基本医疗保险、工伤保险和生育保险药品目录》,会增加患者的住院费用。随着国家医保相关政策的调整,医保支付制度从按照项目付费改为按疾病诊断相关分类(diagnosis related groups,DRGs)病种付费,药品已成为医院的真实成本[22],过度使用IVIg不利于控制药品费用。
3.3 对IVIg超说明书用药的建议及改进措施
2022年3月,新修订的《中华人民共和国医师法》正式实施,其中首次将药品说明书中未明确但具有循证医学证据的药品用法写入法律,为其在临床中的应用提供了法律保障[23]。但《中华人民共和国医师法》中也要求医疗机构建立超说明书用药管理制度,对医师处方、用药医嘱的适宜性进行审核,严格规范医师用药行为。
结合本研究结果,笔者对IVIg超说明书用药提出了一些建议:① 医生应充分掌握IVIg的作用机制,权衡用药利弊。② 医疗机构应对循证医学证据较充分的超说明书用药进行备案,并且在超说明书用药时,告知患者及家属超药品说明书用药的利弊,让患者及家属了解并签署知情同意书,且在使用过程中还应严密监测药品不良反应。对于缺乏循证医学证据的超说明书用药,应限制使用。③ 应加快循证药学专业人才的培养,定期进行专项点评,在循证实践中提升药学服务与审方水平,发现并干预无证据的超说明书用药,促进合理用药[24]。④ 目前虽有一些超说明书用药目录,例如广东省药学会发布的《超药品说明书用药目录》(2021年版)[4]只纳入了一项IVIg超说明书用药。我国药品说明书对适应症的描述比较宽泛,不够清晰,而学术机构和专业协会是规范超说明书用药和提供证据的主力军,应组织针对缺乏证据而又广泛使用的超说明书用药进行多中心研究,建议建立IVIg的超说明书用药目录和相关指南。⑤ 在无可替代的药品或疗法时,需要全方面权衡患者的获益和风险,如涉及 IVIg超说明书用药[25],也应采用推荐的用药方案和疗程。
3.4 本研究的局限性
① 我国 IVIg 药品说明书中的适应症“重症感染”在各指南中并未提及,重症感染的界定比较模糊,尚缺乏统一的标准[26],本研究将重症肺炎、脓毒症、菌血症、感染中毒性休克纳入重症感染的范围,存在一定的主观性。② 本研究只搜索了PubMed和Embase 2个外文数据库,一些超说明书用药证据可能未被数据库收录;而且仅纳入了中英文2个语种,一些研究证据可能以其他语种发表而未检索到。③ 本研究为单中心研究,无法全面收集IVIg超说明书用药。尽管如此,本研究仍在一定程度上反映了目前IVIg超说明书用药的现状。
综上,本院IVIg超说明书用药比例较高,且部分超说明书用药为低证据等级或无证据等级。本院应加强对IVIg超说明书用药的管理,如有条件,应对低证据等级或无证据用药开展多中心、大样本、高质量的随机对照研究,为临床合理用药提供参考。
— 多适应症药物准入评估方法比较研究

