五味子甲素对腹泻型肠易激综合征大鼠肠上皮黏膜屏障功能的保护作用*
耿 峰, 毛 颖, 丛 珊, 杜 娟, 于春雪
(齐齐哈尔医学院附属第二医院药学部,黑龙江 齐齐哈尔 161006)
腹泻型肠易激综合征(diarrhea-predominant irritable bowel syndrome,IBS-D)是一种以腹泻为特征的IBS。目前,IBS-D 主要以对症治疗为主,但存在疗程长,不良反应多,停药后易复发等弊端[1]。因此,继续探索新的IBS-D的治疗方法十分必要。
肠屏障功能障碍和炎症反应是IBS 的主要病理现象[2-3],尤其是IBS-D患者的肠道通透性更高[4]。既往研究发现,IBS患者回肠末端及升结肠的肠黏膜白细胞介素(interleukin,IL)及肿瘤坏死因子α(tumor necrosis factor-α,TNF-α)等促炎介质表达增加[5],以及细胞紧密连接蛋白表达和分布发生改变[6]等与肠道通透性破坏有关。另外,肠上皮黏膜屏障功能是破坏能加剧IBS的炎症反应,且炎症反应也能进一步破坏肠上皮黏膜的屏障功能[7-8]。近年来,研究发现五味子甲素(schizandrin A,SchA)在三硝基苯磺酸诱导的动物溃疡性结肠炎模型中具有明显的抗肠炎作用[9-12],据此猜测 SchA 可能同样对 IBS-D 具有治疗作用。因此,本实验以大鼠IBS-D 模型探讨SchA 是否在IBS-D 中发挥抗炎和维护肠上皮黏膜屏障功能的作用。
材料和方法
1 材料
1.1 实验试剂 番泻叶(购自齐齐哈尔医学院附属第二医院中药房,产地:广西),按王阳等[13]方法用沸水煎药,最终获得含200 g/L 番泻叶(生药)的水煎剂,4 ℃冷藏备用;SchA(纯度>98%;MedChemExpress);末端脱氧核苷酸转移酶介导的dUTP 缺口末端标记(terminal deoxynucleotidyl transferase-mediated dUTP nick-end labeling,TUNEL)试剂盒(Roche);异硫氰酸荧光素标记葡聚糖(fluorescein isothiocyanate-dextran,FITC-dextran)购自杭州新乔生物科技有限公司;IL-6、IL-1β和TNF-α对应的酶联免疫吸附试验(enzyme linked immunosorbent assay,ELISA)试剂盒购自南京建成生物研究所;闭锁小带蛋白1(zonula occludens-1,ZO-1)、闭合蛋白(occludin)、CD68 和CD11b 抗体(Abcam);核苷酸结合寡聚化结构域样受体蛋白3(nucleotide-binding oligomerization domain-like receptor protein 3,NLRP3)、含胱天蛋白酶募集结构域的凋亡相关斑点样蛋白(apoptosis-associated speck-like protein containing a caspase recruitment domain,ASC)和caspase-1(P20)抗体(Cell Signaling Technology);RIPA 裂解液、苯甲基磺酰氟、ECL 化学发光试剂、胱天蛋白酶3 裂解片段(cleaved caspase-3)抗体、GAPDH 抗体和辣根过氧化物酶(horseradish peroxidase,HRP)标记的羊抗兔IgG 抗体(沈阳万类生物科技有限公司);DyLight 488或657标记的羊抗兔IgG荧光Ⅱ抗(武汉艾美捷科技有限公司);苏木精-伊红(hematoxylin-eosin,HE)染色试剂盒和SP 免疫组化试剂盒(北京索莱宝生物科技有限公司)。
1.2 实验动物 30 只6~7 周龄无特定病原体级雄性SD 大鼠(体重190~210 g)购自哈尔滨医科大学实验动物学部,生产许可证号为SCXK(黑)2019-001,饲养于齐齐哈尔医学院实验动物中心,饲养环境为:恒温22~24 ℃、湿度可控(55%~65%)和12 h/12 h 光暗循环的屏障环境,在实验前大鼠可随意饮用水和饲料。
2 方法
2.1 IBS-D 动物模型的建立与分组处理 适应饲养3 d 后,将30 只大鼠随机分为对照组、模型组和SchA治疗组,每组均10 只。参照文献[13-15]方法建立IBS-D大鼠模型:对大鼠进行灌胃20 mL/kg 含200 g/L 番泻叶水煎剂(注:灌胃前将番泻叶水煎剂加热至25 ℃),灌胃 1 h 后,束缚大鼠 2 h,每天 2 次,持续束缚 2 周。模型组和SchA 治疗组大鼠均按照上述方法构建IBS-D 大鼠模型,其中SchA 治疗组在造模后给予灌胃 40 mg/kg SchA[9-10],每天 1 次,持续 2 周;模型组给予等体积生理盐水;对照组不进行IBS-D 造模,仅给予等体积生理盐水。
2.2 大鼠肠痛觉敏感性测定 给药方案结束后,按文献[16-17]方法用腹部撤离反射(abdominal withdrawal reflex,AWR)试验评估各组大鼠内脏敏感性。将大鼠禁水禁食10 h以上,用异氟烷吸入麻醉后,将涂有润滑油的弹性乳胶气囊插入大鼠结肠,待大鼠清醒30 min 后,以5 mmHg 为增量的气压扩张结肠,直到出现背部肌肉收缩且腹部抬离地面时,记录压力值,作为AWR 痛觉阈值。实验重复3 次,每次间隔10 min,取平均值进行分析。
2.3 FITC-dextran 肠道通透性检测 AWR 实验后,分别给各组大鼠灌胃50 mg/kg FITC-dextran。4 h后,取眼眶静脉丛血,并分离血清。按照试剂说明,将血清用磷酸缓冲盐溶液(phosphate-buffered saline,PBS)按1∶10稀释,每只大鼠各取100 μL血清稀释液加入黑底96 孔板中,荧光酶标仪测荧光强度值,根据标准曲线计算血清中FITC-dextran含量。
2.4 HE 染色 麻醉大鼠,处死并分离据肛门远端(约10 cm)肠组织,按照常规法对肠组织进行石蜡包埋,并切为6 μm 厚度的连续切片。切片经烤片、二甲苯脱蜡、梯度乙醇再水化后,用HE染色,在光学显微镜下观察。
2.5 免疫组织化学染色 肠组织切片再水化后,依次经3%H2O2浸泡除去内源性的过氧化氢酶,柠檬酸缓冲液高温修复和10%羊血清封闭非特异性位点后,分别滴加ZO-1和occuldin抗体(均1:500稀释)并37 ℃孵育2 h,用PBS 洗涤后,按照免疫组化试剂盒方法依次孵育Biotin-羊抗兔IgG 和链酶亲和素-POD后,DAB 显色,苏木素复染,光学显微镜下观察染色情况,阳性细胞可见棕黄色颗粒,从至少3 个随机视野采集数字图像进行进一步分析。
2.6 TUNEL 染色 用TUNEL 染色评估大鼠肠组织上皮细胞凋亡情况。肠组织切片再水化后,用不含DNase 的蛋白酶 K 作用 10 min,PBS 洗涤,然后滴加50 μL TUNEL 检测工作液,37 ℃避光孵育 60 min,PBS 洗涤 2 次,DAPI 复染,在荧光显微镜下观察,从至少3个随机视野采集数字图像进行进一步分析。
2.7 免疫荧光染色 肠组织切片再水化后,用10%羊血清封闭非特异性位点后,分别滴加cleaved caspase-3、CD68 和 CD11b 抗体(均 1∶1 000 稀释)并 4 ℃孵育过夜,用PBS 洗涤后,室温孵育Dylight 488 或657 标记的羊抗兔IgG 荧光Ⅱ抗(均1∶1 000 稀释),荧光显微镜观察染色情况,从至少3 个随机视野采集数字图像进行进一步分析。
2.8 肠组织中 IL-6、IL-1β 和 TNF-α 检测 取肠组织,用10 倍体积冷PBS 匀浆。根据ELISA 试剂盒说明书,对各组匀浆液中IL-6、IL-1β和TNF-α测定。
2.9 Western blot 用含有1 mmol/L 苯甲基磺酰氟的RIPA 裂解缓冲液提取肠组织中总蛋白,然后使用增强BCA蛋白分析试剂盒检测蛋白浓度。每样品取40 μg 组织蛋白通过十二烷基硫酸钠-聚丙烯酰胺凝胶电泳分离并转移到聚偏二氟乙烯膜。用5%脱脂乳封闭 2 h 后,用Ⅰ抗[抗 ZO-1、occuldin、NLRP3、ASC 和 caspase-1 抗体(均 1∶2 000),抗 GAPDH 抗体(1∶8 000)]4 ℃孵育过夜后,TBST 洗膜,然后室温下孵育羊抗兔IgG(1∶1 000)2 h,再次洗涤,用ECL化学发光系统检测蛋白质条带并进行分析。
3 统计学处理
采用GraphPad Prism 8.0 软件进行统计分析。计量资料用均数±标准差(mean±SD)表示,多组之间比较采用单因素方差分析,组间均数两两比较采用Bonferroni校正的t检验。以P<0.05为差异有统计学意义。
结 果
1 SchA 增高IBS-D 大鼠痛觉阈值并改善肠粘膜的形态
AWR 试验结果显示,与对照组比较,模型组AWR 阈值显著增高(P<0.01);与模型组比较,SchA组AWR 阈值显著降低(P<0.05),见图1A。大鼠肠切片HE 染色结果显示,对照组肠绒毛完整,绒毛上皮细胞排列整齐;模型组肠绒毛结构破坏且长度缩短,绒毛上皮同样遭受破坏;SchA治疗组肠绒毛损伤减轻,排列趋向整齐,见图1B。
2 SchA改善IBS-D大鼠肠屏障功能
与模型组比较,SchA 组大鼠外周血中FITC-dextran 显著降低(P<0.01);同时免疫组化和 Western blot结果显示,SchA 能显著抑制IBS-D 大鼠肠组织中ZO-1和occludin的蛋白表达(P<0.01),见图2。
3 SchA降低IBS-D大鼠结肠黏膜细胞凋亡
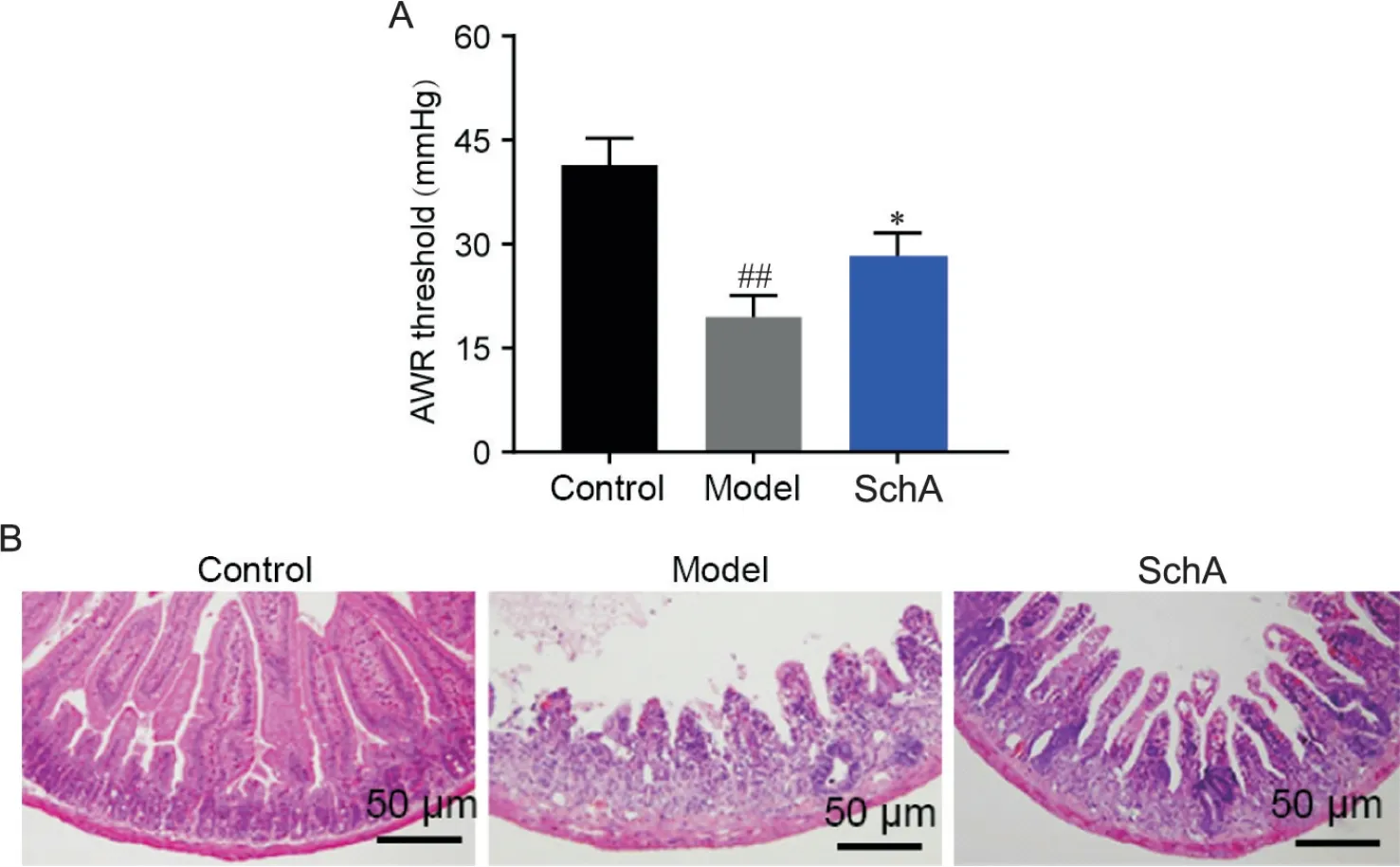
Figure 1. SchA increased pain threshold and improved histomorphological changes of colonic mucosa in IBS-D rats. A:AWR pain threshold;B:histomorphological changes of colonic mucosa(HE staining,scale bar=50 μm). Mean±SD. n=10.##P<0.01 vs control group;*P<0.05 vs model group.图1 SchA增高IBS-D大鼠的疼痛阈值并改善结肠黏膜的组织学形态

Figure 2. SchA improved colonic mucosal barrier function in IBS-D rats. A:the content of FITC-dextran in peripheral blood;B:protein expression of ZO-1 and occludin in colon tissue was detected by immunohistochemistry(scale bar=50 μm);C:protein expression of ZO-1 and occludin in colon tissue was detected by Western blot. Mean±SD. n=10.##P<0.01 vs control group;**P<0.01 vs model group.图2 SchA改善IBS-D大鼠结肠黏膜屏障功能
与对照组比较,模型组大鼠结肠黏膜中TUNEL和cleaved caspase-3 阳性细胞比例均显著增加(P<0.01);与模型组比较,SchA 组结肠黏膜中 TUNEL 和cleaved caspase-3 阳性细胞比例均显著降低(P<0.01),见图3。
4 SchA减轻IBS-D大鼠肠炎

Figure 3. SchA reduced the apoptosis of colonic mucosal cells in IBS-D rats. Mean±SD. n=6.##P<0.01 vs control group;**P<0.01 vs model group.图3 SchA降低IBS-D大鼠结肠黏膜细胞凋亡
免疫荧光显示,模型组结肠黏膜中大量炎症细胞聚集(CD68 和CD11b 分别标记巨噬细胞和中性粒细胞);而SchA 组结肠黏膜中炎症细胞数量减少,见图4A。ELISA结果显示,模型组结肠组织中IL-6、IL-1β 和TNF-α 水平较对照组均显著升高(P<0.01);而SchA 组中上述炎症因子较模型组均显著降低(P<0.01),见图4B。
5 SchA 抑制 IBS-D 大鼠结肠组织 NLRP3 炎症小体通路
与对照组比较,模型组大鼠结肠组织中NLRP3、ASC 和caspase-1 的表达水平均显著增加(P<0.01);与模型组比较,SchA 组结肠中NLRP3、ASC 和caspase-1的表达水平均显著降低(P<0.01),见图5。
讨 论
IBS-D 属于肠道功能性疾病,是中医药治疗的传统优势领域[18]。因此,从中药宝库中开发较理想的治疗IBS-D 的药物将有着十分广阔的应用前景。SchA是从中药五味子干燥成熟果实提取物中的一种木脂素类化合物,其是五味子的主要有效成分之一[19],已被证实其在动物模型中有明显的抗结肠炎作用[9-12]。本研究结果也显示,SchA 在 IBS-D 模型大鼠中具有抗肠炎和保护肠黏膜的作用。
包含IBS-D 在内的多种肠道疾病的发生和发展中均伴随着肠粘膜屏障破坏,且肠粘膜屏障功能的缺陷能导致肠道对微生物群的免疫反应增强进而加剧肠道炎症反应[7-8]。因此,恢复肠屏障功能被认为是治疗IBS-D 的一种潜在的治疗策略[20]。肠屏障功能主要取决于肠道上皮屏障结构的完整性。其中,肠道上皮细胞活性以及肠上皮细胞间紧密连接蛋白的紧密表达分布是维持肠道物理屏障的关键因素[6]。众多研究已经证实,降低肠道黏膜上皮细胞的凋亡,改善肠上皮结构以及增加紧密连接蛋白的表达并改善分布能减轻多种炎性肠病[21-23]。为探讨SchA 对IBS-D 模型大鼠的肠屏障功能的影响,本研究进而观察了SchA 对肠道黏膜结构、肠道黏膜上皮细胞凋亡以及肠道黏膜中紧密连接蛋白(包括occludin 和 ZO-1)表达的影响,与预期一致,SchA 能改善IBS-D 模型大鼠肠粘膜结构,降低肠黏膜细胞凋亡并增加肠道黏膜中occludin 和ZO-1 表达,这些结果证实了SchA 对IBS-D 模型大鼠的肠黏膜屏障具有保护作用。

Figure 4. SchA reduced intestinal inflammation in IBS-D rats. A:CD68 and CD11b(markers of macrophages and neutrophils,respectively)staining images of colon mucosa tissues(scale bar=50 μm);B:the levels of IL-6,IL-1β and TNF-α in colon tissues. Mean±SD. n=10.##P<0.01 vs control group;**P<0.01 vs model group.图4 SchA减轻IBS-D大鼠肠炎
在证明其疗效后,本研究进一步探讨了SchA 在IBS-D 模型大鼠中发挥肠黏膜屏障保护作用的潜在机制。肠道炎症反应的过度激活被认为是发生IBSD 的主要原因之一。另外,肠道炎症反应的过度激活也能导致肠粘膜屏障功能的破坏[7-8]。NLRP3炎症小体可通过caspase-1 和ASC 激活调节先天免疫反应,其中调节IBS肠道炎症反应和肠粘膜屏障功能中起着关键作用。已有研究表明,在多种类型的肠损伤动物模型中,降低肠道NLRP3 炎症小体通路活性能降低肠道炎症和恢复肠粘膜屏障功能[24-25]。且已有研究显示,SchA 对NLRP3 炎症小体活性具有明显的抑制作用[26]。本研究在IBS-D 模型大鼠中也证实了SchA 可抑制肠道NLRP3炎症小体信号通路,提示SchA 在IBS-D 模型大鼠中发挥抗肠炎和维持肠粘膜屏障功能的作用至少部分与其抑制NLRP3炎症小体信号通路有关。
综上所述,本研究结果表明,SchA 在IBS-D 模型大鼠中具有抗肠炎和减轻肠粘膜屏障障碍的作用,且其作用在一定程度上与其抑制NLRP3炎症小体信号通路有关。

Figure 5. Effect of SchA on NLRP3 inflammasome pathway. Western blot was used to detect NLRP3,ASC and caspase-1 expression levels in colon tissues. Mean±SD. n=6.##P<0.01 vs control group;**P<0.01 vs model group.图5 SchA对NLRP3炎症小体通路的影响

