基于UHPLC-QE Plus-MS/MS法分析柴黄颗粒及柴胡中化学成分
陈 晶,傅欣彤,陈有根,郭洪祝
基于UHPLC-QE Plus-MS/MS法分析柴黄颗粒及柴胡中化学成分
陈 晶,傅欣彤,陈有根,郭洪祝*
北京市药品检验研究院 国家药品监督管理局中成药质量评价重点实验室中药成分分析与生物评价北京市重点实验室 北京 102206
基于UHPLC-QE Plus-MS/MS方法分析柴黄颗粒以及柴胡的化学成分,明确其质量特征。以5%氨甲醇溶液超声提取,采用Luna Omega色谱柱(100 mm×2.1 mm,1.6 μm),以乙腈-0.1%甲酸溶液进行梯度洗脱,体积流量0.3 mL/min。电喷雾离子源(ESI),负离子模式下采集。根据精确相对分子质量以及二级离子碎片信息,结合相对保留时间,通过查阅文献以及和对照品比对,进行成分指认。鉴定出柴胡药材中化合物50个;柴黄颗粒中71个化合物,其中36个峰归属于黄芩,33个归属于柴胡。建立的方法能快速、准确分析柴黄颗粒和柴胡化学成分,归纳各主要成分裂解规律,并通过与两者成分比较,发现柴胡配伍前后化学成分的变化,提示柴黄颗粒及柴胡中的质控成分。
柴黄颗粒;柴胡;黄芩;UHPLC-QE Plus-MS/MS;柴胡皂苷v;柴胡皂苷p;柴胡皂苷a;野黄芩苷
柴胡为方中君药,主要有皂苷、挥发油、香豆素、甾醇类成分,黄芩含多种黄酮类衍生物。虽然柴胡黄芩这组药对所含化学成分较多,但目前多集中于对柴胡皂苷a、d和黄芩苷的研究,对于柴胡煎煮前后皂苷成分的整体变化则更鲜有报道。本研究通过液质联用对柴黄颗粒中的化学成分进行分析,因柴胡中具有13, 28-氧环的三萜类化合物,其结构不稳定,在制剂加工过程中易断裂生成次生物,故增加柴胡药材的化学成分分析,通过中成药与药材中化学成分的比对,推断配伍前后皂苷类成分变化规律,从整体上反映物质基础,为实现柴黄颗粒整体控制质量提供依据。
1 仪器与材料
1.1 仪器
超高效液相色谱串联质谱Ultimate 3000/Q Exactive Plus(Thermo公司);DTC-27J型超声波清洗器,湖北鼎泰恒胜科技设备有限公司。
1.2 材料
乙腈为色谱纯(Thermo Fisher),甲酸为质谱级,其它试剂为分析纯。水为屈臣氏蒸馏水。柴胡(北柴胡)对照药材(批号120992-201509)由中国食品药品检定研究院提供。对照品柴胡皂苷a(批号110777- 201912,质量分数94.8%)、柴胡皂苷d(批号110778-201912,质量分数96.3%)、野黄芩苷(批号110842-201709,质量分数91.7%)、黄芩苷(批号110715-201821,质量分数95.4%)、汉黄芩苷(批号112002-201702,质量分数98.5%),为中国食品药品检定研究院提供;柴胡皂苷i(批号DST191109-015,97%),柴胡皂苷b1(批号DST200409-009,质量分数98%),柴胡皂苷b2(批号DST191020-010,质量分数98%),柴胡皂苷c(批号DST191118-007,质量分数98%),柴胡皂苷g(批号DST191118-016,质量分数98%),柴胡皂苷h(批号DST191118-014,质量分数98%),柴胡皂苷f(批号DST191118-013,质量分数98%),柴胡次苷D(批号DST191118-203,质量分数98%),由乐美天医药|德斯特生物提供;尼泊柴胡皂苷k(批号7285,质量分数98%),由NATURE STANDARD提供。柴黄颗粒(批号20191003)购自河南灵佑药业股份有限公司。
2 方法
2.1 色谱条件
2.1.1 色谱条件 十八烷基硅烷键合硅胶柱(Luna Omega色谱柱(100 mm×2.1 mm,1.6 μm),以0.1%甲酸溶液为流动相A,乙腈为流动相B,梯度洗脱(0~3 min,20%→30%B;3~15 min,30%→35%B;15~30 min,35%→65%B;30~35 min,65%→90%B;35~40 min,90%→100%B),体积流量0.3 mL/min,柱温30 ℃,进样量0.5 μL。
2.1.2质谱条件电喷雾(ESI)源,离子源温度:300 ℃,鞘气体积流量40 arb,辅助气体积流量10 arb,扫描范围/150~1200,负离子全扫模式电压3 kV。
2.2 溶液的制备
2.2.1 柴胡药材溶液的制备 精密称取柴胡对照药材0.5 g,加5%氨甲醇溶液25 mL,超声处理30 min,滤过,即得。
基于椒江流域土壤数据,参考梁音等[12]关于我国长江以南东部丘陵地区K因子的研究,完成不同土壤类型K值的赋值.通过查阅文献[13-16],选取与椒江流域自然地理相似区域C、P因子的研究成果,用于流域土壤侵蚀估算.
2.2.2 柴黄颗粒溶液的制备 精密称取柴黄颗粒样品(相当于柴胡药材0.5 g)0.08 g,加5%氨甲醇溶液25 mL,超声处理30 min,滤过,即得。
3 结果
用UHPLC-QE Plus-MS/MS负离子模式分析柴胡和柴黄颗粒5%氨甲醇溶液的质谱总离子流图,如图1所示。因为黄芩中黄酮类成分含量与柴胡中三萜类成分含量不在同一个数量级,在同一张图谱上不能完全反映出来,故根据两者相对分子质量以荷质比660为分界在2个图中展示。查阅大量柴胡、黄芩的文献,建立相应的化学成分数据库,根据准分子离子得到其可能的分子式(误差范围±5×10−6),通过与TCMSP数据库及本实验室建立的数据库鉴定识别其成分。个别化合物经过了对照品进行指认。共识别出柴胡中50个化合物,柴黄颗粒中71个化合物,结果见表1、2。
3.1 柴胡中化合物的质谱裂解规律分析
3.1.1 四糖三萜皂苷类 3号峰负离子/1 151.550 9 [M+HCOO]−,其可能的分子式为C53H86O24,二级碎片中791.42、629.37响应值较高,分别为失去-H2O-CO-xyol-glc-H2O,进而再丢失1个六碳糖葡萄糖所得,/483.31是脱掉1个甲基五碳岩藻糖。通过其裂解规律结合文献报道[1],鉴定为柴胡皂苷v。
3.1.2 三糖三萜皂苷类 6号峰与3号峰的二级碎片相同,其一级质谱中分子离子以[M+HCOO]−存在,/为989.498 17,与柴胡皂苷v相差162即1个六碳糖,查阅文献报道[2]确定为柴胡皂苷v-1。
峰5、11、19的一级质谱中分子离子荷质比为1 003.512 51、1 003.514 95、1 003.514 59,软件推测其分子式均为 C48H78O19,但二级碎片峰不同,峰2/957.50 [M-H]−丢失1个甲基五碳糖形成/811.46 [M-H-rha]−,再丢失1个六碳糖形成/649.39[M-H-rha-glc]−,或者先丢失1个六碳糖形成/795.47[M-H-glc]−,再丢失1个甲基五碳糖形成/649.39 [M-H-glc-rha]−,在/649.39基础上丢失1个六碳糖成/487.34,由此推出3个糖是以支链形式与苷元结合,且甲基五碳糖外侧不再与其它糖基结合,查阅文献报道[3-5]归属了5号峰为柴胡皂苷q,同理归属11号峰为30-β吡喃葡萄糖-30-羟基柴胡皂苷b2,19号峰为柴胡皂苷p。

图1 柴黄颗粒LC-MS/MS基峰离子流图(提取范围170~660,A;提取范围660~1200,B) 及柴胡LC-MS/MS基峰离子流图(C)

表1 柴胡中化学成分鉴定结果

续表1
*经对照品确认的化合物,表2同
*compounds identified by reference standards, same as table 2

表2 柴黄颗粒中化学成分鉴定结果
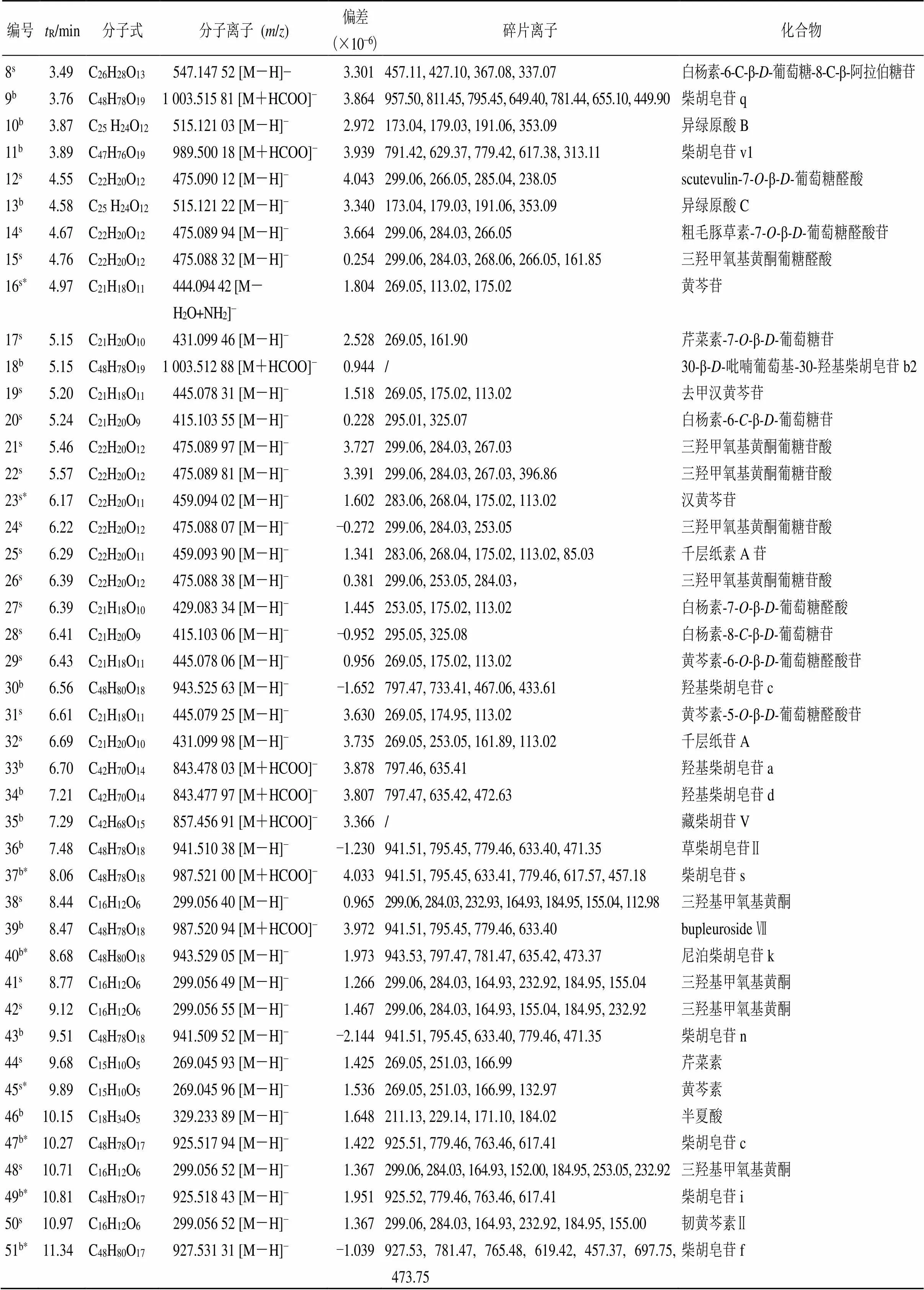
续表2

续表2
s-来源于黄芩 b-来源于柴胡
s-souce ofb-souce of
12号峰通过精确相对分子质量/1 005.529 42 [M+HCOO]−确定其分子式为C48H80O19,根据碎片离子峰/959.52、797.47、635.42、487.34可得出其依次脱掉1个甲酸、2个六碳糖葡萄糖、1个甲基五碳岩藻糖和2个氢,查阅文献报道[6],与11α,16β,23,28-四羟基齐墩果烷-12-烯-3β吡喃岩藻糖基(3→1)-β葡萄糖基(2→1)-β葡萄糖苷一致。
13号峰与18号峰通过精确相对分子质量确定分子式为C48H80O18,裂解规律相同,查阅的文献[7-8]中,羟基柴胡皂苷c和尼泊柴胡皂苷k吻合,峰13出峰时间早,极性大,所以应该对应羟基柴胡皂苷c,峰18对应尼泊柴胡皂苷k,且在相同质谱条件下与尼泊柴胡皂苷k的保留时间和裂解规律一致,验证了推断结果。
14、15、17号峰[M+HCOO]−分子离子峰质荷比为843.476 26、843.476 50、43.477 05,软件推断的化学式相同即为C42H70O14,都出现[M-H-162]−碎片离子,14号峰与15号峰出现 [M-H-162-146-146-18]−、[M-H-162-146-146-18-1]−碎片离子,在丢掉1个六碳糖与甲基五碳糖基础上又失去了1个水,与羟基柴胡皂苷a、d裂解模式相同,16位连有β-OH的羟基柴胡皂苷a极性大于连有α-OH键的羟基柴胡皂苷d,故根据保留时间可确定对应化合物。17号峰碎片离子/456.73是在丢失2个糖之后再断裂1个羟甲基形成的,与文献报道[9]中的bupleurosideXIII裂解规律相同。
同理推算,根据精确相对分子质量和裂解规律结合文献报道[10-12],推算出16、20、22、23、24和37号峰,且20、22号峰与相应的对照品出峰时间和二级碎片一致,结果详见表1。
3.1.3 二糖三萜皂苷类 25号峰/825.464 97 [M+HCOO]−,其响应值与39号峰都非常高,脱掉HCOOH得到准分子离子779.46,再脱去1个葡萄糖(glc)和岩藻糖(fuc)得到617.41、471.35离子,其保留时间和裂解规律与柴胡皂苷a对照品相一致,确定25号峰为柴胡皂苷a,同理确定27、33、39号峰分别为柴胡皂苷b2、柴胡皂苷g、柴胡皂苷d。
26、29、31、40、41、42号峰通过准分子离子峰/865.461 12、865.460 82、865.459 84、865.460 75、865.460 39、865.459 47 [M-H]−分析其分子式均为C45H70O16,其裂解碎片中有脱落丙二酸单酰基的碎片,其他碎片峰与25号峰相近,根据文献报道[13],确认31号峰为6′′--丙二酸单酰柴胡皂苷a,42号峰为6′′--丙二酸单酰柴胡皂苷d,26、29、40、41号峰为丙二酸单酰基与柴胡皂苷a/d中糖基的其他位置结合形成,因具体位置不确定,统称为丙二酸单酰柴胡皂苷a/d。同理推测峰28、30、32、38、43、44、45、48为乙酰柴胡皂苷a或d,再结合其极性判断是葡萄糖上2、3、4、6位分别被乙酰基取代。峰49、50为二乙酰基柴胡皂苷a或d,因取代位置可能性太多[14],未能确定具体取代位置,因此命名时也未明确标注取代位置。
36号峰/809 [M+HCOO]−,碎片峰为763 [M-H]−、601 [M-H-glc]−,均比柴胡皂苷a少1个氧,查阅文献报道[15]确认为柴胡皂苷e。
3.1.4 单糖三萜皂苷类 34、35、46号峰一级质谱以[M+HCOO]−形式存在,质荷比分别为663.412 54、663.413 21、663.412 60,碎片离子[M-H]−均为617.41,比对柴胡药材和柴黄颗粒中/663提取的峰,结合醚键煎煮后结构发生改变的规律,再参考文献数据[16],确认34号峰为柴胡次皂苷F,35号峰是46号峰柴胡次皂苷G的醚键断裂产物柴胡次皂苷D。47号峰不饱和度值比38号峰大1,说明双键数目要多1个,根据文献数据[16]确认为柴胡次皂苷I。
3.1.5 非三萜皂苷类 7,9,10号峰通过荷质比确定分子式均为C25H24O12,其裂解规律相似,均为丢失1个咖啡酰基得到/353.09碎片峰,继而再丢失1个咖啡酰基得到/191.06碎片峰,或者丢失奎宁酸得到/179.03碎片峰,/173.04峰是/191.06碎片峰失去1个水分子所得,推断为苯丙素类化合物异绿原酸,依据其极性[17-18]确定具体归属。21号峰半夏酸[19]分子离子峰/329.233 64 [M-H]−,分子式为C18H34O5,不饱和度仅为2,提示可能为不饱和羟基脂肪酸,/229.14为丢失戊酸所得,去掉丁烷得/171.10,去掉1个水分子得/211.13。黄酮类成分裂解规律同黄芩中的黄酮类成分。
3.2 柴黄颗粒中化合物的质谱裂解规律分析
3.2.1 柴胡中三萜皂苷类成分 成药中柴胡是水煎煮后入药,在煎煮过程中,13,28-氧环不稳定,醚键会断裂生成次生物[10,20-22]。如柴胡皂苷a转化成柴胡皂苷b1和柴胡皂苷g,柴胡皂苷d转化成柴胡皂苷b2。6′′--乙酰柴胡皂苷a转化成6′′--乙酰柴胡皂苷b1,6′′--乙酰柴胡皂苷d转化成6′′--乙酰柴胡皂苷b2。草柴胡皂苷Ⅱ醚键断裂成烯键形成的化合物为柴胡皂苷n,其同分异构体16--草柴胡皂苷Ⅱ则转换成柴胡皂苷s。柴胡皂苷c生成柴胡皂苷h和柴胡皂苷i,柴胡次皂苷F断裂成柴胡次皂苷H和柴胡次皂苷A。以柴胡皂苷c为例,醚键断裂规律见图2,二级裂解碎片及裂解规律见图3。药材与成药中皂苷类成分比对见表3,部分未检出可能因为含量过低。
3.2.2 黄芩中黄酮类成分 碳苷类成分查阅文献报道[23-24],负离子质谱中六碳黄酮碳苷二级碎片中会出现[M-H-60]−、[M-H-90]−、[M-H-120]−离子峰,五碳黄酮碳苷的二级谱图中只能产生脱掉60和90的碎片峰。3号峰负离子一级质谱中准分子离子峰为/547.147 34 [M-H]−,二级碎片峰457.12 [M-H-90]−、427.10 [M-H-120]−、487.13 [M-H-60]−、367.08 [M-H-120-60]−/[M-H-90-90]−、337.07 [M-H-120-90]−说明掉了1个六碳糖和五碳糖,二级碎片及裂解规律见图4,通过比对文献数据[25],推测3号峰为白杨素-6--α--阿拉伯糖-8--β葡萄糖苷,同理推断4~6、8、20、28号峰的归属。

图2 柴胡皂苷c转化成柴胡皂苷h和柴胡皂苷i示意图

图3 柴胡皂苷c裂解过程
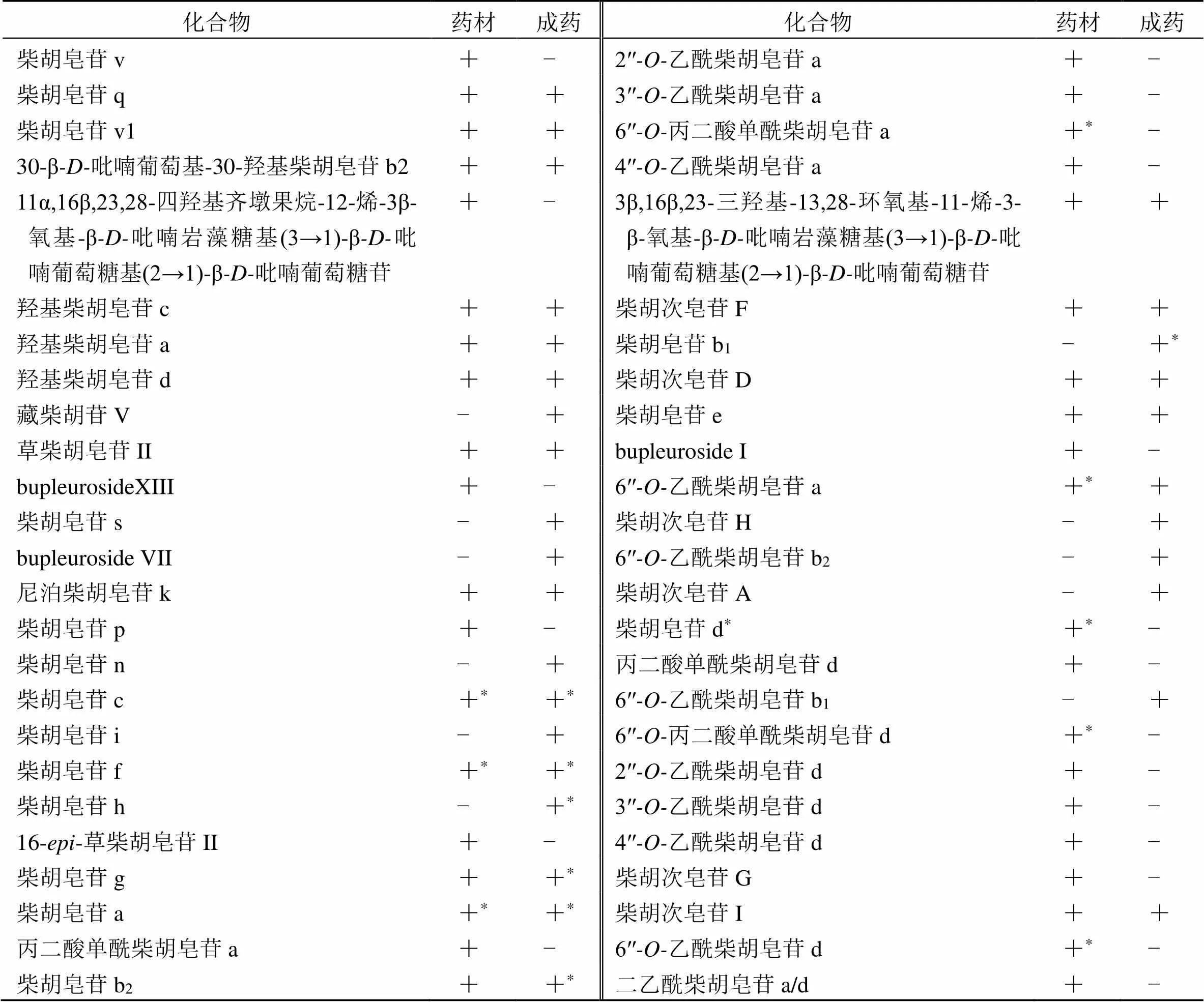
表3 柴胡药材及柴黄颗粒中皂苷类成分组成
“−”未检出,“+”含量低,“+*”含量高
“−” trace, “+”low, “+*” high

图4 白杨素-6-C-葡萄糖-8-C-阿拉伯糖苷裂解过程
葡萄糖醛酸苷类成分葡萄糖醛酸苷类成分二级质谱中有一响应值很高的丢失葡萄糖醛酸的苷元离子,部分可看到脱水分子。如野黄芩苷准分子离子峰/461.073 52 [M-H]−,根据精确相对分子质量确定分子式为C21H18O12,二级碎片离子285.04分别是丢失1分子葡萄糖醛酸和1分子水得到。黄芩提取物中黄芩苷含量高于85%,在5%氨甲醇溶液中黄芩苷的分子离子峰为丢失2个氢所得,二级碎片峰269.05比野黄芩苷碎片离子285.04少1个氧,结构式中应该少1个羟基,其保留时间和碎片离子峰与对照品一致,确定为黄芩苷。对于相对分子质量形同的同分异构体,如19、29、31号峰,查阅文献报道[26-28],再根据结合位置极性大小,在反相柱中的出峰时间确定其具体归属。对于不确定具体取代位置的,则统一命名,如三羟甲氧基黄酮葡糖醛酸。
葡萄糖苷类成分17号峰与32号峰依据其精确相对分子质量推断出分子式为C21H20O10,二级质谱中都有/269.05 [M-H-glc]−碎片离子,也相应能观察到葡萄糖碎片,检索TCMSP数据库,再结合其极性,推断17号峰为芹菜素-7--β葡萄糖苷,32号峰为千层纸苷A。
黄酮苷元类成分黄酮苷元为黄酮类成分,多遵循RDA裂解规律,如黄芩素269.045 96 [M-H]−,脱去1分子水后得到/251.03碎片峰,分子离子峰通过RDA裂解方式得到碎片峰166.99和133.97,然后在黄酮本体(119、101)基础上,根据2个碎片峰的相对分子质量推算出各环上连接的基团,167比119多48,所以A环上连有3个羟基,133是167脱去2个羟基所得。分子离子峰269去掉167后是102,比101多1,B环上未连有其他基团。
3.3 辅料
柴黄颗粒总离子流图中0.74 min和1.15 min的2个峰响应值最高,且质荷比较小,1号峰一级谱图显示[M+HCOO]−峰,二级碎片有去氢准分子离子峰341.11,单糖峰179.06、161.04以及单糖断裂碎片峰119.03、89.02,根据其裂解规律及对照品定位确定为蔗糖,蔗糖在柴胡药材中有少量存在,本实验室依据样品中柴胡的提取方式制备柴胡提取物,发现蔗糖转移率低,对比后确定大部分蔗糖是作为辅料加入。2号峰/[M-Na]−178.053 1,二级谱图中有亚硫酸根离子峰79.96以及去掉1个氧的161.89碎片离子,与文献报道[29]中甜蜜素的裂解规律相同,与甜蜜素对照品保留时间与裂解规律一致,明确为甜蜜素,同时与该企业产品说明书中标明加入的2种甜味剂蔗糖和甜蜜素相吻合。
3.4 质量特征成分
对柴黄颗粒及柴胡药材中的化学成分分析,共识别出柴胡中50个化合物,其中皂苷类42个、苯丙素类4个、黄酮类成分3个及羟基不饱和脂肪酸1个,柴黄颗粒中71个化合物,36个归属于黄芩、33个归于柴胡、11个皂苷类成分相对药材有明显检出,该方法对柴黄颗粒及其中柴胡药味中的成分可以在较短时间内得到很好分离。
从分析结果可以看出,柴黄颗粒化学成分中来自黄芩提取物的成分以黄芩苷为主要代表,均以原形存在,组成基本稳定,黄芩苷在现行质量标准中已经作为质控成分,此外汉黄芩苷、黄芩素、汉黄芩素也可纳入质控范围;从表3柴胡药材及成药中皂苷类成分存在情况判断,来自柴胡中的原型皂苷类成分柴胡皂苷a、f、c,伴随次生皂苷类成分柴胡皂苷b1、b2、h、g,可以作为柴黄颗粒整体质量控制的指标成分组合。柴胡皂苷c、f、a、d,6′′丙二酸单酰柴胡皂苷a、d,6′′乙酰柴胡皂苷a、d可以作为柴胡药材的质控指标性成分,其中6′′丙二酸单酰柴胡皂苷a、d可以用来衡量柴胡药材储存时间长短。
4 讨论
柴胡中具有醚键的皂苷成分不稳定,加入氨可以中和植物中酸,防止皂苷次生化[30],因此为了真实反映柴胡原药材与水煎煮后柴黄颗粒中皂苷类成分,选取药典中柴胡含量测定项下的提取溶剂,即含5%浓氨试液的甲醇溶液进行提取。
柴黄颗粒组方简单,只有柴胡和黄芩提取物两味药,柴胡中的三萜皂苷和黄芩中的黄酮氧苷类成分裂解规律相似,都是苷键易断裂,黄酮碳苷类因为碳苷键较稳定,多从糖基内部断裂,黄酮苷元多遵循RDA裂解规律。
对柴胡药材与成药中成分进行比较时发现,柴胡中有醚键的三萜成分,16位是β-OH的稳定性远大于α-OH,α型醚键原型成分在成药中较难检出。醚键三萜转化成11,13-双烯结构成分要多于9,12-双烯结构,对于部分文献报道的转化成11-甲氧基,12-烯结构,并未检出,可能因为再加甲氧基相对自身双键转化阻力更大。葡萄糖上连有丙二酸酰基的皂苷类在成药中可能因含量过低未有检出,推测其在药材储存和煎煮过程中,酯键断裂,生成柴胡皂苷a/d或其次生产物。
本实验对柴黄颗粒和柴胡的基础成分做了鉴别,尤其对柴胡水煎后入药成分变化以及变化规律做了分析,初步明确了质控指标性成分组合,为柴黄颗粒和柴胡的整体质量控制提供了依据。
利益冲突 所有作者均声明不存在利益冲突
[1] 梁鸿, 赵玉英, 白焱晶, 等. 柴胡皂甙v的结构鉴定 [J]. 药学学报, 1998, 33(4): 282-285.
[2] Liu Q X, Liang H, Zhao Y Y,. Saikosaponin v-1 from roots ofDC. [J]., 2001, 3(2): 139-144.
[3] 罗何生, 赵玉英, 马立斌, 等. 柴胡皂甙q及其甙元的结构鉴定 [J]. 药学学报, 1995(6): 435-439.
[4] 罗何生, 赵玉英, 乔梁, 等. 柴胡皂甙 p的结构鉴定 [J]. 植物学报, 1996, 38(11): 910-913.
[5] Seto H, Ōtake N, Luo S Q,. Isolation of triterpenoid glycosides (saikosaponins) fromand their chemical stmctures [J]., 1986, 50(4): 943-948.
[6] Pistelli L, Bilia A R, Marsili A,. Triterpenoid saponins from[J]., 1993, 56(2): 240-244.
[7] Ebata N, Nakajima K, Hayashi K,. Saponins from the root of[J]., 1996, 41(3): 895-901.
[8] Hinako Ishiguro, Miwa Takeuchi, Akira Namera,. Studies on medicinal plant resources of the Himalayas、Chemical evaluation ofvar.collected in Nepal [J]., 2001, 55(2): 55-60.
[9] Matsuda H, Murakami T, Ninomiya K,. New hepatoprotective saponins, bupleurosides III, VI, IX, and XIII, from Chinese: Structure- requirements for the cytoprotective activity in primary cultured rat hepatocytes [J]., 1997, 7(17): 2193-2198.
[10] Ding J K, Fujino(nee Kimata) H, Kasai R,. Chemical evaluation ofspecies collected in Yunnan, China [J]., 1986, 34(3): 1158-1167.
[11] 方伟, 杨印军, 郭宝林, 等. 藏柴胡中三萜皂苷类成分的研究 [J]. 中国中药杂志, 2016, 41(7): 1251-1256.
[12] 贾琦, 张如意. 柴胡属植物中皂甙化学研究进展 [J]. 药学学报, 1989, 24(12): 961-971.
[13] Ebata N, Nakajima K, Hayashi K,. Saponins from the root of[J]., 1996, 41(3): 895-901.
[14] Seto H, Kawai H, Ōtake N,. Structures of new saponins isolated fromY. Li et S. L. pan [J]., 1986, 50(6): 1613-1620.
[15] Huang H Q, Zhang X, Lin M,. Characterization and identification of saikosaponins in crude extracts from threespecies using LC-ESI-MS [J]., 2008, 31(18): 3190-3201.
[16] 魏晓萌. 锥叶柴胡化学成分及质量控制方法研究 [D]. 北京: 北京中医药大学, 2018.
[17] 段慧芳, 吴啟南, 朱亚莹, 等. UPLC同时测定不同产地金银花中10种成分 [J]. 中草药, 2019, 50(23): 5858-5864.
[18] 郭敏娜, 刘素香, 赵艳敏, 等. 基于HPLC-Q-TOF-MS技术的柴胡化学成分分析 [J]. 中草药, 2016, 47(12): 2044-2052.
[19] 史月姣, 王瑛, 朱惠照, 等. LC-MS快速分析紫苏水煎液中的主要化学成分 [J]. 药物分析杂志, 2015, 35(8): 1417-1423.
[20] 谭利, 赵玉英, 王分, 等. 柴胡皂甙s的结构鉴定 [J]. 植物学报, 1998(2): 176.
[21] 张如意, 陈喜奎, 杨宪斌, 等. 柴胡皂甙m和柴胡皂甙n的结构鉴定 [J]. 药学学报, 1994, 29(9): 684-688.
[22] Shimizu K, Amagaya S, Ogihara Y. New derivatives of saikosaponins [J]., 1985, 33(8): 3349-3355.
[23] 吴新安, 都模勤. 黄酮碳苷类化合物ESIMS-MS裂解规律初探 [J]. 天然产物研究与开发, 2011, 23(6): 1085-1087.
[24] 杨悦, 刘颖, 刘晓谦, 等. 基于超高效液相色谱串联质谱技术的山楂核抗菌、抗氧化药效物质基础研究[J]. 世界中医药, 2021, 16(17): 2527-2532.
[25] Zhang F X, Li Z T, Li M,. An integrated strategy for profiling the chemical components ofand their exogenous substances in rats by ultra-high- performance liquid chromatography/quadrupole time-of- flight mass spectrometry [J]., 2020, 34(18): e8823.
[26] 龙海林. 黄芩表观型化学组成特征及其在基源鉴定中的应用研究 [D]. 北京: 北京协和医学院, 2014.
[27] 周丹丹, 邹秦文, 林瑞超. 基于超高效液相色谱-四级杆-静电场轨道阱质谱的胃复春片化学成分研究[J].世界中医药, 2020, 15(13): 1841-1848.
[28] 柴冲冲, 曹妍, 毛民, 等. 基于HPLC特征图谱、UPLC-Q-TOF/MS定性及多成分定量的黄芩酒炙前后化学成分变化研究 [J]. 中草药, 2020, 51(9): 2436-2447.
[29] 李云飞, 殷红, 杨玲春, 等. 超高效液相色谱-四极杆/静电场轨道阱高分辨质谱快速测定食品中6种甜味剂 [J]. 环境化学, 2016, 35(8): 1737-1740.
[30] 闵宇航, 王京辉, 范妙璇, 等. 柴胡饮片皂苷类成分变化及质量控制研究 [J]. 药物分析杂志, 2014, 34(5): 836-843.
Analysis of chemical constituents of Chaihuang Granules by UHPLC-QE Plus-MS/MS
CHEN Jing, FU Xin-tong, CHEN You-gen, GUO Hong-zhu
NMPA Key Laboratory for Quality Evaluation of Traditional Chinese Patent Medicine, Beijing Key Laboratory of Components Analysis and Biological Evaluation on Chinese Medicine, Beijing Institute for Drug Control, Beijing 102206, China
To analyze and identify the chemical components and characteristic components of Chaihuang Granules (柴黄颗粒) and Chaihu () by UHPLC-QE Plus-MS/MS.The samples were extracted with 5% ammonia-methanol solution by ultrasonic. The analyses was performed on a Luna Omega C18column (100 mm×2.1 mm, 1.6 μm), the mobile phase was acetonitrile−0.1% formic acid solution with gradient elution mode at the flow rate of 0.3 mL/min. Electrospray ion source (ESI) was applied in negative ion mode. The chemical constituents were analyzed by exact relative molecular weight, fragment ion and the relative retention time and comparation with the related literature and reference standards.A total of 50 chemical compounds were identified from, 71 chemical compounds in Chaihuang Granules were identified, among which 36 compounds were attributed to Huangqin ()and 33 compounds were attributed to.The method is fast and highly sensitive for the screening and confirmation of the chemical constituents from Chaihuang Granules and. The fragmentation characteristics were summarized in this paper. By comparing the chemical constituents in Chaihuang Granules and, the chemical composition changes before and after compatibility can be found, which suggested a reference for the quality control components of Chaihuang Granules and.
Chaihuang Granules;;; UHPLC-QE Plus-MS/MS; saikosaponin v; saikosaponin p; saikosaponin a; scutellarin
R284.1
A
0253 - 2670(2022)15 - 4634 - 11
10.7501/j.issn.0253-2670.2022.15.006
2022-03-09
陈 晶(1987—),女,硕士,主管药师,主要从事中药成分分析研究。Tel: 18010281088 E-mail: chenjing4477@163.com
通信作者:郭洪祝,男,博士生导师,主任药师,主要从事中药鉴定、成分分析及药效代谢学研究。Tel: 18010281003 E-mail: guohz@bidc.org.cn
[责任编辑 王文倩]