聚吡咯电化学制备实验的改进
——一个开放式综合实验设计
曾丹黎,张运丰,杜思思,刘凯,刘一诺
中国地质大学(武汉)材料与化学学院,武汉 430078
近年来,π-共轭类有机高分子材料,如聚乙炔、聚苯胺、聚吡咯以及聚噻吩等[1],因其特异的光电性能斩获了来自化学、材料、物理、生物等多个领域科学家的关注,并逐渐在柔性显示、传感、储能以及电磁屏蔽等前沿科技方向上展现出强劲的应用潜力[2]。为使学生领略其作为导电高分子材料的独特魅力,更好地理解共轭、离域、能级、掺杂、氧化还原等抽象概念,共轭聚合物也开始在高等院校相关专业的实验教学中崭露头角。在目前关于共轭聚合物制备的实验教学方案中,以原料廉价易得、导电性能优异的聚苯胺为主[3,4]。然而,吡咯单体毒性极低使得聚吡咯的制备实验安全性更高,因此,不少高校也开始将聚吡咯的制备纳入教学计划。
聚吡咯可采用化学氧化法或电化学氧化法制备,但在教学实验中,通常结合电化学要素在综合实验中展现[5]。电化学制备属于现代合成方法,高效环保,特别适宜作为教学实验进行展示和学习,并且相比于反应时间长、产率低的化学氧化法,电化学制备具有装置简单、用时短、条件易控、产品纯度更高等优点。
通过调研其他高校关于导电高分子电化学制备的已有方案,并在完成本校开展的聚吡咯电化学制备实验后,我们发现单纯的电化学制备其用时短、现象单一、操作性和讨论性不足,导致体验感较差,浪费了一个难得的多学科主题。因此,将激发实验兴趣的元素和引发理论思考的内容融入到创新设计中十分必要。
开放式实验设计是当前教学实验改革的一个突出方向,相比于保守式的任务型实验,开放式实验更能调动学生的动手及思考能力。电化学制备实验给开放式实验设计提供了一个良好的契机——反应快捷以及反应条件多变易控,且与聚吡咯的结构和掺杂状态关联性强,最终反馈于导电性能。因此,我们将开放式实验设计与电导率表征相结合,在原有的方案上进行了丰富和深化:
(1) 实验预习阶段,发送文献供学生学习与讨论,在教师的指导下设计出拟采用的电化学聚合条件:学生可在循环伏安法(CV)、恒电位法、恒电流法、脉冲法等方法上进行选择,同时可搭配不同电位(电流)、反应时间、反应温度、溶液酸度或pH、掺杂剂等条件[6,7]。学生可拟定2–3种反应条件,每种条件仅含有一种变量,每一种变量可设定2–4组变化值。通过这一过程,学生可习得并运用正交实验表辅助实验设计。该阶段教师可在线上开展,符合当前线上线下混合式教学改革设计的理念。
(2) 实验正式进行阶段,按照拟定方案进行聚合实验,得到不同的聚吡咯薄膜,进行编号并测试电导率,通过测试结果发起结果分析与讨论。
(3) 选用导电氧化铟锡(ITO)玻璃作为工作电极,待ITO上沉积出聚吡咯薄膜后,恰好可以在电化学体系中原位通过CV法观察聚吡咯薄膜电致变色现象,并通过该现象深化对共轭聚合物结构与性能的理论认知。
1 实验部分
1.1 实验原理
电化学聚合是在外加电场下,通过调节电化学参数,如电压、电流等,使电解液中单体在惰性电极表面发生氧化偶联而实现。吡咯的结构为含N的五元芳杂环,属于富电子芳杂环,易被氧化聚合。聚合机理如图1所示。简单来讲,吡咯单体首先在电场作用下失去电子,氧化形成阳离子自由基,随后两个吡咯阳离子自由基通过偶联形成二聚体,并放出两个质子,形成中性二聚体;中性二聚体再被氧化形成二聚体阳离子自由基,再与其他自由基反应,逐步使聚合物链增长,如此循环往复便可以得到聚吡咯。

图1 电场作用下吡咯单体的聚合原理示意图
导电高分子具有高度离域的π-共轭主链骨架,但是π电子未受激发时难以在分子链上迁移,导电性能并不理想,甚至不导电。结合无机半导体的掺杂理论,也可对共轭主链进行类似的阴离子(p型,如图2所示)或阳离子(n型)掺杂,掺杂后不仅主链共轭体系有所变化,电导率更是迅速提升,可高达103S·cm-1。相应于掺杂态,未经掺杂的被称为本征态。而在电化学氧化聚合过程中,掺杂过程可认为是“自动”的,因为电解质中的阴离子会对在电场中失去电子的聚合物链发起电荷补偿(图3),最终得到导电薄膜[8]。

图2 聚吡咯的氧化掺杂导电示意图(p型)
聚吡咯具有良好的氧化还原性可逆性能[9],其还原态(本征态)与氧化态(掺杂态)具有不同的共轭体系,能级与能带因而发生变化,呈现出不同的颜色。但在空气中聚吡咯易氧化,只有在特定条件下,比如CV测试中,在较低的电位下才可观察到其呈黄绿色的本征态,同时CV过程中也可以观察到由黄绿色逐渐转变为蓝紫色甚至黑色的现象。图3所示是电致变色机理示意图,与掺杂导电本质上一致,可以认为电致变色是掺杂和去掺杂过程在现象上的具体表达。

图3 电致变色机理示意图
1.2 试剂与材料
本实验中所涉及到的实验药品及相关信息如表1所示。
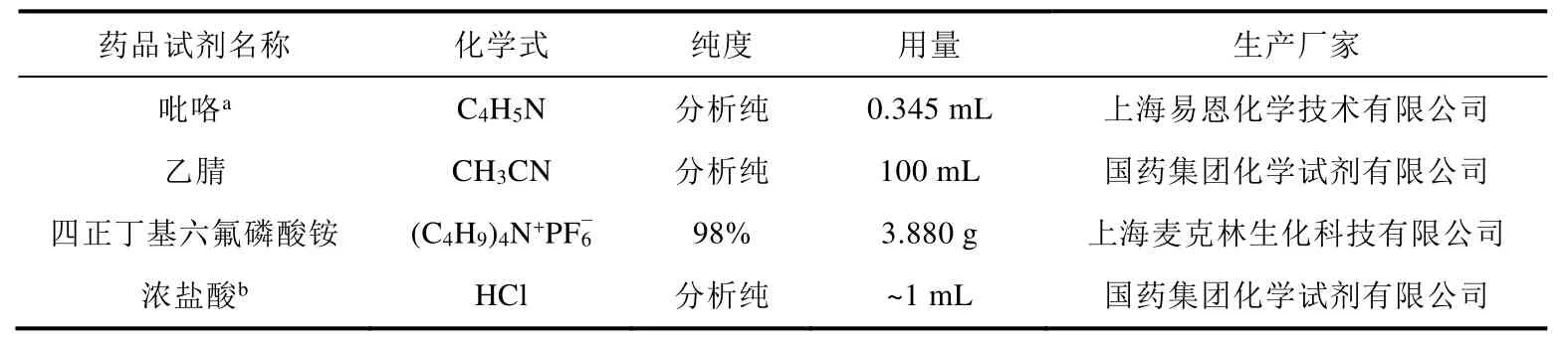
表1 主要实验药品
1.3 仪器和表征方法
100 mL电解池、Pt电极(或者不锈钢片)、ITO导电玻璃(20 mm × 1 mm,12片)、Ag/AgCl参比电极(或者Ag/Ag+电极)、500 μL移液枪、100 mL和250 mL烧杯、100 mL量筒、玻璃滴管、玻璃棒、表面皿、磁子、pH试纸、旋转蒸发仪、螺旋测微仪等。表2为实验主要涉及仪器的信息。

表2 部分实验仪器及设备
电导率测量方法:首先使用螺旋测微仪通过差量法测定聚吡咯薄膜的厚度,将其放于四探针微电阻测量仪上,调整探针高度,使其刺入极片上的聚吡咯(注意不要接触到ITO玻璃的表面),打开软件,在参数界面设置产品厚度,按照软件提示设置合适的电流输出量程,适当调节电流(先粗调后细调)点击测试,任选5个点进行测试,测试完成后,将数据以excel格式导出,并在结果分析中使用平均值。
1.4 实验步骤
1.4.1 配制电解液
称取3.880 g (0.010 mol)四正丁基六氟磷酸铵,用100 mL乙腈溶解于250 mL烧杯中。取出50 mL该溶液放入100 mL小烧杯中,用移液枪移取0.345 mL (0.005 mol)吡咯单体加入该溶液中,搅拌使其混合均匀,倒入电解池中,放入磁子。剩余50 mL电解液放置待用。
1.4.2 搭建三电极体系
将Ag/AgCl电极作参比电极,铂电极作对电极,ITO导电玻璃作工作电极,搭建三电极体系,如图4所示。

图4 三电极体系装置示意图
1.4.3 进行电化学聚合
以恒电位法进行示例。提前打开电化学工作站(CHI)和电脑,工作站需预热半小时。打开CHI的测试软件,点击“方法”,选择“计时电流法”,根据文献报道和实验摸索,调整参数,进行聚合。
(1) 首先选择改变聚合电位,设置电位分别为1.0、1.2、1.4、1.6 V,聚合时间为30 s,聚合温度为室温(25 °C),每完成一次聚合,小心将沉积有聚吡咯的ITO玻璃取下,并进行编号标记为①、②、③、④。
(2) 改变温度,固定聚合电位为1.4 V,聚合时间为30 s,使用冰浴和加热分别在0 °C和40 °C进行聚合,样品编号标记为⑤、⑥。
(3) 改变酸度,即通过加入酸来调节溶液的pH,同样固定聚合电位为1.4 V,聚合时间为30 s。可以使用盐酸、稀硫酸、磷酸以及有机磺酸来进行调节,我们以盐酸进行示例。已知初始配制溶液为中性,在电解液恢复至室温后,往电解液中缓慢加入0.001 mol·L-1稀盐酸(~1滴),用pH试纸进行检测,调节pH至6,进行聚合,样品编号标记为⑦;接着调节pH分别至5 (约0.5 mL稀盐酸)和4 (约5 mL稀盐酸),进行聚合,样品编号分别记为⑧和⑨。
同样地,可通过恒电流法(推荐电流范围为2–10 mA·cm-2,总电量为1 C·cm-2)、循环伏安法(推荐电位范围为0–1.2 V,扫描速度为50 mV·s-1,扫描圈数10–30圈)等电化学方法来进行聚合实验,只需选择对应的方法即可,在此不再赘述。
1.4.4 观察电致变色现象
更换装有另一未加入吡咯的电解液的电解池,选择一片均一且沉积较薄的聚吡咯ITO片(比如样品②),同样搭建三电极体系。点击“方法”,选择“循环伏安法”,扫描电位为-0.8–1.2 V,扫描6圈,扫描速度为10 mV·s-1,观察并记录其电致变色现象。
1.4.5 测试电导率
将得到的聚合物薄膜用乙腈冲洗干净,60 °C烘干后用四探针微电阻测量仪进行电导率的测试并简单分析得到的数据。
1.4.6 实验结束
关闭仪器和电脑。将电极等装置按要求清洁或处理后归置。用塑料药勺轻轻将ITO玻璃上的聚合物刮下并收集。然后将ITO玻璃置于烧杯中用蒸馏水超声清洗3次,最后于干燥箱中60 °C干燥;电解液采用旋转蒸发法回收乙腈。
1.5 注意事项
(1) 连接三电极体系时注意电极夹不要浸入到溶液中,电极应和磁子保持一定的空间,参比电极在使用中内部溶液之液面应高于电解液液面。
(2) 改变酸度时,从小到大改变,也可以通过计算来指导加入酸的量。
(3) 使用CV法来进行电化学聚合时,还原电位推荐设置在0 V以上,避免聚吡咯在对电极上也发生聚合。
(4) 电致变色实验时,需要更换电解液,否则会发生聚合加电致变色的双重现象;尽量选用聚吡咯沉积层薄且均匀的极片,否则将影响变色现象的观察和记录。
(5) 电导率测量时应选择厚度大于500 μm的聚吡咯薄膜,否则误差较大。(6) 清洗ITO玻璃时应小心,谨防表面导电ITO层出现刮擦痕迹。
2 结果与讨论
2.1 对实验结果的讨论
2.1.1 电聚合
通过对比聚合情况以及聚吡咯薄膜的厚度,发现室温下,在1.4 V,聚合时间为30 s时所得薄膜最为均一致密(样品③),因此后续实验均使用该电位和时间。在电位较小时,聚合效率降低,同等时间下所得薄膜较薄。聚合温度也会影响聚合物薄膜的沉积效率,温度低时,反应速率明显减慢。通过图1和图2所示机理过程可知,较多的质子会阻碍偶联反应,因此加入稀盐酸后,聚合也变慢。
2.1.2 电导率
9组样品反应条件及电导率结果如表3所示,电导率大小的示意图如图5所示。分析可知,电导率随温度上升而降低,这也与文献报道相符合[10]。究其原因,是因为吡咯除了能在活性更高的α位产生阳离子自由基以外,也可以在β位产生自由基,温度越高,β位自由基生成越多,参与氧化偶联的比例就越高,这就导致聚合物共轭程度即有序性降低(见图5中插图),继而影响掺杂和导电性能;而温度低时,其有序性增加,导电性能提升。加入稀盐酸后,不仅聚合变慢,并且电导率降低,说明质子的加入影响了聚合与阴离子掺杂[10]。

表3 不同条件下所得极片电导率的测试

图5 聚合条件为1.4 V,30 s时,在不同pH和温度条件下的电导率
2.1.3 电致变色
电致变色的CV最佳扫描范围为-0.8–1.2 V,需选择或制备1–2片沉积较薄的聚吡咯薄膜进行CV测试(减小聚合时间或聚合电位可获得较薄的聚合物层)。图6是聚吡咯进行电致变色时的CV曲线:在-0.2 V即开始氧化,氧化峰出现在约0.4 V,还原峰约为0.3 V。在还原过程中,聚吡咯薄膜颜色由深变浅,逐渐变为浅黄绿色,再氧化时,其颜色又逐渐变为深蓝紫色,此时薄膜还可观察到具有金属光泽。无论聚吡咯极片在何状态下取出,在空气中放置后颜色均逐渐变为深蓝紫色甚至黑色,说明聚吡咯在空气中即可氧化掺杂。
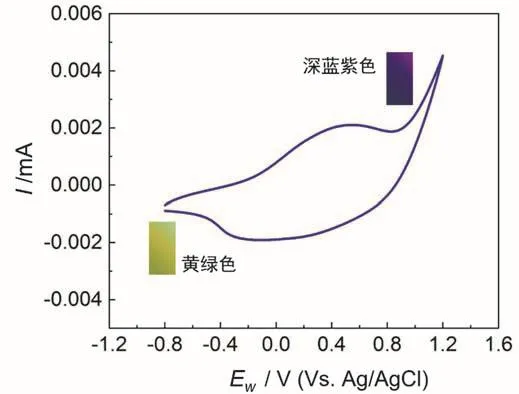
图6 聚吡咯电致变色过程CV曲线
2.2 对于实验改进的讨论
本校原有实验采用的是直流恒流法进行聚吡咯的制备,实验内容偏少,改进后的实验所涉及材料价廉易得,且内容非常充足,更具性价比。具体表现在以下几个方面:
(1) 聚合条件进行开放式探索,实验设计灵活多变,可进行多组实验。教师可根据本实验室的具体情况进行一些条件的指定,也可对一个或多个班级的方案进行统筹;还可根据最新文献进行进一步优化。值得注意的是,如果在实验后选择回收有机溶剂,比如此处的乙腈,则尽量不改变溶剂这一条件。
(2) 使用透明的ITO导电玻璃为工作电极,代替之前的不锈钢极片,方便观察电致变色现象。
(3) 增加了电导率这一表征部分,可发起聚合条件对聚吡咯电导率影响的分析与讨论。根据现有的筛选条件和分析结果,可启发学生对⑤号样品是否电导率最高这一结论进行推导判断,并引导学生思考诸如温度越低电导率是否越高、用其他酸或改变酸度是否结果一致等问题。这些推导或思考可以通过文献或实验加以佐证,培养求真与探索精神。
(4) 综合电解池的组装、电化学工作站的使用、数据处理等操作手段的训练,再结合电致变色、CV图谱解析、掺杂原理等理论性知识的学习,使学生的综合能力得到锻炼。
2.3 对于教学方法改进的讨论
从一个任务型实验到一个开放式设计实验,也对教师的教学提出了更高要求。可体现于以下几个方面:
(1) 可借助预习阶段的文献阅读和讨论部分,将导电高分子的发现与发展中的思政元素巧妙融入课程学习中。
(2) 教师作为实验的“组织者”,更强调组织学生进行文献调研、方案拟定和对各组的实验方案进行统筹规划,并有意识地在实验过程中和实验结束后组织讨论时进行科研思维的启蒙。
(3) 开放式设计将进一步推进线上线下混合式教学改革,这也是实验教学发展的一个趋势。
3 结语
实验改进后,可行性高、内容丰富、涉及面广、综合性强,涵盖了有机化学、电化学、高分子化学与物理以及仪器分析等诸多二级学科,更贴合现代化学学科发展;实验时间分配更合理,适宜4学时实验课程(将聚合条件探索内容进行适度增加,也可适合6或8学时实验);开放式设计与表征相结合的方案,强调文献调研和实验探索,可敦促学生将理论与实践更好地结合起来,有利于学生专业知识体系的建立以及创新思维和科研能力的培养,对教师的教学方法和课堂设计提出了挑战,也更契合本科实验教学与时俱进的改革要求。

