合金成分对熔炼法制备ODS钢的影响
王 政, 冯 越, 张元祥
(东北大学 轧制技术及连轧自动化国家重点实验室, 沈阳 110819)
受环境制约、气候变化等因素影响,未来能源发展方向将向绿色、高效、低碳、清洁转变[1].核能是满足能源供应的重要支柱之一,受到了人们的广泛关注[2].由于核聚变是宇宙中产生能量的主要来源,也是几乎所有陆地能源的间接来源,对未来能源供应具有巨大贡献[3].目前材料问题是限制聚变能发展的一个重要因素[4-5].氧化物弥散强化(ODS)钢由于具有良好的高温性能和抗中子辐照能力,是核聚变堆包层结构的首选材料[6].因此,制备出高性能ODS钢对加速商用聚变堆的应用具有重要意义.
ODS钢中的氧通常由氧化物引入,研究学者相继向合金中引入SiO2、Al2O3、MgO、TiO2、ZrO2和Y2O3等不同氧化物并进行了大量研究[7],相应结果表明,相对于其他氧化物,弥散分布的Y2O3粒子不仅可以更加有效地钉扎位错,提高室温强度,并且还具有良好的高温强度,提高了合金的抗高温蠕变性能,除此之外,Y2O3还可以吸纳辐照产生的空位与核聚变堆内嬗变产生的氦,进而改善合金的抗辐照性能[8-10],因此,人们对Y2O3为主要弥散相的ODS钢的制备工艺进行了大量研究.
自ODS钢被提出以来,主要采用粉末冶金法进行制备且性能最佳,可以使Y2O3氧化物质点均匀分布在钢中.然而,这种方法制备ODS钢存在工艺流程长、单批次产量小、批次间稳定性差等缺点[11-12].此外,Tanigawa等[13]对聚变示范堆所需的包层结构材料进行了估算,发现包层结构材料总质量将达到76 t,若每两年更换一次,运行30年也需要1 140 t结构材料.由于缺乏大型生产装备,粉末冶金工艺很难生产出如此大规模的ODS钢构件,这也成为粉末冶金制备ODS钢的致命缺陷.因此,利用工艺简单、经济性好且易工业化生产的熔炼工艺制备ODS钢引起了人们的广泛关注.但是由于Y2O3的热稳定性高、与钢液的润湿角大且密度低于钢液的密度,导致其在熔炼过程中短时间内团聚上浮而无法引入到钢中[14-15].
针对以上问题,本文通过对合金成分进行设计,采用真空铜模吸铸工艺制备4种Fe-Cr-Y-O试样,分析试样的显微组织特征和力学性能,对比研究熔炼法制备ODS钢时不同试样中Y2O3的上浮情况,为利用熔炼工艺制备性能优异的ODS钢提供了有益指导.
1 试 验
1.1 合金的原料与成分设计
试验原料包括:工业纯铁、金属铬、金属钇、单质硅、钛铁、氧化亚铁粉末和前驱粉.工业纯铁、金属铬、金属钇、单质硅的纯度均大于99.9%,钛铁中钛含量为40%,氧化亚铁粉末为微米级颗粒且纯度为99.999%.利用高能球磨制备前驱粉,包含5%钛、5%氧化钇和90%铁.共设计了4种试验钢,其编号和化学成分如表1所示.
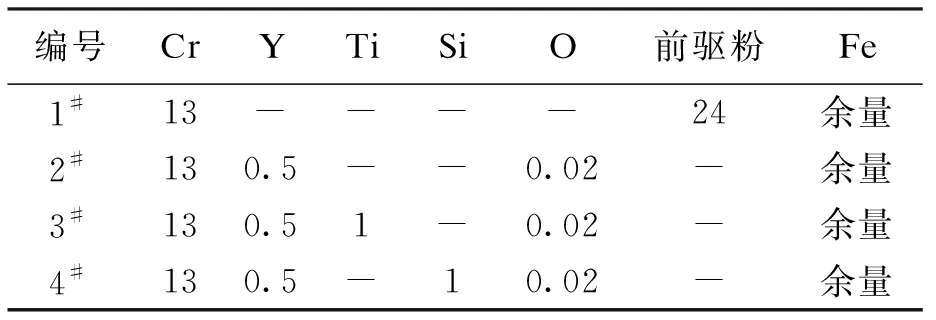
表1 试验钢的化学成分(w)Tab.1 Chemical compositions of experimental steels (w) %
1.2 合金制备与热处理工艺
利用真空吸铸工艺制备试验钢,首先在真空电弧熔炼炉中对配好的原料进行熔化,得到合金铸锭,其质量约60 g.为了避免成分的不均匀性,铸锭需反复熔化3次以上,每次熔化时间为30 s,熔化电流为400 A,熔化过程中观察铸锭表面状态并计时.对合金铸锭进行最后一次熔化后快速吸铸,使得钢液在模具中快速凝固成型,便可获得所需合金成分的小型板状试样,其尺寸为74 mm×20 mm×4 mm.几种不同试验钢的熔化过程分别为:1#钢:所有原料同时熔化;2#钢:先将Fe、Cr、FeO粉末熔化成铸锭后,再加入Y进行熔化;3#钢:先将Fe、Cr、FeO粉末熔化后加入Y和Ti进行熔化;4#钢:先将Fe、Cr、FeO粉末熔化后加入Y和Si进行熔化.为了检验Y2O3最终是否以固溶的形式存在于钢中,将上述板料经过线切割取样后进行高温时效处理,并在1 000 ℃下分别保温0.5、1、1.5、2、2.5、3、5和8 h后空冷.
1.3 合金组织与性能表征
将时效处理后的试样预磨后进行抛光,然后对其进行化学腐蚀,腐蚀剂选用浓度为4%的FeCl3溶液,最后采用OLYMPUS型金相显微镜对其显微组织进行观察.为了进一步观察材料的微观组织形貌并对其化学成分进行分析检测,采用附带能谱仪(EDS)的ZEISS ULTRA 55型扫描电镜(SEM)对经过金相抛光腐蚀后的试样进行观察,采用维氏显微硬度计测量其显微硬度,所用载荷为200 g,保压时间为10 s,测试多个点位,取其平均值作为最终结果.采用FEI G2 F20型透射电子显微镜(TEM)观察试样的微观形貌,并采用JEOLJXA-8530F型电子探针(EPMA)观察试验钢中元素的分布情况.
2 试验结果
2.1 金相显微组织
对在1 000 ℃下保温2 h后的4种试验钢分别进行金相显微组织观察,结果如图1所示.由图1可见,1#钢晶粒比较粗大,柱状晶贯穿试样的整个厚度范围;2#钢中晶粒的长宽比约为2.96,长约145.87 μm,宽约49.28 μm;3#钢出现枝晶,一次枝晶间距较小,组织细密,分布在枝晶间的元素偏析范围较小,成分较为均匀;4#钢呈现出铸件的典型组织,可观察到垂直于型壁排列的柱状晶和中心等轴晶组织.此外,4种试验钢基体的组织类型均为铁素体.

图1 试验钢的金相组织Fig.1 Metallographic microstructures of test steels
2.2 SEM和EDS结果
由于受到金相显微镜放大倍数的限制,未观察到合金中的第二相,因此,为了进一步研究合金中的第二相分布情况,采用扫描电镜对在1 000 ℃下保温2 h后的4种试验钢进行观察,结果如图2所示.由图2可见,1#钢中颗粒数量极少,密度较低,几乎不可见,而在2#和3#钢内发现了平均直径约为2~4 μm的颗粒,其形状近似圆形,4#钢中的颗粒数量较多,分布密集,且颗粒尺寸相对较小,平均直径约为0.5~2 μm.此外,2#和4#钢中的颗粒随机均匀地分布在铸锭内部,而3#钢中的颗粒大多分布在晶界附近.

图2 试验钢的SEM照片Fig.2 SEM micrographs of test steels
为了进一步确定上述颗粒的组成,对4种合金试样的第二相颗粒进行了能谱分析,结果如表2所示.由表2可见,1#钢仅含有元素Fe、Cr、O、Ti,不存在元素Y.2#、3#和4#钢中均包含元素Y和O,可以推断基体内含有由元素Y和O构成的第二相.可见,采用2#、3#和4#钢的铸造方法可以将微米级Y2O3颗粒引入钢基体中.
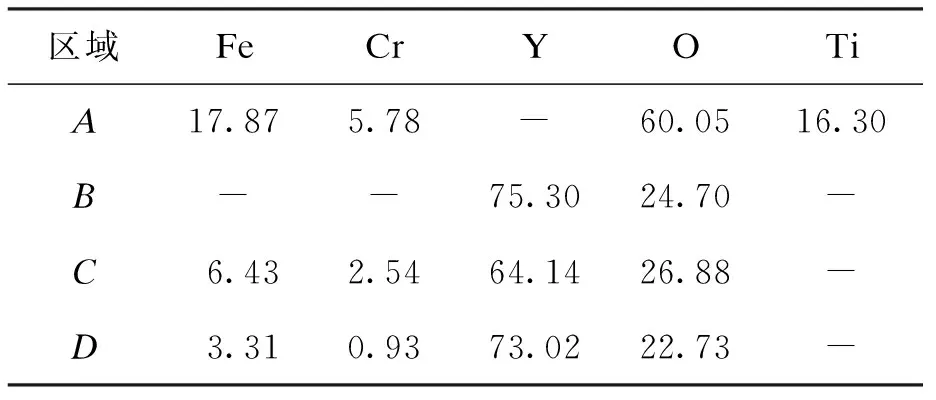
表2 试验钢的EDS结果(w)Tab.2 EDS results of test steels (w) %
2.3 时效硬化曲线
为了探究4种试验钢内第二相粒子的析出情况,分别将其在1 000 ℃下保温不同时间后空冷,从而进行时效处理,随后测定显微硬度,结果如图3所示.由图3可见,在整个时效过程中1#、2#和3#钢的显微硬度值基本保持不变,其中1#和2#钢的硬度相近,且明显低于3#钢,这是由于3#钢中Ti可以细化合金晶粒,晶粒尺寸的降低能够提高位错运动阻力与合金抵抗局部变形的能力,从而提高了钢的硬度.此外,4#钢的硬度相对较高,且随着时效时间的增加,4#钢的硬度呈现先逐渐升高随后达到饱和的变化趋势.当时效时间为0.5 h时,4#钢的硬度约为143 HV,当时效时间为1.5 h时,4#钢的硬度达到饱和,饱和值约为164 HV.
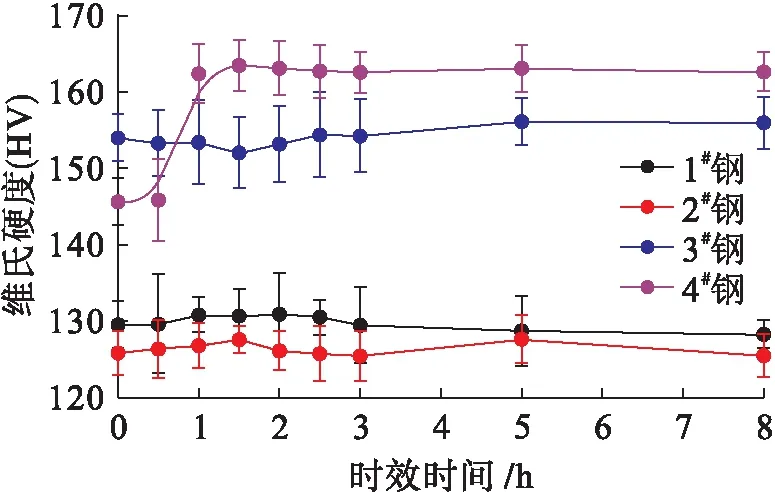
图3 试验钢的显微硬度Fig.3 Microhardness of test steels
3 分析与讨论
3.1 纳米级第二相颗粒存在证明
针对4#钢硬度的变化趋势,对时效时间为2 h的试样进行透射观察,结果如图4所示.由图4可见,试验钢内部含有弥散细小的纳米级颗粒,即4#钢经过一定时间的时效后内部可以析出第二相.

图4 1 000 ℃时效2 h后4#钢的TEM图像Fig.4 TEM image of 4# steel after aging at 1 000 ℃ for 2 h
合金的宏观力学性能变化与时效过程中微观组织演化密切相关,因此,显微硬度的变化可以很好地反映晶粒内部第二相的析出过程.1#、2#和3#钢的显微硬度随着时效时间的增加变化不大,而4#钢的显微硬度随着时效时间的增加变化较大,且该显微硬度的变化正好可与晶粒内部纳米级第二相的析出过程一一对应.初始时效阶段合金元素固溶于基体内部,固溶强化起主导作用,强化效果较弱,材料的硬度值较低.随着时效过程的进行,第二相逐渐脱溶析出,材料基体成分逐渐降低,位错弓出第二相所需要的力更大,即细小弥散的第二相对位错的阻碍作用更强,此时弥散强化作用的增加程度大于固溶强化作用的减少程度,弥散强化起主导作用,因而试验钢的硬度逐渐升高.随着时效时间的继续增加,材料基体元素逐渐减少,第二相析出的驱动力逐渐降低,最终第二相析出达到饱和状态,其含量不再变化,因而试验钢的硬度也达到最大值.可见,在材料成分中添加合金元素Si可以促进含有纳米级颗粒ODS钢的制备.
3.2 纳米级Y2O3形成机理
3.2.1 熔池反应过程
在熔化过程中对试验钢的观察发现,1#钢液熔化时其表面未发生变化,而熔化后炉腔内发现了脱落的表皮;2#钢在熔化10 s的时间内,铸锭上表面出现了明显的膜层;3#钢在熔化时间约为15 s时铸锭表面出现了膜层;而4#钢在熔化24 s之后其表面才会发生变化.可以推测这是由于1#钢在熔化过程中Y和O的反应十分迅速,Y2O3以极快的速度在短时间内团聚上浮致使来不及观察到相应现象.而4#钢中Si先和O发生反应,随后Y争夺O并与O结合形成Y2O3,即在一定的熔化时间内,Si的加入能够有效推迟Y和O的反应,延长了Y2O3的形成时间,从而对Y2O3的上浮起到抑制作用,具体反应过程示意图如图5所示.
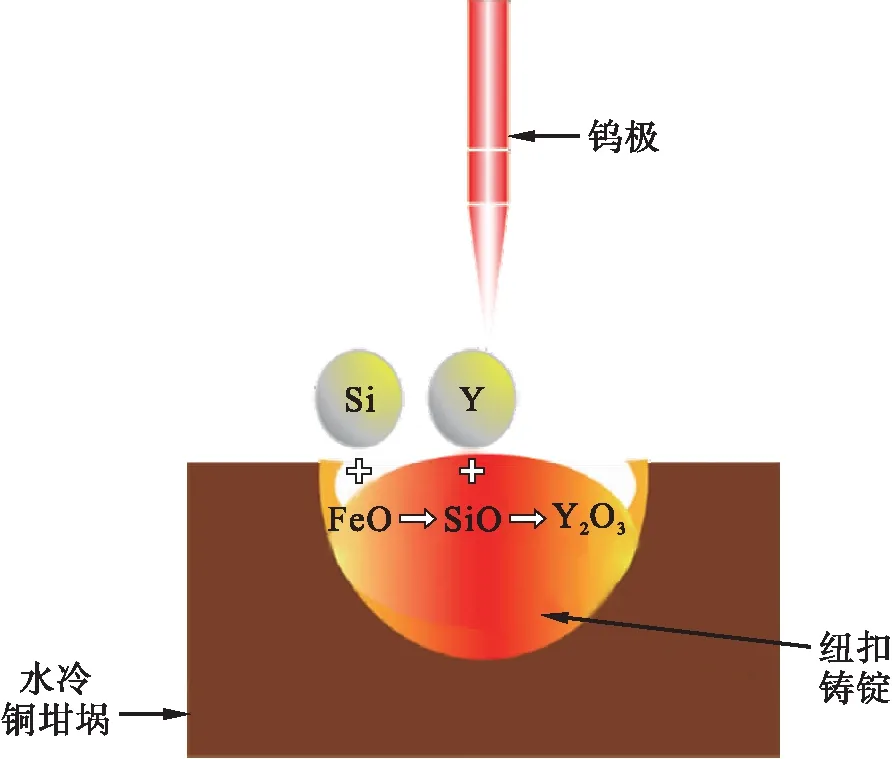
图5 熔池反应过程示意图Fig.5 Schematic diagram of molten pool reaction process
3.2.2 铸锭上表面成分
为了进一步探究Y2O3在熔炼过程中的上浮情况,通过电子探针采用面扫方式对4种试验钢在熔化后形成铸锭的上表面部分进行观察,结果分别如图6~9所示.
由图6可见,在1#钢表皮和内部未发现元素Y的存在,表明Y2O3不仅未存在于钢的内部,而且也未在钢表面聚集,结合熔化过程中的观察结果可知,Y2O3熔化时由于上浮速度过快导致其大部分成为炉渣,因此,采用这种方法制备ODS钢是不可行的.由图7可见,在2#钢中Y和O元素在表皮部分聚集,厚度约为22 μm.虽然2#钢内部存在含Y的氧化物颗粒,但仅是由一小部分Y2O3聚集粗化形成的,大量Y2O3在熔化过程中上浮到了钢表面,形成一层Y2O3膜层.由图8可见,3#钢中表皮部分富集的Y和O相比于2#钢较少,但仍有较多的Y和O存在于铸锭表面.由图9可见,4#钢表皮部分基本不存在Y元素,且O含量也较少,这与熔化时观察到的4#钢表面在熔化较长时间后才发生变化的结果一致,再次验证了在利用熔炼法制备ODS钢时Si元素抑制Y2O3上浮的有效性.

图6 1#钢面扫结果Fig.6 Surface scanning results of 1# steel
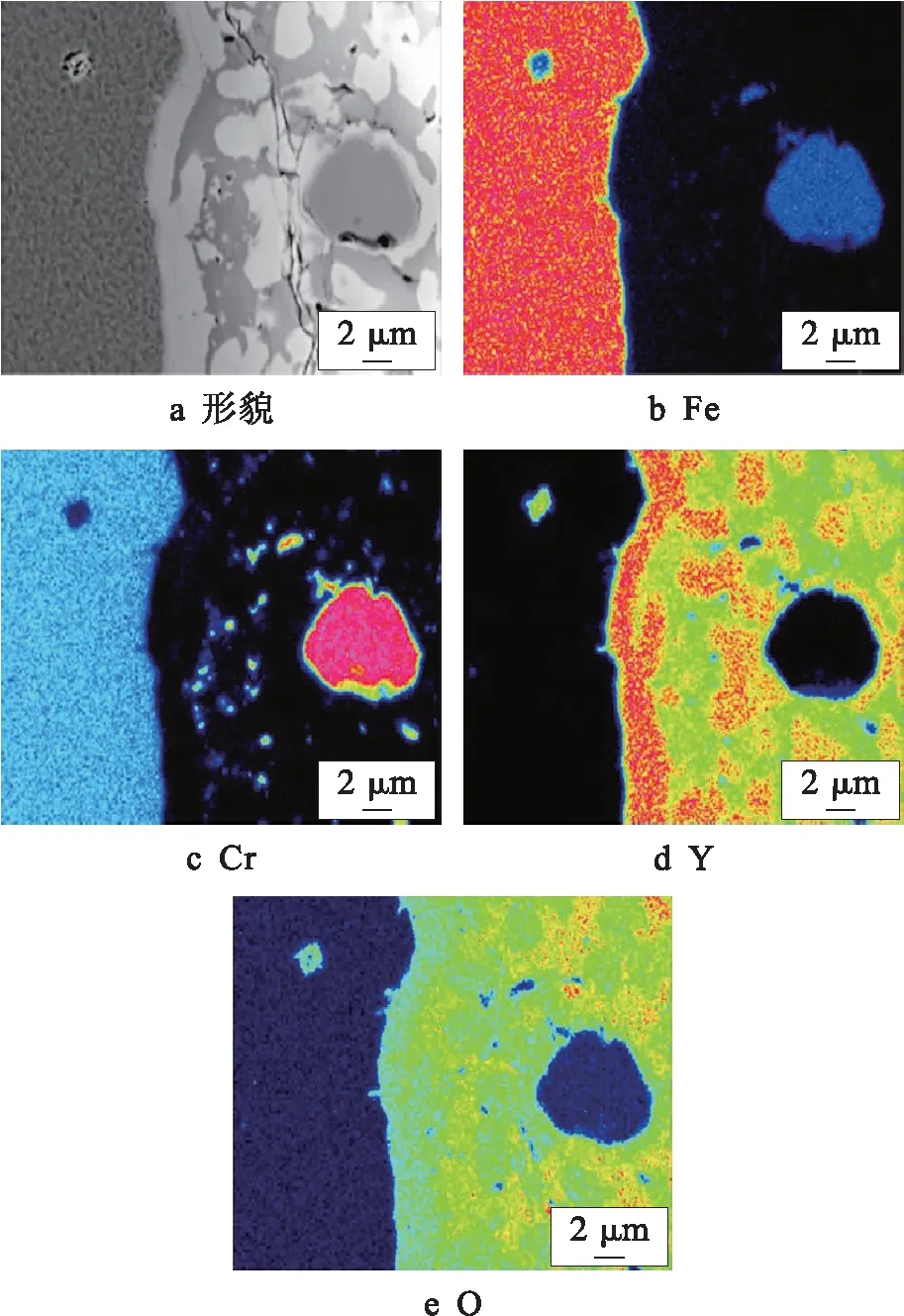
图7 2#钢面扫结果Fig.7 Surface scanning results of 2# steel

图8 3#钢面扫结果Fig.8 Surface scanning results of 3# steel

图9 4#钢面扫结果Fig.9 Surface scanning results of 4# steel
3.3 成分工艺优化
基于上述试验结果可知,利用熔炼法制备ODS钢时可以添加微量的合金元素Si,并采用先加氧,最后添加Si和Y的熔炼方式.由于Si的加入使得铸锭表面在熔化24 s后发生变化,因此,可将熔化时间控制在20 s以内,从而更好地抑制Y2O3的上浮,最终获得含有更多纳米级颗粒且性能优良的ODS钢.
4 结 论
通过以上分析可以得到如下结果:
1) 熔炼时通过最后熔化Y的工艺进行ODS钢的制备,可以引入少量微米级Y2O3颗粒,在此基础上添加合金元素Ti可以细化晶粒,提高硬度,对抑制Y2O3上浮起到一定作用.
2) 在最后熔化Y的基础上添加合金元素Si可以推迟Y2O3的形成及上浮时间,铸锭表面基本不存在Y元素,且O含量也较少,并通过一定时间的时效处理,铸锭中可以析出呈弥散分布状的纳米级第二相粒子.元素Si的加入能够制备出含纳米级氧化物颗粒的ODS钢,并使其力学性能得到改善.

