可穿戴人工肾再生透析液中尿素清除策略
李茂云,禹 虹,蒋依凡,聂淑慧,郭 勇
(杭州师范大学药学院,浙江 杭州 311121)
1 可穿戴人工肾
近年来,慢性肾脏病(Chronic Kidney Disease, CKD)已经成为严重危害人类健康的全球性公共卫生问题.在全球范围内,CKD的发病率在8%—16%之间且逐年增加[1-2].根据王海燕教授在2012年发表的全国性CKD研究结果显示,我国CKD发病率达10.8%,患者人数将近1.2亿[3-4].据不完全统计,在我国,其中终末期肾脏病(End-Stage Renal Disease, ESRD)的患病率在2012年为237/每百万人口[5].由于肾脏供体有限,大部分ESRD患者只能接受血液透析或腹膜透析以维持生命.
目前,我国90%以上的透析患者使用血液透析方法,他们需要频繁地去医院治疗(3次/周,约4 h/次),透析期间患者需要一直躺在病床上,这给患者的日常生活造成了极大的不便.另外,每次透析需要消耗大量的透析液(>100 L)及相关耗材,这不仅是一笔不菲的费用(如门诊透析患者的透析直接相关费用约占整体医疗费用的65%),而且也对环境造成一定的污染.为了解决上述问题,研究人员提出了可穿戴人工肾(Wearable Artificial Kidney, WAK,图1)的概念[6-9].通过再生透析液,减少透析液的用量,使微型化透析仪成为可能,因此患者可以将透析仪穿戴在身上实现随时随地的透析,从而提高患者的生活质量.另外ECRI(Emergency Care Research Institute)研究所预测WAK的治疗费用仅为传统血液透析治疗费用的60%—70%[10].WAK的先驱者Victor Gura于2007年在英国以及2016年在美国分别进行了WAK的人体试验,实验结果显示WAK能有效清除代谢产物以及维持血液电解质平衡等,患者比使用传统的透析仪具有更积极的反馈且表示会把WAK推荐给其患友[11-12].荷兰的Neokidney公司也于2015年开发了一款WAK原型机并预计在2020年进行人体试验.
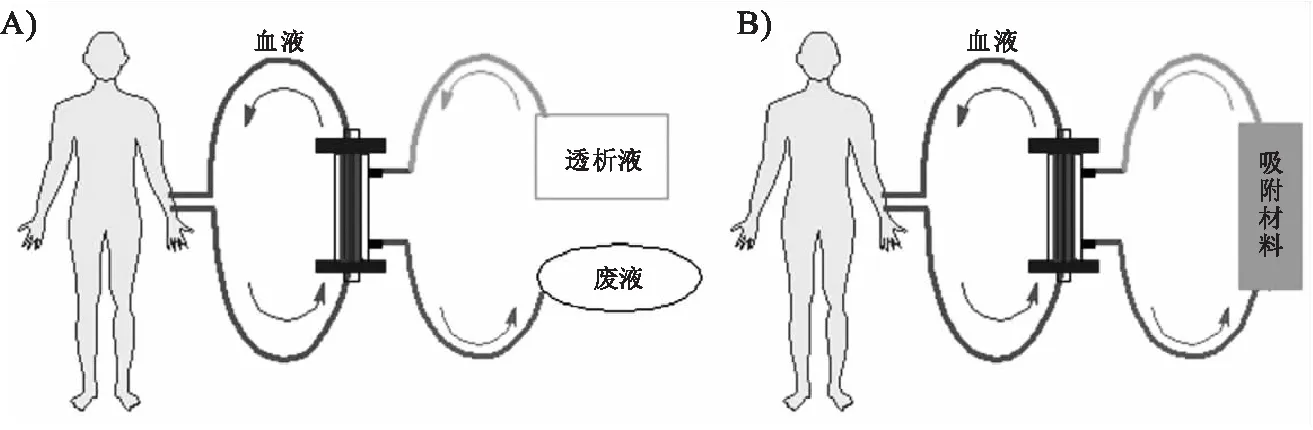
图1 (A)传统的血液透析方法以及(B)可穿戴式人工肾的示意图Fig.1 Scheme of (A) conventional hemodialysis and (B) wearable artificial kidney
目前,研发WAK的最大瓶颈是制备一种高效的尿素吸附材料用以清除经透析扩散到透析液中的尿素.血液中尿素的清除方法主要有两种,一种是使用脲酶先将尿素催化降解成NH4+,再用离子交换树脂清除NH4+[13-14];另一种方法是用吸附材料直接通过共价或非共价等方法与尿素成键,从而将尿素从血液中清除[15-16].前文提到的WAK主要使用第一种方法用以清除尿素,但是该方法有两大主要缺陷:其一,当产生的NH4+因离子交换树脂饱和而无法被继续清除时,这些残留的NH4+的毒性要比等量尿素的毒性更强[17];其二,尿素分解过程中会产生CO2,产生的CO2逐渐在器件内累积,导致血压以及透析液流速的间歇性变化,影响最终透析效果甚至导致透析失败[11].因此,越来越多的科研人员将研究方向聚焦在第二种方法上,由此开发出各种各样的基于化学键(非共价键、金属配位键、共价键)的尿素吸附材料.本文主要综述基于非共价法的尿素吸附材料.
2 尿素
在人体内,蛋白质和其他含氮营养物质经过代谢变成铵,这些铵在肝脏中通过尿素循环转化成尿素.尿素通过血液运输到肾脏,最后通过尿液排出体外.尿素是主要的非蛋白类的含氮化合物,约占肾脏氮排泄的90%.根据当天蛋白质的摄入量,成年人尿素每日排出体外物质的量可达240—470 mmol.如果这些生成的尿素无法尽快从人体内排出,就会导致血液内的尿素浓度升高,引起一系列的毒副作用,表现出恶心、失眠、腹泻等症状,严重的会发展成尿毒症.一般来说,尿素是一种非常不活泼的化合物:尿素在生理pH值下不带电荷,既不非常亲核也不非常亲电.在水溶液中,尿素与微量的分解产物铵离子和氰酸根离子(0.1%—0.8%)处于平衡状态(式1).原则上,氰酸根离子可以在酸性条件下与H2O进一步反应,形成CO2和NH3(式2).然而,在生理条件下,氰酸根离子与H2O的反应非常缓慢,分解产物铵离子和氰酸根离子在较小程度上仍然存在.
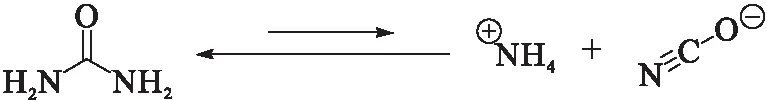
(1)
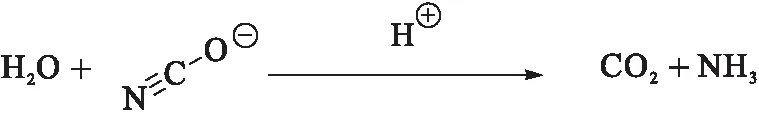
(2)
尽管人体对于在10—20 mmol/L范围内轻度升高的尿素浓度是可以耐受的,但尿素浓度超过20 mmol/L则会产生毒性,比如抑制胰岛素活性和破坏胃肠道屏障.因此,必须避免人体尿素浓度过高.为了消除每日240—470 mmol的尿素产量,同时在每日8 h透析下将尿素浓度保持在20 mmol/L以下,透析期间的尿素清除率应至少为25—49 mL/min,从而使24 h平均清除率为8—16 mL/min.
3 尿素吸附剂
若一种吸附剂能与尿素特异性且高效结合,它将成为可穿戴人工肾的理想材料,因为它与酶以及电化学降解尿素不同,不会有潜在有害副产物的生成.吸附剂主要通过和尿素形成氢键或者范德华力等非键相互作用,或作为亲核试剂与尿素反应形成共价键来达到尿素吸附的作用.最近的研究表明吸附剂具备有效去除透析液中尿素的潜力,其中包括无机物基吸附剂(如活性炭、硅、沸石、MXenes)、壳聚糖基吸附剂、分子印迹聚合物(MIPs)基吸附剂和含(多)羰基化合物的吸附剂.其中含(多)羰基化合物的吸附剂通过共价作用吸附尿素,不在本文的讨论范围.接下来的章节将对上述其余几种材料进行详细的综述.
3.1 无机物基尿素吸附剂
研究最早最多的无机物基尿素吸附剂是活性炭(AC),它是一种炭化活性材料,其比表面积一般在500~1 500 m2/g范围内.AC主要通过非共价相互作用吸附尿素,故大多数类型的活性炭对尿素的吸附能力都很低,最大吸附容量仅约为0.2 mmol/g[18-20].由于尿素在活性炭上的吸附是放热的,而尿素从活性炭上的解吸是吸热的.因此,可通过适当降低温度来提高吸附量.然而,由于人体温度的限制而无法过低降低温度,故由此法得到的尿素吸附容量仍然较低.
此外,二氧化硅也被用作尿素吸附剂.某些形式的二氧化硅,如介孔硅SBA-15和MCM-41,由于其具有较高的比表面积(一般为400~900 m2/g)和较小的孔道( ±10 nm ),因此可以用来吸附尿素.Cheah等人报道了SBA-15和胺化SBA-15的最高尿素吸附容量分别为7.9 mmol/g和8.7 mmol/g (38 mmol/L尿素水溶液的条件下).如此高的尿素吸附容量可能与他们使用的尿素浓度的测定方法未被验证有关.因为他们文章中作为参比的市售AC的尿素吸附容量也达到了5.4 mmol/g,远远高于我们之前综述的0.2 mmol/g[21].
沸石是纳米多孔晶体材料,主要由硅和氧化铝组成.沸石被广泛用作吸附剂和离子交换剂,沸石作为尿素吸附材料也偶有报道.Cheng等人研究了沸石ZSM-5对尿素的吸附作用,发现其最大尿素吸附容量(0.70 mmol/g)高于活性炭(0.41 mmol/g)和氧化石墨烯(0.45 mmol/g)[20].
近年来,二维材料由于其高比表面积等特性正受到越来越多的关注,其中具有O-、OH-和F-表面基团的二维过渡金属碳化物材料( MXenes )也被报道为新型尿素吸附剂用于透析液再生,如图2所示.MXenes是叠层的纳米片层,每层厚度约为1 nm,尺寸为1~4 μm.这些材料的通式是Ti3C2TX,其中TX表示通过氢键和偶极相互作用结合尿素的O-、OH-或F-等表面基团.尽管已报道的MXenes在37 ℃下对尿素的结合能力较低(0.12 mmol/g),但作者指出,这些材料结合尿素是很有前景的,因为MXenes代表了一大批不同组成的材料,可以进一步探索寻找最佳的尿素吸附剂[22].
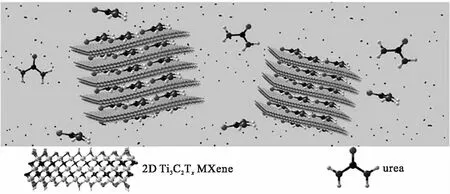
图2 MXenes吸附尿素示意图[22]Fig.2 Scheme of urea adsorbed by MXenes
3.2 壳聚糖基尿素吸附剂
壳聚糖(CS,图3)是甲壳素的部分脱乙酰聚合物(脱乙酰度> 50 %),是由随机分布的β- 1,4 -连接的D-葡萄糖胺和N-乙酰-D-葡萄糖胺单元组成的线性多糖[23-25]. CS中的氨基由于可以与尿素、蛋白质、核酸、胆固醇等多种生物分子中的基团形成氢键和偶极作用而对它们具有吸附能力.因此,CS及其衍生物在许多医药和生物医学方面都有应用,包括在药物递送系统、组织工程、伤口敷料和疫苗输送中的应用[26-27].
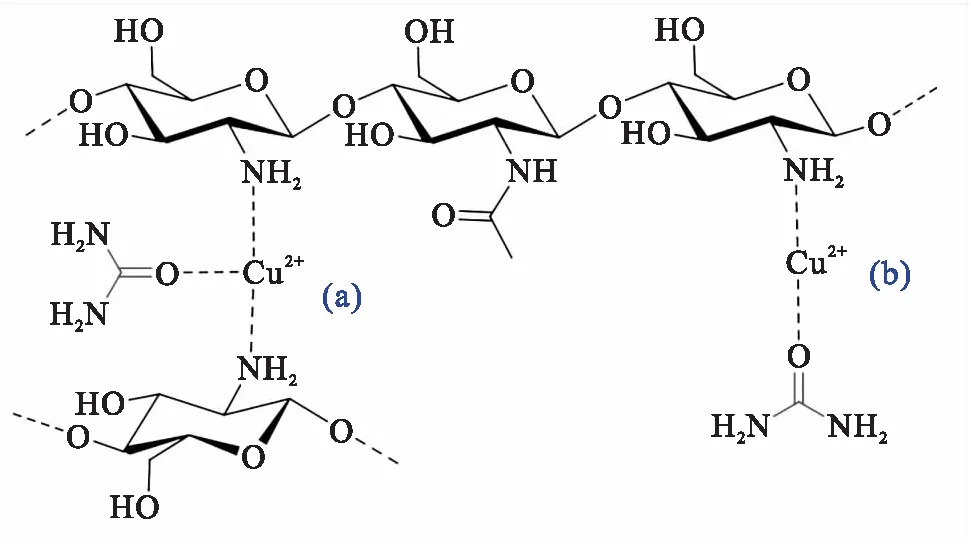
(a)桥接模型 (b)吊坠模型图3 CS/Cu2+/尿素配合物的配位模型Fig.3 Coordination model for CS/Cu2+/urea complex
Jing等人利用CS来稳定氧化纤维素基尿素吸附剂,并开发了一种由90%氧化纤维素内核和10%CS涂层组成的膜,其尿素结合容量为0.14 mmol/g[28].尽管CS能够通过氢键结合尿素,但因为它结合尿素的能力太低,无法应用于可穿戴人工肾.因此,人们尝试多种方法来提高它结合尿素的能力[29-35].目前,最常研究的方法是CS先与金属离子通过配位键络合,然后金属离子未占用的d轨道可以和尿素结合从而吸附尿素.由于配位键通常比氢键强,因此尿素优先与金属离子结合.在众多的金属离子中,Cu2+与尿素结合的研究最为广泛,因为Cu2+与其他金属离子相比,具有与尿素相对较高的亲和力(Cu2+≫Hg2+>Zn2+>Cd2+>Ni2+>Co2+~Ca2+).此外,制造CS/金属离子络合物是一个简单的过程,可以直接通过将CS浸入含有金属离子的水溶液中来实现[24].为了获得对尿素有高结合能力的CS/Cu2+复合物,关键是增加CS的Cu2+上载含量,可通过提高复合物的可接触性(通过应用大孔隙率或更小的颗粒)或通过增加氨基的含量来实现.Chen等人制备了Cu2+负载CS-丝纤维蛋白混合膜,通过观察发现尿素浓度22 mmol/L下其尿素结合能力为0.3 mmol/g.因为CS-纤维蛋白共混膜很致密,限制了壳聚糖上与氨基结合的Cu2+对尿素的可及性.当通过制备孔径为25~35 μm的大孔CS膜来改善与氨基结合Cu2+的可接触性时,与丝素共混膜相比,CS中Cu2 +的负载量增加,导致尿素结合容量从0.3 mmol/g显著增加到1.3 mmol/g[30,36].除了CS/Cu2+复合物膜,人们也在探索CS/Cu2+吸附颗粒能否用于吸附尿素[29,31-33].Pathak等人比较了CS/Cu2+膜和颗粒的尿素结合能力,发现膜的尿素结合能力略低于颗粒.此外,尿素吸附量随着粒径的减小而增加,这可能是由于较小颗粒的表面积增加,因此官能团的可接触性增加[32].
尽管上述研究表明,通过与金属离子络合可以增加CS的尿素结合力,但CS在水中与金属离子形成络合物的能力有限,因为CS的大部分氨基和羟基彼此与水分子形成氢键[36-37].Chen等人研究表明,通过将CS的氨基与戊二醛部分交联,形成CS金属离子配合物的能力增强[38].尽管与戊二醛反应消耗了部分氨基,但交联过程阻止了剩余氨基与羟基形成氢键,导致整体上更多的氨基可用于CS-金属离子复合物的形成[35,39].此外,Wilson等人推测,除了CS未反应的氨基外,源自戊二醛的醛基也可以络合Cu2+,通过将Cu2+与戊二醛交联的CS反应制备CS/Cu2+复合物,其最大吸附容量达到了4.4 mmol/g,如图4所示[35].
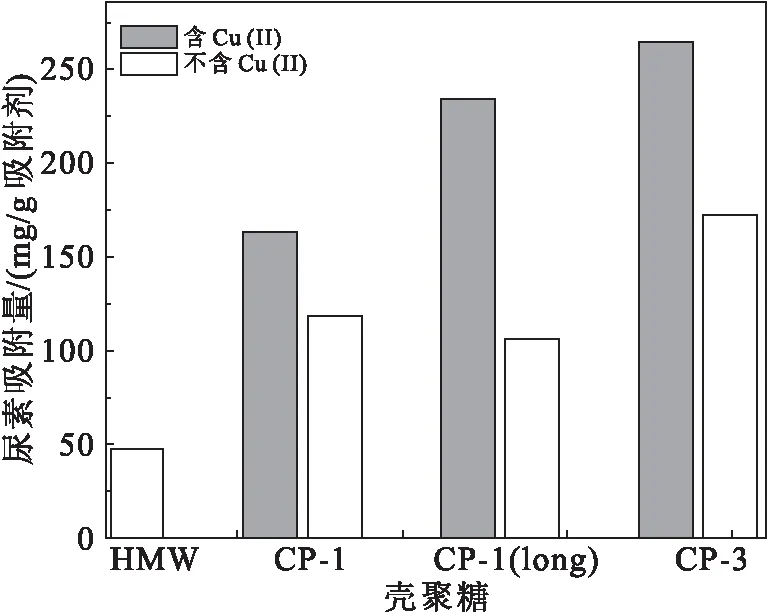
图4 含铜离子及不含铜离子的交联壳聚糖对尿素的最大吸附容量Fig.4 The maximum urea uptake of cross-linked CS with or without Cu2+
综上所述,CS/Cu2+配合物具有较高的尿素结合能力,在进行戊二醛交联时,其尿素结合能力更强.然而,可穿戴人工肾的应用中,潜在Cu2+浸出是一个值得重视的问题.此外,戊二醛浸出是另一个安全问题.
3.3 基于分子印迹技术的尿素吸附剂
分子印迹是一种相对新颖的技术,用于合成与模板分子(如尿素)在形状、大小和结合位点方面具有互补性的聚合物[40-42].图5是分子印迹聚合物(MIP)的制备过程原理.从制备技术上来说,分子印迹聚合物的合成不需要复杂的有机合成和分子设计,是比较简单并且容易调整的.而与具有特异性识别能力的天然抗体相比,分子印迹聚合物具有优异的化学性质、热稳定性、可再生性和溶剂抗性的性质[43].在应用于可穿戴人工肾时,因为人体中的某些其他含氮物质也会随着尿素一起进入透析液中,而这些含氮溶质可能会与尿素竞争尿素吸附剂,但具有特异性识别尿素功能的尿素吸附剂就可避免这一现象的发生.由于其独特的特异性识别功能,分子印迹聚合物已广泛应用于色谱分离、传感、药物传递和催化等领域[44-47].
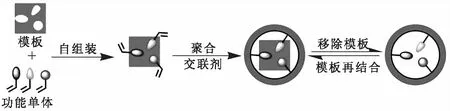
图5 分子印迹聚合物(MIP)制备示意图Fig.5 Scheme of the preparation of molecular imprinting polymers
MIP制备过程主要包括以下几步:首先,模板分子和互补的功能单体通过共价或非共价结合形成可逆复合物;随后,可逆复合物与过量的交联剂聚合,使可逆复合物固定于聚合物基体.当模板分子从聚合物中移除时,剩下的结构就与模板分子互补.因此,最后获得的聚合物可以选择性吸附溶液中的模板分子.
至今为止,已有多篇文献报道了以尿素为模板分子制备分子印迹聚合物用以吸附清除尿素[48-56].Alizadeh等人以甲基丙烯酸为功能单体,乙二醇二甲基丙烯酸酯为交联剂,在乙腈中反应得到了尿素印迹的聚合物,其对尿素的吸附容量达到了6.3 mmol/g[54].这是一个值得注意但可疑的发现,第一点是因为在理论上这种聚合物与尿素的结合能力最大只有0.28 mmol/g.第二点是在合成过程中,他们使用的是乙腈作为溶剂,这是一种理想的状态.在乙腈中,印迹吸附剂的羧基很可能被质子化,而在实际应用中,大部分吸附实验都是在缓冲溶液中进行的,比如透析液.在这些缓冲溶液中,印迹聚合物的羧基就有可能被去质子化,从而改变吸附剂与尿素的特定结合.而该作者在这两个问题上都没有发表意见,这也导致这篇文章的可信度存在问题.
此外,如果一种大分子具有合适的官能团,即使在制备中不添加交联剂,这种大分子也可以用来制备以尿素为模板的分子印迹聚合物[48-53,56].比如,将溶有尿素和聚乙烯-聚乙烯醇共聚物的二甲基亚砜蒸发,然后用乙醇和水进行萃取除去尿素,这就形成尿素分子印迹聚合物的膜.尽管在加工过程中没有加入交联剂,但是尿素分子印迹聚合物的膜仍然显示出良好的印迹质量.在尿素浓度为16.7 mmol/L时,尿素吸附容量为0.4 mmol/g(图6)[56].此外,壳聚糖也可以应用于尿素分子印迹聚合物的设计中[48,50-51].
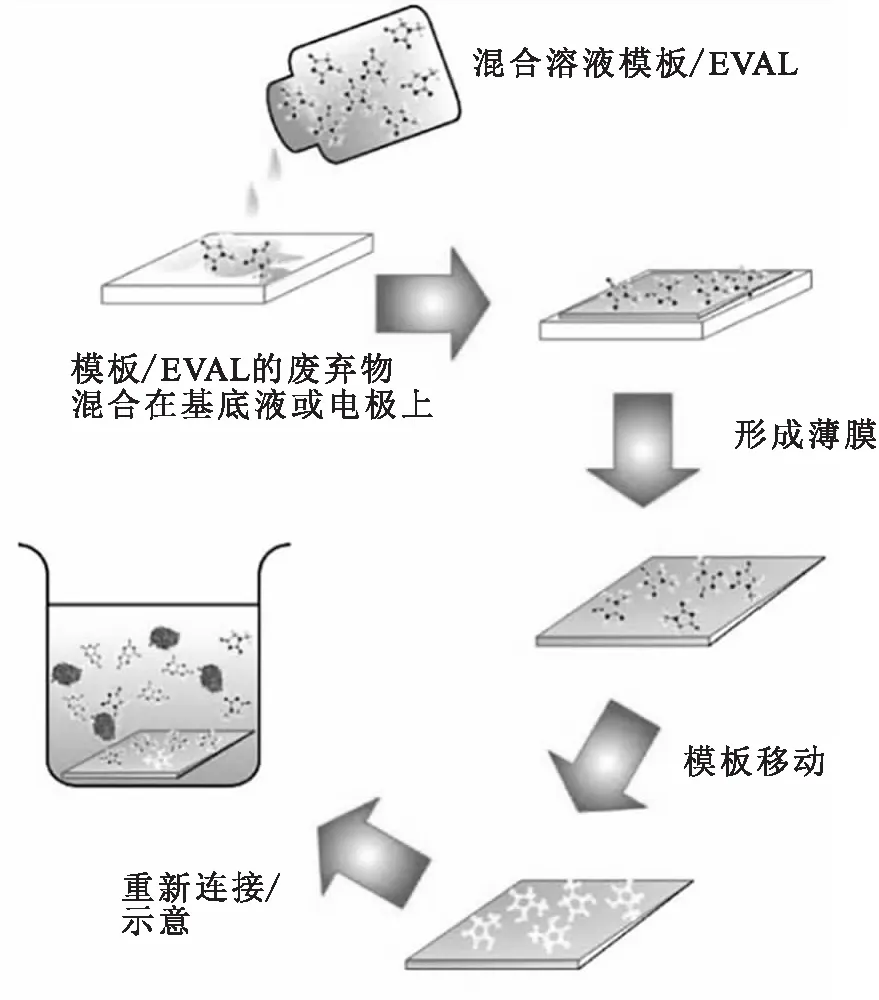
图6 分子印迹聚合物(MIP)电极制备示意图Fig.6 Scheme of the preparation of molecular imprinting EVAL sensing electrode
4 结论与展望
开发可穿戴人工肾的最大挑战是开发有效的尿素清除技术.目前科学家们已探索多种方法,比如酶水解、电化学分解、物理吸附和化学吸附,但这些方法都存在各自的缺点.
本文主要综述了基于非共价法的尿素吸附材料.高特异性、高结合能力、具有快速动力学特性、不释放毒副产物的尿素吸附剂还有待探索.活性炭和沸石对尿素的亲和力太低,不适合在可穿戴人工肾中应用.未来可能会研发出对尿素具有高结合能力和高亲和力的沸石或改良的活性炭.二氧化硅对尿素具有较高的吸附能力,但在可穿戴性人工肾中加入二氧化硅仍需要实验来验证这一设想.
以戊二醛做交联剂的壳聚糖/铜离子复合物吸附剂具有较高的尿素结合能力.然而,这样的吸附剂存在一个重要的问题,那就是潜在的铜离子浸出对人体的影响.
相对其他方法来说,尿素分子印迹聚合物具有极大优势,因为它可以和尿素进行特异性结合.但是合成尿素吸附剂的分子印迹技术仍处在非常早期的阶段.大部分获得的尿素分子印迹聚合物主要用于尿素的检测,只有极少数的研究关注尿素结合后透析液的再生问题.此外,现有特异性识别是基于氢键的相互作用,这可能会导致缓冲液中的水与尿素竞争性结合吸附剂,使尿素分子印迹聚合物的利用率降低,这就需要大量的“非功能交联剂”来维持聚合物的结构,从而降低了交联剂的最大结合能力,这也是该方法另外一个缺点.共价或配位印迹有可能避免这些缺点,但仍需要进一步探索.
总之,目前没有一种去除尿素的方法可以让可穿戴的透析设备用于人体.但是随着不同的尿素去除策略技术的发展,在不久的将来,便携式透析液再生系统和轻量级可穿戴人工肾有可能实现并造福人类.

