聚降冰片烯荧光传感器识别三磷酸鸟苷
曹迁永,陈 茜,祝文斌
(南昌大学化学系,南昌 330031)
核苷酸是遗传物质重要的组成部分,是一种信使分子。GTP是核苷酸中的一种,参与人体中许多重要的生化反应,同时也是细胞信息交流的中间媒介[1-2],广泛存在于生命体中[3]。例如,GTP能调节Ca2+诱导的胰岛素分泌,同时也能刺激神经轴突生长等[4]。同时,其代谢异常会导致一系列的生理疾病[5],如高尿血酸症、乳清酸尿症等[6]。因此,实时、灵敏检测GTP显得尤为重要。
近些年以来,GTP识别与快速灵敏检测已有大量文献报道。其中荧光化学传感器由于简捷、灵敏度高等优点引起人们广泛关注[7]。一些小分子荧光受体已经被用于GTP识别[8,9]。由于有机小分子具有生物相溶性差、稳定性不高、荧光量子产率低及信号弱等缺点,使其在生物学上的应用受到限制。而聚合物传感器可很好地解决这一缺点[10]。与此同时,由于GTP与其他核苷酸结构高度相似性,目前已报道的GTP传感器选择性不高[11],因此该领域需要更深层次的探索。
鉴于其独特的开环易位聚合特性,降冰片烯在能源、医药、生物成像和传感等领域受到广泛关注[12]。以降冰片烯为载体的聚合物传感器用于金属离子及阴离子识别也有相关报道[13-15]。基于此,本文合成了一种萘功能化的三唑鎓聚降冰片烯荧光化学传感器P1,研究了聚合物及其对应单体在水溶液中对GTP及其他阴离子的荧光识别能力,并揭示了聚合物客体与GTP分子间识别原理。
1 实验部分
1.1 药品及仪器
本试验所有溶剂均为分析纯,2-萘磺酸钠、降冰片烯二酸酐、溴乙胺氢溴酸盐、溴丙炔、三甲基氧鎓四氟硼酸盐、Grubbs催化剂、阴离子钠盐均从百灵威化学试剂公司购买。
使用了恒温磁力搅拌器(SH-7,常州精仪有限公司)来作为反应平台;利用核磁共振仪(DD2-400MR,美国Agilent公司)确定产物结构;HITACHI公司UV 3010仪器测试物质吸收光谱,而物质的发射光谱在HITACHI公司F-4500荧光光谱仪上测试。
1.2 检测限及络合常数的计算
络合常数的计算:
根据Benesi-Hildebrand方法,荧光滴定的数据结合GTP与聚合物P1按照1:1络合比计算得来。
在方程中I0代表聚合物P1没有加入GTP时的荧光强度,I代表聚合物P1结合GTP的实时荧光强度,I′代表聚合物P1完全结合GTP时的荧光荧光强度。
检测限(DL)的计算:
DL=3σ/K
公式中σ空白测量值的平均标准偏差值,K是线性拟合的斜率。
1.3 紫外光谱和荧光光谱的测试
不同阴离子钠盐首先用去离子水配成其母液(1.0 mmol),而聚合物及单体的母液(2.0 mmol)在DMSO中配制。荧光及紫外-可见光谱的测试浓度10 μmol,用体积为2 mL石英比色皿。在阴离子滴定光谱试验中,阴离子母液滴入到测试溶液(2 mL)中的体积量很少,可以忽略不计,整个体积恒定为2 mL。
1.4 合成
1.4.1 化合物1的合成
化合物1的制备参照文献[16]。
1.4.2 化合物2的合成
在N2氛围下,称取化合物1(314.2mg,1 mmol)和NaN3(162.5 mg,2.5 mmol)加入反应瓶中。用CH3CN(5 mL)溶解,于40 ℃下搅拌5小时。旋干溶剂,粗产物通过柱色谱以二氯甲烷纯化的到化合物2(268 mg,97.0%)。
1.4.3 化合物3的合成
化合物3的制备参照文献[16]。
1.4.4 化合物4的合成
于N2条件下,称取化合物3(201.2 mg,1 mmol)和2(276.3 mg,1 mmol)溶解在少量DMF溶液中,搅拌均匀后,加入CuSO4·5H2O(50 mg,0.2 mmol)和抗坏血酸钠(70 mg,0.4 mmol),于40℃下搅拌2小时。加水析出沉淀,抽滤、洗涤得粗产物,粗产物通过柱色谱(洗脱剂为CH2Cl2:MeOH=98:2,v/v)纯化的化合物4(458.4 mg,96.0%)。1H NMR(400 MHz,DMSO-d6)δ8.43(s,1H),8.15(dd,J=12.3,8.2 Hz,2H),8.10~7.97(m,2H),7.86~7.75(m,2H),7.75~7.65(m,2H),5.98(s,2H),4.41(s,4H),3.36(s,2H),3.30~3.17(m,4H),1.53(s,2H);13C NMR(101 MHz,DMSO-d6)δ177.21,142.23,137.40,134.69,132.14,129.89,129.63,129.18,128.25,127.94,124.07,122.55,52.17,49.57,45.74,44.77,42.93,40.66,40.37,40.14,39.83,39.62,39.41,33.46。
1.4.5 化合物5的合成
于N2条件下,称取三甲基氧鎓四氟硼酸盐(152 mg,1.0 mmol)和化合物4(239 mg,0.5 mmol)溶于二氯甲烷中,室温下搅拌48h。旋干溶剂,粗产物经多次重结晶后,得化合物5(275 mg,94.8%)。1H NMR(400 MHz,DMSO-d6)δ8.73(s,1H),8.40(s,1H),8.13(d,J=6.6 Hz,2H),8.04(d,J=8.4 Hz,2H),7.77~7.64(m,3H),6.06(s,2H),4.72(s,2H),4.62(s,2H),4.23(s,3H),3.40(s,2H),3.33(s,2H),3.24(s,2H),1.54(s,2H);13C NMR(101 MHz,DMSO-d6)δ177.15,135.00,131.04,130.02,129.63,129.37,128.24,127.94,122.44,53.78,52.24,46.01,44.86,40.34,40.03,39.91~39.87,39.71,39.40,39.14~38.68,38.61,30.21。
1.4.6 化合物P1的合成
在N2氛保护下,称取化合物5(58 mg,0.1 mmol)、第三代Grubbs化剂(G3)(41.5 mg,0.05 mmol)溶于二氯甲烷(5mL)中,室温下反应5h,随后加入乙烯基乙醚(1.5 ml)继续搅拌,然后加入甲醇析出沉淀,抽滤、洗涤后得聚合物P1(52 mg,90%收率)。1H NMR(400 MHz,CDCl3)δ8.42(d,J=33.2 Hz,2H),8.04(s,2H),7.76(s,1H),7.66(s,2H),7.30(s,1H),6.36(s,1H),5.46(s,2H),4.79(s,2H),4.60(s,2H),4.28(s,3H),3.37(s,2H),3.32~3.08(m,2H),2.84(s,1H),1.66(s,1H),1.27(s,1H)。
2 结果与讨论
2.1 合成的结构与表征
图1为聚合物P1的合成路线。首先,化合物1与NaN3经叠氮反应得到化合物2,然后化合物2与化合物3在硫酸铜催化下经点击反应合成化合物4。在三甲基氧鎓四氟硼酸盐的作用下,化合物4三唑环上5-位引入甲基,得到含三唑鎓阴离子识别位点的单体5。在第三代格拉布催化剂作用下,单体5经开环易位反应得到聚合物P1。比较聚合物及单体化合物5的1H NMR谱,可以看到原来单体5中降冰片烯位于6.06×10-6化学位移上的烯氢消失,聚合物在5.46×10-6出现了1个新峰,并且降冰片烯的桥接亚甲基的氢峰裂分为2个新峰。
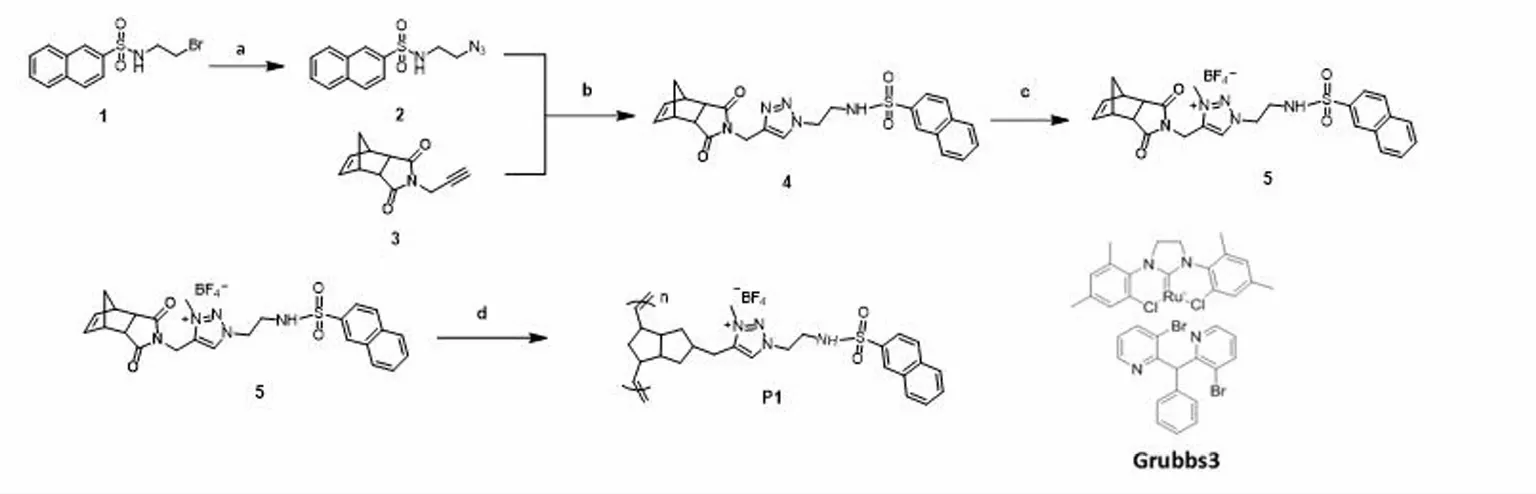
图1 聚合物P1的合成路线:a) NaN3,DMF;b) CuSO4·5H2O,NaVc,DMF;c) 三甲基氧鎓四氟硼酸盐,DCM;d) Grubbs催化剂,DCMFig.1 The synthesis route of polymer probe P1:a) NaN3,DMF;b) CuSO4·5H2O,NaVc,DMF;c) Trimethyloxonium tetrafluoroborate,DCM;d) Grubbs catalyst,DCM
2.2 单体化合物5在水溶液中的阴离子识别能力研究

λ/nm
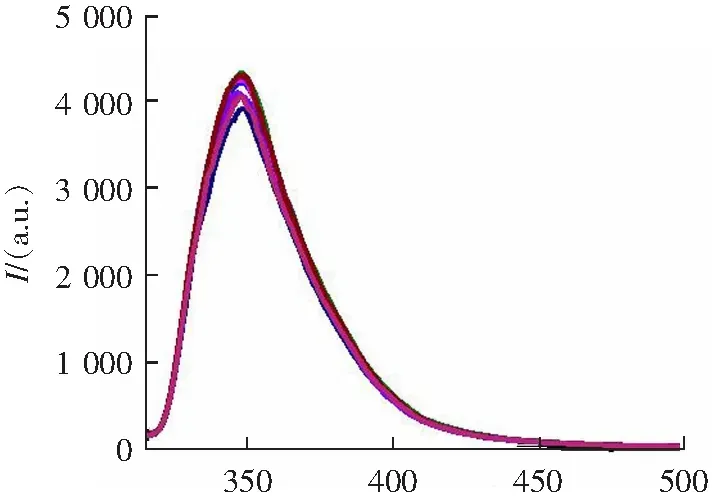
λ/nm
2.3 聚合物受体P1在水溶液中阴离子识别能力研究
同时笔者研究了聚合物受体P1(10 μmol,基于聚合物单体计)在水相中对不同阴离子的识别能力。在水溶液中,聚合物与单体紫外吸收光谱相似,但它们之间的荧光光谱却有很大的不同。如图3a所示,在280 nm激发波长下,聚合物P1在400 nm处出现了发射峰,较单体350 nm发射峰的发生了很大的红移,这可能归因于聚合物支链萘荧光团间发生π-π堆积作用的结果。
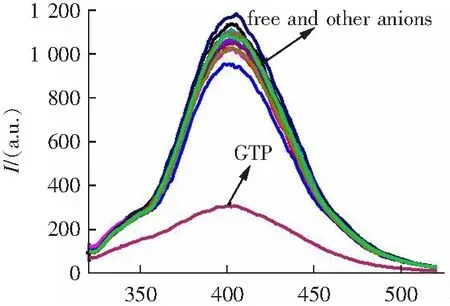
λ/nm
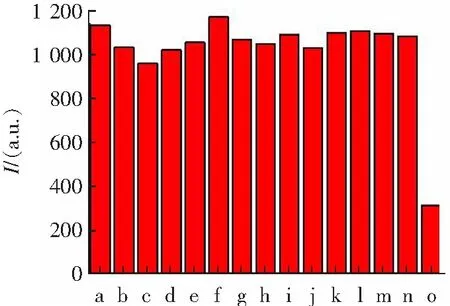
图3 a) 聚合物P1(10 μmol)在水溶液(含0.5% DMSO)中滴加50 μmol不同阴离子荧光光谱变化图;b) 在400 nm处荧光选择性柱状图Fig.3 a) The emission spectra of P1(10 μmol) before and after addition of 50 μmol various anions in aqueous solution containing.b) The relative emission intensity of P1 at 400 nm upon addition various anions
通过聚合物P1对GTP进行了荧光滴定。从图4a中可看出,随着GTP逐渐加入,聚合物受体位于400 nm处的聚集态发射峰快速下降。当滴加4倍摩尔量GTP时,其荧光强度不再下降。这些滴定数据通过Benesi-Hildebrand公式线性拟合表明P1与GTP间为1:1络合,络合常数为3.52×104mol·L-1(图4c)。同时,当GTP浓度在0~10 μmol时与P1荧光强度呈现出很好的线性关系,根据3σ/K公式可计算出P1对GTP的检测限低至0.585 μmol(图4d)。

λ/nm
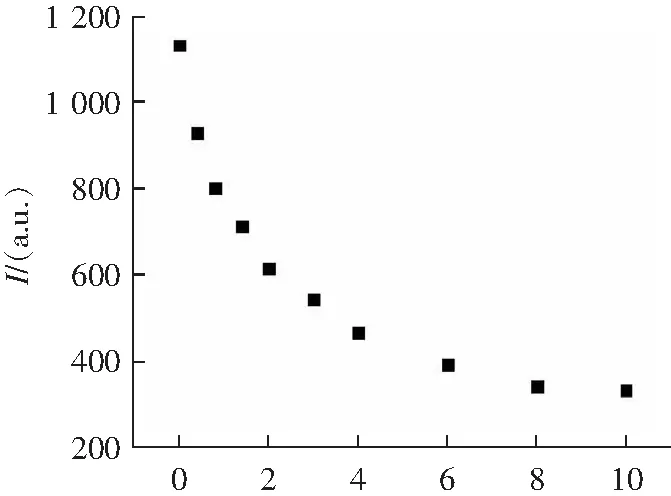
[GTP]/eq
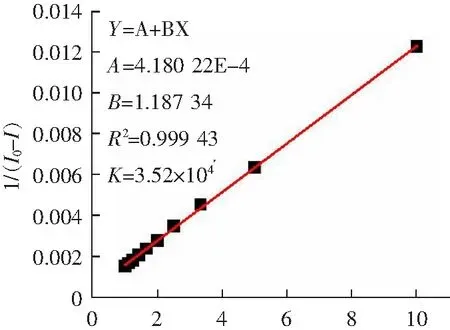
1/[GTP]
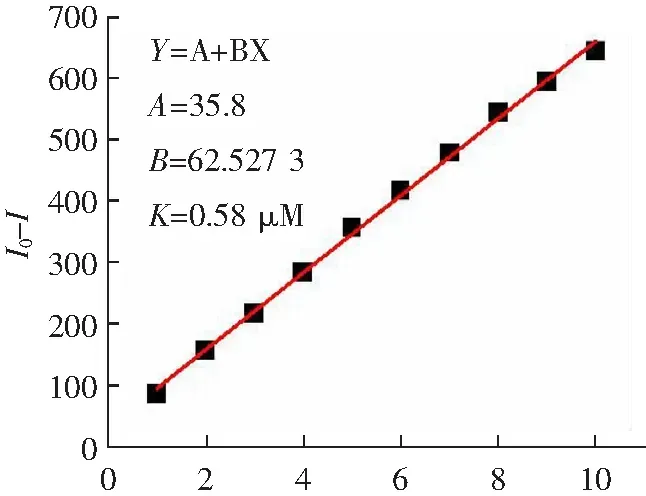
[GTP]/μmol
2.4 聚合物P1水中识别GTP竞争阴离子及不同pH值影响
作为一个好的探针,对不同共存离子的抗干扰性也非常重要。因此,笔者进一步研究了水溶液中聚合物P1在其他共存离子时对GTP的识别性质。如图5a所示,当有其他阴离子存在时P1识别GTP较仅存在GTP时荧光信号并没有明显的变化,表明聚合物P1对GTP有很好的选择性,可不受其他核苷核或阴离子干扰。同时研究了聚合物P1在不同pH值时对GTP识别性能的影响(图5b)。结果表明,在pH 6~8范围内,聚合物P1对GTP的荧光识别性能基本不受影响,保证其可用于中性水溶液及生理环境时识别GTP。
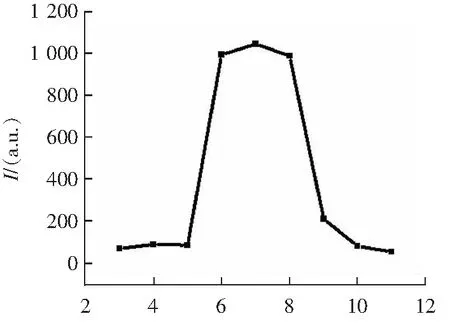
pH
2.5 聚合物P1与GTP的络合机理
根据上述荧光光谱数据,笔者假定了聚合物P1与GTP的作用机理。如图6所示,聚合物P1中存在萘荧光团在400 nm聚集体发光。当滴加GTP时,三唑鎓/酰胺与GTP带负电荷的三磷酸根通过氢键/静电引力作用,而GTP中的鸟苷碱基对与萘环通过π-π作用增强了主客体的相互作用。这样导致G碱基对与萘生色团的PET荧光猝灭,同相关文献报道一样[17]。有意思的是,对于单体5对GTP并无荧光识别能力,表明聚合物链对受体分子的空间受限能很好的增加受体分子的选择性与灵敏性。

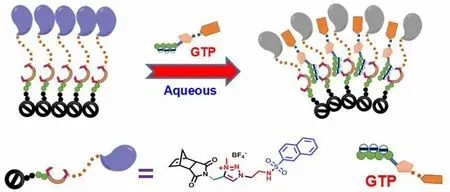
图6 聚合物P1识别GTP的机理图Fig.6 The proposed binding mechanism between P1 and GTP
3 结论
本文成功设计、合成了一种以萘为荧光团,含有三唑鎓和酰胺识别位点降冰片烯聚合物。在水相溶液中,该聚合物对GTP有很好的荧光猝灭响应,且不受其他核苷酸如ADP、AMP、ATP、UTP的干扰。相比于其单体的识别性质,表明聚合物链能增强受体分子的离子识别选择性,达到对分析物的特异性识别,同时该聚合物传感器对GTP的络合常数为3.52×104mol·L-1、检测限低至0.585 μmol。

