新型萘/苝酰亚胺取代丁二炔衍生物的合成及拓扑聚合
刘情情, 王普, 王永帅, 赵曼, 董焕丽
新型萘/苝酰亚胺取代丁二炔衍生物的合成及拓扑聚合
刘情情1,2, 王普1,2, 王永帅1,2, 赵曼1, 董焕丽1,2
(1. 中国科学院化学研究所, 北京分子科学国家重点实验室, 有机固体重点实验室, 北京 100190; 2. 中国科学院大学, 北京 100049)
经5步反应制备了萘/苝酰亚胺取代的端炔和碘炔单体, 通过Sonagashira偶联反应合成了2个新型对称丁二炔单体浅黄色粉末2-[4-(4-{4-[7-(庚-3-基)-1,3,6,8-四氧亚基-1,2,3,6,7,8-六氢异喹啉并[6,5,4-def]异喹啉-2-基]苯基}丁-1,3-二炔基)苯基]-7-(辛-4-基)-1,2,3,6,7,8-六氢异喹啉并[6,5,4-def]异喹啉-1,3,6,8-四酮(diNDI)和暗红色粉末2-[4-(4-{4-[1,3,8,10-四氧亚基-9-(二十三烷-12-基)-1,2,3,8,9,10-六氢异喹啉并[6',5',4':9,1,2]蒽并[6,5,10-def]异喹啉-2-基]苯基}丁-1,3-二炔基)苯基]-9-(二十三烷-12-基)-1,2,3,8,9,10-六氢异喹啉并[6',5',4':9,1,2]蒽并 [6,5,10-def]异喹啉-1,3,8,10-四酮(diPDI), 产率分别达60%和70%. 由于NDI和PDI基元的强吸电子作用, diNDI和diPDI表现较低的最低未占分子轨道(LUMO)能级, 分别为‒3.80和‒3.70 eV. 单晶数据表明, 萘酰亚胺基元的分子间氢键及-作用对diNDI分子堆积结构起主导作用, diNDI呈层状堆积模式. 由差示扫描量热(DSC)实验结果可知, diNDI丁二炔经加热可发生固态聚合. 加热条件下diNDI的紫外-可见吸收光谱及原位拉曼光谱特征峰以及在波长532 nm激光强度为10%的辐照条件下原位拉曼光谱特征峰的变化均表明diNDI微纳晶发生了非常规的1,4-加成聚合, 并且新生成的共轭主链是无序的, 同时发现激光辐照条件下更易促进聚合反应.
丁二炔; 萘/苝酰亚胺侧基; 单晶结构; 拓扑聚合
共轭高分子半导体材料近年来发展迅速, 基于高分子薄膜的光电器件在很多领域展现了重要应用前景[1~4]. 但高分子材料由于其分子量巨大且呈多分散性、 分子间相互作用复杂及分子链容易缠绕等特性, 薄膜中存在大量晶界缺陷, 这限制了其电荷传输特性的进一步提高以及对于高分子材料基本物性的研究[5~7].与薄膜相比, 单晶具有分子排列长程有序、 结构确定、 无晶界及缺陷密度低等特点, 是研究材料结构与性能关系等本征特性的优良载体[8~11]. 目前基于有机小分子半导体单晶及器件方面的研究已经获得了重要进展, 但是共轭高分子单晶的研究一直滞后, 大尺寸高分子晶体的获得一直都是高分子学科领域中的挑战之一[12~15]. 拓扑化学聚合是一类直接由单体单晶到聚合物单晶的固相反应, 该反应无需溶剂、 环境友好、 立体和区域选择性高, 是用来制备大尺寸高分子晶体的有效方法[16]. 1,3-丁二炔类材料(DA)是目前报道的最早一类通过单体晶体内固态拓扑化学聚合反应制备的晶态共轭高分子材料, 其电子可以沿着共轭碳-碳三键、 碳-碳双键骨架高度离域, 表现出优异的电学和非线性光学等特性[17~19]. 对于满足堆积方式的丁二炔类化合物晶体, 其经光照、 加热或高压等方式可获得高分子晶体[18,20,21]. 本课题组前期研究了10,12-二十五碳二炔酸(PCDA)的聚合物单晶发现在平行和垂直聚丁二炔高分子链方向的电荷传输呈各向异性, 沿聚合物链方向的空穴迁移率可达42.7 cm2/(V·s), 比沿堆积方向的链间电荷传输大近两个数量级. 这是第一次基于单个共轭聚合物单晶研究链内和链间的电荷传输关系, 并证明了链内电荷传输在柔性电子器件中的重要性[7]. 聚丁二炔(PDA)因其独特的光电特性而作为智能防伪材料受到越来越多的关注, 许多新型丁二炔分子已被设计和合成出来. 为了丰富分子内或分子间氢键, 研究人员在丁二炔的1,4位对称或不对称地引入含羧酸、 羟基、 氨基、 酯基、 酰胺基及磺酸酯基等的杂烷基侧基, 利用氢键作用影响单体晶体的堆积, 以利于固态拓扑化学聚合[18,20]. 含烷基侧基的聚丁二炔链在施加刺激后, 一般会发生颜色变化, 聚合物晶体会由蓝色转变为红色, 从而具有优异的生物标定或化学传感特性[22~24]. 另外, 在丁二炔的1,4位对称或不对称地引入氮、 硫、 芳烃或杂芳烃基也是一种增加丁二炔的共轭骨架长度的常用方法. 研究发现, 含芳香类丁二炔聚合物的可见光吸收边缘红移, 共轭长度增加, 聚丁二炔类材料的光电性能得到提高[25,26].
本文通过在丁二炔的1,4位引入芳香酰亚胺基元来提高单体的共轭长度, 同时由于萘酰亚胺或苝酰亚胺基元间具有较强的堆积作用及自组装调控能力[27~29], 芳香酰亚胺基元的强堆积不仅影响单体晶体的堆积方式, 还会影响分子间的电荷传输, 在芳香酰亚胺基元间形成电子传输通道, 拓扑聚合后获得双极性共轭高分子晶体. 因此, 本文经5步反应合成了芳香酰亚胺取代的新型对称丁二炔单体萘酰亚胺苯基丁二炔2-[4-(4-{4-[7-(庚-3-基)-1,3,6,8-四氧亚基-1,2,3,6,7,8-六氢异喹啉并[6,5,4-def]异喹啉-2-基]苯基}丁-1,3-二炔基)苯基]-7-(辛-4-基)-1,2,3,6,7,8-六氢异喹啉并[6,5,4-def]异喹啉-1,3,6,8-四酮(diNDI)和苝酰亚胺苯基丁二炔2-[4-(4-{4-[1,3,8,10-四氧亚基-9-(二十三烷-12-基)- 1,2,3,8,9,10-六氢异喹啉并[6',5',4':9,1,2]蒽并[6,5,10-def]异喹啉-2-基]苯基}丁-1,3-二炔基)苯基]-9-(二十三烷-12-基)-1,2,3,8,9,10-六氢异喹啉并[6',5',4':9,1,2]蒽并[6,5,10-def]异喹啉- 1,3,8,10-四酮(diPDI), 并测试了diNDI和diPDI单体的光物理和电化学性质, 同时还得到了diNDI的单晶结构并对其堆积方式及分子间相互作用进行了分析, 发现相邻diNDI单体分子间除了有C—H…相互作用外, 还存在分子间氢键, diNDI单体在晶体中呈层状堆积模式. diNDI单晶在加热或光照后的紫外-可见吸收光谱及原位拉曼光谱等实验结果表明diNDI单晶发生了非常规的1,4-加成反应, 这可能是因为萘酰亚胺基元的堆积自组装能力过强, 萘酰亚胺基元间的相互作用为诱导分子堆积的主要作用力, 使单体分子的堆积不能很好地满足1,4-加成的拓扑化学[30]. 本文工作对后续进一步合成新型丁二炔分子具有重要指导意义.
1 实验部分
1.1 试剂与仪器
萘单酰亚胺单酐(1a)和苝单酰亚胺单酐(1b)(纯度98%), 杭州奥德科技有限公司; 对碘苯胺(纯度98%), 上海安耐吉化学有限公司;-二甲基甲酰胺、 二氯甲烷、 三氯甲烷、 石油醚、 乙酸乙酯和四氢呋喃, 分析纯, 康科德科技有限公司; 三乙胺(纯度99%)、 四丁基氟化铵(1 mol/L的四氢呋喃溶液)、 醋酸钾(纯度99%)、 四-(三苯基膦)-钯(纯度99%)和氘代试剂, 北京百灵威科技有限公司; 三甲基硅乙炔(纯度98%), 梯希爱(上海)化成工业发展有限公司; 碘单质, 分析纯, 国药集团化学试剂有限公司; 柱层层析硅胶购于步琦(北京)科技有限公司.
Bruker 400 MHz型核磁共振波谱仪(1H NMR和13C NMR), 瑞士Bruker公司, 溶剂和内标分别为氘代氯仿和四甲基硅烷; Flash EA 1112型元素分析仪, 意大利Thermo Scientific公司; Ultraflextrem型高分辨基质辅助激光解析串联离子回旋共振质谱仪(HR-MALDI-FT-ICR-MS), 德国Bruker公司; Olympus BX51显微镜, 北京普瑞赛司仪器有限公司; STA 409 PC型热失重分析仪(TGA), 耐驰科学仪器商贸(上海)有限公司, 测试条件为N2气氛围, 升温速率10 K/min; Q2000型差示扫描量热仪(DSC), 美国TA仪器公司, N2气氛围, 升降温速率均为10 K/min; CHI660C电化学工作站,上海晨华科技股份有限公司, 以铂电极为工作电极, Ag/AgCl电极为参比电极, 对电极为铂丝, 四丁基六氟磷酸为支持电解质, 以超干三氯甲烷作为溶剂, 样品浓度1×10‒3mol/L; 理论计算研究使用Gaussian 16软件平台, 采用B3LYP泛函、 6-31G**基组进行几何结构的优化和能级计算; Hitachi Model UH4150型分光光度仪(UV-Vis), 日本Hitachi公司, 光学带隙由公式gopt=1240/onset计算获得; Bruker Multimode 3型原子力显微镜(AFM), 德国Bruker公司; LabRAM HR Evolution型显微共焦激光拉曼光谱仪(Raman), 法国Horiba公司, 测试激光波长为532 nm.
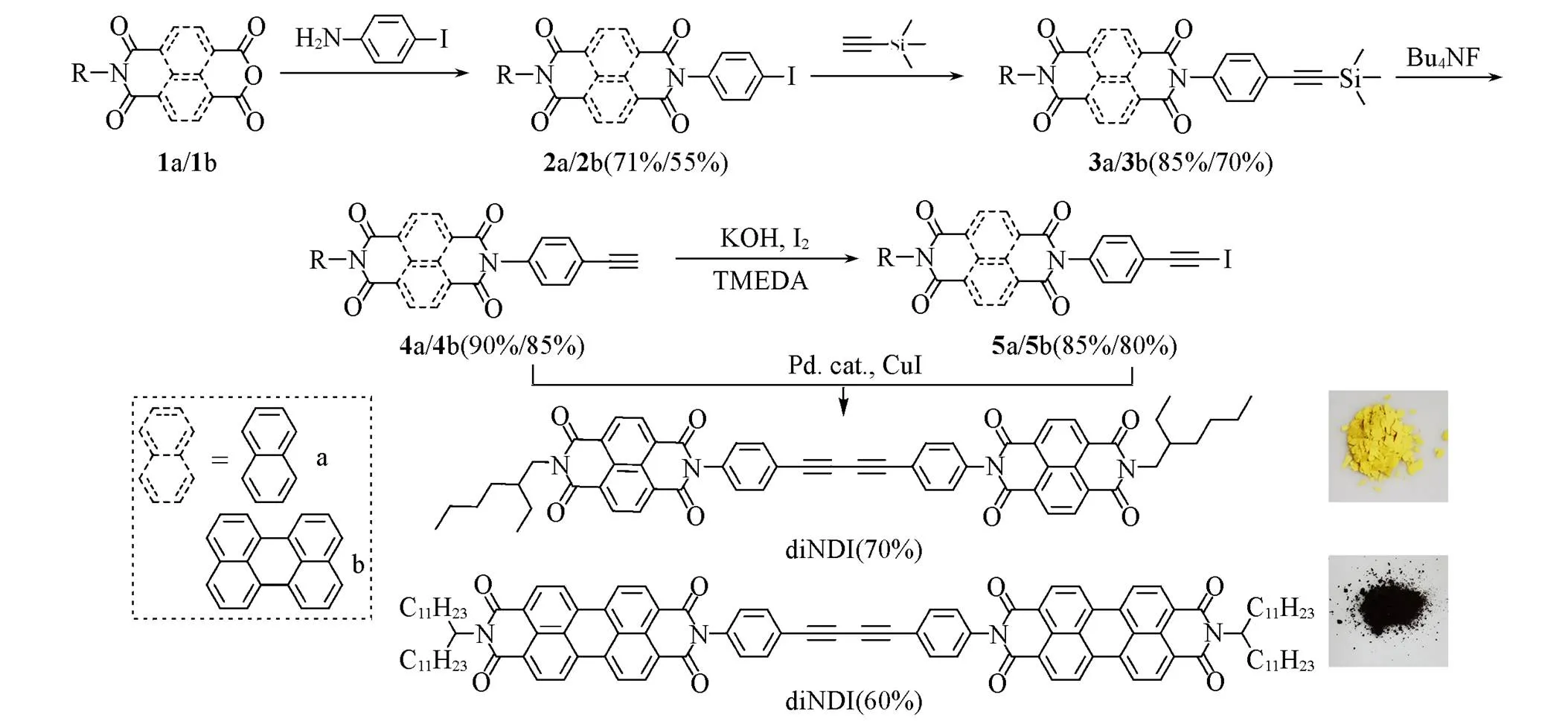
Scheme 1Synthetic routes of diNDI and diPDI
1.2 实验过程
萘酰亚胺苯基或苝酰亚胺苯基代端炔的Glaser偶联产率较低, 主要得到碘代炔烃产物. 因此, 本文在此基础上改进了合成路线, 如Scheme 1所示, 经5步反应得到芳香酰亚胺取代的端炔和碘炔单体, 再由该单体经Sonagashira偶联反应合成2种新型对称丁二炔单体, 最终得到浅黄色固体diNDI和暗红色固体diPDI, 产率分别达到60%和70%.
1.2.1萘酰亚胺苯基碘(2a)/苝酰亚胺苯基碘(2b)的合成在100 mL反应瓶中依次加入4.0 mmol化合物萘单酰亚胺单酐(1a)或苝单酰亚胺单酐(1b)和40 mL-二甲基甲酰胺, 氩气鼓泡15 min后加热溶解底物, 并于130 ℃回流1 h; 向反应瓶中滴加10 mL溶解了8.0 mmol对碘苯胺的-二甲基甲酰胺溶液, 滴加完成后加热回流反应12 h; 由薄层色谱(TLC)监测反应至完全, 停止反应; 旋转蒸干溶剂并用二氯甲烷和水洗涤萃取, 合并有机相, 旋转蒸干得到的粗产物经硅胶柱层析进行分离提纯, 洗脱剂为石油醚/二氯甲烷(体积比为3∶1). 产物2a为乳白色固体粉末, 产率为71%.1H NMR(400 MHz, CDCl3),: 8.80(s, 4H), 7.91(d,=7.5 Hz, 2H), 7.08(d,=7.5 Hz, 2H), 4.16(t,=7.4 Hz, 2H), 2.01~1.90(m, 1H), 1.44~1.28(m, 8H), 0.98~0.93(m, 3H), 0.92~0.86(m, 3H). 产物2b为深红色固体粉末, 产率为55%.1H NMR(400 MHz, CDCl3),: 8.66(d,=7.9 Hz, 4H), 8.54(d,=8.1 Hz, 4H), 7.90(d,=8.4 Hz, 2H), 7.13(d,=8.4 Hz, 2H), 5.19~5.15(m, 1H), 2.26~2.22(m, 2H), 1.98~1.80(m, 2H), 1.35~1.20(m, 36H), 0.84(t,=6.8 Hz, 6H).
1.2.2萘酰亚胺苯基三甲基硅乙炔(3a)/苝酰亚胺苯基三甲基硅乙炔(3b)的合成在50 mL Schlenk反应瓶中依次加入1.0 mmol化合物2a或2b, 2%(摩尔分数)的催化剂Pd[P(Ph)3]2Cl2和4%(摩尔分数)的CuI, 并用氩气置换3次; 向反应瓶中加入20 mL四氢呋喃和5 mL三乙胺; 于30 ℃下向反应瓶中缓慢滴加1.2 mmol三甲基硅乙炔, 于65 ℃下搅拌反应6 h; 由TLC监测反应至完全, 停止反应; 旋转蒸干有机溶剂并用二氯甲烷和水洗涤萃取, 合并有机相, 旋转蒸干得到的粗产物经硅胶柱层析进行分离提纯, 洗脱剂为二氯甲烷. 产物3a为米白色固体粉末, 产率为85%.1H NMR(400 MHz, CDCl3),: 8.78(s, 4H), 7.65(d,=8.5 Hz, 2H), 7.28(s, 1H), 7.25(s, 1H), 4.21~4.09(m, 2H), 2.00~1.91(m, 1H), 1.47~1.24(m, 9H), 0.98~0.86(m, 6H), 0.28(s, 9H). 产物3b为深红色固体粉末, 产率为70%.1H NMR(400 MHz, CDCl3),: 8.73~8.62(m, 8H), 7.65(d,=8.1 Hz, 2H), 7.30(d,=8.2 Hz, 2H), 5.22~5.15(m, 1H), 2.28~2.20(m, 2H), 1.89~1.84(m, 2H), 1.32~1.20(m, 36H), 0.84(t,=6.8 Hz, 6H), 0.28(s, 9H).
1.2.3萘酰亚胺苯基乙炔(4a)/苝酰亚胺苯基乙炔(4b)的合成在50 mL反应瓶中加入2 mmol化合物3a或3b, 并加入60 mL四氢呋喃使其溶解; 向反应瓶中加入0.5 mL 1 mol/L四丁基氟化铵的四氢呋喃溶液, 室温条件下搅拌反应2 h; 由TLC监测反应至完全, 停止反应; 旋转蒸干溶剂, 得到的粗产物经硅胶柱层析进行分离提纯, 洗脱剂为石油醚/乙酸乙酯(体积比为20∶1). 产物4a为黄色固体粉末, 产率为90%.1H NMR(400 MHz, CDCl3),:8.80(s, 4H), 7.69(d,=7.7 Hz, 2H), 7.30(d,=7.6 Hz, 2H), 4.16(t,=7.3 Hz, 2H), 3.16(s, 1H), 1.98~1.94(m, 1H), 1.47~1.24(m, 8H), 0.97~0.87(m, 6H).13C NMR(101 MHz, CDCl3),: 163.07, 162.81, 134.83, 133.25, 131.44, 131.09, 128.67, 127.03, 126.49, 123.29, 78.51, 77.23, 44.71, 37.96, 30.73, 28.64, 24.08, 23.04, 14.07, 10.61. HR-MALDI-FT-ICR-MS, C30H26N2O4([M])计算值(实验值),/: 478.188709(478.189257). 产物4b为深红色固体粉末, 产率为85%.1H NMR(400 MHz, CDCl3),: 8.71~8.59(m, 8H), 7.69(d,=8.4 Hz, 2H), 7.34(d,=8.5 Hz, 2H), 5.20~5.16(m, 1H), 3.16(s, 1H), 2.24(m, 2H), 1.87(m, 2H), 1.33~1.20(s, 35H), 0.84(t,=6.9 Hz, 6H).13C NMR(101 MHz, CDCl3),: 163.29, 133.17, 131.80, 128.82, 123.30, 123.07, 123.00, 78.22, 54.89, 32.38, 31.91, 29.62, 29.59, 29.55, 27.01, 22.67, 14.09. HR-MALDI-FT-ICR-MS, C55H61N2O4([M]+)计算值(实验值),/: 813.462585(813.462488).
1.2.4萘酰亚胺苯基碘乙炔(5a)/苝酰亚胺苯基碘乙炔(5b)的合成在50 mL反应瓶中加入1.8 mmol化合物4a或4b, 并加入10 mL四氢呋喃使其溶解; 加入碘单质和3.6 mmol醋酸钾, 室温条件下搅拌反应8 h; 由TLC监测反应至完全, 停止反应; 旋转蒸干有机溶剂, 用乙酸乙酯萃取反应液(30 mL×3), 合并有机相, 用真空旋转蒸发仪旋转蒸干有机溶剂, 得到的粗产物经硅胶柱层析进行分离提纯, 洗脱剂为石油醚/乙酸乙酯(体积比为30∶1). 产物5a为浅黄色固体粉末, 产率为85%.1H NMR(400 MHz, CDCl3),:8.80(s, 4H), 7.62(d,=8.3 Hz, 2H), 7.28(d,=8.3 Hz, 2H), 4.18~4.11(m, 2H), 1.99~1.93(m, 1H), 1.45~1.24(m, 8H), 0.97~0.87(m, 6H).13C NMR(101 MHz, CDCl3),: 163.07, 162.81, 134.79, 133.42, 131.45, 131.10, 128.61, 127.05, 127.04, 126.47, 124.45, 77.22, 44.71, 37.96, 30.72, 28.64, 24.08, 23.04, 14.07, 10.61. HR-MALDI-FT-ICR-MS, C30H25IN2O4([M])计算值(实验值) ,/: 604.085357(604.085099). 产物5b为深红色固体粉末, 产率为80%.1H NMR(400 MHz, CDCl3),: 8.58(d,=7.9 Hz, 4H), 8.43~8.40(m, 4H), 7.60(d,=8.4 Hz, 2H), 7.35(d,=8.5 Hz, 2H), 5.18~5.14(m, 1H), 2.27~2.22(m, 2H), 1.93~1.87(m, 2H), 1.36~1.17(m, 36H), 0.84(t,=6.8 Hz, 6H).13C NMR(101 MHz, CDCl3),: 135.35, 133.34, 131.86, 128.75, 123.34, 123.04, 54.87, 32.37, 31.91, 29.61, 29.58, 29.54, 29.32, 26.99, 22.67, 14.09. HR-MALDI-FT-ICR-MS, C55H60IN2O4([M]+)计算值(实验值),/: 939.359233(939.357791).
1.2.5diNDI/diPDI的合成在50 mL Schlenk反应瓶中依次加入0.5 mmol化合物5a或5b、 0.5 mmol化合物4a或4b、 2%(摩尔分数)催化剂Pd[P(Ph)3]4和2%(摩尔分数)CuI, 并用氩气置换3次; 然后向反应瓶中加入10 mL四氢呋喃和5 mL三乙胺; 室温条件下搅拌反应5 h, 由TLC监测反应至完全; 反应液用真空旋转蒸发仪旋转蒸干, 并用三氯甲烷萃取反应液(30 mL×3), 合并有机相, 得到的粗产物用氯仿和甲醇重结晶. 产物diNDI为浅黄色固体粉末, 产率为70%.1H NMR(400 MHz, CDCl3),: 8.82(s, 8H), 7.75(d,=7.7 Hz, 4H), 7.34(d,=7.8 Hz, 4H), 4.22~4.12(m, 4H), 1.98~1.93(m, 2H), 1.42~1.32(m, 16H), 0.98~0.87(m, 12H).13C NMR(101 MHz, CDCl3),: 133.65, 131.52, 131.13, 128.92, 127.13, 77.49, 23.05, 14.07, 10.62. HR-MALDI-FT-ICR-MS, C60H50N4O8([M])计算值(实验值),/: 954.362316(954.363604). 产物diPDI为暗红色固体粉末, 产率为60%.1H NMR(400 MHz, CDCl3),:8.77~8.54(m, 16H), 7.75(d,=8.3 Hz, 4H), 7.37(d,=8.3 Hz, 4H), 5.22~5.14(m, 2H), 2.29~2.21(m, 4H), 1.93~1.84(m, 4H), 1.32~1.20(m, 72H), 0.84(t,=6.8 Hz, 12H).13C NMR(101 MHz, CDCl3),:163.33, 135.29, 133.57, 131.92, 129.03, 123.39, 123.06, 77.21, 32.37, 31.91, 29.62, 29.59, 29.55, 29.33, 27.00, 22.67, 14.11. HR-MALDI-FT-ICR-MS, C110H119N4O8([M]+)计算值(实验值),/: 1623.902243(1623.901022).
2 结果与讨论
2.1 单体的光物理和电化学性质
图1(A)为室温下单体的固态粉末与三氯甲烷稀溶液(1×10‒5mol/L)的紫外-可见吸收光谱. 稀溶 液中diNDI(曲线)和diPDI(曲线)单体刚性较大, 分子振动小, 光谱中精细峰较明显[27]. 而固态聚 集态下分子间作用力较强, diNDI(曲线)和diPDI(曲线)吸收边均红移; diNDI单体吸收边onset约为416 nm, 经计算光学带隙(Δgopt)约为2.98 eV; diPDI单体吸收边onset约为571 nm, 经计算光学带隙约为2.18 eV. 利用循环伏安法(CV), 以二茂铁为外标进行了diNDI和diPDI的循环伏安实验[图1(B)]. CV曲线的还原区电化学行为是完全可逆的过程, 表明diNDI(曲线)和diPDI(曲线)分子保持良好的电化学稳定性[31]. 根据CV曲线的起峰点, 经计算得出diNDI和diPDI的最低电子未占分子轨道 (LUMO)能级值分别为‒3.80和‒3.70 eV, LUMO能级减去光学带隙得到最高电子占据分子轨道 (HOMO)能级(diNDI和diPDI分别为‒6.78和‒5.88 eV), 与萘/苝酰亚胺单体能级相比, diNDI和diPDI分子上的双芳香酰亚胺取代基对丁二炔能级影响较大[32].

Fig.1 Normalized UV⁃Vis absorption spectra(A) and cyclic voltammetry curves(B) of diNDI and diPDI
(A)diNDI, powder;. diNDI, dilute trichloromethane solution;diPDI, powder;diPDI, dilute trichloromethane solution.(B)diNDI;. diPDI.
为了进一步了解丁二炔单体的电子云分布, 通过理论计算(Gaussian 16软件平台)模拟了diNDI和diPDI的HOMO和LUMO能级电子云分布图. 从图2可以看出, diNDI和diPDI的LUMO能级存在轨道简并, 电子云主要分布在受体萘酰亚胺或苝酰亚胺基元上; 而HOMO轨道的电子云分布在给体丁二炔基元上, 显示出较明显的HOMO与LUMO轨道电子云分离. 具体的实验及计算能级如表1所示.

Fig.2 Molecular orbital diagrams with selected isodensity frontier molecular orbitals mainly involved in the electronic transitions of diNDI(A) and diPDI(B)

Table 1 Summary of tested and calculated energy levels
Calculated from the solid absorption onsets according to Δgopt=1240/onset;. LUMO levels were obtained by CV;calculated energy levels of diNDI and diPDI.
2.2 diNDI的晶体结构
为了研究丁二炔单体衍生物的分子排列, 室温下在三氯甲烷-甲醇(体积比3∶1)体系中分别生长diNDI和diPDI单体的单晶. 通过液相扩散法获得了diNDI浅黄色单晶, 而diPDI由于取代烷基链过长, 仅得到了黏稠的块状产物, 未得到单晶. 经X射线单晶衍射分析可知, diNDI晶体属于单斜晶系,2/空间群, 晶格常数为=3.93615(12) nm,=0.52254(2) nm,=2.57293(8) nm,=90°,=104.440°,=90°. 单分子diNDI的单晶结构如图3(A)所示, 因其分子内萘酰亚胺基元位阻原因, 苯基和萘酰亚胺基元之间呈现72.83°的分子内扭角. diNDI整体分子堆积方式如图3(B)所示, 为简洁起见, 删掉萘酰亚胺上的烷基链仅保留了主体部分. diNDI分子整体呈层状堆积, 层间距为0.467 nm, 同时相邻两层间堆积呈对称关系. diNDI层内堆积方式如图3(C)所示, 相邻单体分子间的C1—C1′间距离为0.5225 nm, C1—C4′间距离为0.6444 nm. 相邻diNDI单体分子间除了有C—H…相互作用外, 还存在分子间氢键, 包括萘酰亚胺基元和苯基间的C—H…O键(分别为0.2625和0.2326 nm). 而碳链部分主要以空间位阻的形式影响堆积, 没有分子间相互作用的影响. diNDI层间堆积方式如图3(D)所示, 其分子间相互作用主要为萘酰亚胺基元和相邻分子的取代烷基链的氢键C—H…O(0.2593 nm), 二者同时影响单体分子的组装堆积, 具体晶胞参数见表2. 通过溶剂辅助自组装法, 我们在三氯甲烷的气氛下将 diNDI的三氯甲烷稀溶液滴在未修饰的二氧化硅基底上析出棒状单晶[图4(A)], 实验表明diNDI单晶在0°和45°偏光镜下显示出明显的消光, 这表明diNDI分子在单晶中高度有序排列[图4(B, C)]. AFM测试结果[图4(D)]显示单晶表面光滑, 厚度约170 nm. 将单晶数据用Mercury软件进行晶体生长模拟, 计算结果表明, diNDI可能沿[010]方向生长[图4(E)]. diNDI规整的棒状晶体结构有利于后续的拓扑聚合研究.

Fig.3 Crystal structures of diNDI
(A) Molecular conformation; (B) typical layer packing; (C) intralayer multi-short intermolecular interaction;(D) interlayer multi-short intermolecular interaction.

Table 2 Crystal data and structure refinements of diNDI

Fig.4 Optical microscopy image(A) and polarized images(B, C) and AFM height image(D) of diNDI crystals and predicted growth morphology of diNDI(E)
(A) The optical microscopy image; (B) Polarized image under crossed 0°; (C) Polarized image under crossed 45°.
2.3 diNDI的热学性质
通过TGA和DSC对diNDI单体的热学性质进行了研究. TGA分析[图5(A)]表明, diNDI的热分解 温度(d, 对应5%的质量损失)在412 ℃左右. 在分解温度以下对diNDI进行了循环两次的DSC测试 [图5(B)], 实验结果显示, 第一次扫描循环曲线在升温过程中于203 ℃出现放热峰, 降温过程中没有对应的峰产生, 而且第二次扫描循环时不再出现放热峰, 说明diNDI丁二炔单体在升温过程中发生了固相聚合反应, 但是固态聚合是否为丁二炔的1,4-加成反应还需进一步验证[33].
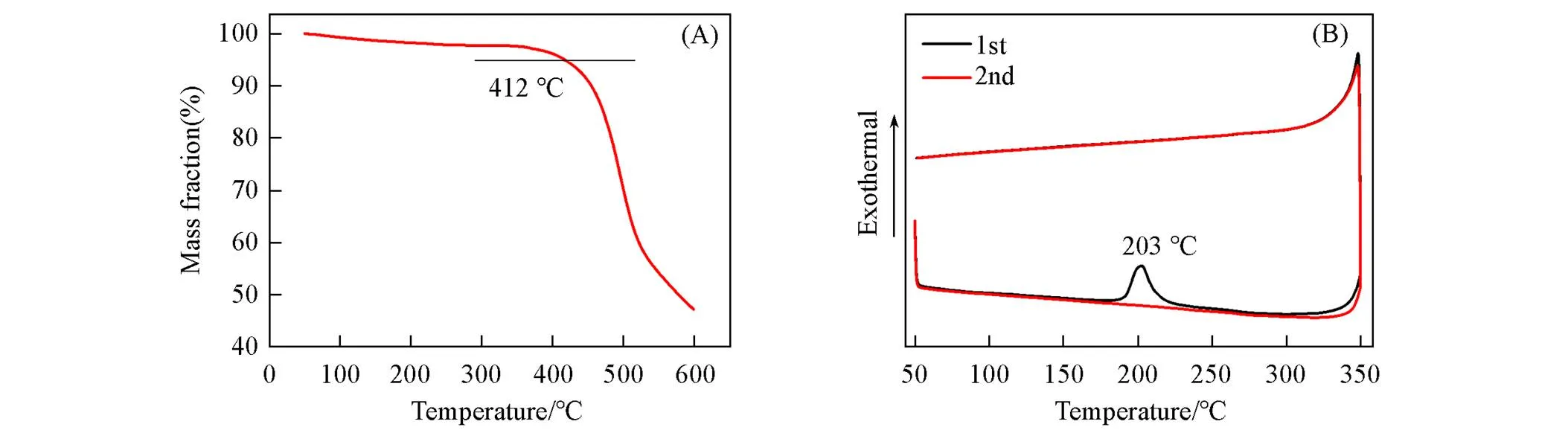
Fig.5 TGA curves(A) and first and second⁃scan DSC thermograms(B) of diNDI under nitrogen atmosphere with a heating or cooling rate of 10 ℃/min
2.4 diNDI微纳晶的拓扑聚合
加热和光照是丁二炔单体发生拓扑聚合常用的实验条件. 首先, 本文研究了加热条件下diNDI微纳晶的拓扑聚合. 由DSC结果可知, diNDI单体在203 ℃出现明显的放热峰, 本文选择放热峰的起始位置190 ℃对微纳晶进行加热及原位测试. 由图6(A)可见, diNDI微纳晶单体在加热过程中紫外-可见光谱吸收边明显红移, 加热时间至3和6 h时峰形变化不大, 并且在500~600 nm左右没有出现新的激子吸收峰, 初步表明diNDI丁二炔碳-碳三键可能是以扭曲的结构而不是以常规的1,4-加成反应形成完全共轭的聚合物主链[34]. 本文同时进行了不同加热时间下diNDI的原位拉曼光谱测试[图6(B)], 实验结果显示丁二炔单体碳-碳三键的特征峰(约2208 cm‒1)在加热后强度逐渐减弱, 并且DSC测试残余样品的拉曼单体特征峰消失, 但没有出现1,4-加成反应生成的碳-碳三键的特征峰(约2100 cm‒1), 也证明了diNDI丁二炔单体的碳-碳三键在固态条件下发生了非常规的1,4-加成聚合反应. 加热前后diNDI微纳晶的颜色和形貌基本没有变化[图(7)], 可能是聚合度太低, 晶体中主要还是单体分子的原因.

Fig.6 UV⁃Vis absorption spectra(A) and micro⁃Raman spectra with 532 nm laser(B) of diNDI microcrystal as a function of the heating time

Fig.7 Optical microscopy images of diNDI crystal with different heating times at 190 ℃
(A) Monomer. Time/min: (B) 1; (C) 3; (D) 6; (E) 10.
本文还研究了激光辐照对diNDI微纳晶拓扑聚合的影响. 采用波长532 nm-10%激光强度对二氧化硅基底上的diNDI微纳晶进行不同时间的激光辐照[图8(A)], 并进行原位拉曼光谱测试. 图8(B)实验结果显示, 随着激光照射时间的延长, diNDI丁二炔碳-碳三键的特征峰(约2208 cm‒1)强度逐渐变弱, 但是没有新生成的碳-碳三键特征峰(约2100 cm‒1). 丁二炔中的碳-碳三键特征峰在辐照10 min后强度基本不再变化, 说明激光辐照更容易促进聚合反应, 但聚合后的共轭链是无序的[35]. 同时, 本文还观察到原位测试后的单晶表面变暗(图9), 可能是由于晶体表面的diNDI分子局部无序聚合导致的.

Fig.8 Schematic of experimental setup for laser irradiation(A) and in⁃situ Raman spectra of diNDI crystal irradiated with 532 nm laser for different times(B)
. Monomer. Time/min:. 1;. 3;. 6;. 10.

Fig.9 Optical microscopy images of diNDI crystal irradiated with 532 nm laser for different times
Time/min: (A) 0; (B) 1; (C) 3; (D) 6; (E) 10.
3 结 论
通过5步反应制备了芳香酰亚胺端炔和碘炔单体, 再经Sonagashira偶联反应合成了2种新型对称丁二炔单体diNDI和diPDI, 产率分别达到60%和70%.由光物理及电化学测试得到diNDI和diPDI的LUMO能级分别为‒3.80和‒3.70 eV, HOMO能级分别为‒6.78和‒5.88 eV. 通过液相扩散法得到diNDI浅黄色单晶并解析了单晶结构. diNDI的单晶数据表明, 萘酰亚胺基元间氢键及-作用影响diNDI分子间的组装堆积. 基于TGA及DSC实验分析, diNDI丁二炔经加热可发生固态聚合. 测试了加热条件下diNDI的紫外-可见吸收光谱和原位拉曼光谱特征峰以及波长532 nm激光强度10%辐照条件下原位拉曼光谱特征峰的变化, 结果表明, diNDI微纳晶在加热或激光辐照条件均发生了非常规的1,4-加成拓扑聚合, 这归因于其特殊的分子堆积结构, 同时发现激光辐照条件可促进聚合反应的发生. 本课题组后续的工作会进一步对芳香酰亚胺类取代的丁二炔衍生物进行研究, 包括丁二炔单体的不对称改造、 堆积方式的调控以及后续拓扑聚合条件的筛选等系列研究.
[1] Wang Y., Sun L. J., Wang C., Yang F. X., Ren X. C., Zhang X. T., Dong H. L., Hu W. P.,, 2019,(6), 1492—1530
[2] Lin C. C., Peng B. Y., Li H. Y., ,, 2021,(6), 1672—1684(林城策, 彭博宇, 李寒莹. 高等学校化学学报, 2021,(6), 1672—1684)
[3] Ni Z. J., Wang H. L., Dong H. L., Dang Y. F., Zhao Q., Zhang X. T., Hu W. P.,, 2019,(3), 271—277
[4] Yao Z. F., Li Q. Y., Wu H. T., Ding Y. F., Wang Z. Y., Lu Y., Wang J. Y., Pei J.,, 2021,(3), 378—387
[5] Dong H. L., Hu W. P.,, 2016,(11), 2435—2443
[6] Shao W., Dong H. L., Jiang, L., Hu W. P.,, 2011,(4), 590—600
[7] Yao Y. F., Dong H. L., Liu F., Russell T. P., Hu W. P.,, 2017,(29), 1701251
[8] Wang C. L., Dong H. L., Jiang L., Hu W. P.,, 2018, 47(2), 422—500
[9] Zhang X. T., Dong H. L., Hu W. P.,, 2018,(44), 1801048
[10] Xie Z. Y., Liu D., Zhang Y. H., Liu Q. Q., Dong H. L., Hu W. P.,, 2020,(6), 1179—1193(谢子仪, 刘单, 张逸寒, 刘情情, 董焕丽, 胡文平. 高等学校化学学报, 2020,(6), 1179—1193)
[11] Wang P., Liu D., Wang Y. S., Zhang P., Yu P. P., Wang M. C., Zhen Y. G., Dong H. L., Hu W. P.,, 2020,(11), 2909—2912
[12] Zhao K. F., Zhang Q., Chen L., Zhang T., Han Y. C.,, 2021,(5), 2143—2154
[13] Wang Z. L, Gao M. Y., He C. Y., Shi W. C., Deng Y. F., Han Y., Ye L., Geng Y. H.,, 2021,(7), 2108255
[14] Dong H. L., Yan Q. Q., Hu W. P.,, 2017,, 1246—1260(董焕丽, 燕青青, 胡文平. 高分子学报, 2017,, 1246—1260)
[15] Dong H. L., Jiang S. D., Jiang L., Liu, Y. L., Li H. X., Hu W. P., Wang E. J., Yan S. K., Wei Z. M., Xu W., Gong X.,, 2009,(47), 17315—17320
[16] Yan Q. Q., Yao Y. F., Dong H. L., Hu W. P.,, 2016,(10), 1007—1022(燕青青, 姚奕帆, 董焕丽, 胡文平. 中国科学: 化学, 2016,(10), 1007—1022)
[17] Wegner G.,1969,, 824—832
[18] Li Q. Y., Yao Y. F., Qiu G. G., Zhang P., Dong H. L., Hu W. P.,,2016,(24), 2688—2706(李清源, 姚奕帆, 仇格格, 张盼, 董焕丽, 胡文平. 科学通报, 2016,(24), 2688—2706)
[19] DeCicco R. C., Luo L., Goroff N. S.,, 2019,(8), 2080—2089
[20] Hema K., Ravi A., Raju C., Pathan J. R., Rai R., Sureshan K. M.,, 2021,(6), 4062—4099
[21] Zhang P. J., Tang X. Y., Wang Y. D., Wang X., Gao D. X., Li Y. P., Zheng H. Y., Wang Y. J., Wang X. X., Fu, R. Q., Tang M. X., Ikeda K., Miao P., Hattori T., Sano-Furukawa A., Tulk C. A., Molaison J. J., Dong X., Li K., Ju J., Mao H. K.,, 2020,(41), 17662—17669
[22] Lee S., Kim J. Y., Chen X., Yoon J.,,2016,(59), 9178—9196
[23] Weston M., Tjandra A. D., Chandrawati R.,, 2020,(2), 166—183
[24] Choi Y. J., Park S., Yoon W. J., Lim S. I., Koo J., Kang D. G., Park S., Kim N., Jeong K. U.,, 2020,(39), 2003980
[25] Lin F. J., Yang C. W., Chen H. H., Tao Y. T.,, 2020,(27), 11763—11771
[26] Martin I. J., Shih K. C., Nieh M. P., Kasi R. M.,, 2020,(11), 4501—4510
[27] Kobaisi M. A., Bhosale S. V., Latham K., Raynor A. M., Bhosale S. V.,, 2016,(19), 11685—11796
[28] Wurthner F., Saha-Moller C. R., Fimmel B., Ogi S., Leowanawat P., Schmidt D.,, 2016,(3), 962—1052
[29] Seo J., Kantha C., Joung J. F., Park S., Jelinek R., Kim J. M.,, 2019,(19), 1901342
[30] Ikeshima M., Katagiri H., Fujiwara W., Tokito S., Okada S.,, 2018,(10), 5991—6000
[31] Zhang H. D., Gu P. P., Zhang F., Du M. X., Ye K. Q., Liu Y.,, 2021,(12), 3571—3578(张慧东, 谷盼盼, 张芳, 都明旭, 叶开其, 刘宇. 高等学校化学学报, 2021,(12), 3571—3578)
[32] Guo S., Wu W., Guo H., Zhao J.,, 2012,(8), 3933—3943
[33] Doan T. H., Talbi I., Lohier J. F., Touil S., Alayrac C., Witulski B.,, 2016,, 127—134
[34] Ikeshima M., Mamada M., Minami T., Tokito S., Okada S.,, 2016,(10), 1013—1018
[35] Maeda K., Hong L., Nishihara T., Nakanishi Y., Miyauchi Y., Kitaura R., Ousaka N., Yashima E., Ito H., Itami K.,, 2016,(34), 11001—11008
Synthesis and Topochemical Polymerization Study of Naphthalene/perylene Imides Substituted Diacetylene Derivatives
LIUQingqing1,2, WANGPu1,2, WANGYongshuai1,2, ZHAOMan1, DONGHuanli1,2*
(,,,,100190,;,100049,)
Naphthalene/perylene imide substituted terminal alkyne and iodide monomers were prepared by a five-step reaction. Two new symmetric diacetylene monomers, pale yellow powder 2-(2-ethylhexyl)-7-{4-[7-(2-ethylhexyl)-1,3,6,8-tetraoxo-1,2,3,3a,5a,6,7,8-octahydroisoquinolino[6,5,4-def]isoquinolin-2-yl]buta-1,3-diynyl}- 1,2,3,6,7,8-hexahydroisoquinolino[6,5,4-def]isoquinoline-1,3,6,8-tetraone(diNDI) and deep red powder 9-{4-[1,3,8,10-tetraoxo-9-(tricos-12-yl)-1,2,3,8,9,10-hexahydroisoquinolino[6',5',4':9,1,2]anthra[6,5,10-def]isoquinolin-2-yl]buta-1,3-diynyl}-2-(tricos-12-yl)-1,2,3,8,9,10-hexahydroisoquinolino[6',5',4':9,1,2]anthra[6,5,10-def]isoquinoline-1,3,8,10-tetraone(diPDI), were synthesized by the Sonagashira coupling reaction with yields up to 60% and 70%, respectively. Due to the strong electron-withdrawing of NDI and PDI side groups, they exhibited deeper lowest unoccupied molecular orbital energy levels of -3.80 and -3.70 eV, respectively. The single crystal data of diNDI showed that the intermolecular hydrogen bonding and-interaction of naphthalene imide units mediated the intermolecular assembly of diNDI, showing a layer packing model. The differential scanning calorimetry results indicated that diNDI polymerized in solid-state under heating. The changes in the UV-Vis absorption andRaman spectra of diNDI under heating and 532 nm-10% laser irradiation condition indicated that diNDI microcrystals might react to form a distorted structure instead of a fully conjugated backbone that usually resulted from the regular 1,4-addition. The laser irradiation conditions were found to facilitate the polymerization reaction.
Diacetylene; Naphthalene/perylene imides side group; Single crystal structure; Topochemical polymerization
O621.25
A
10.7503/cjcu20220091
2022-02-15
2022-04-04.
董焕丽, 女, 博士, 研究员, 主要从事有机光电功能材料与器件方面的研究. E-mail: dhl522@iccas.ac.cn
国家自然科学基金(批准号: 21875259, 51725304)和北京分子科学国家研究中心项目(批准号: BNLMS-CXXM-202012)资助.
Supported by the National Natural Science Foundation of China(Nos.21875259, 51725304) and the Beijing National Laboratory for Molecular Sciences, China(No.BNLMS-CXXM-202012).
(Ed.: W, K, M)

