多孔二氧化硅微球对制革工业废水中蛋白质的吸附分离研究
强涛涛, 朱润桐
(陕西科技大学 轻工科学与工程学院 轻化工程国家级实验教学示范中心, 陕西 西安 710021)
0 引言
蛋白质是生命的物质基础,它作为一种生物大分子,可以在体内执行多种生物学功能,如酶的催化、能量运载和储存、免疫保护等[1].然而,在工业(如制革业、农业以及制药业等)生产过程中存在着蛋白质的损失,尤其是制革工业废水中含有大量的可溶性蛋白质,这不仅会导致自然资源的富养化和恶化,而且对水生生物产生毒性作用[2-3].因此,构建一种高效的、简单的分离纯化废水中蛋白质的方法具有重要意义.
随着技术的发展,许多新的技术被应用到蛋白质分离纯化中,如色谱法、沉淀法、层析法、电泳法、超滤法、离心法、膜分离技术、吸附法等[4-6],其中吸附法凭借其操作简单、耗时短、易于加工、成本低等优点成为蛋白质分离研究中广泛应用的一种技术[7].目前,已开发了各种吸附剂,如金属氧化物、气凝胶、有机聚合物、二氧化硅等.其中,SiO2因其具有低毒性、良好的生物相容性、易于功能化的表面、可调的粒径以及有序多孔的孔道结构等优点,故被广泛应用于催化载体、吸附与分离、药物缓控释以及生物传感器等诸多领域[8-9].程金瑜等[10]采用水热法制备了多孔二氧化硅微球,并在一定范围内,对罗丹明B的吸附率达到99%;陈宏等[11]采用改性的Stober法合成了介孔二氧化硅纳米球(MSN),这种材料可显著提高对Mo(VI)的吸附效率及能力;Palantavida等[12]制备了圆盘状的介孔二氧化硅且具有吸附多种有机化合物的能力.因此,二氧化硅可作为去除废水中蛋白质的高效吸附剂.
本文开发了一种以生物质为模板的新型吸附剂,用于分离废水中的蛋白质.利用BA栲胶为生物质模板合成多孔SiO2微球吸附剂.由于BA栲胶具有两亲性,它既可以酚羟基和磺酸基为亲水位点,又可以芳香环为疏水位点,并在水中形成胶束,从而有助于控制TEOS水解速率并促进规整的多级孔SiO2微球的合成.探究多孔SiO2微球在不同实验条件下对蛋白质的吸附性能,并为高效简单地去除废水中的蛋白质提供了新的思路.
1 实验部分
1.1 试剂与仪器
1.1.1 主要试剂
十六烷基三甲基溴化铵(CTAB),分析纯,天津市大茂化学试剂厂;正硅酸乙酯(TEOS)、十二烷基磺酸钠(SDS),分析纯,天津市科密欧化学试剂有限公司;BA栲胶,工业级,四川德赛尔化工有限责任公司;十二水合磷酸氢二钠(Na2HPO4),分析纯,西陇科学股份有限公司;磷酸二氢钠(NaH2PO4),分析纯,天津市盛奥化学试剂有限公司;无水乙醇,分析纯,天津市富宇精细化工有限公司;氨水,分析纯,天津市天力化学试剂有限公司;溶菌酶(LZ),分析纯,上海蓝基生物科技有限公司;氢氧化钠、浓盐酸,分析纯,漯河市致远化工有限公司;牛皮制革软化废水,工业级,河北东明牛皮制革有限公司.
1.1.2 主要仪器
场发射扫描电镜 S4800,日本理学;比表面仪 ASAP2460,美国麦克仪器;纳米粒度表面电位分析仪 Nano-ZS90,美国Malvern公司;红外光谱仪 Vertex70,德国布鲁克公司.
1.2 制备方法
以BA栲胶为生物质模板,通过溶胶-凝胶工艺制备多孔二氧化硅(SiO2)微球,然后将反应产物煅烧去除模板.具体步骤如下:
称取0.016 mol CTAB(1.457 9 g)和0.02 mol BA栲胶(0.78 g)分别溶解于20 mL的去离子水中,并在室温下搅拌20 min至全部溶解.然后,将0.5 mL氨水、5 mL去离子水和10 mL乙醇配成溶液添加到CTAB和BA栲胶的混合物中,并将混合物搅拌30 min.随后,将含有2 mL的TEOS和10 mL的乙醇溶液滴加到混合物中,并搅拌6 h.然后,乙醇洗涤三次,并于40 ℃烘箱陈化24 h.最后,将反应混合物在550 ℃下煅烧5 h得到最终样品多孔SiO2微球.
1.3 吸附实验
1.3.1 多孔SiO2微球的Zeta电位测定
利用0.1 M氢氧化钠或浓盐酸溶液调节初始pH(2.0~8.0),将0.01 g的多孔SiO2微球加入到上述不同pH溶液中,超声30 min后,利用纳米粒度表面电位分析仪测定材料的Zeta电位.
1.3.2 单因素优化实验
LZ被用作理论模型蛋白来研究多孔SiO2微球的蛋白质吸附性能.将LZ溶解于不同pH(4.5、5、6、7、8、9)的PBS缓冲液(NaH2PO4和Na2HPO4),并称取0.1 g多孔SiO2微球置于10 mL的LZ溶液(0.5 mg/mL)中,在恒温振动器中室温下震荡240 min,然后离心(5 000 rpm,5 min),采用分光光度计法于278 nm处测量上清液吸光度,探究pH对多孔SiO2微球吸附能力的影响.在最佳pH下,分别探究时间、溶液初始浓度、吸附剂用量等因素对多孔SiO2微球吸附能力的影响.根据公式(1)、(2)分别计算出吸附率和吸附容量:
qt=(C0-C)V/M
(1)
R=(C0-C)/C0×100%
(2)
式(1)、(2)中:R为吸附率(%);qt为吸附容量(mg/g);C0、C为吸附前后蛋白质浓度(mg/g);V为蛋白质溶液体积(mL);M为吸附剂质量(mg).
1.3.3 吸附动力学和吸附热力学
为了研究多孔SiO2微球对LZ的吸附机理,通过线性拟合得到准一级和准二级动力学模型.根据公式(3)、(4)进行计算:
ln(qe-qt)=lnqe-k1t
(3)
(4)
式(3)、(4)中:qt为时间t(min)的吸附量(mg/g);qe为材料的平衡吸附量(mg/g);k1为准一级反应速率常数(min-1);k2为准二级反应速率常数(g/mg/min).
为了研究LZ与多孔SiO2微球之间相互作用,通过Langmuir和Freundlich模型进行模拟和分析.根据公式(5)、(6)进行计算:
qe=bqmCe/(1+bCe)
(5)
lnqe=lnkf+1/nlnCe
(6)
式(5)、(6)中:qm为理论的吸附平衡量(mg/g);b为Langmuir等温吸附常数;kf、n为Freundlich等温吸附常数.
2 结果与讨论
2.1 SEM分析
图1为多孔SiO2微球的SEM图.从图1可以看出,所合成的多孔SiO2为球形,且每个多孔SiO2微球直径大概有10 nm左右.

图1 多孔SiO2微球的SEM图
2.2 BET分析
图2(a)、(b)为不加生物质BA栲胶模板的多孔SiO2微球(SiO2-0)的N2吸附-脱附等温线和孔尺寸分布图,以及多孔SiO2微球(SiO2-1)的N2吸附-脱附等温线和孔尺寸分布图.
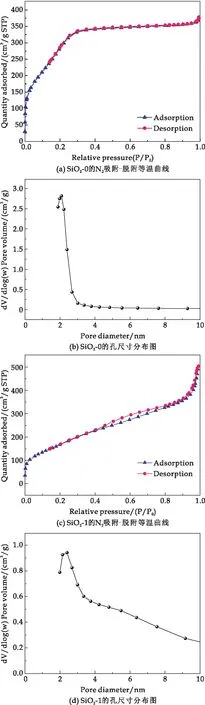
图2 多孔SiO2微球的N2吸附-脱附等温曲线和 孔尺寸分布图
从图2(a)和2(c)可以看出,SiO2-0和SiO2-1的N2吸附-脱附等温曲线都属于典型的IV型等温线,表明所合成的材料均具有介孔结构.然而,当合成不加BA栲胶的多孔SiO2微球(如图2(a)所示)时,N2吸附-脱附等温曲线具有较小的H4磁滞回线,说明SiO2-0上含有一些孔径较小的介孔结构.但当加入BA栲胶时,材料的等温曲线包含H2磁滞回环,相对压力P/P0=0.4.相比于SiO2-0,SiO2-1的分压增加,表明样品中介孔的数量和尺寸进一步增加,故N2的吸附增加[13-15].从孔尺寸分布图中可以得出SiO2-0平均孔径在2.4 nm(如图2(b)所示),而SiO2-1的平均孔径在5.3 nm左右(图2(d)).使用BJH方法计算样品的平均孔径和孔体积,如表(1)所示,SiO2-0和SiO2-1分别为2.48 nm和0.420 3 cm3/g以及5.38 nm和0.736 0 cm3/g.通过比较可以得出BA栲胶的加入对合成较大孔径的介孔结构有重要作用.同时从孔尺寸分布图中也能证明所合成的SiO2微球是具有多孔结构的.

表1 多孔SiO2微球的孔道结构参数
2.3 FT-IR分析
图3为多孔SiO2微球的FT-IR图.从图3可以明显看出,出现了SiO2的特征峰.其中,在464 cm-1、802 cm-1处出现的特征峰对应为Si-O-Si弯曲振动峰,在1 091 cm-1处的特征峰对应为Si-O-Si对称伸缩振动峰,而在3 313 cm-1处出现的特征峰为结构水中的-OH对称伸缩振动峰[16].结果表明,所合成的多孔微球材料为SiO2.

图3 多孔SiO2微球的FT-IR图
2.4 BA栲胶模板对多孔SiO2微球吸附性能影响
图4为不加BA栲胶合成的多孔SiO2微球(SiO2-0)和加入BA栲胶合成的多孔SiO2微球(SiO2-1)吸附LZ的影响图.从图4可以看出,SiO2-1的吸附容量和吸附率远远高于SiO2-0.说明加入BA栲胶有利于合成较大孔径的多孔SiO2微球,同时BET分析结果也证实了这一结果.
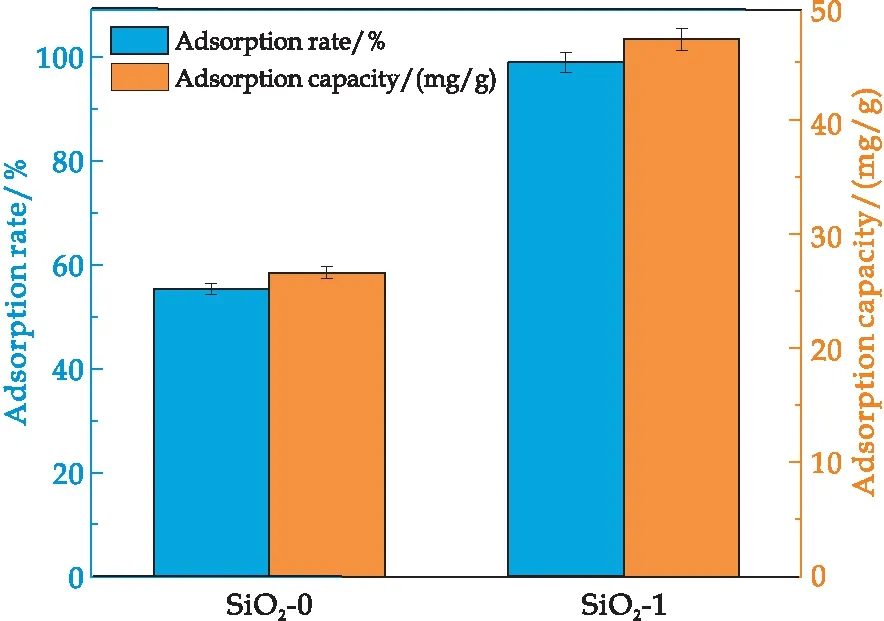
图4 BA栲胶对多孔SiO2微球吸附LZ的影响图
2.5 吸附单因素优化实验结果
2.5.1 pH对多孔SiO2微球吸附性能的影响
由于溶液的pH会影响吸附剂和蛋白质分子的表面电荷,而最大吸附容量的最佳pH是蛋白质和吸附剂带相反电荷时的pH.如图5所示,在不同pH条件下,探究0.1 g多孔SiO2微球吸附10 mLLZ(0.5 mg/mL)溶液240 min时吸附性能变化情况.可以看出,随着LZ溶液pH的增加,吸附容量和吸附率也随之增加.

图5 pH对多孔SiO2微球吸附LZ的影响

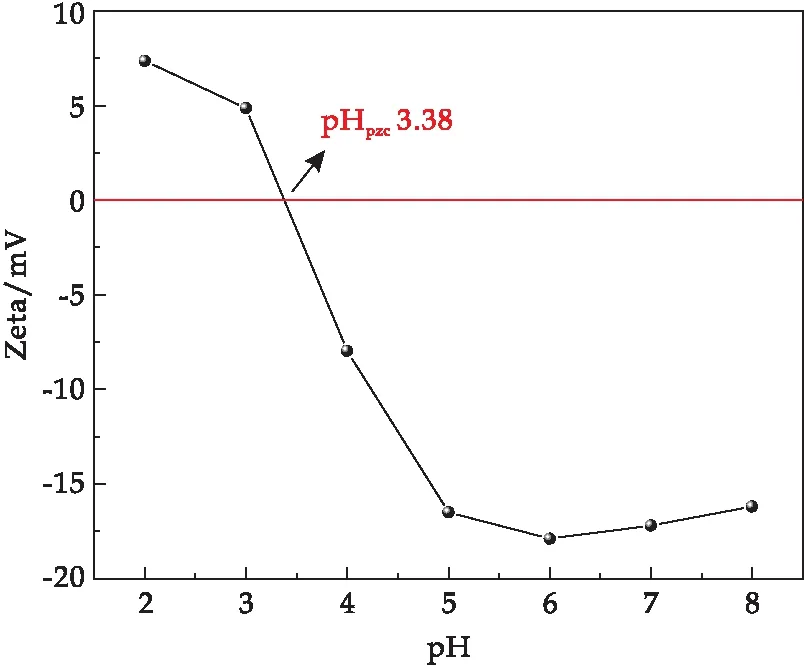
图6 多孔SiO2微球的Zeta图
2.5.2 蛋白质初始浓度对多孔SiO2微球吸附性能的影响
图7为不同LZ初始浓度对多孔SiO2微球吸附性能的影响.从图7可以看出,随着LZ浓度从0.2 mg/mL增加到0.8 mg/mL,多孔SiO2微球对LZ的吸附容量迅速增加,但当蛋白质浓度增加到0.9 mg/mL后,材料对LZ的吸附量变化趋于平缓,说明LZ初始浓度的升高有利于提高多孔SiO2微球的吸附能力,这是由于初始浓度为吸附提供了重要的推动力来克服液相和固相之间的传质阻力,而吸附平台是因为多孔SiO2微球对LZ的吸附达到了饱和状态[19].

图7 蛋白质初始浓度对多孔SiO2微球 吸附LZ的影响
2.5.3 吸附剂用量对多孔SiO2微球吸附性能的影响
图8表示不同多孔SiO2微球吸附剂用量对LZ吸附性能的影响.从图8可以看出,随着吸附剂用量的增加,对LZ的吸附率在不断增加而吸附容量在不断减小.这是因为吸附剂用量的增加会使材料对LZ吸附结合位点增多,故吸附率在不断增加,但少量的吸附剂会更加充分的利用吸附位点和表面积,使得吸附容量更大[20].当吸附剂用量达到0.1 g时,继续增加吸附剂用量,多孔SiO2微球对LZ吸附率基本保持不变,此时吸附率为95%,吸附容量为45.8 mg/g.
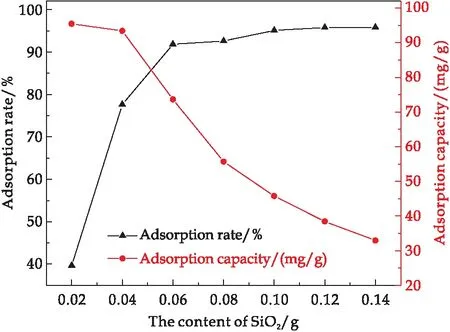
图8 吸附剂用量对多孔SiO2微球吸附LZ的影响
2.5.4 吸附时间对多孔SiO2微球吸附性能的影响
图9表示吸附时间对多孔SiO2微球吸附LZ的变化曲线.从图9可以看出,在0~240 min之间,材料对LZ的吸附容量和吸附率迅速增加,这是由于这一阶段吸附剂上存在着大量的空置吸附位点,而随着吸附时间的推移,吸附率与吸附容量增长幅度趋于平缓,说明多孔SiO2微球对LZ的吸附趋于平衡状态.
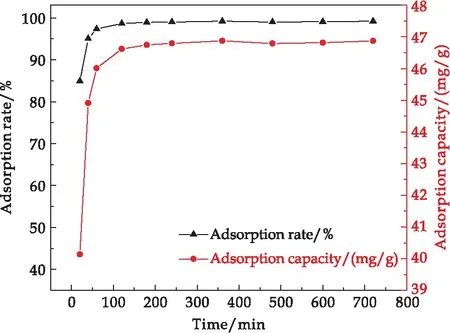
图9 吸附时间对多孔SiO2微球吸附LZ的影响
2.6 吸附机理研究
2.6.1 吸附动力学模型
为了研究多孔SiO2微球对LZ的吸附机理,通过线性拟合得到准一级和准二级动力学模型,如图10和表2所示.从表2所示相关参数可以看出,多孔SiO2微球对LZ的准一级动力学模型的拟合相关系数R2=0.630 86,而准二级动力学模型的拟合相关系数R2=0.999 99,说明材料对LZ的吸附机理更符合准二级动力学模型.因此,动力学主要受化学吸附活性位点支配,吸附过程是以化学吸附为主[21].

表2 多孔SiO2微球吸附LZ的相关动力学 模型参数

图10 多孔SiO2微球对LZ吸附的动力学拟合曲线
2.6.2 吸附热力学模型
为了研究LZ与多孔SiO2微球之间相互作用,通过Langmuir和Freundlich等温模型进行模拟和分析,如图11和表3所示.从表3所示相关参数可以看出,多孔SiO2微球对LZ的Langmuir等温模型的拟合相关系数R2=0.972 84,而Freundlich等温模型的拟合相关系数R2=0.971 39,说明材料对LZ的吸附机理更符合Langmuir等温模型.结果表明,LZ在多孔SiO2微球上主要是通过单层吸附发生的[22].

表3 多孔SiO2微球吸附LZ的相关热力学 模型参数
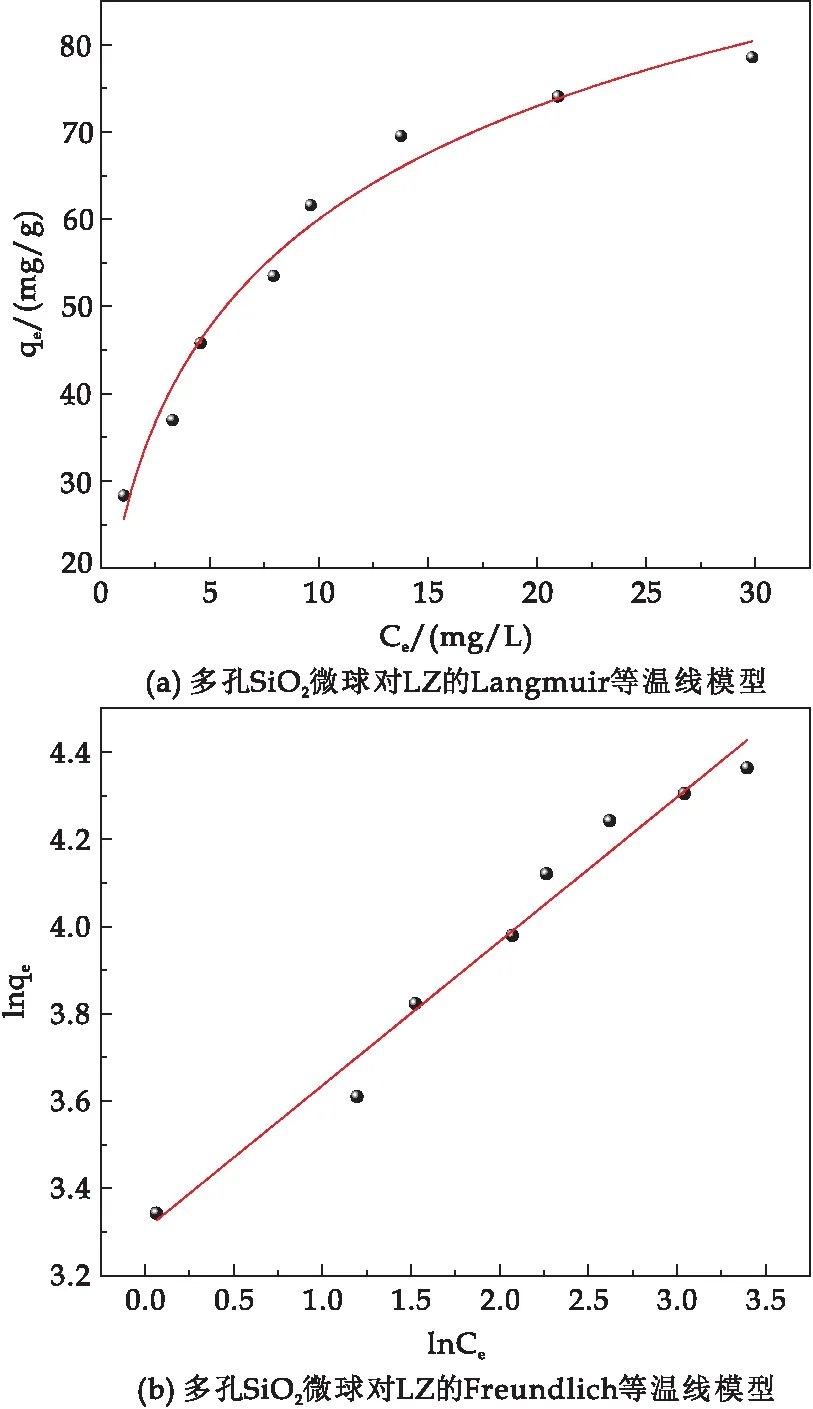
图11 多孔SiO2微球对LZ的吸附等温线模型
2.7 多孔SiO2微球的解析与循环实验
为了探究多孔SiO2微球的再生性,对其进行了多次解析与循环实验,其结果如图12所示.本文采用0.5%的SDS溶液作为洗脱液,然后连续进行了6次循环解析实验.从图12可以看出,在经历了6次循环实验后,多孔SiO2微球对LZ的吸附率仍能保持在80%以上,表明所制备的材料具有可再生性.

图12 多孔SiO2微球的解析与循环图
2.8 多孔SiO2微球的实际应用实验
为了探究多孔SiO2微球的实际应用性能,采用制革软化废水作为实际样本进行吸附实验,其结果如图13所示.At为t(h)时,多孔SiO2微球对实际废水样品的紫外吸光度,A0为实际制革废水样品紫外吸光度.从图13可以看出,随着时间的推移,均有At/A0<1.0,结果表明,多孔SiO2微球对实际制革工业废水的蛋白质具有一定的吸附效果.证明了本研究制备的多孔SiO2微球吸附剂可以在一定程度上解决制革工业废水中蛋白质的污染问题,从而实现蛋白质的高附加值利用.

图13 多孔SiO2微球的实际应用图
3 结论
(1)以生物质材料BA栲胶为模板,采用模板法合成SiO2,并通过SEM、BET、FT-IR等仪器进行表征分析,所合成的SiO2是具有多孔结构的微球.
(2)多孔SiO2微球对LZ具有优异的吸附效果,在吸附pH 8、蛋白质初始浓度0.9 mg/mL、吸附剂用量0.1 g、吸附时间240 min时,多孔SiO2微球对LZ的吸附效果最佳.
(3)多孔SiO2微球对LZ进行吸附机理分析,结果表明,吸附过程符合准二级动力学模型拟合曲线和Langmuir等温模型,说明LZ在多孔SiO2微球上主要是通过单层吸附发生的.
(4)经过6次循化吸附后,多孔SiO2微球对LZ的吸附率仍达到80%以上,且对实际制革工业废水中蛋白质的去除具有一定的效果.

