皖南蝮蛇抑瘤组分Ⅰ急性毒理研究
王晓庆,支 慧,胡浩然,周 珏,田大皓,江玉华,卢林明
(皖南医学院病理解剖学教研室,安徽 芜湖 241002)
蛇毒做为一种生物毒素[1],是由多种天然毒性蛋白构成的混合物,含有多种蛋白质以及一些小分子物质。研究证实不同种类的蛇毒腺分泌的毒液含有的化合物的结构与性质均不相同,且对其他生物呈现的毒性也不相同[2]。随着生物化学、药理学、分子生物学等学科的发展蛇毒的临床应用研究得到了长足的发展。国内外的蛇毒研究所均证实蛇毒组分具有溶栓作用、促凝作用、镇痛作用、降压作用以及抗肿瘤作用[3-5]。
AHVAC-Ⅰ是通过阴阳离子交换柱和凝胶G50分子筛技术从皖南蝮蛇蛇毒粗毒中提取的一种成分。前期研究发现AHVAC-Ⅰ抑制多种肿瘤细胞的增殖,如胃癌细胞SGC7901[6]。随着AHVAC-I抗肿瘤作用的广泛研究和应用,为将其推上临床,其成分的安全性必须得到实验证实。
中位致死剂量(LD50)测定被广泛认定是评估蛇毒组分的急性致死毒性的主要方法[7]。除了要确定蛇毒引起的动物致死的LD50值,我们认为全面的急性毒性研究还应当包括局部组织的病理变化(如出血、坏死)以及脏器功能的损伤亦十分重要。鉴于LD50受到蛇毒组分的毒源、实验动物的类型以及毒液的给药途径的影响[8-9],本文将从小鼠LD50值、给药后小鼠主要脏器结构与功能的改变等方面,对AHVAC-I腹腔注射给药后小鼠的急性毒性进行较为深入的研究,初步了解其毒性剂量和有效剂量之间的差别,确定其毒性靶器官,为后续研究提供实验依据。
1 材料与方法
1.1 实验材料
1.1.1 实验动物 清洁级昆明种小鼠,4~6周龄,体重18~22 g,雌雄各半,由皖南医学院实验动物中心提供,饲养生活环境温度控制在20 ℃左右,湿度(50±10)% 环境下饲养1周,使其适应新环境,足量饮食,饱水。
1.1.2 药品 AHVAC-Ⅰ为皖南医学院蛇毒研究所提纯制备的冻干粉,临用前双蒸水溶解成适用浓度。谷丙转氨酶(ALT)试剂盒、谷草转氨酶(AST)试剂盒、肌酐(CR)试剂盒、尿素氮(BUN)试剂盒均购自南京建成生物工程研究所。
1.1.3 仪器 电子天平 (JJ224BC,常熟市双杰),切片机(RM2245,LEICA),酶标仪(KHB,上海科华),显微镜(BA600-4,Motic)。
1.2 实验方法
1.2.1 AHVAC-Ⅰ溶液配制 取1 mg AHVAC-Ⅰ冻干粉,临用前1 mL双蒸水溶解,制成1 mg/mL的AHVAC-Ⅰ母液。
1.2.2 毒性实验剂量分组 腹腔注射给药,采用半数致死剂量法[10]。先预实验,再正式实验。
1.2.3 预实验 将观察1周的健康清洁级小鼠随机分成3组,每组6只,雌雄各半,用递次稀释3倍的
AHVAC-Ⅰ溶液按体重进行腹腔注射给药,注射量均为0.2 mL,连续观察7 d。以小鼠全部死亡以及小鼠全部存活的剂量,计算出AHVAC-Ⅰ腹腔注射最大最小致死量(LD0)以及最小最大致死量(LD100)分别为1.00 mg/kg,4.25 mg/kg,组间距r=0.7,n=5。
1.2.4 正式实验 120只健康小鼠随机分成6组(每组20只,雌雄各半),分别为空白对照组和5个AHVAC-Ⅰ剂量组。按照最高剂量与最低剂量的公比系数(q=0.70)设计中间剂量,剂量分别设置为1.00 mg/kg、1.44 mg/kg、2.06 mg/kg、2.96 mg/kg、4.25 mg/kg,分别命名为AHVAC-I A~E组,另设生理盐水为空白对照组。
1.3 小鼠行为观察实验前禁食12 h,给药后30 min内,连续观察;药后 30 min~2 h,每15 min观察1次;药后2 h~4 h每30 min观察1次;药后4 h~8 h,每1 h观察1次;药后8 h~24 h,每4 h观察1次;给药后第2天起,每d观察1次。按一般观察项目指征指导原则观察小鼠,包括动物外观、活动状态、精神状态,有无鼻、口、眼异常分泌物以及死亡情况,连续观察7 d。
1.4 小鼠血清生化检测7 d后将剩余存活小鼠,用毛细管从小鼠眼球每只采血1.5 mL,采用试剂盒(mlbio),ELISA法检测血清学谷丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)、肌酐(CR)、尿素氮(BUN)水平。
1.5 病理形态学观察取小鼠心、肝、肺、肾、脑等主要脏器,在0.9%生理盐水洗涤,在滤纸上脱水,4%甲醛固定,脱水包埋,病理切片,HE染色,显微镜下观察并拍照。
1.6 统计学分析采用SPSS 19.0软件统计,计量资料以“均值±标准差”表示,组间比较用单因素方差分析方法,两组间均属比较采用t检验,以P<0.05表示差异有统计学意义。
2 结果
2.1 小鼠行为学观察AHVAC-I各剂量组小鼠出现不同程度的中毒反应,如走路不稳、行动迟缓,被毛蓬乱且出现竖毛、精神萎靡、嗜睡乏力、畏寒怕冷,且中毒反应随剂量加大而加重。其中4.25 mg/kg、2.96 mg/kg和2.06 mg/kg三个剂量组小鼠在腹腔注射蛇毒后出现肌肉僵硬、运动失衡、抽搐后死亡。存活的实验动物在7 d观察期内其精神、活动、食欲、睡眠逐渐恢复正常。
2.2 急性毒性实验量效关系结果及LD50的计算结果
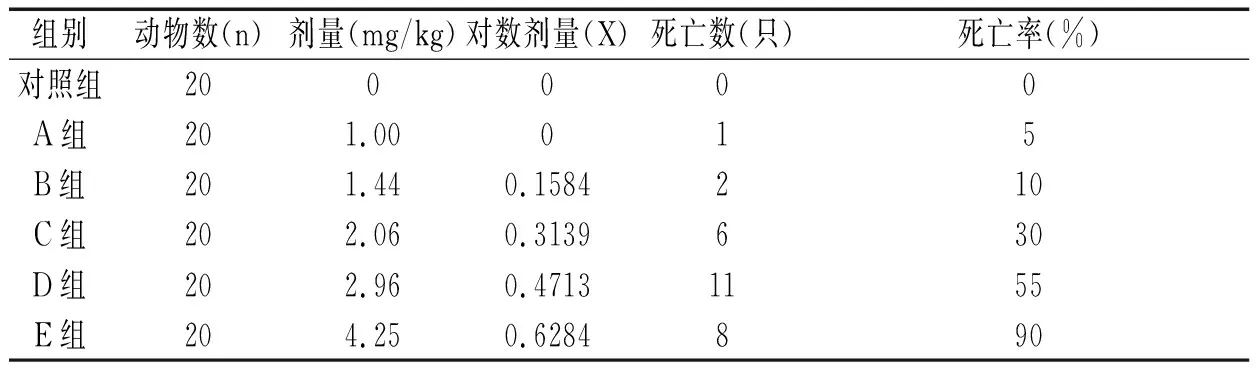
表1 蛇毒 AHVAC-I腹腔注射对小鼠的急性毒性情况性
通过预实验和正式实验,小尾腹腔给药的LD100、LD50及LD0值见表1,LD50取值按95%的可信限为标准。小鼠腹腔注射AHVAC-Ⅰ后的48 h内累积死亡曲线见图1。
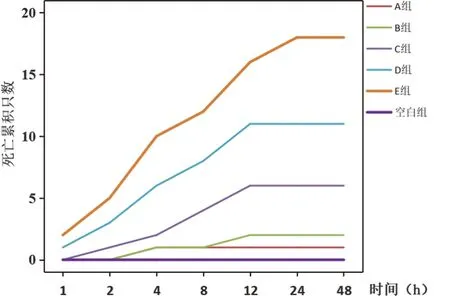
图1 小鼠尾腹腔注射AHVAC-I 后的48 h内累积死亡曲线
2.3 血清生化指标检查结果根据LD50值,1.00 mg/kg与1.44 mg/kg蛇毒组例入低剂量组,2.06 mg/kg蛇毒组为中剂量组,2.96 mg/kg蛇毒组例入高剂量组。与对照组小鼠相比,低剂量组小鼠的肝功能指标(ALT、AST)和肾功能指标(CR、BUN)水平均无改变,中、高剂量组小鼠的ALT、AST、CR、BUN均显著高于对照组(P<0.05)(见表2)。
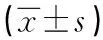
表2 AHVAC-I对小鼠血液生化指标的影响
2.4 病理观察大体标本见肝脏、肾脏、心脏、脑大小无明显变化。镜检发现对照组肝、肾、心、脑、肺组织均未见异常表现(图4~图5中A)。实验组里低剂量组小鼠的肝组织无病理改变(图2B),但中剂量组肝组织可见部分肝细胞轻度水肿,胞体增大,胞浆透亮(图2C),高剂量组肝组织可见肝细胞点状坏死,肝细胞水肿,双核增多(图2D)。
低剂量组小鼠的肾组织无病理改变(见图3B),但中剂量组肾组织可见部分肾小球水肿,囊腔变小,肾小管轻度水肿(见图3C),高剂量组肾组织可见肾小球水肿囊腔变小甚至消失,周围肾小管轻度水肿(见图3D)。其他脏器心脏(见图4) 、肺脏(见图5) 、脑组织(见图6)与对照组相比未见明显异常。
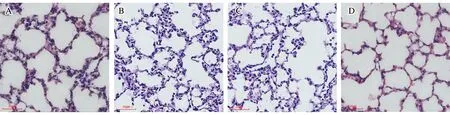
图5 小鼠腹腔注射AHVAC-I后肺组织切片(×200)
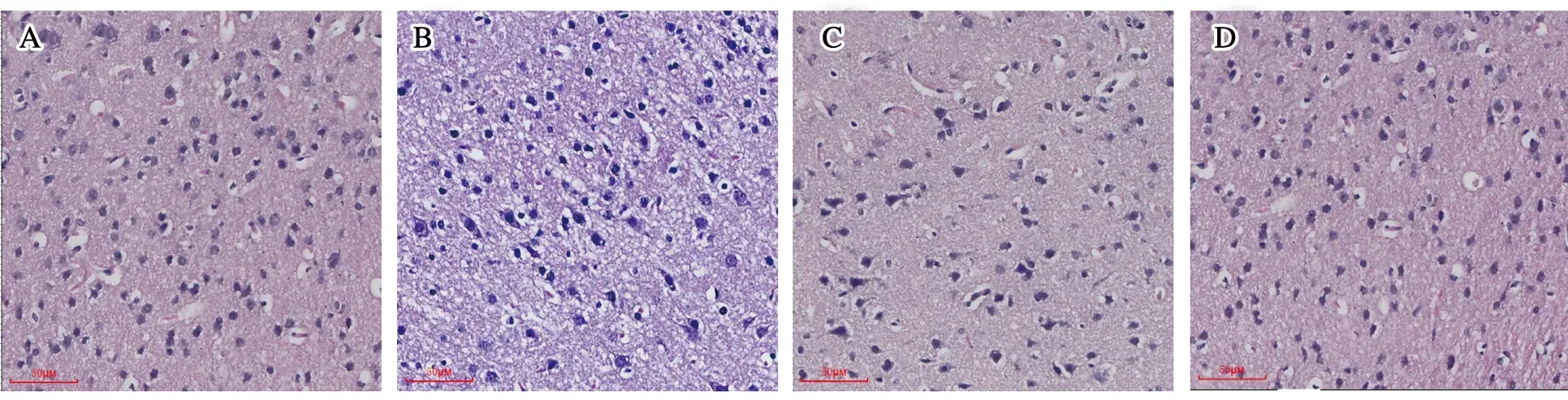
图6 小鼠腹腔注射AHVAC-I后脑组织切片(×200)
3 讨论
分离纯化单一蛇毒组分为将蛇毒开拓其成为有用的新型生物工具提供了可能性。然而,将蛇毒成分广泛利用的前提条件之一是须充分考虑到其生物毒性,因此全面的评估有活性的蛇毒组分的毒性是研究发过程中不可或缺的一环。AHVAC-Ⅰ作为蛇毒的成分,虽然已被多项研究证实可有效抑制肿瘤细胞的增殖,然而AHVAC-Ⅰ的体内毒性研究尚未展开。因此,开展AHVAC-I的急性毒性实验,对于推广AHVAC-I在抑制肿瘤方面应用十分必要。
中位致死剂量(LD50)测试被认为是评估蛇毒AHV-PI的急性毒性的“黄金标准”[7]。为了确定AHVAC-I腹腔给药小鼠的LD50,我们使用“Bliss方法”计算。本次研究的结果表明小鼠腹腔注射AHVAC-I的LD50值为2.585 mg/kg,95%可信限为2.233~3.069 mg/kg。对各组小鼠的行为学观察结果表明,小鼠腹腔注射AHVAC-I导致的急性毒性表现主要为走路不稳、蜷缩、昏厥性抽搐死亡;通过计算得出这一结果表明,AHVAC-I的是有毒性的,但是相较于蓝海等提出的LD50为2 mg/kg[11]的蝮蛇蛇毒,做为蝮蛇组分之一的AHVAC-I的毒性要小于传统的蝮蛇蛇毒。
给药 7 d后,自实验小鼠眼球采血1.5 mL,生化指标表明中剂量(2.06 mg/kg)组和高剂量组(2.96 mg/kg)小鼠体内反映肝肾功能的ALT、AST、CR和BUN水平显著高于对照组,但低剂量(1.00 mg/kg,1.44 mg/kg)组小鼠的肝肾功能指标与对照组相比无差异。可见,低剂量腹腔注射AHVAC-I没有造成小鼠肝、肾功能的损伤,但伴随着剂量的增加,小鼠肝、肾功能受到损伤。由此,我们认为低剂量的AHVAC-I腹腔注射的安全性是可以得到保证的。
进一步的病理学观察发现低剂量(1.00 mg/kg,1.44 mg/kg)组小鼠的肝、肾、心、肺、脑组织均未有病理改变,但中(2.06 mg/kg)、高(2.96 mg/kg)剂量组小鼠的各重要组织脏器有出现病理改变。其中中剂量组小鼠的病理改变主要表现为肝、肾组织细胞的变性,但高剂量组小鼠的肝组织病理损伤严重,可见坏死。这表明中毒剂量的AHVAC-I的靶器官主要为肝脏,肝细胞成片的坏死可能是其引发实验动物死亡的主要原因。这一结果与蝮蛇毒可导致肝、肾损伤的早前研究结果相吻合[12-15]。由于相较于中高剂量AHVAC-I对肝肾的损伤,低剂量的AHVAC-I对于小鼠的组织脏器无明显损伤,我们认为低剂量的AHVAC-I的安全性是较高的。
AHVAC-I的主要功能是抑制肿瘤细胞的生长,课题组先前的实验结果表明1.00 mg/kg剂量的AHVAC-I即可有效地对荷瘤鼠SCG-7901胃癌发挥抑瘤作用[6]。本次急性中毒实验的结果更是进一步表明虽然AHVAC-I是有毒性作用的,但在有效抑癌剂量腹腔给药的过程中对实验动物无中毒表现,且各主要脏器无病理改变和功能损伤。
综上所述,在药效学的剂量下有效抑瘤浓度的AHVAC-I不会引发机体中毒反应,这为临床用药安全提供了保障。

