疏风平颤汤加减联合STN-DBS手术对帕金森病病人EGF、抗氧化功能的影响
葛静雅,刘慧群,刘 畅,赵腾跃
帕金森病(Parkinson′s disease,PD)是中老年人常见病之一,由多巴胺神经元退变或死亡导致纹状体多巴胺明显减少的神经系统变性疾病[1-2]。疏风平颤汤由《万病回春》中疏风汤演化而来,其治疗主要以疏风止颤为主,重在补益气血、镇静止颤、滋补肝肾。丘脑底核脑深部电刺激术(deep brain stimulation of subthalamic nucleus,STN-DBS)可有效治疗帕金森病,改善帕金森病病人的临床症状[3]。研究表明,表皮生长因子(epidermal growth factor,EGF)具有促神经元生长活性,对神经功能具有一定的改善作用[4-5]。研究表明,抗氧化功能、EGF可能与帕金森病的发生、发展存在一定的联系[6]。但疏风平颤汤加减联合STN-DBS手术对治疗帕金森病的研究较少。鉴于此,本研究探讨疏风平颤汤加减联合STN-DBS手术对帕金森病病人EGF、抗氧化功能的影响,为临床治疗帕金森病提供参考。
1 资料与方法
1.1 临床资料 选取2018年7月—2020年11月在保定市脑血管病医院就诊的帕金森病病人152例作为研究对象,其中男92例,女60例,年龄41~78岁;病程3~11年;体质指数(body mass index,BMI) 22~26 kg/m2;帕金森病的改良Hoehn-Yahr(H-Y)分期:Ⅰ期19例,Ⅱ期120例,Ⅲ期13例;吸烟史23例,饮酒史24例。按照随机数字表法分为对照组和联合组,每组76例。两组一般资料比较,差异均无统计学意义(P>0.05)。详见表1。本研究经医院伦理委员会批准,所有病人及家属均知情同意并签署知情同意书。
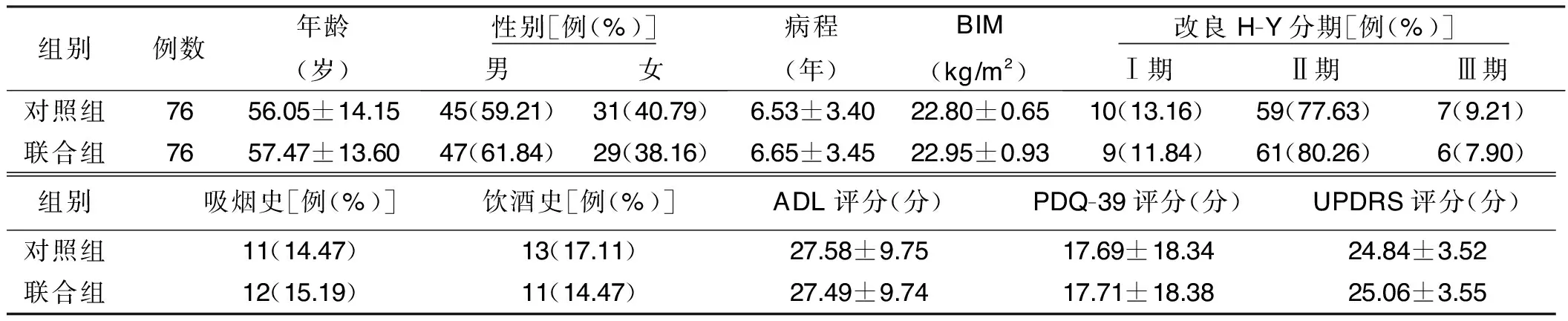
表1 两组病人一般资料比较
1.2 诊断标准 中医诊断标准参照《中医内科学》[7]中肝肾阴虚型帕金森病诊断标准,主要症状:头部、肢体震颤,动作迟缓,肢体拘痉;次要症状:精神萎靡,头晕耳鸣,腰膝酸软,健忘少寐,失眠多梦,大便秘结,舌质红,舌苔薄白,脉弦细。西医诊断标准符合《帕金森病的诊断》[8]中关于帕金森病的诊断标准。
1.3 纳入与排除标准 纳入标准:经影像学检查确诊者;改良H-Y分期为Ⅰ~Ⅲ期者。排除标准:继发性帕金森或帕金森叠加综合征者;对本研究药物过敏者;原发性帕金森病者;有手术禁忌证者;生活完全不能自理或行动障碍者;改良H-Y分期>Ⅲ期者;伴随严重脏器功能障碍、精神障碍、风湿性疾病者;依从性差,不能按时服药者。
1.4 治疗方法 对照组采用STN-DBS手术进行治疗:病人于手术前行左旋多巴冲击试验,试验前72 h停服多巴胺受体激动剂,试验前12 h停服复方左旋多巴制剂以及其他抗PD药物。试验药物采用复方左旋多巴标准片,使用剂量以之前第1次服用的抗PD药物换算为左旋多巴等剂量的1.5倍。空腹状态下,先进行UPDRS-Ⅲ评分作为基线,30 min后服用复方左旋多巴标准片,于服药后0.5 h、1 h、2 h、3 h分别进行1次UPDRS-Ⅲ评分,最大改善率=(服药前基线UPDRS-Ⅲ评分-服药后最低UPDRS-Ⅲ评分)/服药前基线UPDRS-Ⅲ评分×100%,由两位神经专科医师评估、计算最大改善率,取平均数作为受试者服用复方左旋多巴的最大改善率,最大改善率≥30%考虑进行手术。术前采用头颅MRI扫描,计算手术靶点,MRI影像上丘脑底核(STN)为可视靶点,STN的靶点坐标值为:Z=前联合-后联合(AC-PC线)下4~6 mm,Y=AC-PC线中点后1~3 mm,X=旁开11~13 mm。穿过STN背外侧的最长路径,于局部麻醉下,行头皮切开、颅骨钻孔,于头架定位下测试术中电生理,将微电极检测的STNSTN外放电信号记录下来,检测电极穿过STN长度,根据穿过STN的长度用微推进器将刺激电极的四个触点最大程度放置在STN里。于术中外接程控仪,检测病人的副反应阈值及症状改善情况。联合组在对照组基础上于术后服用疏风平颤汤:龟板20 g,酸枣仁20 g,羚角15 g,黄芪15 g,天麻10 g,当归10 g,川芎10 g,白僵蚕10 g,生地10 g,熟地10 g,生甘草6 g。随证加减:肢体僵硬失灵者加蜈蚣2条,鸡血藤15 g;肢体明显拘痉者加木瓜6 g,白芍12 g;震颤明显者加地龙9 g,全蝎6 g。每日1剂,水煎后取200 mL,分早晚服用。两组病人共治疗3个月。
1.5 观察指标
1.5.1 血清指标检测 分别于治疗前、治疗1个月后、治疗3个月后采集病人次日清晨空腹静脉血4 mL, 3 000 r/min离心10 min,分离血清,-80 ℃保存。采用酶联免疫吸附法对EGF、脑源性神经营养因子(brain derived neurotrophic factor,BDNF)、胶质细胞源性神经营养因子(glial cell line derived neurotrophic factor,GDNF)、超氧化物歧化酶(superoxide dismutase,SOD)、谷胱甘肽(glutataione,GSH)、丙二醛(malondialdehyde,MDA)水平进行检测[9]。
1.5.2 中医证候评分 观察病人肢体震颤、运动徐缓、肢体拘痉以及精神萎靡症状,制定帕金森病病人中医证候评分量表,按照无症状、轻度、中度、重度,分别计0分、1分、2分、3分,分数越低代表改善情况越好[10]。
1.5.3 疗效判定标准 治疗3个月后评定疗效。肢体震颤、拘痉等临床症状消失为显效;肢体震颤、拘痉等临床症状明显改善为有效;病人肢体震颤、拘痉等临床症状无明显改善或加重为无效。
1.5.4 不良反应 统计病人治疗3个月内不良反应发生情况,包括颅内积气、颅内出血、皮肤破溃、便秘、多动、心悸。

2 结 果
2.1 两组EGF、BDNF、GDNF水平比较 治疗1个月后、治疗3个月后,两组EGF、BDNF、GDNF水平均较治疗前升高,差异均有统计学意义(P<0.05);与对照组比较,治疗1个月后、治疗3个月后,联合组EGF、BDNF、GDNF水平更高,差异均有统计学意义(P<0.05);与治疗1个月比较,两组治疗3个月后EGF、BDNF、GDNF水平均升高(P<0.05)。详见表2。

表2 两组EGF、BDNF、GDNF水平比较(±s) 单位:pg/mL
2.2 两组SOD、GSH、MDA水平比较 治疗1个月后、治疗3个月后,两组MDA水平较治疗前降低,SOD、GSH水平较治疗前升高,差异均有统计学意义(P<0.05);与对照组治疗1个月后、治疗3个月后比较,联合组MDA水平更低,SOD、GSH水平更高,差异均有统计学意义(P<0.05);与治疗1个月比较,两组治疗3个月后MDA水平降低,SOD、GSH水平升高,差异均有统计学意义(P<0.05)。详见表3。

表3 两组SOD、GSH、MDA水平比较(±s)
2.3 两组中医证候评分比较 治疗1个月后、治疗3个月后,两组病人肢体震颤、运动徐缓、肢体拘痉、精神萎靡评分均较治疗前降低,差异均有统计学意义(P<0.05);与对照组治疗1个月后、治疗3个月后比较,联合组治疗1个月后、治疗3个月后肢体震颤、运动徐缓、肢体拘痉、精神萎靡评分降低更明显,差异均有统计学意义(P<0.05);与治疗1个月比较,两组治疗3个月后肢体震颤、运动徐缓、肢体拘痉、精神萎靡评分降低,差异均有统计学意义(P<0.05)。详见表4。

表4 两组中医证候评分比较(±s) 单位:分
2.4 两组不良反应比较 治疗3个月后,联合组不良反应总发生率低于对照组,差异有统计学意义(P<0.05)。详见表5。

表5 两组不良反应比较 单位:例(%)
2.5 两组临床疗效比较 治疗3个月后,联合组总有效率高于对照组,差异有统计学意义(P<0.05)。详见表6。
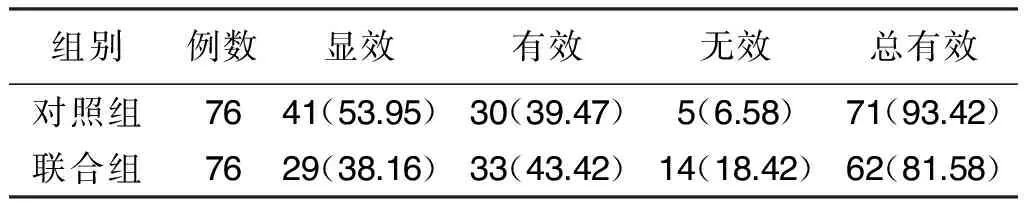
表6两组临床疗效比较 单位:例(%)
3 讨 论
黑质纹状体多巴胺含量的减少是帕金森病的主要病理改变,是一种慢性神经系统变性疾病,使病人不仅出现便秘、失眠、嗅觉障碍等症状,还可能导致病人吞咽困难、言语障碍、运动失衡等,病情严重者可能会危及生命[11-12]。帕金森病的主要临床表现为静止、强直性震颤、动作缓慢等,在初期确诊时,就已经有20%左右的病人出现较轻的认知障碍,随着病情的发展大多数病人会逐渐发展为痴呆[13-14]。因此,早发现、早治疗对提高帕金森病病人的生活质量及健康具有重要意义。在中医学中,帕金森病归属于“颤症”范畴,其以手足颤抖、头部摇动且无法控制为主要特征的病症,《赤水玄珠》记载:“此病壮年鲜有,不能制肾火,极为难治”[15-16]。现代中医研究表明,帕金森病与肝肾亏虚紧密相关,其主要病机为气血不足、筋失濡养、肝肾阴虚或阴虚动风而导致的肢体拘挛及震颤[17-18]。疏风平颤汤中龟板具有养心安神、滋阴补血之效;酸枣仁养心补肝、宁心安神;羚角清热镇痉、息风平肝;黄芪益气固表、滋阴养血;天麻可平甘、息风止痉;当归、川芎、生地、熟地补血通络、益精填髓;白僵蚕可化痰解痉、祛风散结;生甘草补中益气、调和诸药。本研究在疏风平颤汤药方的基础上加入蜈蚣、鸡血藤,可息风镇颈、通络止痛,改善肢体僵硬;木瓜、白芍可治湿痹拘挛、四肢挛急疼痛,有平抑肝阳、敛阴止汗之功效,可改善肢体拘痉;地龙、全蝎具有通络除痹、息风止痉之效,可使震颤症状明显改善。
研究报道,STN-DBS可治疗僵硬或震颤的帕金森病病人,改善病人肢体僵硬及异动症,且其对病人的神经具有一定的保护作用[19]。EGF可调节细胞的分化与生长,其与帕金森病病人的认知程度具有一定的关系[20]。在帕金森病的病理进程中神经细胞因子分泌不足与神经元损害密切相关,BDNF与GDNF是2种不同来源、可促进神经元修复的神经营养因子,对病人的神经功能具有一定的改善作用[21]。在本研究中,疏风平颤汤加减联合STN-DBS手术可升高帕金森病病人EGF、BDNF、GDNF水平,改善病人认知功能及神经功能。其机制可能为DBS通过抑制被刺激核团的病理性活动达到功能性损毁的效果,或是DBS可抑制大脑复杂的神经结构网络。
在健康人群体内的氧化-抗氧化水平处于动态平衡状态,若体内氧化-抗氧化水平失衡会使多巴胺能神经元变性死亡[22]。SOD、GSH、MDA均为氧化应激指标,顾晔等[23]研究发现,帕金森病病人SOD、GSH水平较低,MDA水平较高,提示其是反映病人氧化应激状态的重要指标。在本研究中,疏风平颤汤加减联合STN-DBS手术可升高SOD、GSH水平,降低MDA水平,改善病人抗氧化功能。本研究结果显示,疏风平颤汤加减联合STN-DBS手术可降低肢体震颤、运动徐缓、肢体拘痉、精神萎靡症状评分,改善病人临床症状,降低并发症总发生率,提高治疗有效率。
综上所述,疏风平颤汤加减联合STN-DBS手术可升高帕金森病病人EGF、BDNF、GDNF、SOD、GSH水平,降低MDA水平及并发症总发生率,提高病人认知功能,改善病人神经功能、抗氧化功能及临床症状,降低并发症总发生率,进一步提高治疗有效率。

