水系锌离子电池金属负极的挑战与优化策略
王心怡,李维杰,韩 朝,刘化鹍,窦世学
(卧龙岗大学创新校区超导与电子材料研究所,澳大利亚卧龙岗 2522)
随着能源需求日益增长,传统化石燃料面临枯竭。太阳能、风能等可再生清洁能源的发展和研究成为了必然[1]。然而,这些可再生能源的应用受到了气候、时空及地理条件等限制,对研究顺利开展造成了挑战。相比之下,可充电电池显示出了稳定性好、储能方便的优势[2-7]。归因于循环寿命长、能量密度和可充电性高等优点,锂离子电池占据着电动汽车和便携电子设备的主导地位[8-9]。然而,锂离子电池的技术发展受到了潜在的安全隐患和锂资源减少的限制[10]。金属锌(Zn)因具有高理论容量(820 mA·h/g)、低电镀/剥离电位(-0.76 V 相对于标准氢电极[SHE])[11-13]、易加工等优点而在其他碱金属中脱颖而出,成为了可持续储能系统的重点研究方向之一[14-16]。以锌为负极的锌基电池,如锌-空气电池[17-18]、Zn-V2O5电池[19-20]、Zn-MnO2电池[21-22]已经被广泛研究。更重要的是其高导电性、高功率密度、在水中的高稳定性和安全性,奠定了ZIBs 作为未来重点研究方向的基础。然而枝晶形成和界面副反应阻碍了其实际应用[23-29],它们会严重影响电池的稳定性和使用寿命,极易导致电池故障。
为了解决这些现有问题,科研工作者通过对界面枝晶生长机制分析,从不同的角度提出了改善锌负极传统固液界面稳定性的策略。比如基于锌负极电极片本身的改造[30-31],还有优化电解液[32-33]、在电解液中引入添加剂[34-35]、优化隔膜设计[36-37]等方法来提高锌电镀/剥离过程中的可逆性,延长电极的循环寿命。本文梳理了水系锌离子电池的储能机制及影响电池性能的现存问题,将解决腐蚀和枝晶问题的方法分为锌负极改性和电解液优化两大类,如图1 所示。锌负极改性主要包括锌负极合金化处理、结构改造和界面保护三种形式,电解液优化则细分为不同锌盐对比,电解液添加剂和凝胶电解液三种方式。通过对近期的研究回顾以及不同解决策略之间的对比分析,总结了锌负极保护的特点,提出了未来水系锌离子电池负极的发展方向。
图1 锌负极/电解液界面优化策略Fig.1 Optimization strategy of zinc anode/electrolyte interface
1 锌离子电池负极的传统储能机制与特点
可充电ZIBs 的主要组成部分为锌金属负极、可容纳锌离子的正极、电解液和隔膜。能量的存储是基于正极和负极之间Zn2+的迁移。类似于传统锂离子电池,正极主体材料中锌离子的嵌入/脱出是主要的储能机制,而锌负极的反应可以简单概括为电镀/剥离机制[38]。通常,ZIBs 在中性或弱酸性电解液中负极的反应可以概括为

在放电过程中,负极锌金属形成锌离子,在电解液中扩散随后向正极迁移,嵌入正极材料结构中。同时从负极释放出的电子流向正极,被正极接收[39];充电过程则相反,正极释放锌离子,随着在电解液中扩散到负极并在电场作用下被还原。锌的成核和生长过程决定了锌的沉积质量[25],然而这一过程通常是不均匀的。为了完成成核行为,Zn2+需要超过与成核过电位相对应的势垒,如图2 所示。而且Zn 在界面处成核越困难,成核过电位就越大[40],所以电场分布和离子浓度都会影响Zn 的成核过程[41]。电场强度不均匀就会出现尖端效应,为靠近尖端的Zn 提供更大的成核吸引。离子浓度较高或是离子传输较快则有效降低了成核势垒。由于锌表面不规则和重复循环过程中电解液和锌负极的反应,锌负极现存的问题成为了ZIBs 进一步发展的主要挑战和障碍。

图2 (a)锌成核过程能垒;(b)锌沉积过程电压曲线[25]Fig.2 (a)The energy barrier at the zinc nucleation process;(b)Typical voltage profile during zinc deposition[25]
2 锌负极现存问题
2.1 腐 蚀
由于锌金属比较活泼,氧化还原电位低,锌金属非常容易自发进行自腐蚀和电化学腐蚀反应[42]。具有高热力学活性的锌负极,极易与水性电解液反应,加快腐蚀速率,形成不可逆的副产物[43]。在大多数碱性电解液中,由于锌低于氢的氧化还原电位,锌可以自发形成腐蚀微电池产生严重的枝晶和非导电的钝化副产物,例如Zn(OH)2[44],导致电池容量衰减,库仑效率降低。在中性和弱酸性电解液中,这种现象有所改善,锌负极有了更好的可逆性[45]。锌负极处可逆的锌离子和锌之间的转变是在理想情况下锌负极唯一的反应过程。然而,事实上由于水溶液的狭窄电化学稳定窗口(1.23 V)和Zn2+/Zn(-0.76 V)的低标准电位,在电镀/剥离过程中存在难以捉摸的问题,锌负极表面依旧会发生复杂的副反应[46]。除此之外,还存在库仑效率低,电解液消耗等问题[47]。锌金属在反复充放电循环过程中被大量消耗,形成溶解度低并且电性差的惰性副产物。
将锌金属浸入弱酸性ZnSO4电解液中,几天后可以观察到Zn4(OH)6SO4生成,之后Zn4(OH)6SO4会被水合变成Zn4(OH)6SO4·5H2O。这表明锌金属发生快速腐蚀,附着在锌表面的副产物形成的松散层允许电解液继续接触锌表面,所以腐蚀会持续进行[48]。锌金属的腐蚀会导致电池容量衰退,减少锌负极的可反应比表面积,充电效率下降。除此之外,电极表面产生的惰性腐蚀物质会阻碍Zn2+传输,降低了负极的可逆性。构建稳定的电极/电解液界面,防止负极和电解液直接接触可以有效缓解腐蚀现象[49]。
2.2 锌枝晶
锌的沉积和溶解是电池循环中的主要过程。在锌离子向负极扩散的过程中会优先在吸附电场强、有成核位点的地方形成凸起。这些初始的凸起进一步加剧了锌表面的电场不均,随着循环次数增加,随后扩散的锌离子优先吸附在凸起的尖端,聚集在小凸起周围,进一步加剧枝晶生长,如图3所示[50]。除了较高的过电位和较高的电流密度之外,电场分布不均匀和离子浓差极化大所引起的局部成核和成核势垒高导致成核位点少是锌枝晶产生的主要原因。严重的枝晶问题会刺破隔膜并且导致电池发生短路,甚至是有“死锌”(断裂的枝晶)产生[28]。因此抑制锌枝晶的形成对锌基电池的实际应用至关重要。

图3 碱性电解液中锌枝晶的形成及生长机制[50]Fig.3 The formation and growth mechanism of zinc dendrites in alkaline electrolyte[50]
在pH 值不同的电解液中,锌枝晶的形态也有很大不同。在中性和弱酸性电解液中,锌枝晶为六边形的片状物,这是六边形密堆积的晶体结构[31]。在碱性电解液中,锌枝晶的形成与Zn(OH)2-4的不稳定性有关,极易分解成惰性氧化锌层阻止锌离子有序扩散[51],由于这种热力学不稳定性,碱性电解液中锌枝晶的形成尤为严重。相比之下,弱酸性电解液已经相对削弱了锌枝晶刺破隔膜的能力[52]。
根据上述机理的梳理结果,电极的电化学极化和电解液中锌盐的类别和浓度都会影响锌枝晶的形成和生长过程[53-54]。因此,抑制枝晶生长的本质是覆盖枝晶的形成位点[55]或者是增加电极的表面积[56]。
3 锌负极材料改性方法
3.1 合金化处理
在水系电解液中,锌负极容易遭受不均匀的金属沉积,金属电极的表面往往形成不导电的氧化物或是氢氧化物[57]。这将导致金属锌和电解液被消耗,增加阻抗,电池性能也会随之下降。将其他特性不同的金属或非金属与锌结合在一起作为负极的方式可以对锌负极进行有效调节[25]。锌的成核势垒在不同的基材之间存在着显著的差异。
Zhang 等[58]将可溶性银(Ag)与锌反应形成金属合金。表面Ag溶解到Zn中形成固溶体的表面层[图4(a)],其晶体结构与纯锌金属具有的六方最密堆积(HCP)晶体结构相同,因此可以作为缓冲层,消除后续锌沉积的成核屏障,以低势垒让锌成核。通过使用光学显微镜观察[图4(b)],发现沉积在Ag-Zn 电极上的Zn 成核是均匀的,在完全放电状态下没有观察到“死锌”。
将惰性金属引入Zn 负极,可以在一定程度上缓解腐蚀现象。Cai 等[48]通过简单的置换反应在锌负极表面引入抗腐蚀性好、具有高导电性的铜(Cu)构建锌铜合金[图4(c)],来抑制在硫酸锌(ZnSO4)电解液中氧化形成的氢氧化锌硫酸盐。在对称电池组装30天之后,电极片没有新的副产物出现[图4(d)],表明Cu/Zn良好的防腐特性。经过Cu修饰后的锌负极腐蚀速率变低,电化学性能变好。在Zn-Cu||MnO2全电池中,500 次循环之后的容量为初始容量的94.2%[图4(e)]。
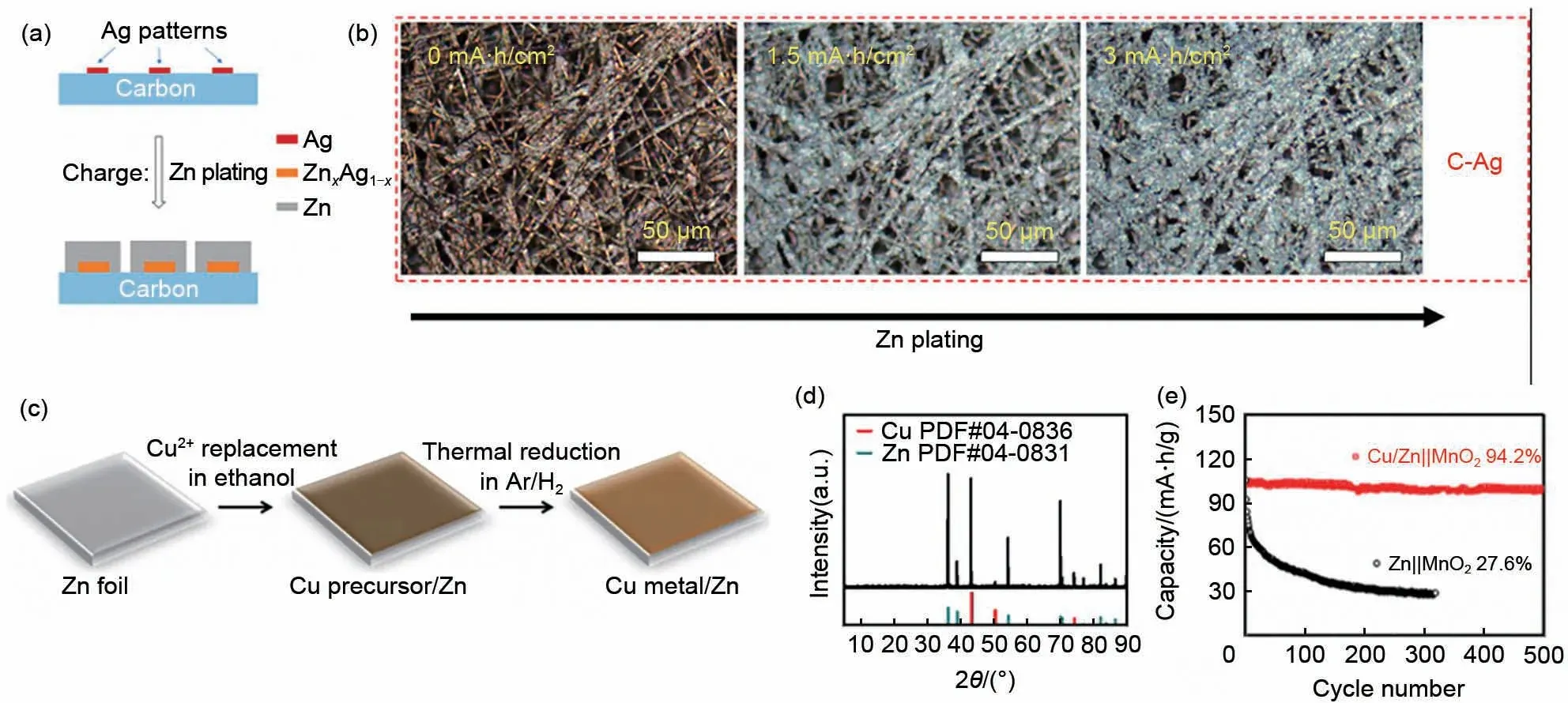
图4 (a)镀锌示意图[58];(b)Zn电镀和C-Ag电极的光学显微镜分析[58];(c)Cu/Zn电极的制备过程示意图[48];(d)Cu/Zn-30电极的XRD图像[48];(e)Zn||MnO2 和Cu/Zn||MnO2全电池的循环性能[48]Fig.4 (a)Schematic of the seeded Zn plating on the Ag islands patterned on carbon paper[58];(b)Operando optical microscopy analysis of Zn plating and C-Ag electrodes[58];(c)Schematic illustration of the fabrication process of the Cu/Zn electrode[48];(d)The XRD result of Cu/Zn-30d electrode[48];(e)Cycling performance of Zn||MnO2 and Cu/Zn||MnO2 full cells[48]
3.2 负极表面结构改造
在锌负极的改进策略中,对锌表面进行结构改造,构建三维(3D)结构是抑制枝晶产生从而提高负极性能的有效方法,这种方法可以增加反应表面积,降低局部电流密度并使电场分布均匀,促进金属离子均匀沉积[59]。导电性良好的碳基结构和高孔隙率的多孔金属骨架常用作Zn负极的3D基板。
Kang等[60]采用恒电流电沉积法在3D多孔铜骨架上电沉积锌,沉积的Zn均匀地包覆在铜骨架上,随着Zn 不断沉积,骨架内部的孔隙被逐渐填满。3D 多孔铜骨架出色的导电性和开放式结构能够降低极化,抵消由于Zn 电镀/剥离引起的体积变化,避免了Zn 箔上出现凸起和枝晶,确保锌的均匀电镀/剥离[图5(a)],显著提高了3D Zn 负极的循环稳定性。在3D Zn||MnO2电池中[图5(b)],在0.4 A/g的电流密度下300次循环之后,放电容量几乎维持不变,展示出了非常好的循环性能。

图5 (a)3D锌负极和平面锌箔负极上的锌沉积/剥离工艺示意图[60];(b)在含有2 mol/L ZnSO4和0.5 mol/L MnSO4的电解液中,3D Zn负极或平面Zn箔负极的全电池的循环性能[60];(c)裸锌和Zn@ZnO-3D的形态[62]Fig.5 (a)Schematic diagrams of Zn deposition/stripping processes on 3D Zn electrodes and planar Zn foil electrodes[60];(b)Cycling performance of full cells with 3D Zn anodes or planar Zn foil anodes in the electrolyte containing 2 mol·L-1 ZnSO4 and 0.5 mol·L-1 MnSO4[60];(c)Morphology of bare Zn and Zn@ZnO-3D[62]
在解决了锌负极表面不平整的问题之后,调节锌负极中Zn2+的传输动力学也尤为重要。缓慢的Zn2+转移是阻碍动力学,降低电化学性能的主要因素[61]。Xie 等[62]通过液相合成法使氧化锌(ZnO)以3D 结构的形式原位均匀生长在锌箔表面。由于ZnO 界面呈现均匀的三维分布,不仅可以通过避免尖端效应的方式降低局部电流密度,还可以减少界面副反应。用反向散射电子图像(BSEI)分析Zn@ZnO-3D 的表面形貌[图5(c)],与裸Zn(Bare Zn)呈现的表面不同的是,改性后的负极表面出现了分布良好的网络互连纳米多孔结构。Zn@ZnO-3D||MnO2全电池在0.5 A/g 下循环500 次之后容量保持率接近100%。
很多结构优化后的骨架上仍然可以观察到锌枝晶,这是因为相对光滑的骨架上锌的沉积成核位点有限,所以成核活性位点的增加对抑制枝晶生长有关键影响。Jian等[63]通过化学镀的方式在铜网格上涂覆纳米多孔锡(Sn)层作为锌负极的主体(NSH)。NSH 为Zn 沉积提供了大量的成核位点,使得电场均匀。Sn 拥有氢(HER)过电位和抑制枝晶的性能,在电镀/剥离过程中,锌被引导均匀成核随后沉积在NSH 上。这是因为NSH 的纳米结构表面可以同时调节Zn2+和电场的分布,有效引导锌均匀的成核,从而在NSH上实现均匀的锌沉积。Shangguan等[64]通过微乳液法首次构建3D分层花状锌酸钙(CZO),这种结构由多个互连的菱形CZO 纳米片构成。与共沉积法制备的菱形和六边形CZO 不同,花状CZO 具有更好的高倍率性能和循环稳定性。因为花状结构能够增强比表面积,提供了大量活性位点,促进了活性材料和电解液的密切接触。
3.3 锌负极界面保护
由于锌的耐腐蚀性较差,在锌表面附着保护层可以使其表面更加稳定。常见的附着保护层的方式主要分为两类:人工附着法(如电沉积法、溶胶-凝胶法、滴涂法等)和原位生长法。通过引入涂层可以变相调节电极/电解液界面,提供更多成核位点,促进锌均匀沉积的同时减轻副反应[65]。
Cao等[66]通过电沉积法将磷(P)插入到锌晶格中形成锌磷保护层(ZnP),镀层中的P 原子有利于锌离子实现快速的离子转移并降低锌电镀/剥离过程中的电化学反应能垒。在50 mA/cm2的电流密度下沉积1 min 可以得到光滑的负极表面,过长的沉积时间会导致金属表面出现颗粒,负极表面不再平整。以MnO2为正极的全电池在电流密度为1 A/g时循环1000 次后仍可提供154.4 mA·h/g 的高放电容量。
Liang等[41]通过溶胶-凝胶法制备ZrO2纳米颗粒涂层,被包裹的Zn 负极表现出更低的极化、更高的库仑效率和更长的循环寿命[图6(a)]。ZrO2涂层可有效防止锌负极腐蚀和氧化锌致密化。该涂层不仅可以为Zn2+提供更多的成核位点,从而引导均匀的Zn 电镀/剥离,对于析氢反应还有较高的过电位,以消除氢气析出。因此,该层可以显著改善锌负极在高性能锌基电池循环过程中的可逆性。
Chen 等[67]将含有三氟甲磺酸锌[Zn(TfO)2]的聚丙烯腈(PAN)溶液滴在锌箔上制备了聚合物涂层(PANZ@Zn)。由于Zn(TfO)2的加入,PAN涂层具有优异的亲水性,降低了锌负极的界面电阻[图6(b)]。通过聚合物网络中的微通道以及Zn2+与氰基(−CN)之间的络合效应,PANZ 涂层不仅能够促进溶解的Zn2+在PANZ膜中的均匀传输,还能够引导均匀的电沉积。由于枝晶刺穿隔膜,在循环之后有玻璃纤维粘附在裸Zn 表面[图6(c)],然而PANZ@Zn 的涂层可以保持平整并且紧密粘附在Zn表面。
Han 等[68]首次提出用双功能金属铟(In)层作为腐蚀抑制剂和成核剂装饰锌表面。通过将裸锌箔浸入具有良好化学惰性的三氯化铟(InCl3)得到了修饰层[图6(d)]。In 基底比Zn 基底对Zn 原子具有更高的吸附能,表明In具有良好的亲Zn能力,使Zn原子优先沉积在其上,因此In可以诱导Zn均匀沉积。在ZnSO4电解液里浸泡8 天后,修饰后的Zn 负极没有出现副产物的特征峰[图6(e)]。对称电池优异的循环稳定性能几乎是裸Zn的10倍[图6(f)]。
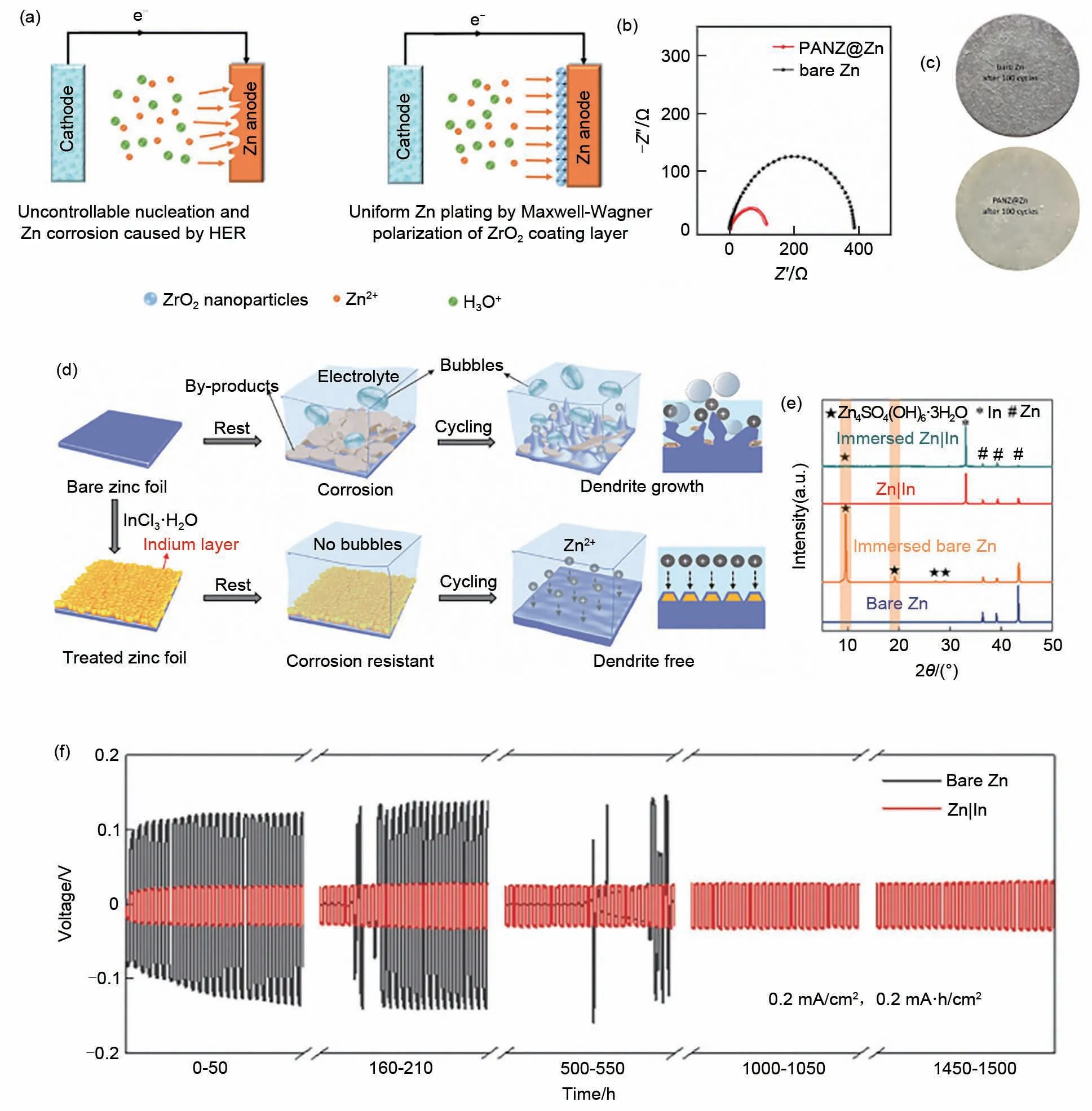
图6 (a)裸Zn负极和ZrO2涂层Zn负极的电镀剥离工艺示意图[41];(b)具有裸Zn和PANZ@Zn负极的对称电池的电化学阻抗谱(EIS)[67];(c)循环100圈后,裸Zn负极侧和PANZ@Zn负极的图像[67];(d)裸Zn 和Zn/In负极在水性ZnSO4电解液中的示意图[68];(e)裸Zn和Zn/In负极在浸入ZnSO4电解液之前和之后的XRD图像[68];(f)裸Zn和Zn/In对称电池的循环性能[68]Fig.6 (a)Schematic the stripping/plating processes of the bare Zn anode and the ZrO2-coated Zn anode[41];(b)Electrochemical impedance spectra(EIS)of symmetric cells with bare Zn and PANZ@Zn anodes[67];(c)After the 100th cycle,digital picture of bare Zn anode side and PANZ@Zn side[67];(d)Schematics of the behaviour of bare Zn and Zn/In anodes in an aqueous ZnSO4 electrolyte[68];(e)XRD patterns of bare Zn and Zn/In before and after immersion in the aqueous ZnSO4 electrolyte[68];(f)The cycling performance of bare Zn and Zn/In in symmetric cells[68]
研究人员还采取了多种涂层的方式来改善锌负极的稳定性,关于近几年锌负极的涂层材料的部分研究进展,如表1所示。

表1 近期锌负极涂层研究总结Table 1 Summary of recent research on zinc anode coating
4 电解液优化
4.1 不同锌盐对比
不同酸碱度的锌盐电解液会对锌离子电池的性能产生不同的影响。通常来说,中性或弱酸性电解液在锌离子电池中较有优势,碱性锌电池由于不可逆的问题,会产生枝晶和大量的惰性不可逆副产物[80]。然而,何种类型的电解液盐可以促进ZIBs发挥出最佳的工作性能仍然存在着争议,因此需要深入了解电解液盐与电池电化学性能之间的关系。
Zhou 等[81]在Zn||δ-CaVO 电池中对比了常用的三种电解液ZnSO4、Zn(CF3SO3)2和Zn(ClO4)2。在所有电流密度下,δ-CaVO 与Zn(CF3SO3)2电解液的比容量都大于ZnSO4或Zn(ClO4)2电解液的比容量[图7(a)]。在-20 ℃时使用Zn(CF3SO3)2电解液的电池,比容量可以达到229.5 mA·h/g。经过200次循环后,使用ZnSO4和Zn(ClO4)2电解液的电池负极表面比较粗糙[图7(c)],覆盖着许多黑色凸起,而使用Zn(CF3SO3)2电解液的电池锌负极表面保持光滑且没有黑色凸起,表明Zn(CF3SO3)2更有利于锌电镀/剥离工艺。Zn//Zn 电池的测试结果证实了Zn(CF3SO3)2电解液明显优于ZnSO4和Zn(ClO4)2电解液[图7(b)]。
除了锌盐的类别之外,不同浓度的同一锌盐也会对电池的寿命产生影响。Sun等[82]对比了不同浓度的Zn(BF4)2在Zn||四氯苯醌(TCBQ)电池中的应用。随着浓度从1 mol/L 到4 mol/L,Zn(BF4)2电解液的凝固点越来越低[图7(d)],水分子中氢键的相互作用减弱,进一步实现超低凝固点。在-30 ℃时1000 次循环后容量保持率为94%,即使在-95 ℃时,Zn||TCBQ 电池也能提供78 W·h/kg 的高比能量。
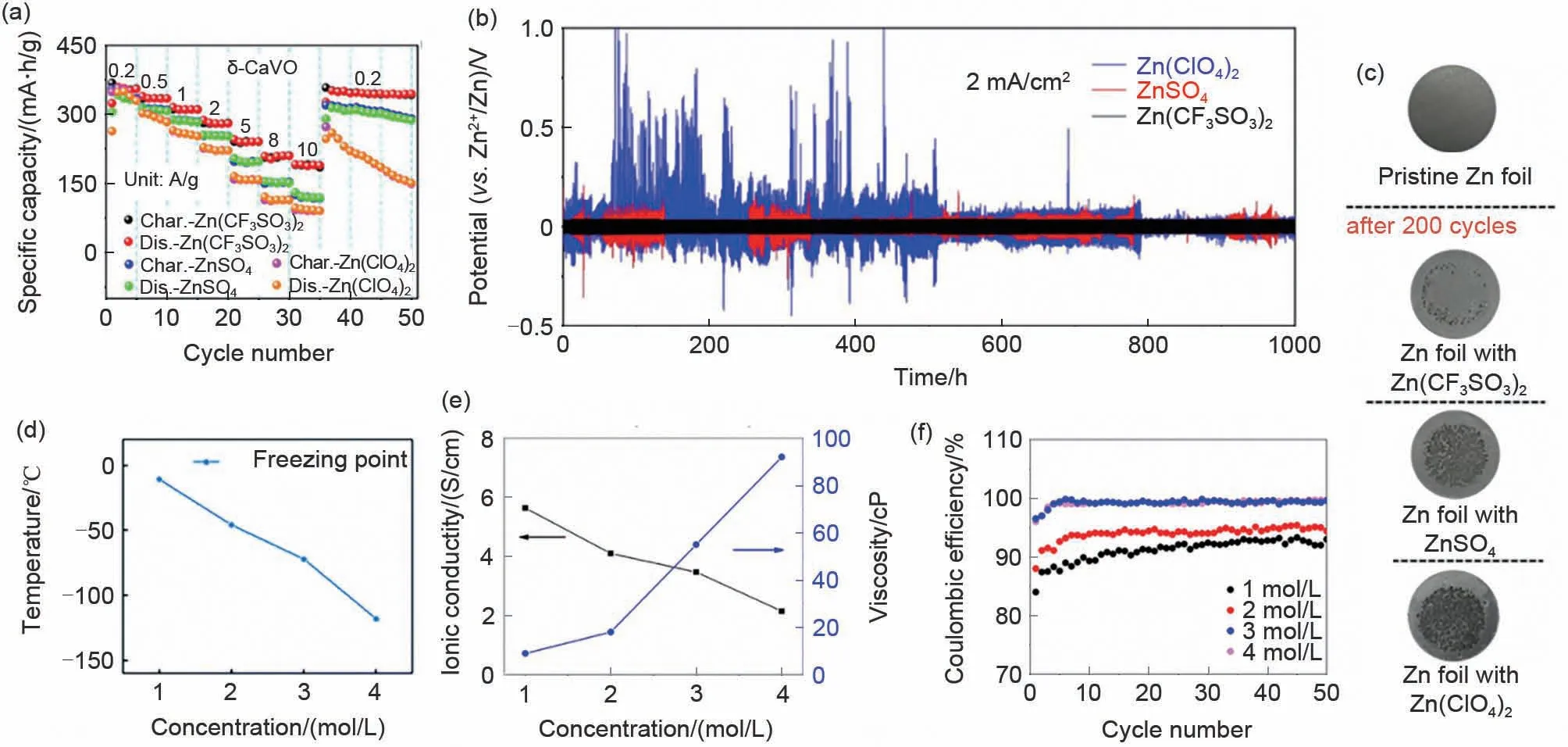
图7 (a)倍率性能[81];(b)具有不同电解液的Zn||Zn对称电池曲线[81];(c)锌箔的循环后照片[81];(d)不同浓度Zn(BF4)2电解液溶剂的凝固点[82];(e)不同浓度的Zn(CF3SO3)2电解液的黏度和离子电导率[83];(f)不同浓度Zn(CF3SO3)2电解液的CE曲线[83]Fig.7 (a)Rate performances[81];(b)GCD curves of Zn||Zn symmetric cells with different electrolyte salt[81];(c)Characterization results of the Zn foils[81];(d)The freezing points of different concentrations of Zn(BF4)2 electrolyte solvent[82];(e)Characterization of aqueous Zn(CF3SO3)2 electrolyte with different concentrations(1-4 M)viscosity and ionic conductivity[83];(f)CE curve of different concentration of Zn(CF3SO3) 2 electrolyte[83]
Zhang 等[83]研究了ZnCl2、ZnNO3、ZnSO4和Zn(CF3SO3)2四种电解液在以ZnMn2O4尖晶石作为正极材料的电池中的应用。在ZnCl2和ZnNO3电解液中Zn 的可逆电化学沉积/溶解行为不稳定,Zn(CF3SO3)2和ZnSO4电解液则能够表现出较宽的电化学窗口。与ZnSO4相比,Zn(CF3SO3)2表现出更好的可逆性和更快的Zn 沉积/溶解动力学。这归因于体积大的CF3SO3–阴离子(相对于具有双电荷的SO42–)减少了Zn2+阳离子周围的水分子数量,并减少了溶剂化效应,从而促进Zn2+传输和电荷转移。通过对比不同浓度的Zn(CF3SO3)2,3 mol/L Zn(CF3SO3)2溶液作为电解液具有3.47 S/cm 的离子电导率[图7(e)],库仑效率随着盐浓度的增加而增加[图7(f)]。由此得知,分子体积较大的锌盐更能有效抑制溶剂化效应,提供更宽的电化学窗口;较高的盐浓度可以降低水的活度并抑制副反应,从而提高电极在水溶液中的循环稳定性和容量保持率[84]。
4.2 电解液添加剂
添加电解液添加剂是提高电池性能的方式之一,添加剂能够促进锌负极和电解液界面的固态电解质界面膜(SEI)形成[85],抑制金属负极枝晶生长[86],提高电池能量密度等[87]。常用的添加剂大致可以分为聚合物、有机分子和金属离子[88-91]。电解液添加剂通常由于其亲锌疏水的特性吸附在锌负极表面调节局部电流分布,或者是阴阳离子在协同作用下改变锌离子的溶剂化结构,从而对负极产生保护作用并且有效地抑制了副反应。
Guo 等[92]运用了阴阳离子协同作用保护Zn 负极。将低成本的氯化锂(LiCl)加入3 mol/L ZnSO4电解液中,在阳离子(Li+)和阴离子(Cl–)的协同作用下提高了循环寿命和稳定性。Li+提供氧化物层屏蔽效果,通过原位形成的Li2O/Li2CO3屏蔽层,有效抑制了Zn枝晶的生长[图8(a)]。为了确定保护层的组成,通过拉曼光谱分析循环后的锌负极表面[图8(b)],加入添加剂之后,副产物Zn4SO4(OH)6(ZHS)的特征峰被明显抑制,并且在528 和1093 cm–1位置出现了Li2O和Li2CO3的特征峰。Cl–的加入将电解液pH值降低为2.3左右,接近于抑制ZHS和ZnO生长的最佳值,这有助于降低极化并增强离子传输。
电池在循环前形成的双电层(EDL)结构对于构建SEI 有着关键影响[93-94]。Huang 等[95]将界面稳定剂糖精(Saccharin,Sac)引入ZnSO4中,调节稳定的负极/电解质界面(AEI)上的EDL。将抛光打磨后的Zn 箔分别在去离子水和糖精(Sac)溶液中浸泡7 天,在去离子水中浸泡的Zn 箔的XRD 图谱中出现ZnO 的特征峰[图8(c)],没有在Sac 溶液中浸泡的Zn箔出现,这充分说明了Sac的抑制腐蚀作用。亲锌性质使得Sac 阴离子化学吸附在锌金属表面,稳定的吸附能使得水偶极子从Zn 表面脱离,从而形成了贫水结构EDL[图8(d)]。这种EDL 不仅可以抑制腐蚀反应,还可以调节Zn2+的扩散。在循环过程中,Zn 负极被含ZnSO3、ZnS 的独特SEI 膜覆盖,进而调节Zn2+沉积行为。在添加剂的作用下,Zn||Zn 在10 mA/cm2下能够循环550 h,Zn||MnO2全电池可以在循环7500次后保持100 mA·h/g的可逆容量。
添加剂的用量关系着电解液的成本,降低添加剂的使用量可以进一步促进锌离子电池商业化成为可能。Bayaguud 等[96]首次将表面活性剂型电解质添加剂硫酸四丁基铵(TBA2SO4)的添加量控制为0.0029 g/L 应用在锌离子电池中。非氧化还原剂TBA+阳离子以静电吸附方式聚集在Zn 负极表面形成了Zn2+排斥机制,通过对电解液中水合锌离子的屏蔽作用来调节初始晶核形成,并抑制后续枝晶生长。在对称电池中,在2 mA/cm2的电流密度下可以稳定循环超过300 h,在Zn||MnO2全电池中,在1 A/g 的电流密度下达到300 次循环的寿命和94%的容量保持率[图8(e)]。可见新型阳离子表面活性剂型TBA2SO4添加剂改善了电化学性能。

图8 (a)锌箔在不同电解液中剥电镀/剥离循环过程中的形貌演变示意图[92];(b)Zn负极在含或不含添加剂的电解液中循环后的表面拉曼光谱[92];(c)浸泡在水和电解液中的锌箔XRD图像[95];(d)在Sac/ZnSO4和ZnSO4电解液中循环的锌沉积示意图[95];(e)不同电解液中Zn||MnO2和3D-Zn||MnO2的循环性能和库仑效率比较[96]Fig.8 (a)Schematic illustrations of morphology evolution for Zn foils with different electrolytes during Zn stripping/plating cycling[92];(b)Raman spectra of Zn anode surface after long cycling process with or without additives[92];(c)The XRD patterns of pristine Zn plate,Zn plate soaked in water,and Zn plate soaked in Sac/water[95];(d)The Schematic diagrams for Zn deposition cycled in Sac/ZnSO4 and ZnSO4 electrolyte[95];(e)Cycling performance and CE comparison of Zn||MnO2 and 3D-Zn||MnO2 batteries in the different electrolytes[96]
除了表面活性剂之外,共溶剂在水系锌离子电池领域也能发挥作用。Shi等[97]将无水乙腈(ACN)和水按体积比1∶3的比例加入1 mol/L Zn(CF3SO3)2电解液,ACN 可以在锌表面累积并且屏蔽游离水分子,CH3CN和H2O之间的N—H键将部分取代水分子之间的氢键,有效抑制水被还原为氢气。同时和水相比,ACN 分子更容易积累在Zn 金属表面,阻止水分子和负极接触,进一步抑制了析氢。
4.3 凝胶电解液
凝胶电解液作为一种新型电解液材料,结合了液体电解液和固体电解液的优点,有效避免了电解液中存在大量活性水分子而导致的界面副反应,从而保护锌负极[98]。通常来说,凝胶电解液的挥发性低、官能团丰富、力学性能好,改善了水性电解液的不足之处。除此之外,凝胶电解液在柔性电池、可穿戴电池的应用中有无限潜力,有望在未来应用在实际生活中[99]。
Tang 等[100]基于海藻酸钠和Zn2+之间的相互作用,采用离子交联法制备了分层3D的具有出色柔韧性的锌藻酸盐凝胶(Alg-Zn)[图9(a)]。Zn2+的迁移受到羧酸根基团的限制(Malagurski 2017)[101][图9(b)],起到离子交联剂的作用。因此枝晶生长被抑制,能够实现均匀的锌沉积。循环后的Zn 负极的XRD测试显示出和裸Zn 相似的曲线[图9(c)],这表明Alg-Zn显著抑制了界面副反应。Alg-Zn凝胶电解液的亮点是恢复能力强,在电池充放电循环10 次之后搁置60 h 再循环50 次,循环仍然非常平稳,没有任何明显的电压增加。

图9 (a)Alg-Zn电解液的图像[100];(b)Alg-Na和Alg-Zn的分子结构[100];(c)循环前后锌箔的XRD图像[100];(d)具有不同盐浓度的HGE的EIS[102];(e)具有不同浓度PAMPSZn水凝胶电解质的Zn||Zn对称电池的EIS图像[103]Fig.9 (a)Photographs of the Alg-Zn electrolyte[100];(b)The molecular formulas of Alg-Na and Alg-Zn[100];(c)XRD patterns of the Zn foil before and after cycles[100];(d)EIS of the HGE with different salt concentrations[102];(e)EIS spectra of Zn||Zn symmetric cells with different concentrations of PAMPSZn hydrogel electrolyte[103]
不同浓度的电解液将会对凝胶电解液的性能起到决定性影响。Lin 等[102]在聚合物框架中结合双功能溶剂己二腈(AND)和水合盐Zn(ClO4)2·6H2O 制备了一种价格低、安全性高、有效减少副反应的凝胶电解质(HGE)。Zn(ClO4)2·6H2O 水合盐可以将水引入HGE,当浓度为2 mol/L 时[图9(d)],HGE 有较高的离子导电率,更大的电化学窗口,同时不影响电压稳定性。Zn||Zn 电池能够在0.2 mA/cm2下循环2000 h不短路。Cong等[103]采用离子交换和自由基聚合的方式合成了聚2-丙烯酰胺-2-甲基-1-丙磺酸锌(PAMPSZn)水凝胶电解液。PAMPSZn有-聚阴离子链和限制Zn2+传输的通道,有效限制了界面之间的副反应并引导Zn2+在锌金属负极表面均匀地电镀和剥离。当Zn2+浓度为1 mol/L 时,离子电导率最高[图9(e)],离子导电率随着浓度的增加先增大后减小。PAMPSZn 拥有出色的长循环稳定性,在电流密度为5.0 mA/cm2时,Zn||Zn 对称电池可以稳定循环超过100 h,优于相似条件下所有已知研究。
环境友好的概念可以巧妙地运用在水凝胶电解液的研究中。Wang等[104]基于环境友好和绿色化学的理念,以面团和添加剂氯化钠、碳酸钾为原料,研究了可以承受高温并在脱水/水合过程中保持稳定结构的凝胶电解液。球形淀粉和三维面筋网络结构为离子传输提供途径[105]。以单壁碳纳米管/聚苯胺(SWCNTs/PANI)为正极,Zn||(SWCNTs/PANI)在电流密度为0.1 A/g时放电容量为137.8 mA·h/g,并且在不同的弯曲状态下容量几乎没有变化。Li等[106]通过自由基共聚的方式将木质素磺酸钠(SL)引入聚丙烯酰胺(PAM)中,在室温下合成了具有高黏附性,高离子电导率的凝胶电解液。在45°~80°弯曲变形中实现了100%的容量保持率,超强的附着力有效降低了电极材料和电解质之间的界面电阻。在柔性Zn||MnO2电池中起到了良好的保护锌金属表面避免枝晶生长的作用。
常见的凝胶电解液分为无交联、物理交联和化学交联三种方式,不同的交联方式给凝胶电解液带来了不同的性能,其中化学交联的方式让凝胶电解液的热稳定性更强,网络结构更稳定,但是目前并未发现三种不同的交联方式对锌负极保护效果有显著差异[107]。
5 总结与展望
本综述介绍了锌金属负极在中性或弱酸性电解液中遇到的挑战,主要包括腐蚀反应和枝晶形成。腐蚀主要是由于锌的不可逆消耗,锌负极与电解液发生副反应。枝晶形成主要是由于锌负极表面成核位点不足和电场强度分布不均匀引起。这两者之间是相辅相成的,副产物的产生会更加阻碍锌离子均匀扩散,而枝晶使得比表面积扩大、电解液浓度改变,从而加剧了腐蚀。同时,将锌负极改性方案分为锌负极自身设计以及电解液优化两方面,对近年来最新的研究进行梳理总结。尽管在中性或酸性电解液中水系锌离子电池已经取得了很多进展,但是仍旧可以在以下几个方面开展深入研究。
(1)改善碱性电解液中锌负极与电解液界面的反应,改变锌离子溶剂化结构,减缓枝晶和腐蚀现象。改变水系锌离子电池仅在中性和弱酸性电解液中性能较好的现状,拓宽电解液盐的选择范围。除此之外,还可以改变隔膜的种类,为了防止被枝晶刺破可以选择机械稳定性好的隔膜与碱性电解液搭配使用,比如多孔膜、离子交换膜。
(2)优化改性策略,尝试将锌负极自身设计和电解液优化的方式结合在一起,双重延长电池寿命。通过将不同的优化策略复合加成的方式,同时解决多个现存问题。比如将锌负极界面保护和电解液添加剂策略结合,在提供更多成核位点、促进锌均匀沉积的同时屏蔽游离水分子,有效抑制析氢。
(3)改性材料的选择需要考虑成本以及对环境的影响,尽量避免使用对环境和人体危害较大的物质。选择可研究的材料时需要考虑降低成本和回收循环,低成本、低污染的环保型材料可以推动水系锌离子电池的进一步发展。此外,将低毒性的水系锌离子电池应用在可穿戴设备上也是非常有潜力的研究方向。

