水系有机液流电池电化学活性分子研究现状及展望
彭 康,刘俊敏,唐珙根,杨正金,徐铜文
(中国科学技术大学化学与材料科学学院,安徽合肥 230026)
长期以来,世界能源的发展过度依赖化石能源,导致资源紧张、气候变化、环境污染等问题日益突出[1-2]。因此,不断提高可再生能源(太阳能、风能、潮汐能等)的开发利用比重,建立以储能为核心的多能互补能源体系,是我国《能源发展“十四五”规划》提出的主要任务之一。目前,我国集中式光伏发电和风力发电都已排名世界第一,但是二者发电存在间歇性和不稳定性,无法直接并入电网使用,导致大量电能陷入闲置浪费的困境。为了解决风电光伏产业的“并网难题”,实现可再生能源发电的平滑输出和削峰填谷,各种大容量储能技术的发展势在必行[3-4]。其中,电化学类储能技术不受地质、地形、环境的限制,可以直接对电能进行存储和释放,极具行业前景。
电化学储能技术主要包括各种二次电池,其中锂离子电池占据了市场的主导地位,份额高达80%。然而,锂离子电池需使用低沸点可燃有机电解液,同时锂离子嵌入机制导致的金属锂枝晶生长问题尚未实质性解决,规模化应用存在很高的安全风险。另一方面,作为电化学储能技术的可选技术路径,具有电容量和功率解耦优势的水系全钒液流电池采用不同价态钒离子的稀硫酸水溶液作为正、负极电解液,更加安全可靠[5]。但是,稀有金属钒的纯度、成本和储量问题,以及强酸对管道设备的腐蚀问题,对水系全钒液流电池的长久稳定性造成了极大挑战[6]。
水系有机液流电池[7-12],工作原理与水系全钒液流电池相同(如图1 所示)。但水系有机液流电池采用来源广泛的有机分子作为电化学活性物质,不仅可以大大降低氧化还原电对的成本,通过合理的分子设计,还可以提高其可设计性,如对电压、电化学反应动力学、溶解性和稳定性的改善,以及优化其与非氟化质子膜、阴离子膜、自具微孔膜[13-14]甚至透析膜[15]的可匹配性,是发展下一代高安全、低成本、大容量储能技术极具潜力的研究方向。水系有机液流电池正极电解质分子,根据氧化还原活性基团的不同,主要分为氮氧自由基[16-18]、有机金属配合物[19-21]和杂环类化合物[22]。而负极电解质分子,最主要的发展体现在蒽醌衍生物[23-27]和紫精衍生物[28-32]。目前,国内外研究人员针对不同种类的电解质分子开展了大量的研究工作。本文基于水系有机液流电池研究现状,重点围绕能量密度、功率密度、效率和循环寿命四个重要性能参数对水系有机液流电池进行综述,并通过与磷酸铁锂电池、铅碳电池、水系全钒液流电池等技术对比,展望其发展前景。

图1 水系有机液流电池示意图Fig.1 Schematic of aqueous organic redox flow battery
1 水系有机液流电池性能参数
水系有机液流电池的四个重要性能参数:能量密度、功率密度、效率和循环寿命,其影响因素较为复杂。具体而言,能量密度取决于电池电压、电解质分子电化学氧化还原反应转移电子数、电解质分子浓度等;功率密度取决于电池电压、膜的面电阻、电解质分子电化学氧化还原反应速率常数等;效率取决于电解质分子的化学稳定性、膜的选择性、膜的面电阻、充放电电流密度等;循环寿命取决于电解质分子的化学稳定性、电解质分子的跨膜扩散速率等。厘清水系有机液流电池性能与电解质分子和隔膜材料之间的关系,有助于开发满足商业预期的水系有机液流电池。
1.1 能量密度
水系有机液流电池的电容量定义为单位体积电解液储存的电量,如公式(1)所示
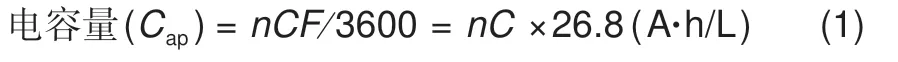
其中n是电解质分子电化学氧化还原反应转移电子数;C是电解质分子浓度。水系有机液流电池的能量密度通过公式(2)计算
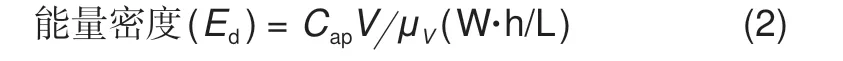
其中V是电池电压;μV是体积因子(μV=1+低电解液浓度侧的浓度/高电解液浓度侧的浓度)。受限于水解离电压(理论值1.23 V),水系有机液流电池电压较低,需要电解质分子具有更多的电化学氧化还原反应转移电子数和更高的水溶解度。
以水系有机液流电池负极电解质分子甲基紫精(MV2+)为例,MV2+发生一步电子转移还原成MV∙+自由基阳离子,电极电势为-0.45 V(vs. SHE),该过程反应速度快且高度可逆,而进一步降低电势[-0.76 V(vs. SHE)],自由基阳离子MV∙+继续得到电子还原为非离子型MV0分子时,MV0分子在水溶液中溶解度极低,导致第二步电子转移过程不可逆。因此,为了实现紫精类衍生物在水相中的两电子过程,提高电池能量密度,Debruler等人[28]采用不同修饰基团对紫精进行亲水改性,实现两电子还原产物的溶解,如图2 所示。进一步地,Luo 等人[33]将平面的噻唑并噻唑(TTz)骨架引入到紫精骨架中,得到[(NPr)2TTz]Cl4[图3(a)],通过扩展π 共轭结构和电子离域范围,提高中间态自由基的稳定性,使得两步电子转移过程可逆性增强;Hu 等人[34]采用“共轭自调控策略”进行分子结构设计,利用可旋转的苯基在空间上隔离两个吡啶盐活性中心,构建了一个可开关的共轭系统(APBPy)Cl4[图3(b)],实现紫精衍生物的一步两电子。为了实现单分子的多电子储能,Huang等人[31]首次提出多电活性中心(Multiple Redox Center,MRC)设计理念,通过将致密电子存储单元(三嗪环)与自由基稳定单元(吡啶盐环)进行桥联,成功构建可进行六电子可逆氧化还原反应的三吡啶盐三嗪多电子分子(TpyTz)6,如图4 所示。该分子作为负极电解质分子实现四电子的稳定充放电,0.50 mol/L组装的电池容量达到33.0 A·h/L。

图2 储存两电子的紫精衍生物合成路线[28]Fig.2 Synthesis of Two-Electron Storage Viologen Molecules[28]

图3 [(NPr)2TTz]Cl4[33]和(APBPy)Cl4[34]分子结构Fig.3 Molecular structures of(a)[(NPr)2TTz]Cl4[33]and(b)(APBPy)Cl4[34]
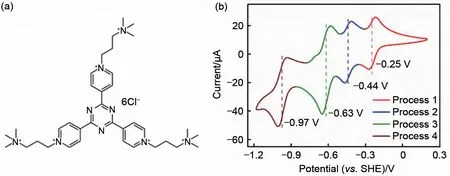
图4 (TpyTz)6的(a)分子结构及(b)循环伏安图[31]Fig.4 (a)Molecular structure and(b)cyclic voltammogram of(TpyTz)6[31]
另外,电解质分子醌类(quinone)和喹喔啉(quinoxaline)衍生物可实现两电子可逆氧化还原,在相同电解质分子浓度下,储存的电量是单电子电解质分子的两倍,因此备受研究人员关注[35-42]。提高基于该类电解质分子的水系有机液流电池能量密度,往往从降低还原电势和提高溶解度两个角度入手。Huskinson等人[23]在Nature杂志上报道了基于蒽醌-2,7-二磺酸二钠(AQDS)负极电解质分子的水系有机液流电池[图5(a)],通过在AQDS 上引入两个羟基降低其还原电势[图5(b)],将电池开路电压提升11%。而Hu 等人[27]将AQDS 的反离子Na+替换成[图5(c)],利用和AQDS2-的氢键相互作用,将AQDS 的溶解度从0.58 mol/L 提升至1.9 mol/L[图5(d)]。
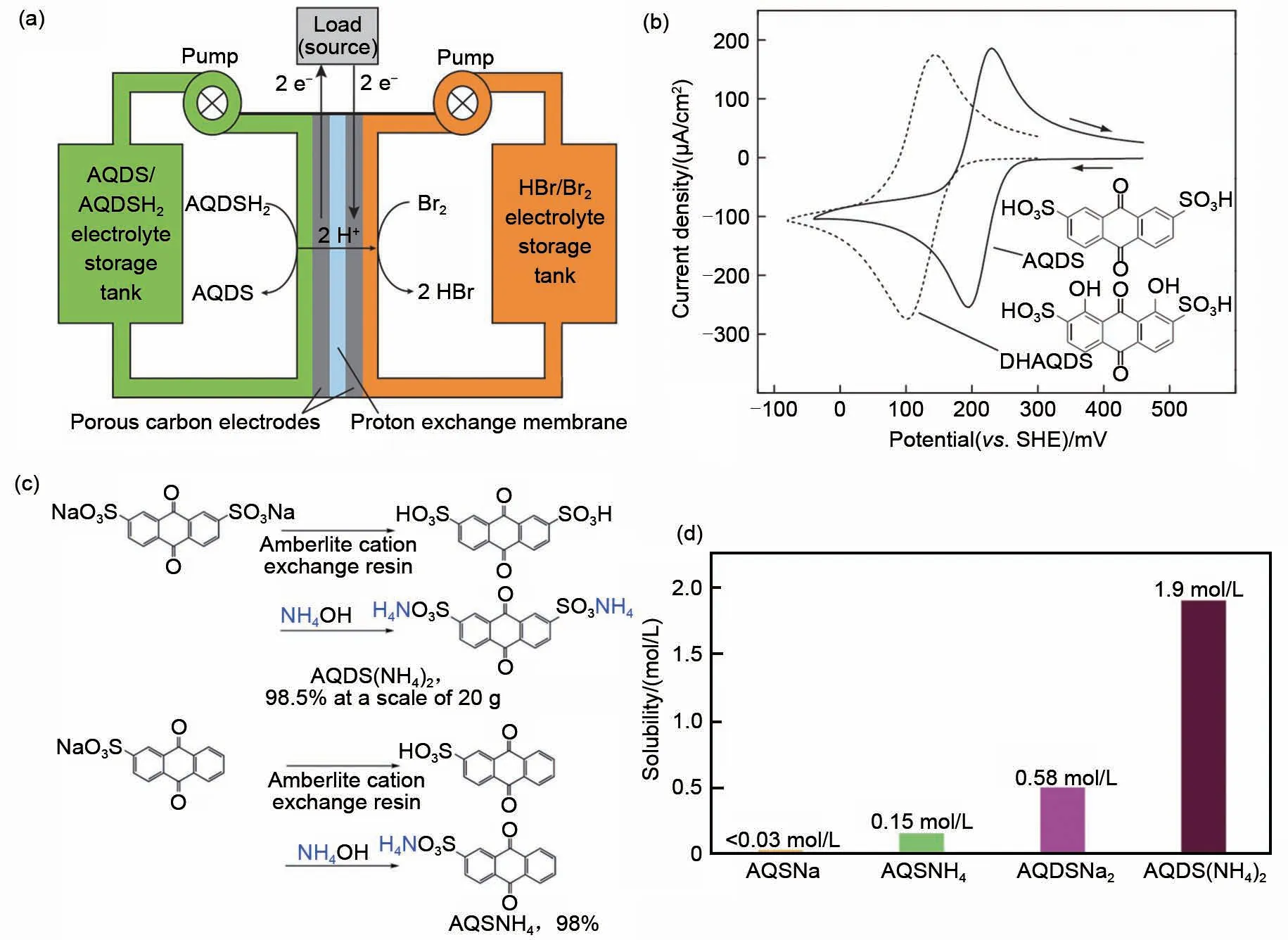
图5 (a)AQDS/HBr电池原理图[23];(b)AQDS和DHAQDS的循环伏安图[23];(c)AQDSNH4 和AQS(NH4)2的合成路线[27];(d)AQSNa、AQSNH4、AQDSNa2、AQDS(NH4)2溶解度对比[27]Fig.5 (a)Schematic of AQDS/HBr cell[23];(b)Cyclic voltammogram of AQDS and DHAQDS[23];(c)Synthesis of AQDSNH4 and AQS(NH4)2[27];(d)A comparison of the solubility of AQSNa,AQSNH4,AQDSNa2,and AQDS(NH4)2[27]
水系有机液流电池正极电解质分子方面,Janoschka等人[17]利用三甲胺基替换4-OH-TEMPO上的羟基得到了N,N,N-2,2,6,6-七甲基哌啶-氮-氧自由基-4-铵(TEMPTMA)氯化物电解质分子,由于三甲胺的吸电子作用更强,TEMPTMA/MV的理论电压比4-OH-TEMPO/MV 提高0.15 V,且TEMPTMA的水溶性更优。Liu等人[18]报道了4-[3-(三甲铵基)丙氧基]-2,2,6,6-四甲基哌啶-氮-氧自由基(TMAPTEMPO)氯化物电解质分子。TMAP-TEMPO 在水中的溶解度为4.62 mol/L,是目前已报道的各类TEMPO 衍生物的最高值,这主要是由于在TEMPO 主体结构中引入荷电侧链基团后,极大地增大了分子极性,进而增强了其在水中的溶解。
除了分子结构改性,研究人员还通过调节支持电解质与有机活性分子间的相互作用来提高有机活性分子的水溶性。Huang等人[43]以3 mol/kg咪唑类盐作为支持电解质,基于咪唑基团与氮氧自由基的分子间相互作用(静电吸引作用和氢键作用)[44],实现了4.3 mol/L 4-OH-TEMPO 的溶解,如图6(a)、(b)所示。同时,该支持电解质还实现了甲基紫精二电子还原态MV0的溶解。Ding等人[45]基于向湿性增溶策略,引入尿素作为支持电解质,将电解质分子对苯二酚的溶解度增强3 倍,如图6(c)所示。此外,低共熔电解质[46-48]和靶向氧化还原电解质[49-50]也是高能量密度液流电池的研究方向。
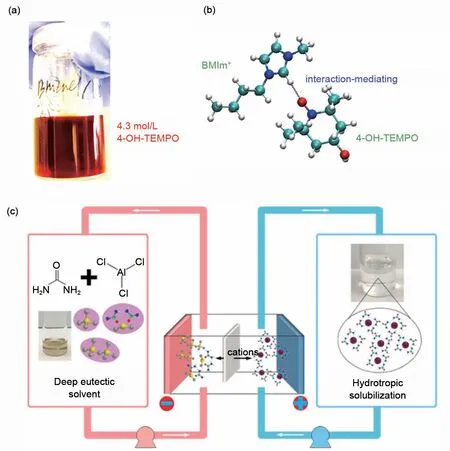
图6 (a)4.3 mol/L 4-OH-TEMPO溶解于3 mol/kg BMImCl/H2O溶液中的实物照片[43];(b)咪唑基团与氮氧自由基的分子间相互作用力示意图[43];(c)氧化还原液流电池中向湿性增溶策略[45]Fig.6 (a)Photograph of a solution containing 4.3 mol/L 4-OH-TEMPO in 3 mol/kg BMImCl/H2O at room temperature[43];(b)Schematic illustration of the interactions between the imidazolium group and the organic solute[43];(c)Hydrotropic solubilization for hybrid ion redox flow batteries[45]
表1总结了代表性电解质分子的电化学氧化还原反应转移电子数、溶解度、电势、理论电容量以及文献出处。提高电解质分子的可转移电子数是提高电解质分子理论电容量最显著的手段,而为了实现电解质分子二电子或者多电子的充放电稳定性,往往需要引入共轭基团。另一方面,对电解质分子进行亲水改性,如引入季铵基、磺酸基、羟基、磷酸基、咪唑基等,是提高电解质分子理论电容量最直接的手段。同时,可以考虑在正极电解质分子上引入吸电子基团提高电势或在负极电解质分子上引入给电子基团降低电势,从而提高电池电压,进一步提升电池能量密度。而从支持电解质与活性分子相互作用角度出发提升活性分子水溶性或改变其电势也是提升电池能量密度的常用策略。高能量密度有利于降低水系有机液流电池储能系统的整体造价,提高其在大规模储能市场的竞争力[51]。
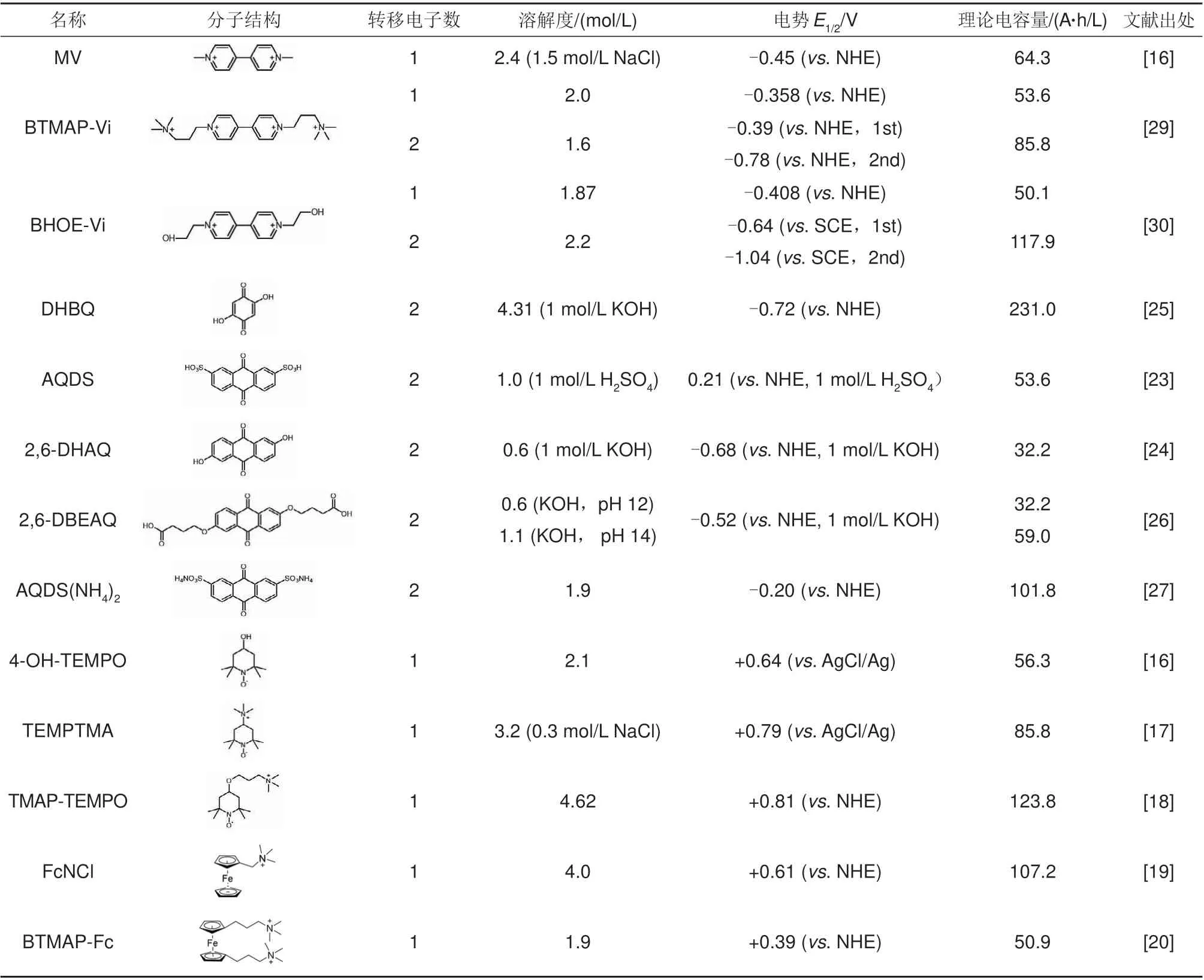
表1 代表性电解质分子的电化学氧化还原反应转移电子数、溶解度、电势、理论电容量以及文献出处Table 1 Number of electrons,solubility,potential,theoretical capacity,and reference of representative electrolyte molecules
1.2 功率密度
水系有机液流电池的功率密度随电解质分子电化学氧化还原反应速率常数、膜的面电阻以及电池电压的不同,通常处在50~300 mW/cm2范围。放电功率密度依据公式(3)计算
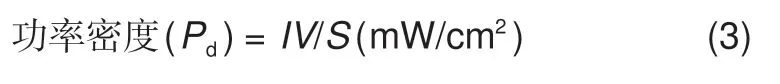
其中,I是放电电流;V是输出电压;S是隔膜的有效面积。
增大电解质分子氧化还原反应速率常数可以提高电池的功率密度,通常涉及电解质分子结构调控和电极性能调控。Sun等人[52]采用这两种策略,将2,5-二羟基-3,6-二甲基-1,4-苯醌(DMBQ)的电子转移电阻分别降低了48.1%或55.8%,搭配亚铁氰化钾组装的全电池的最大放电功率密度提高了49.4%或60.7%。从图7可以看出,DMBQ在玻碳电极上的动力学性质较差,而通过将DMBQ 的两个甲基基团替换为两个甲氧基合成2,5-二甲氧基-3,6-二羟基-1,4-苯醌(DMOBQ),氧化还原峰间距从440 mV缩小至260 mV;而在玻碳电极表面涂覆上氮和硫共掺杂的多孔碳微米棒(N/S-CMRs)催化剂,氧化还原峰间距可以缩小至80 mV。表2 和图8 更加直观地反映出电解质分子氧化还原反应速率常数对电池功率密度的影响。
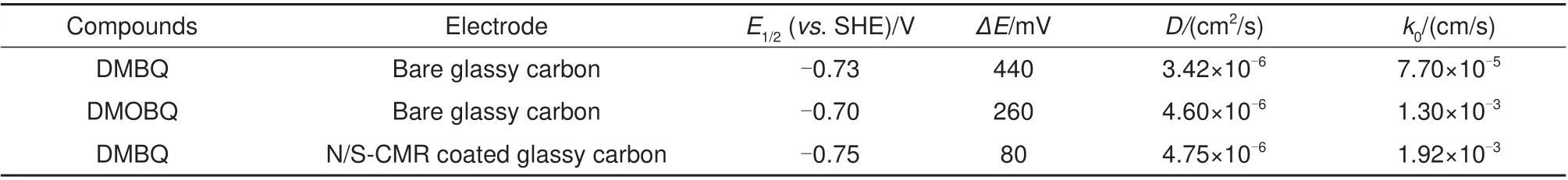
表2 DMBQ、DMOBQ和DMBQ在涂覆催化剂电极上的氧化还原电位E1/2,氧化还原峰间距ΔE和氧化还原动力学参数[52]Table 2 Redox potential E1/2,oxidation-reduction peak separation ΔE,and redox kinetics of DMBQ and DMOBQ on varied electrodes[52]
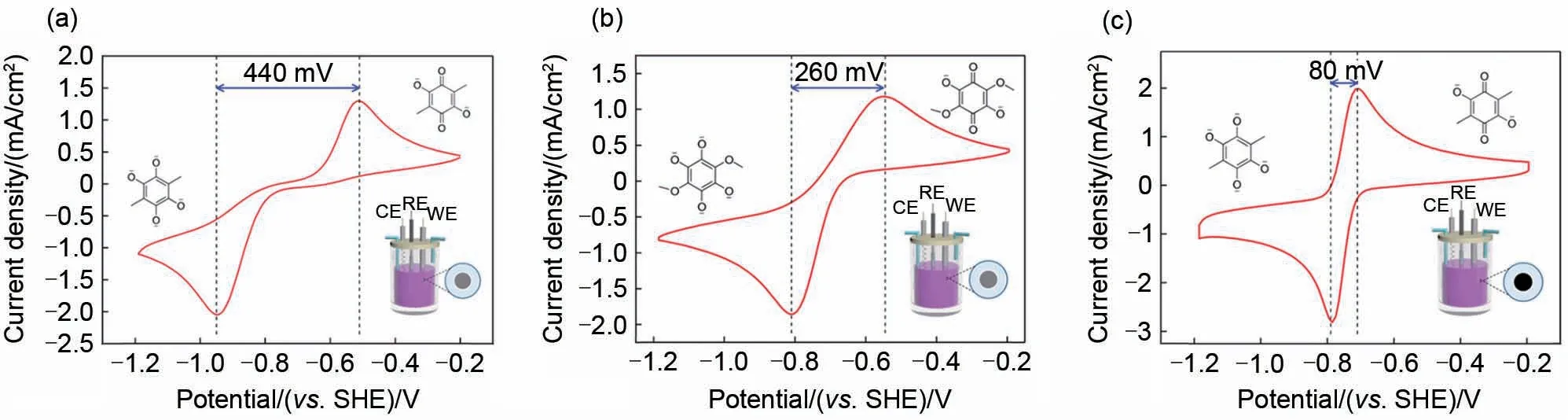
图7 (a)DMBQ和(b)DMOBQ在玻碳电极上的循环伏安图;(c)DMBQ在涂有N/S-CMRs的玻碳电极上的循环伏安图[52]Fig.7 Cyclic voltammograms of(a)DMBQ and(b)DMOBQ on glassy carbon electrode;(c)DMBQ on glassy carbon electrode coated with N/S-CMRs,respectively[52]
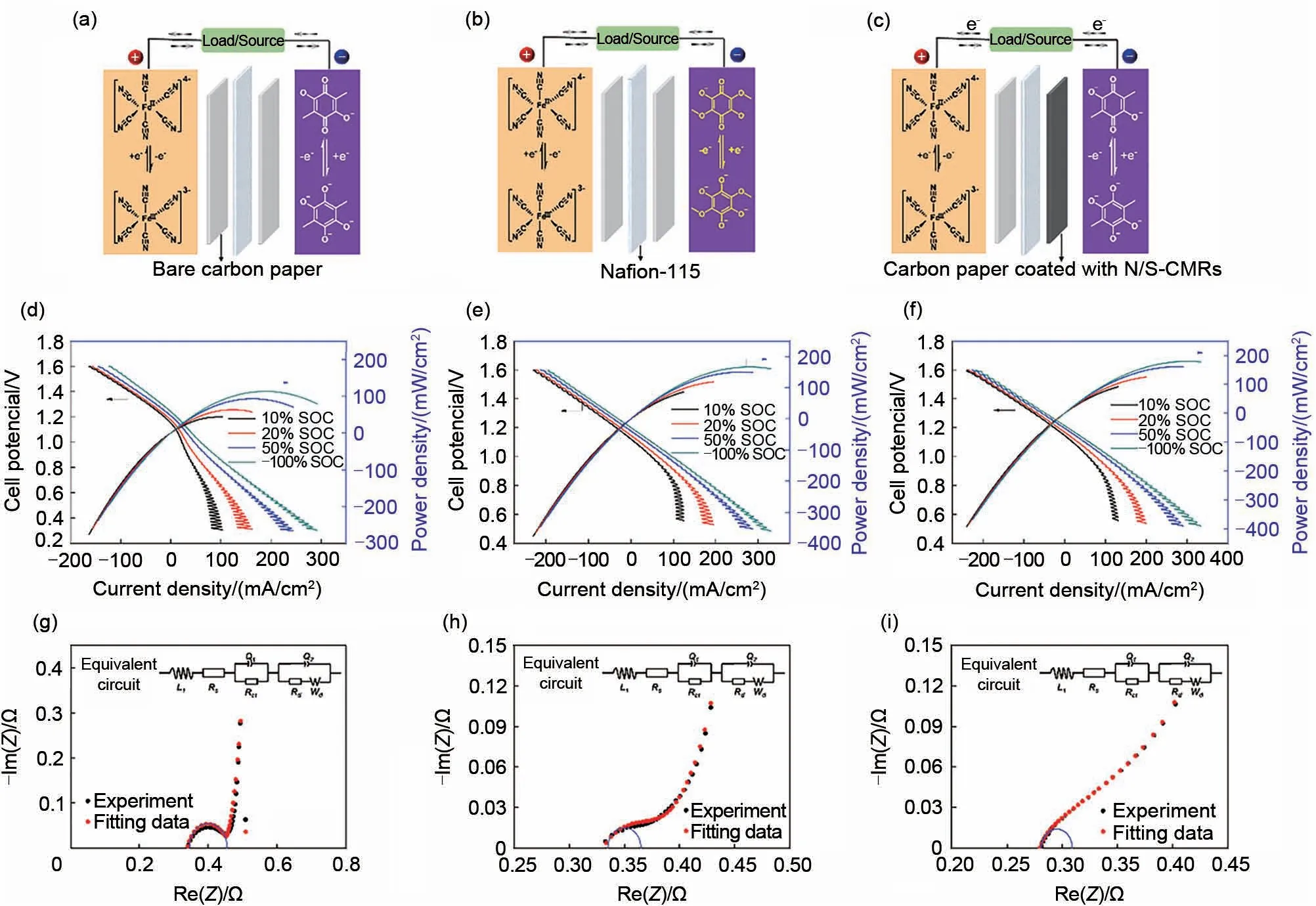
图8 电池原理图、电池的极化曲线以及实验和拟合的电化学阻抗谱[52]Fig.8 Schematic of cells,polarization curves of the assembled cells,and experimental and fitted electrochemical impedance spectroscopy(EIS)of the assembled cells[52]
此外,膜的面电阻也将直接影响电池的功率密度。Yang等人[25]在DHBQ/K4Fe(CN)6电池中分别装配Nafion 212 膜(面电阻1.10 Ω·cm2),Nafion 115膜(面电阻2.11 Ω·cm2)和Nafion 117 膜(面电阻2.60 Ω·cm2),发现低电阻的Nafion 212 可以使电池最大放电功率密度达到300 mW/cm2,如图9所示。

图9 装配(a)Nafion 212膜,(b)Nafion 115膜和(c)Nafion 117膜的DHBQ/K4Fe(CN)6电池的电化学性能[25]Fig.9 Electrochemical performance of a DHBQ/K4Fe(CN)6 cell assembled with(a)Nafion 212 membrane(N212),(b)Nafion 115 membrane(N115)and(c)Nafion 117 membrane(N117)[25]
相对于非水系电池,水系有机液流电池由于离子在水溶液中的快速传导而展现出高功率密度。通过调控电解质分子母核上的取代基种类、数量、空间位阻,可以直接调控活性分子的氧化还原电势及氧化还原反应速率常数,进而改善电池的功率密度。优化电极性能和降低膜面电阻,也是提高电池功率密度的有效策略。
1.3 效 率
水系有机液流电池效率包含库仑效率ηCE、电压效率ηVE和能量效率ηEE。库仑效率ηCE是放电过程释放的电容量QD与充电过程消耗的电容量QC之比,如公式(4)所示反映电池系统的可逆性。

能量效率ηEE是放电过程释放的能量与充电过程储存的能量之比,如公式(6)所示
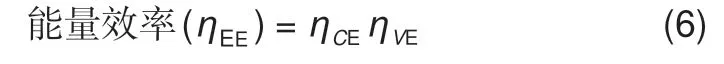
电压效率和能量效率主要受膜的面电阻和充放电电流密度影响。
由于文献[18]报道的充放电测试一般在很短时间内完成,电解质分子不可逆的副反应和跨膜渗透的发生程度较小,所以库仑效率接近100%。如220 h 完成0.1 mol/L TMAP-TEMPO 的1000 圈循环测试、80.6 h 完成0.5 mol/L TMAP-TEMPO 的200 圈循环测试、171.7 h 完成1.5 mol/L TMAPTEMPO 的250 圈循环测试,每圈循环测试的时间均不足1 h,库仑效率均在99.9%左右,如图10所示。

图10 (a)0.1 mol/L、(b)0.5 mol/L和(c)1.5 mol/L TMAP-TEMPO正极电解液所组装的TMAP-TEMPO/BTMAP-Vi电池性能测试[18]Fig.10 Performance of TMAP-TEMPO/BTMAP-Vi cell assembled with(a)0.1 mol/L,(b)0.5 mol/L and(c)1.5 mol/L TMAP-TEMPO chloride in posolyte[18]
电压效率和能量效率受膜的面电阻和充放电电流密度影响较大,膜的面电阻越小,电压效率和能量效率越高;充放电电流密度越小,电压效率和能量效率也越高。如图11(a)所示,不同电流密度下测试FcNCl/MV电池搭配不同阴离子交换膜的能量效率。三种阴离子交换膜的面电阻依次是DSV膜(1.70 Ω·cm2)

图11 (a)40~100 mA/cm2电流密度下FcNCl/MV电池搭配不同阴离子交换膜(DSV、AMV、ASV)的能量效率测试结果[53];(b)20~200 mA/cm2电流密度下4-OH-TEMPO/MV电池搭配不同阴离子交换膜(QPFPAE-x、DSV)的能量效率测试结果[54]Fig.11 (a)Energy efficiency vs.the cycle number from 40 to 100 mA/cm2 of the FcNCl/MV AORFBs with different membranes using 2.0 mol/L NaCl supporting electrolyte[53];(b)Energy efficiency of the 4-OH-TEMPO/MV batteries with QPFPAE-x and DSV membranes from 20 to 200 mA/cm2[54]
提高电池能量效率,可以采用降低膜的面电阻策略,但降低膜的面电阻往往也会降低膜对电解质分子的阻隔能力,造成电解质分子渗透严重。为了突破离子膜材料选择性和传导能力的瓶颈,同时提供高离子传导能力和高选择性,徐铜文教授和杨正金教授课题组[14]提出:利用离子在受限空间内受到的增强电荷相互作用,加速离子传递,提高传导性;利用限域孔筛分效应,提高选择性。基于此思路,Zuo 等人[14]开发了一种新型的阳离子膜材料:磺化自具微孔离聚物膜(SPX-BP 膜)。以SPX-BP-0.95 为隔膜组装的K4[Fe(CN)6]/DHAQ 水系有机液流电池的膜电阻仅为0.70 Ω·cm2,60 mA/cm2电流密度下能量效率为88%,在1000 圈的连续循环过程中,能量效率基本保持不变,库仑效率接近100%,如图12所示。

图12 (a)K4[Fe(CN)6]/DHAQ电池原理图;(b)不同电流密度下,K4[Fe(CN)6]/DHAQ电池搭配不同阳离子交换膜(Nafion 117、SPX-HFP-0.63、SPX-BP-0.61)的能量效率测试结果;(c)60 mA/cm2电流密度下,搭配SPX-BP-0.95膜的K4[Fe(CN)6]/DHAQ电池长时间恒流充放电循环测试结果[14]Fig.12 (a)Schematic of K4[Fe(CN)6]/DHAQ cell;(b)Energy efficiency of K4[Fe(CN)6]/DHAQ cells assembled with Nafion 117,membranes from SPX-HFP-0.63,SPX-BP-0.61,as functions of current density;(c)Long-term galvanostatic cycling of a K4[Fe(CN)6]/DHAQ cell assembled with SPX-BP-0.95 at 60 mA/cm2[14]
降低电池内阻分压占比,也可以采用提高电对电压的策略。如图13(a)所示,Huang 等人[32]设计了理论电势差1.51 V的氧化还原电对,正极电解质分子通过吸电子基团提高电势差,负极电解质分子通过给电子共轭基团降低电势差。全电池搭配商业化DSV 膜,在60 mA/cm2电流密度下的能量密度高达85.7%[图13(b)],在100 mA/cm2电流密度下的能量密度也达到了77.5%[图13(c)]。
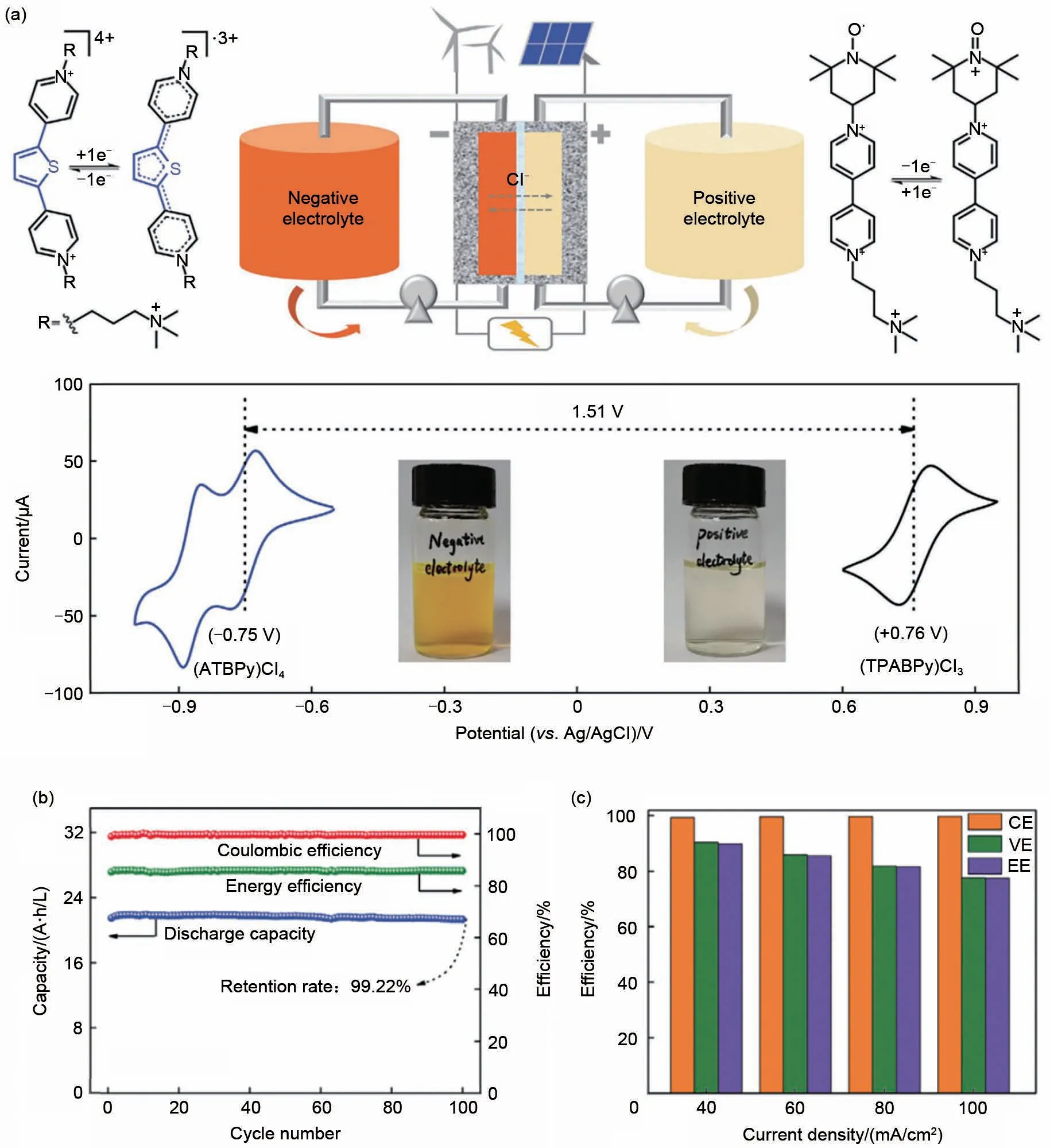
图13 (a)1.51 V全电池及半电池反应示意图;(b)60 mA/cm2电流密度下循环测试性能;(c)不同电流密度下的库仑效率、电压效率及能量效率[32]Fig.13 (a)The schematic of the full cell(1.51 V)and the corresponding half-cell reactions;(b)cycling performance at 60 mA/cm2;(c)corresponding efficiencies(CE:coulombic efficiency,VE:voltage efficiency,EE:energy efficiency)at different current densities[32]
无论水系有机液流电池是用于发电侧可再生能源并网减少弃光弃风,还是企业用户侧峰谷价差套利,能量效率都是核心的性能参数。能量效率越高,意味着能量储存和释放的过程中损失的能量越少,才能保证可再生能源的高效利用。
1.4 循环寿命
水系有机液流电池的循环寿命在不考虑电池结构和电极材料磨损的情况下由电解液电容量的循环稳定性决定。而电解液电容量的衰减,一方面来源于电解质分子的化学降解,另一方面来源于电解质分子的跨膜渗透。因此,提高电解质分子的化学稳定性和减弱电解质分子的跨膜渗透,是提升电池循环寿命最重要的两条路径。Kwabi等人[55]将电池电容量衰减分为四个等级:高(>1%/d)、中(0.1%~1%/d)、低(0.02%~0.1%/d)和极低(≤0.02%/d)。电池循环寿命越长,电解液补充或更换的频次越低,将会大大降低电解液的使用成本。
有机电解质分子易在水溶液中发生各种化学降解反应,图14 总结了部分有机电解质分子的主要降解路径,包括迈克尔加成、亲核取代、水解、歧化、二聚、互变异构等反应[55]。针对不同的降解路径,可以尝试不同的电解质分子结构调控策略进行稳定性优化。如2,6-DBEAQ在碱性条件下易被氢氧根、羧酸根亲核进攻[图15(a)][26],而将2,6-DBEAQ的羧酸根换成磷酸根制备2,6-DPPEAQ[图15(b)],不仅可以在较低pH 值条件下溶解电解质分子,还可以规避羧酸根,使电池的电容量衰减速率从0.05%/d[图15(c)]降低至0.014%/d[图15(d)][56]。进一步地,在蒽醌母核上基于碳碳键连接上亲水基团,而不是碳氧键,可以消除SN2 或者SNAr 降解反应,使电池的电容量衰减率降低至<1%/d[图15(e)][57]。同时也可以注意到,电解液体系的pH 对循环稳定性也有很大影响。

图14 部分有机电解质分子的主要化学降解路径[55]Fig.14 The main chemical decomposition mechanisms for some redox-active molecules[55]
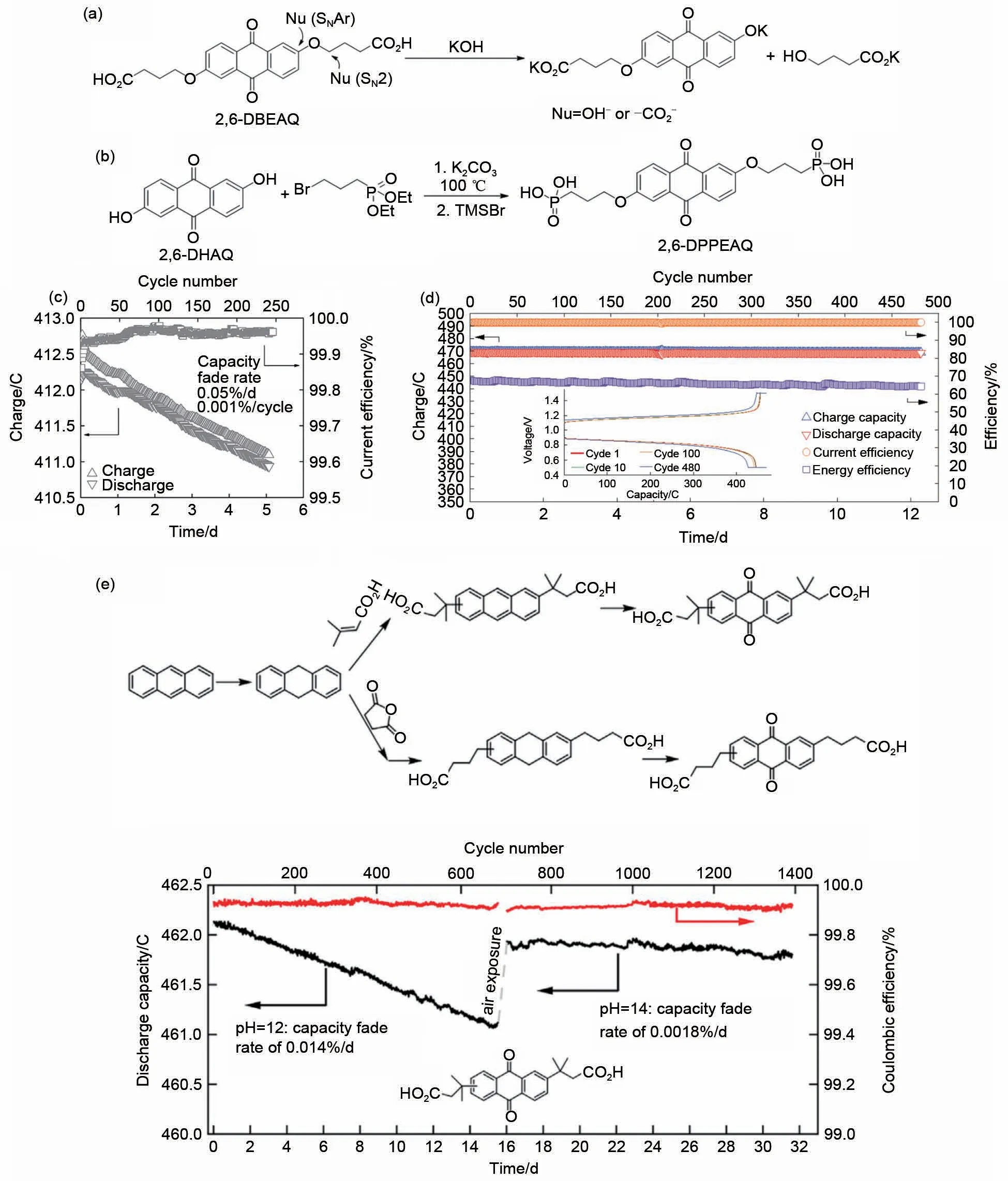
图15 (a)2,6-DBEAQ的化学降解机理[56];(b)2,6-DPPEAQ的合成路径[56];(c)2,6-DBEAQ/K4Fe(CN)6电池性能表征[26];(d)2,6-DPPEAQ/K4Fe(CN)6电池性能表征[56];(e)DPivOHAQ 和DBAQ的合成路径,及DPivOHAQ/K4Fe(CN)6电池性能表征[57]Fig.15 (a)Proposed decomposition mechanisms for 2,6-DBEAQ[56];(b)Synthetic route for 2,6-DPPEAQ[56];(c)Performance of 2,6-DBEAQ/K4Fe(CN)6 cell[26];(d)Performance of 2,6-DPPEAQ/K4Fe(CN)6 cell[56];(e)Synthetic route for DPivOHAQ and DBAQ,and Performance of 2,6-DPivOHAQ/K4Fe(CN)6 cell[57]
二聚体的形成也是有机电解质分子常见的衰减副反应,如图16所示,抑制了二聚体(DHA)24-的形成,Goulet 等人[58]采用SOC 控制和引入氧气降低中间产物含量的策略;抑制TEMPO类分子和紫精类分子二聚,Liu等人[18]和Hu等人[29]均采用了增大分子空间位阻和电荷斥力的策略。TMAP-TEMPO 相较4-OH-TEMPO而言,不仅化学结构更加稳定,跨膜(AMV膜)渗透系数也下降了一半。4-OH-TEMPO和TMAP-TEMPO跨膜渗透系数分别为1.34×109和6.40×10-10cm2/s,这主要是由于引入荷电的侧链后,一方面TMAP-TEMPO的分子尺寸增大,阻碍了其通过AMV 离子隔膜,另一方面荷正电基团的存在导致TMAP-TEMPO 与AMV 离子隔膜中荷正电的功能基团之间存在静电排斥效应,也极大地降低了其渗透速率。BTMAP-Vi相较MV而言,也是相同的效果。近期,Hu等人[59]搭配正极N2-TEMPO和负极[(NPr)2V]Cl4,组装的全电池展现出极高的循环稳定性,如图17所示。
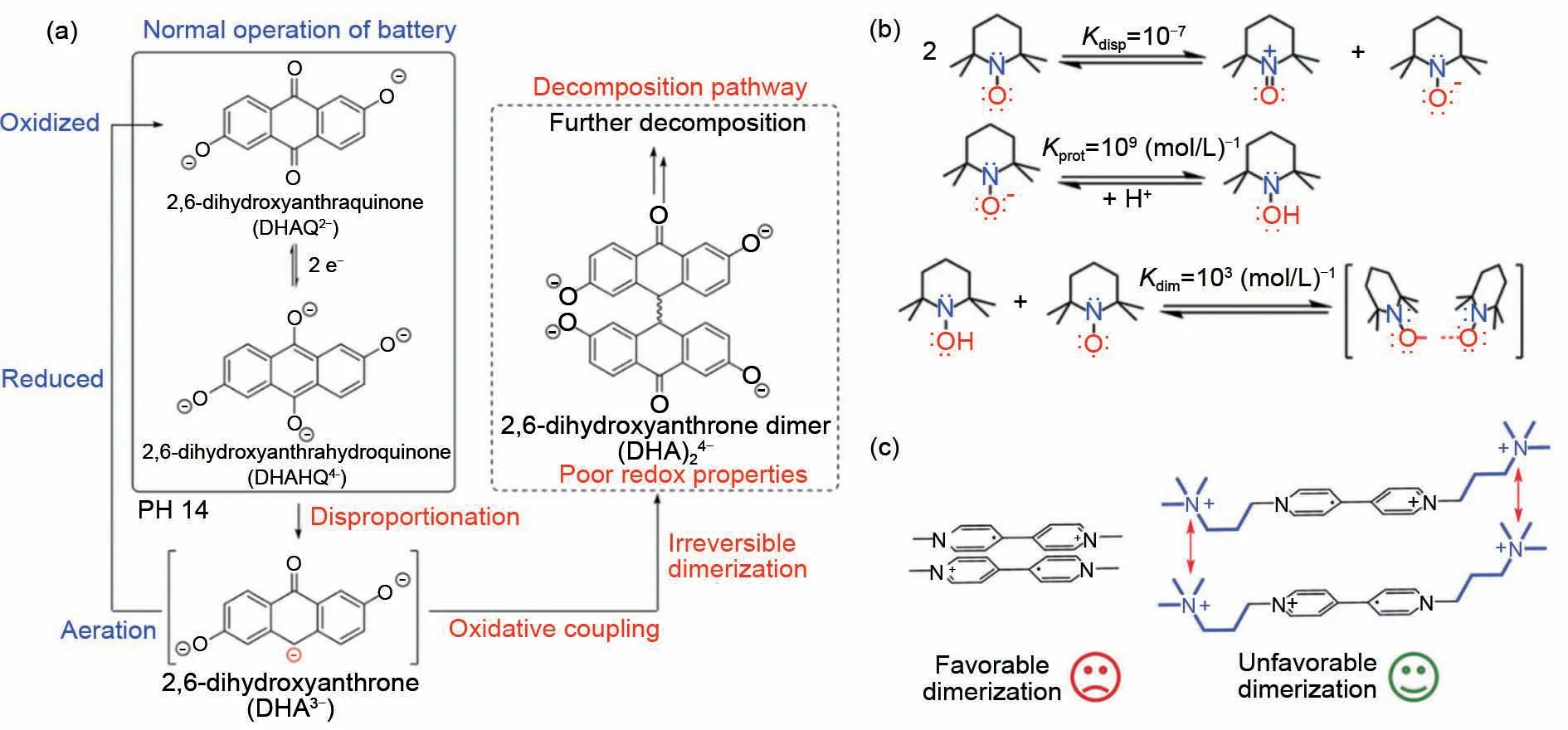
图16 部分有机活性分子的二聚反应[29,58,60]Fig.16 Dimerization of some redox-active molecules

图17 N2-TEMPO/[(NPr)2V]Cl4电池原理示意图及电解质分子反应[59]Fig.17 Schematic illustration of N2-TEMPO/[(NPr)2V]Cl4 AORFB and its battery reactions[59]
除了电解质分子结构改性,研究人员还通过调控隔膜孔结构和孔径分布去降低电解质分子的跨膜渗透。Tan等人[61]基于含有tröger's碱或amidoxime基团的固有微孔性聚合物合成了一种具有窄分子大小通道的亲水离子膜,该膜精细控制的亚纳米孔结构对小有机分子具有高的尺寸排阻选择性,应用于FMN-Na/K4Fe(CN)6和2,6-DHAQ/K4Fe(CN)6电池体系,均展现出高容量保持率,如图18所示。

图18 (a)亲水微孔膜高效离子传导和筛分的工作原理图;(b)FMN-Na/K4Fe(CN)6和(c)2,6-DHAQ/K4Fe(CN)6电池搭配不同隔膜的循环稳定性测试[61]Fig.18 (a)Working principle of hydrophilic microporous membranes for fast ion transport and high ionic and molecular selectivity;Cycling stability of(b)FMN-Na/K4Fe(CN)6 and(c)2,6-DHAQ/K4Fe(CN)6 batteries with various membranes[61]
电极材料的选择也会改变水系有机液流电池的循环稳定性。Xu等人[42]测试了碳纸、碳布在同样的电池体系和测试条件下对电池循环稳定性的影响,如图19 所示。考虑到水系有机液流电池的充放电是典型的化工过程,电极材料的更优选择,可以保证电解质分布的均一性、电流密度分布的均一性、内容温度分布的均一性,从而减少电池内部局部极化,提升电池循环稳定性。

图19 (a)碳纸、(b)碳布对电池循环稳定性的影响[42]Fig.19 Discharge capacity and Coulombic efficiency(CE)and are plotted as functions of time and cycle number with(a)carbon paper or(b)carbon cloth as electrode[42]
表3总结了部分水系有机液流电池循环稳定性测试结果。水系有机液流电池循环稳定性的影响因素较为复杂,涉及电解质分子化学稳定性、隔膜选择性、体系pH、电解液浓度、支持电解质种类、碳毡结构、充放电方式、电池运行环境等,提升水系有机液流电池循环稳定性是一项系统性工程。
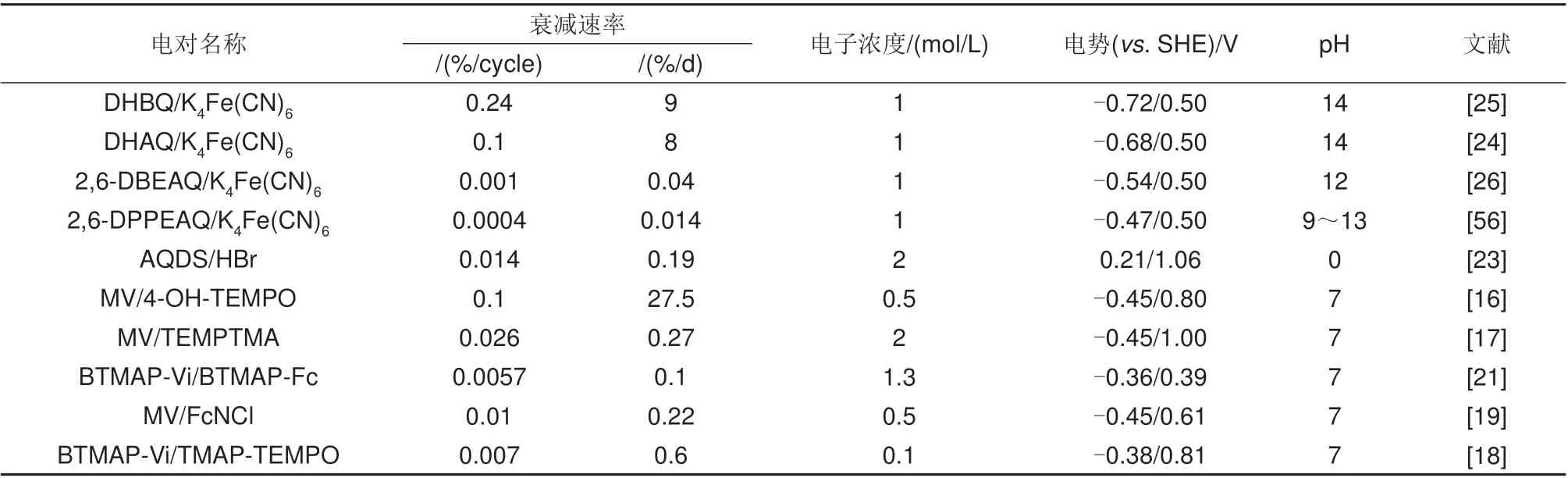
表3 部分水系有机液流电池循环稳定性测试结果Table 3 Summary of some aqueous organic redox flow battries’cycling stability
2 水系有机液流电池展望
为了实现“碳中和”、“碳达峰”的双碳目标,发展大规模储能技术势在必行。抽水储能占据了储能市场90%以上份额,但是抽水储能对地质、地形要求很高,进一步发展的局限性较大。电化学储能市场,锂离子电池的综合性能最优,但安全性问题目前无法从本质上解决。2021 年6 月22 日,国家能源局就《新型储能项目管理规范(暂行)(征求意见稿)》公开征求意见。征求意见稿指出:在电池一致性管理技术取得关键突破、动力电池性能监测与评价体系健全前,原则上不得新建大型动力电池梯次利用储能项目。同时,该征求意见稿还对电网提出了要求,要求电网应公平无歧视,为新型储能项目提供电网接入服务。因此,未来的几年时间,各种新型电化学储能技术将进入百花齐放的蓬勃发展期。
表4 总结并对比了磷酸铁锂电池、铅碳电池、水系全钒液流电池、水系有机液流电池的技术参数。磷酸铁锂电池的能量密度和能量效率具有巨大优势,亟需解决的是安全性问题;铅碳电池虽然成本较低,但服役年限较短、环保压力较大;水系全钒液流电池的服役年限长达20 年,是目前商业化较为成熟的长时储能技术,国内水系全钒液流电池生产企业主要有大连融科、北京普能、上海电气、武汉南瑞等。度电成本是现阶段水系全钒液流电池发展的最大制约因素,但随着市场化、规模化推进,水系全钒液流电池的成本有希望逐年下降。
水系有机液流电池由于正负极电解质分子种类繁多、高性能隔膜尚待开发、电池管理缺少研究,表中技术参数波动范围较大。结合德国电池公司Jena Batteries GmbH 的商业示范项目和国内宿迁时代储能科技有限公司的研发阶段成果来看,能量密度≥30 W·h/L,最大放电功率密度≥300 mW/cm2,能量效率≥80%,循环容量衰减≤0.05%/d的水系有机液流电池有望参与长时储能市场竞争。具体而言:①有机电解质分子的溶解度达到钒电解质分子的溶解度水平(≥1.6 mol/L),有机电解质电对理论电势差达到1.2 V 以上,水系有机液流电池即可实现和水系全钒液流电池相当的能量密度;②水系全钒液流电池使用全氟磺酸膜传导H+,理论上比水系有机液流电池更容易实现高功率密度,但随着水系有机液流电池专用隔膜的研究深入,两者将在功率密度上相当;③水系全钒液流电池安全工作的温度一般限制在10~40 ℃,温度过高或过低均会导致电解液析出堵塞管道,因此水系全钒储能系统会通过控温保证电池安全。控温会引起能量损耗,而水系有机液流电池对温度没有水系全钒敏感,如果水系有机液流电池的能量效率≥80%,其系统能效将更有优势;④循环容量衰减是水系有机液流电池发展的最大挑战,按照Micheal 教授等[55]对循环衰减划分的极低等级(≤0.02%/d)推算,连续测试(24 h)情况下电池容量20%的损失对应1000 天。而实际应用过程中,储能系统一天的充放电时间一般均为4 h,因此电池容量20%的损失对应3000天(8~10 年)。虽然有机电解质分子成本较低、回收再利用容易实现,可以采用补液、换液的方式恢复电池容量,但水系有机液流电池具备市场竞争力至少需要循环容量衰减处于低等级(0.02%~0.1%/d)。
3 结语
当前,我国的储能产业尚处于市场培育期,发展市场导向的新型储能技术尤为重要。水系全钒液流电池是目前受认可的长时储能技术,具有相同工作原理和技术优势的水系有机液流电池虽然在能量密度(≥30 W·h/L)、功率密度(最大放电功率密度≥300 mW/cm2)和效率(库仑效率约100%,电压效率、能量效率≥80%)方面和水系全钒液流电池相当,但循环稳定性离水系全钒液流电池还存在一定差距。水系有机液流电池通过电解液、隔膜、电极、BMS、PCS 等的综合优化,预期循环容量衰减≤0.05%/d,实现全生命周期成本与水系全钒液流电池相当,从而进入电化学储能市场。

