应用K-Clip 系统经导管治疗左心瓣膜置换术后重度三尖瓣反流1 例
郑帆 张晓春 陈莎莎 李明飞 李伟 潘翠珍 郭克芳 潘文志周达新 葛均波
1 临床资料
患者 女,63岁,因“二尖瓣、主动脉瓣机械瓣置换术后10年,劳力性胸闷气促1年”于2021年11月7日入住复旦大学附属中山医院心内科。患者10年前因风湿性二尖瓣、主动脉瓣重度狭窄及中度反流行机械瓣置换术,术后规律随访超声心动图,提示三尖瓣反流(tricuspid regurgitation,TR)进行性加重。近1年患者开始出现劳力性胸闷气促,活动耐量减退,双下肢浮肿,静息情况下仍有症状,经药物保守治疗无好转。入院N末端B型脑钠肽前体(amino-terminal probrain natriuretic peptide,NT-proBNP)324 pg/ml。心电图示:心房颤动。CT提示心影明显扩大,未见肺淤血征象。冠状动脉基于CT血管造影(computed tomographic angiography,CTA)未见异常。超声心动图示:重度TR(图1A),右心房、右心室扩大,右心功能轻度受损,三尖瓣收缩期位移(tricuspid annular plane systolic excursion,TAPSE)16 mm,左心大小及功能良好,二尖瓣、主动脉瓣机械瓣功能良好。右心导管检查示:右心房压15/6/10 mmHg(1 mmHg=0.133 kPa),肺动脉压30/14/21 mmHg。6 min步行试验(6 minute walking test,6MWT)136 m。临床诊断:三尖瓣关闭不全(重度),二尖瓣、主动脉瓣机械瓣置换术后,持续性心房颤动,纽约心脏病协会(New York Heart Association,NYHA)心功能分级Ⅳ级。美国胸外科医师学会(Society of Thoracic Surgeons,STS)评分17.5%。患者同意接受K-Clip(中国,上海汇禾医疗科技有限公司)手术。该研究获得复旦大学附属中山医院医学伦理委员会的批准(批准文号:2021-032R),治疗策略均符合《赫尔辛基宣言》,并已获得书面知情同意。
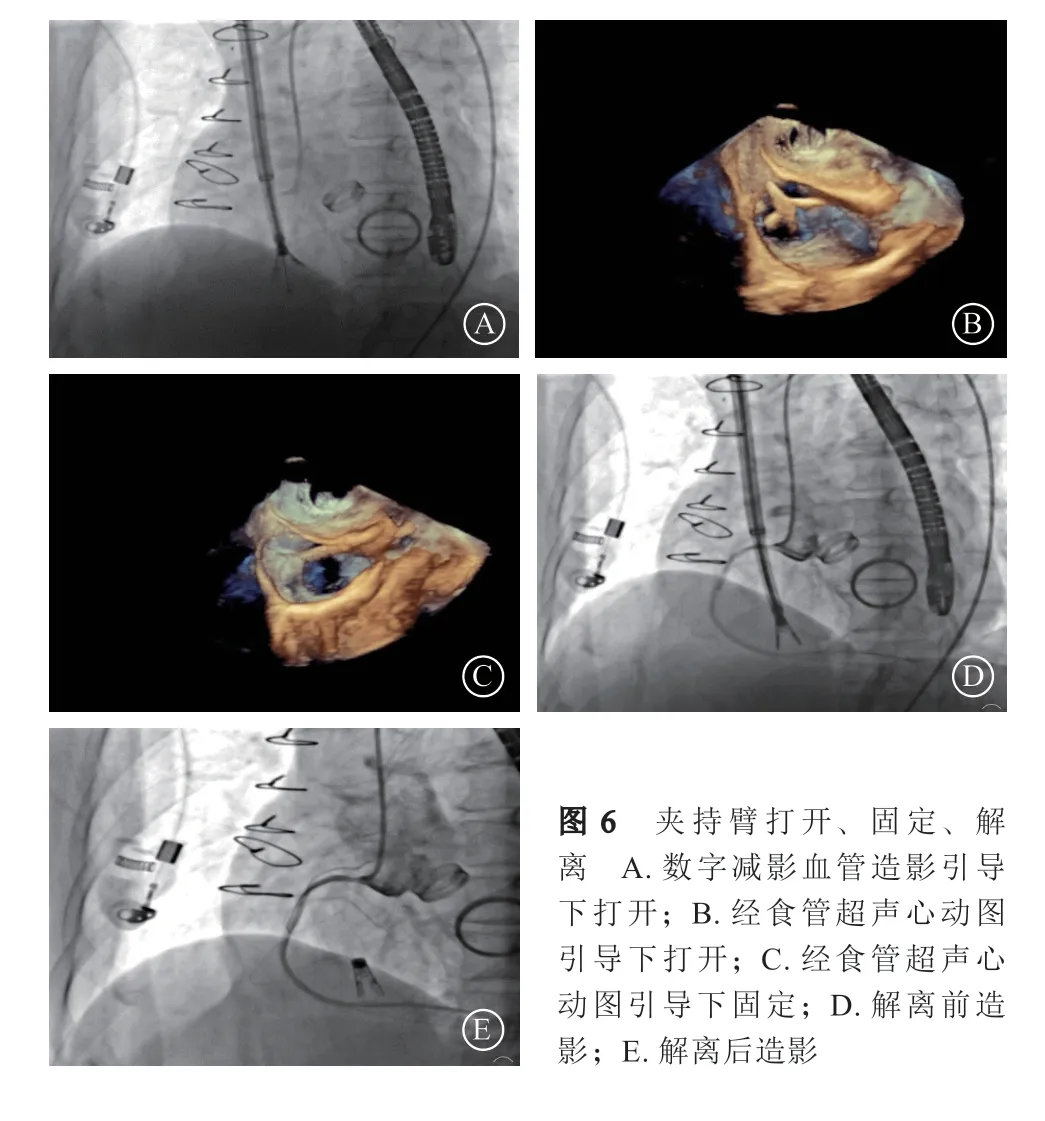
K-Clip术前CT分析结果:三尖瓣环周长147.0 mm,面积1605.7 mm2,最大直径55.9 mm;后瓣瓣环(P)长度50.1 mm;隔瓣瓣环(S)长度52.8 mm;前瓣瓣环(A)长度42.2 mm(图1B~C)。术中以右冠状动脉作为术中标示,后瓣瓣环中点位于右冠状动脉后三叉处(后瓣偏后),三尖瓣环短轴面足位9°+左前斜位59°,长轴面足位25°+右前斜位34°(图2A~B);右心房上下径85.223 mm,左右径57.397 mm,前后径47.559 mm(图2C~E)。 患者前瓣至后瓣中部瓣环与冠状动脉靠近,拟缩环靶点部位为后瓣中点(图3)。于2021年11月10日静脉复合麻醉下应用K-Clip系统行三尖瓣瓣环修复术:收集术前超声心动图影像后,穿刺右侧颈静脉;数字减影血管造影(digital subtraction angiography,DSA)下行右冠状动脉造影,滞留通体显影导丝。前后位下将加硬导丝送入下腔静脉,沿加硬导丝送入输送鞘管及扩张内芯,大鞘管显影环至右心房中下部,接近右冠状动脉导丝下缘。在二维和三维经食管超声心动图(transesophageal echocardiography,TEE)引导下撤离内芯及加硬导丝,滞留大鞘管位于下腔静脉口处。DSA正位下从大鞘管内送入小鞘管(二者头端齐平);大鞘管先回撤4 cm,小鞘管再撤离1 cm,短轴面小鞘管弯头端指向后瓣中点方向(图4)。经胸超声心动图示右心两腔切面引导下微调弯小鞘管弯头端,将夹子头端指向瓣环(超声辨识冠状动脉、瓣环、瓣叶)。攻入锚定螺丝。DSA、超声心动图下牵拉测试,判断是否已经锚定牢固(图5)。DSA下短轴面打开夹持臂,平行靠近瓣环;三维TEE引导下夹持臂夹合瓣环(两脚靠瓣环)。DSA下短轴面行右冠状动脉造影示右冠状动脉血流通畅;TEE提示TR由4+减为2+,确认夹子的位置稳定性后解离夹子;右冠状动脉造影再次确认右冠状动脉血流通畅(图6)。术后患者NT-proBNP较前升高,予小剂量利尿剂治疗,患者自觉症状逐渐缓解,出院前NT-proBNP降至298 pg/ml。术后1个月随访活动后气促、乏力等症状明显缓解,6MWT 190 m,日常活动轻度受限。三尖瓣瓣环修复治疗术前、术后随访超声心动图、NYHA心功能分级结果见表1。
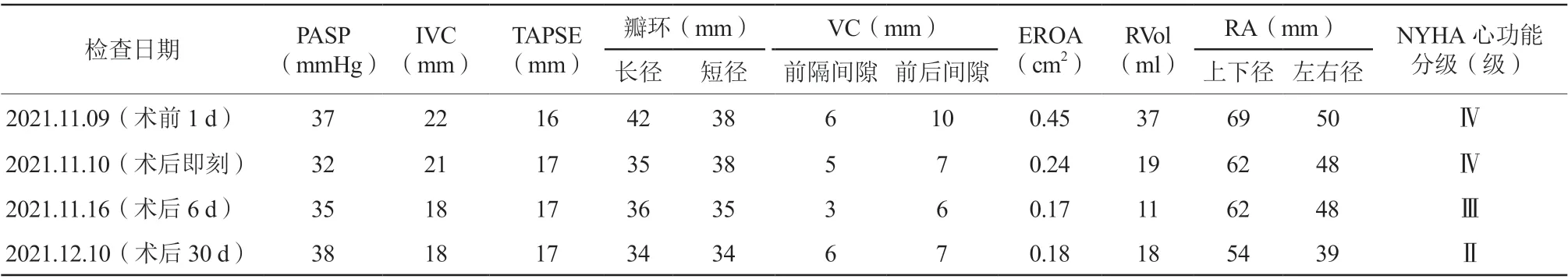
表1 手术前后超声心动图及NYHA 心功能分级结果
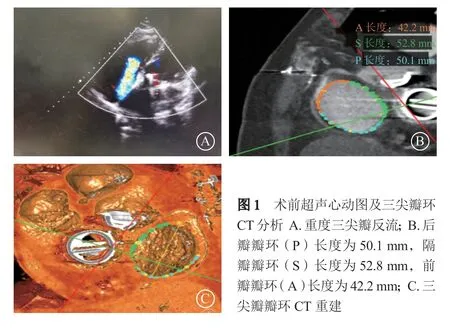
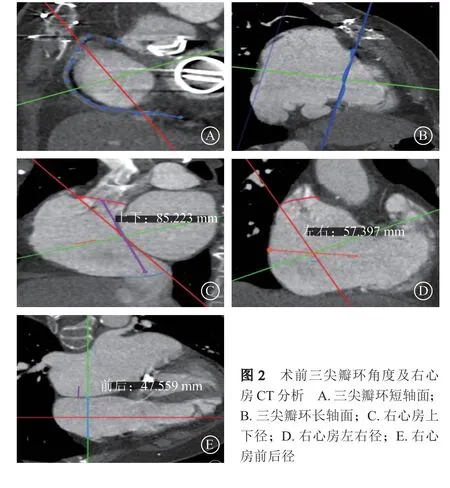
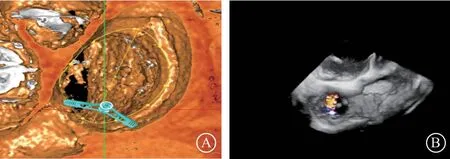
图3 术前CT、经食管超声心动图心房视角分析 A.CT 模拟后瓣中点为靶点部位;B.术前经食管超声心动图后瓣部位
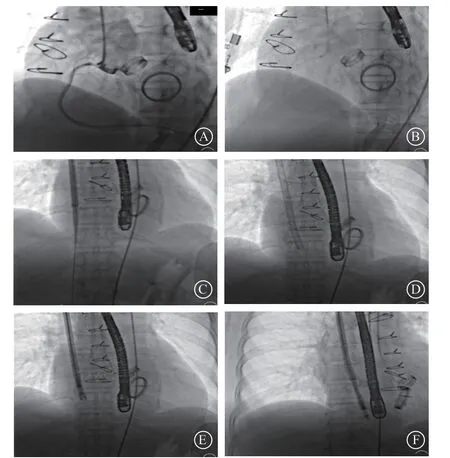
图4 术中数字减影血管造影影像 A.右冠状动脉造影;B.滞留通体显影导丝;C.大鞘管送至右心房中下部;D.撤出内芯及加硬导丝;E.小鞘管与大鞘管头端平齐;F.小鞘管弯头端指向后瓣中点
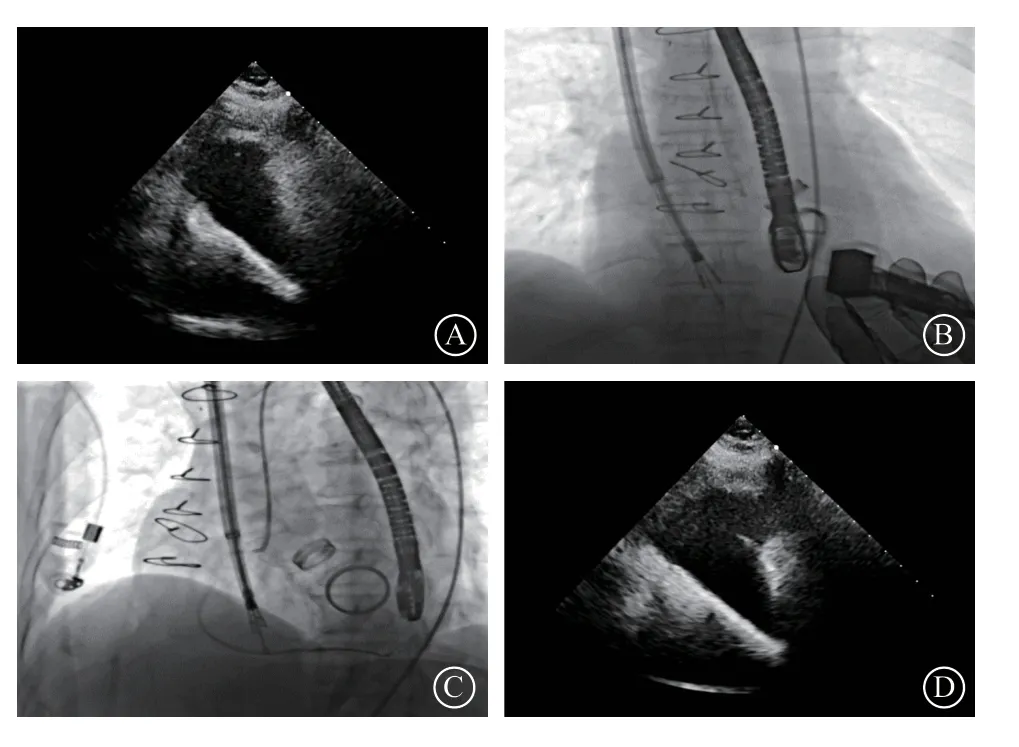
图5 攻入锚定螺丝及稳定性测试 A.超声心动图引导下夹子头端指向瓣环;B.攻入锚定螺丝;C.数字减影血管造影下牵拉;D.经食管超声心动图下牵拉
2 讨论
TR是最常见的右心疾病,根据发病原因可分为原发性和继发性TR[1],其中继发性TR主要由左心系统瓣膜疾病引起。继发的迟发性TR是左心瓣膜置换术(特别是二尖瓣置换术)的重要并发症,可导致患者活动能力下降且提示预后不良[2-3]。目前左心瓣膜机械瓣置换术后引起TR的机制未明,可能与以下几个因素有关:(1)既往研究表明可能是左心衰竭、左心房压升高、肺动脉高压等导致右心负荷增加的因素所引起[2];(2)可能与相对主动脉瓣、二尖瓣狭窄有关;(3)与长期心房颤动引起的心房心肌病、继发双房扩大,进而导致三尖瓣环扩大和右心室扩张,从而造成的乳头肌移位相关[4]。本例患者属于第(3)种情况,二尖瓣、主动脉瓣机械瓣置换术后左心功能良好,右心导管提示肺动脉压力不高,有可能跟近期术前良好的容量管理有关,考虑此患者继发性TR可能由于瓣环重塑导致。长期持续性心房颤动也是引发TR的重要因素,在孤立性TR中,没有肺动脉高压的情况下,右心室长度正常,但在基部扩张情况下显示更多的是环状增大[5-6]。此外,初次手术未能识别和纠正TR也可能是导致迟发性TR的原因。目前指南推荐,二尖瓣手术如伴随三尖瓣功能障碍,应同期行三尖瓣修复[7]。但本例患者行左心瓣膜置换术时TR仅是轻微的,如二尖瓣手术时,同期预先行三尖瓣修复该患者是否能获益,值得进一步探讨。
本例患者在10年前行主动脉瓣、二尖瓣瓣膜置换术,术后复旦大学附属中山医院门诊规律随访,于2021年11月7日因“二尖瓣、主动脉瓣机械瓣置换术后10年,劳力性胸闷气促1年”入院,分析其症状发生与TR相关:(1)10年前行主动脉瓣、二尖瓣瓣膜置换术,术后TR进行性加重,从轻微逐步进展成中重度,与患者逐渐加重的胸闷气促症状较匹配。(2)患者以体循环淤血(双下肢浮肿及胃肠道淤血)为主要体征。超声心动图提示左心系统功能尚可(左心室射血分数59%),瓣口面积相对稳定,未出现新的左心瓣膜相关问题,右心功能下降,重度TR,TAPSE下降,肺动脉压正常。CT提示心影增大,未见肺淤血症状。既往无基础肺病情况。综合考虑,诊断为右心衰竭,重度TR为患者胸闷气促的主要原因,左心房增大合并心房颤动导致的左心功能不全(NTproBNP升高)是次要原因。故考虑对TR进行干预治疗。
目前中重度TR已被证实可以增加患者死亡风险[8],因此,纠正或减少TR是改善患者预后的重要目标。临床上TR的干预措施主要有外科干预、内科干预、药物保守治疗[9],目前修复三尖瓣的金标准仍然是外科干预。而临床上TR患者出现症状时,往往处于晚期,多数心功能较差,无法耐受二次开胸手术及体外循环的打击,这也是外科手术干预死亡风险高的其中一个原因,这就导致部分患者丧失手术机会。此外,药物保守治疗效果也不佳。在2021年欧洲心脏病学会(European Society of Cardiology,ESC)三尖瓣治疗指南[7]中,TR修复的Ⅰ类适应证仅适用于需要手术的二尖瓣、主动脉瓣病变患者(B级证据),在无法耐受外科手术的患者中,经导管治疗症状性严重的TR患者在有经验的心脏中心是可行的;针对外科高危的严重TR患者,三尖瓣环修复是一个潜在可行的方式。本例患者经药物保守治疗后效果不佳,且外科干预风险高,因此,对此患者决定采用微创治疗方案。目前TR介入方法主要有三尖瓣瓣环成形术、缘对缘瓣叶修复术及三尖瓣置换术。目前尚未有批准上市的三尖瓣瓣膜置换系统,其中EVOQUE、Navi Gate、Lux Valve等瓣膜置换产品仍处于临床试验阶段。但既往研究表明,部分患者在置换三尖瓣后死亡,考虑系瓣膜置换后,三尖瓣前向血流急剧增加,肺血明显增加,肺动脉压力明显上升,发生严重的心力衰竭导致死亡,这提示更应严格把握TR置换瓣膜的适应证。首先对于继发性TR合并右心功能不全的患者,TR可能是一种代偿性的表现,即刻关闭TR可能会让右心室来不及代偿而出现急性右心衰竭,这也是三尖瓣置换术后的主要死亡原因,故置换多用于原发性TR且右心功能减退不明显的患者,对于继发性TR尤其是右心功能不全的患者需要谨慎选择;其次继发性TR多数情况下三尖瓣形态是正常的,更多的是瓣环的扩张,TR可能是潜在机体的一种代偿和保护机制,完全减少TR未必是好事。而三尖瓣缘对缘修复如果夹合位置不恰当,可能导致瓣上流速增快。而本例患者是左心瓣膜置换术后继发重度TR,主要是瓣环的扩张,而非瓣膜自身病变,故从发病机制而言,选择了K-Clip系统修复TR作为该患者的首选方案。应用K-Clip系统经颈静脉路径行三尖瓣瓣环修复术,其原理与外科Kay术式类似:通过刚性成形夹折叠三尖瓣后叶瓣环使三尖瓣形成二瓣化,缩小瓣环直径,改善瓣叶对合,进而减少反流而非阻断反流。本例患者术后TR由4+减为2+,且随着随访时间的延长,患者右心房大小、TR程度、三尖瓣环都有减小趋势,考虑可能原因为患者术前重度TR,但左右心室收缩功能正常,TR量减小后右心前负荷减小,右心房室扩张减轻,三尖瓣瓣环进一步缩小,且会增加左心输出量,形成良性循环,随访时间延长,患者TR可能进一步减轻。而改善最明显的是患者的临床症状和心功能状态。提示三尖瓣瓣环成形术可能是继发性TR治疗的未来趋势。
K-Clip系统在三尖瓣后叶瓣环缩环术式中的应用,类似于Trialign系统工作的原理,均通过后叶瓣环成形实现三尖瓣二瓣化,其临床研究结果可作为参考。Trialign系统经颈静脉路径,在瓣环内置入缝线,通过锁定装置将2根缝线收紧,导致三尖瓣二瓣化,最终结果是通过缝合垫片、折叠三尖瓣后瓣瓣环来实现[10]。SCOUT-1试验[11]已证实Trialign系统安全有效。Trialign系统存在定位要求高,置入缝线困难,且存在置入不当撕脱瓣叶风险。K-Clip系统通过术前CT精确测量及对右冠状动脉风险评估,术中应用2D及3D TEE和DSA精确引导,夹合后叶瓣环,旷置三尖瓣前瓣环,减少部分TR,残余部分TR,通过减少TR减轻体循环淤血,同时增加左心射血量,改善症状。因此,K-Clip系统对于左心瓣膜置换术后继发性TR患者可能是更为合适的一种选择,但需评估右冠状动脉狭窄风险。该患者应用K-Clip行修复术后右心系统较前缩小,术后患者出现NT-proBNP进一步升高,考虑TR减轻后,三尖瓣前向血流增加导致肺血增加,经利尿后症状好转。1个月后随访6MWT较术前明显提高。这进一步提示缩后瓣环,旷置前瓣环可能是更好的治疗方案。
综上所述,TR作为临床上被忽视的右心系统疾病,外科干预和药物治疗往往效果欠佳。三尖瓣介入干预方式可能是未来TR的重要治疗方式。应用K-Clip系统经颈静脉路径行三尖瓣环修复术,手术创伤小,安全性及有效性好,可改善左心瓣膜置换术后继发性TR和心功能。但目前完成例数较少,其临床安全性和有效性仍需大规模随机对照研究验证。此外,针对不同原因导致的TR,如何选择获益人群及筛选最佳适应证,以及改善其远期效果的研究仍然任重道远。
利益冲突 所有作者均声明不存在利益冲突

